一测多评法同时测定克感额日敦片中9 种成分
2020-11-02季正栋唐丽丹房燕冬
季正栋 苏 丹 唐丽丹 房燕冬
(1.南京医科大学附属常州市第二人民医院药剂科, 江苏 常州213003; 2.常州四药制药有限公司研发中心, 江苏 常州213004)
克感额日敦片由栀子、苦参、土木香、诃子、悬钩子木、川楝子、山柰7 味药材加工而成,主要用于瘟病初期、感冒发烧、咳嗽、全身酸痛、头痛、咽喉肿痛、胸胁刺痛等临床病症的治疗,但现行质量标准[1]及文献[2⁃5]仅对其所含单一成分进行定量分析。中药制剂组成复杂,有效成分繁多,多种成分协同发挥作用以达到临床疗效,故仅检测单一成分难以对其质量进行全面评价,但传统多指标成分控制方法存在对照品用量大、质量不稳定、不易获得、价格昂贵等不足。
一测多评法利用中药有效成分之间存在的内在函数和比例关系,有效地解决了上述难题,同时该方法不仅普遍用于同类型成分的同时测定,在不同类型成分中也逐步得到应用[6⁃9]。因此,本实验采用一测多评法,以栀子苷为内标,建立栀子新苷、羟异栀子苷、京尼平龙胆双糖苷、苦参醇I、苦参酮、槐属二氢黄酮G、异土木香内酯、土木香内酯的相对校正因子,测定克感额日敦片中上述成分含有量,以期为该制剂全面质量控制提供新的方法和思路。
1 材料
Agilent 1200 型高效液相色谱仪(美国Agilent公司);LC⁃20AD 型高效 液相色谱仪(日本Shimadzu 公司);CP225D 型电子天平(德国Sarto⁃rius 公司);KQ⁃500E 型超声波清洗器(昆山市超声仪器有限公司)。土木香内酯(批号110760⁃201811,纯 度99.4%)、异土木 香内酯(批 号110761⁃201806,纯 度97.4%)、栀子苷(批 号110749⁃201919,纯度97.1%)对照品均购自中国食品药品检定研究院。栀子新苷(批号CFS201901,纯度98.0%)、苦参醇I(批号CFS201702,纯度98.0%)对照品均购自武汉天植生物技术有限公司;羟异栀子苷(批号17101622,纯度99.1%)、京尼平龙胆双糖苷(批号18030422,纯度98.4%)、苦参酮(批号18060822,纯度97.7%)、槐属二氢黄酮G(批号18060622,纯度99.7%)对照品均购自上海同田生物技术股份有限公司。克感额日敦片(每片重0.25 g,批号34181003、34181106、34190205)购自内蒙古天奇中蒙制药股份有限公司。乙腈为色谱纯;其余试剂均为分析纯。
2 方法与结果
2.1 溶液制备
2.1.1 对照品溶液 精密称取栀子新苷、羟异栀子苷、京尼平龙胆双糖苷、栀子苷、苦参醇I、苦参酮、槐属二氢黄酮G、异土木香内酯、土木香内酯对照品适量,甲醇制成各成分质量分数分别为0.232、0.898、1.634、2.982、0.454、1.876、0.412、0.998、1.766 mg/g 的贮备液,各精密吸取2.5 mL,甲醇稀释,即得(各成分质量分数分别 为 11.6、44.9、81.7、149.1、22.7、93.8、20.6、49.9、88.3 μg/g)。
2.1.2 供试品溶液 取片剂适量,除去薄膜衣后研细,精密称取0.4 g,精密加入25 mL 甲醇[10⁃11],密塞,称定质量,超声处理60 min[10⁃11],放 冷,甲醇补足减失的质量,摇匀,0.45 μm 微孔滤膜过滤,即得。
2.1.3 阴性样品溶液 按片剂处方工艺,分别制备缺栀子、缺苦参、缺土木香的阴性样品,按“2.1.2” 项下方法制备,即得。
2.2 色谱条件 Agilent ZORBZX SB⁃C18色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈(A)⁃0.05%磷酸(B),梯度洗脱(0~10.0 min,9.0%A;10.0~29.0 min,9.0%~35.0% A;29.0~51.0 min,35.0%~52.0% A;51.0~65.0 min,52.0%~60.0%A;65.0~75.0 min,60.0%~9.0%A);体积流量0.9 mL/min;柱温30 ℃;检测波长238 nm(0~29.0 min,栀子新苷、羟异栀子苷、京尼平龙胆双糖苷、栀子苷)[12⁃14]、295 nm(29.0~51.0 min,苦参醇I、苦参酮、槐属二 氢黄酮G)[15]、220 nm(51.0~75.0 min,异土木香内酯、土木香内酯)[16];进样量10 μL。
2.3 方法学考察
2.3.1 系统适用性试验 精密吸取对照品、供试品、阴性样品溶液适量,在“2.2” 项色谱条件下进样测定,结果见图1。由此可知,各成分色谱峰峰形对称,分离度均大于1.5,理论塔板数按各成分计均不低于4 000,色谱图基线平稳,阴性无干扰。
2.3.2 线性关系考察 精密吸取“2.1.1” 项下贮备液适量,甲醇制成20 倍质量浓度差的对照品溶液Ⅰ~Ⅵ,在“2.2” 项色谱条件下进样测定。以溶液质量浓度为横坐标(X),峰面积为纵坐标(Y)进行回归,结果见表1,可知各成分在各自范围内线性关系良好。
2.3.3 精密度试验 精密吸取“2.1.1” 项下对照品溶液,在“2.2” 项色谱条件下进样测定6 次,测得栀子新苷、羟异栀子苷、京尼平龙胆双糖苷、栀子苷、苦参醇I、苦参酮、槐属二氢黄酮G、异土木香内酯、土木香内酯峰面积RSD 分别为1.26%、0.93%、0.57%、0.55%、1.17%、0.96%、1.22%、1.01%、0.63%,表明仪器精密度良好。
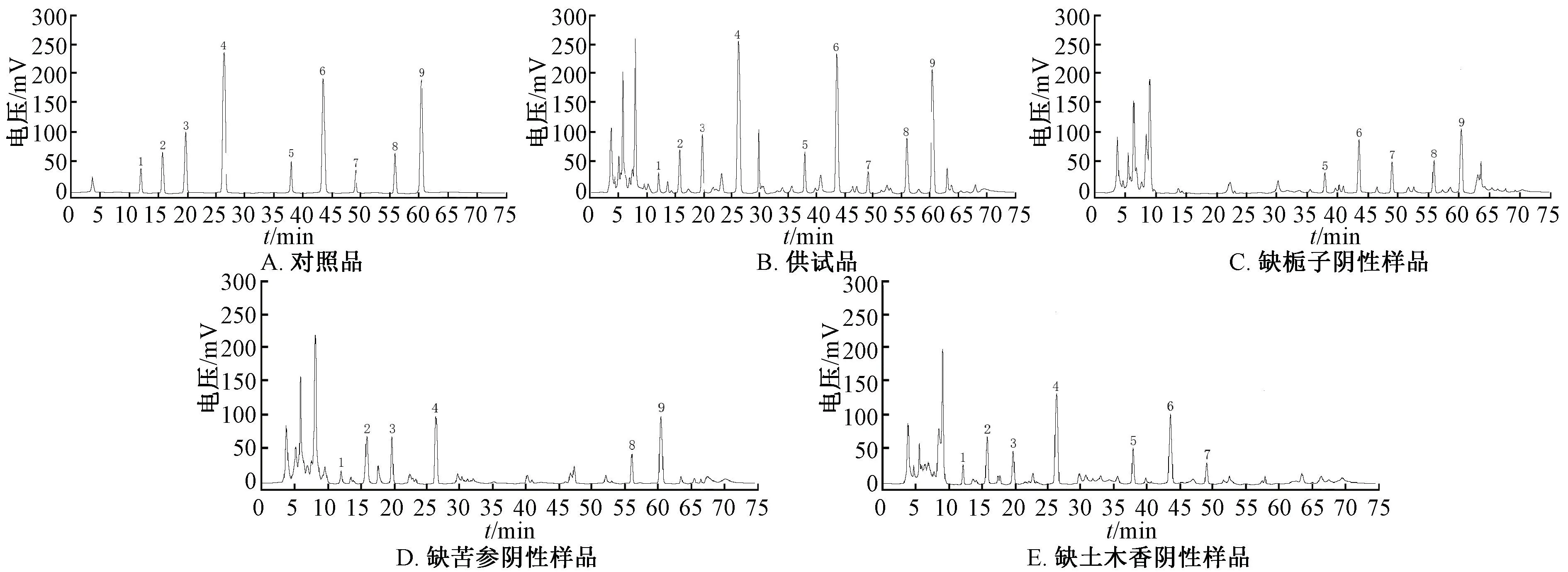
图1 各成分HPLC 色谱图Fig.1 HPLC chromatograms of various constituents
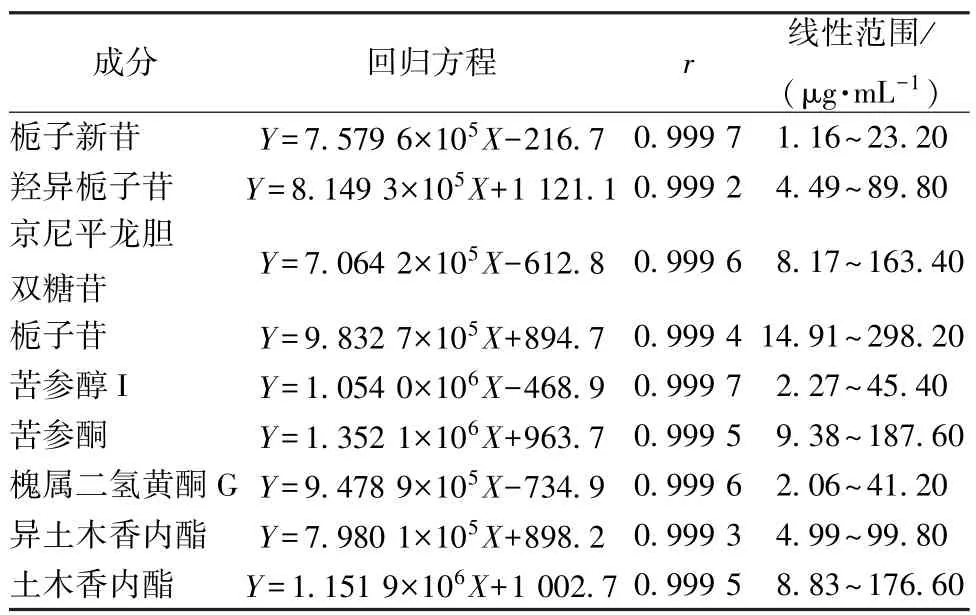
表1 各成分线性关系Tab.1 Linear relationships of various constituents
2.3.4 重复性试验 取同一批片剂,按“2.1.2”项下方法平行制备6 份供试品溶液,在“2.2” 项色谱条件下进样测定,测得栀子新苷、羟异栀子苷、京尼平龙胆双糖苷、栀子苷、苦参醇I、苦参酮、槐属二氢黄酮G、异土木香内酯、土木香内酯含有量RSD 分别为1.58%、1.25%、0.96%、0.89%、1.38%、1.14%、1.61%、1.37%、0.99%,表明该方法重复性良好。
2.3.5 稳定性试验 取新配供试品溶液1 份,于0、2、4、6、10、12 h 在“2.2” 项色谱条件下进样测定,测得栀子新苷、羟异栀子苷、京尼平龙胆双糖苷、栀子苷、苦参醇I、苦参酮、槐属二氢黄酮G、异土木香内酯、土木香内酯峰面积RSD 分别为1.23%、1.01%、0.61%、0.59%、1.22%、0.94%、1.18%、0.97%、0.70%,表明溶液在12 h内稳定性良好。
2.3.6 加样回收率试验 取各成分含有量已知的同一批片剂,除去薄膜衣后研细,精密称取9 份,每份0.2 g,精密加入对照品溶液(栀子新苷0.128 mg/mL、羟异栀子苷0.506 mg/mL、京尼平龙胆双糖苷0.932 mg/mL、栀子苷1.966 mg/mL、苦参醇I 0.302 mg/mL、苦参酮1.194 mg/mL、槐属二氢黄酮 G 0.238 mg/mL、异土木 香内酯0.682 mg/mL、土木香内酯1.126 mg/mL)0.5、1.0、1.5 mL 各3 份,按“2.1.3” 项下方法制备供试品溶液,在“2.2” 项色谱条件下进样测定,计算加样回收率。结果,栀子新苷、羟异栀子苷、京尼平龙胆双糖苷、栀子苷、苦参醇I、苦参酮、槐属二氢黄酮G、异土木香内酯、土木香内酯平均加样回收率(RSD)分别为96.94%(1.26%)、99.13%(1.42%)、98.96%(0.99%)、99.37%(0.86%)、97.92%(1.50%)、100.00%(0.76%)、98.67%(0.90%)、98.99%(0.84%)、97.86%(1.00%)。
2.4 相对校正因子测定 精密吸取“2.3.2” 项下对照品溶液Ⅰ~Ⅵ,在“2.2” 项色谱条件下进样测定。以栀子苷为内标,计算其他8 种成分的相对校正因 子fk/s,公式为fk/s=fk/fs=(CkAs)/(CsAk),其中Ck为其他成分含有量,Ak为其他成分峰面积,Cs为内标含有量,As为内标峰面积,结果见表2。

表2 各成分相对校正因子Tab.2 Relative correction factors of various constituents
2.5 耐用性试验
2.5.1 仪器、色谱柱 精密吸取“2.1.2” 项下对照品溶液,在“2.2” 项色谱条件下进样测定,考察Agilent 1200、LC⁃20AD 色谱仪,以 及 Agilent ZORBZX SB⁃C18、Waters Symmetry C1、Diamonsil C18色谱柱(250 mm×4.6 mm,5 μm)对相对校正因子的影响,结果见表3,可知均无明显影响(RSD<3%)。

表3 不同仪器、色谱柱对相对校正因子的影响Tab.3 Effects of different instruments and columns on relative correction factors
2.5.2 体积流量 精密吸取“2.1.2” 项下对照品溶液,在“2.2” 项色谱条件下进样测定,考察体积流量0.7、0.8、0.9、1.0、1.1 mL/min 对相对校正因子的影响,结果见表4,可知均无明显影响(RSD<3%)。
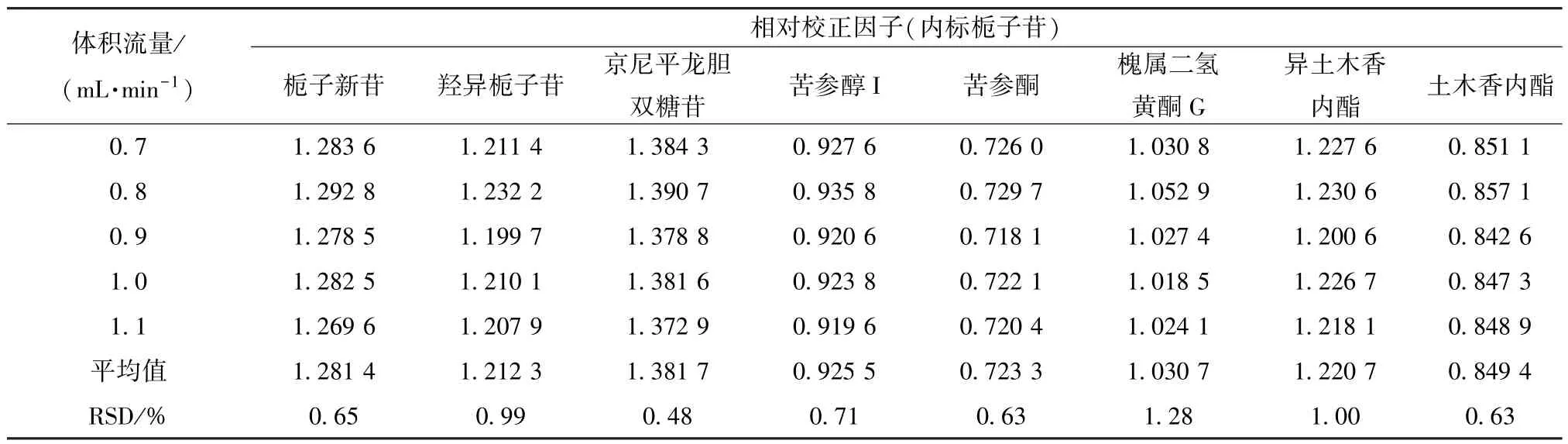
表4 不同体积流量对相对校正因子的影响Tab.4 Effects of different volumetric flow rates on relative correction factors
2.6 色谱峰定位 精密吸取“2.1.2” 项下对照品溶液,在“2.2” 项色谱条件下进样测定,以栀子苷为内标,采用相对保留时间法对色谱峰进行定位,结果见表5。
2.7 样品含有量测定 取3 批片剂,按“2.1.3”项下方法制备供试品溶液,在“2.2” 项色谱条件下进样测定,分别采用外标法和一测多评法测定含有量,结果见表6。由此可知,2 种方法所得结果接近,相对平均偏差(RAD)均小于3%。
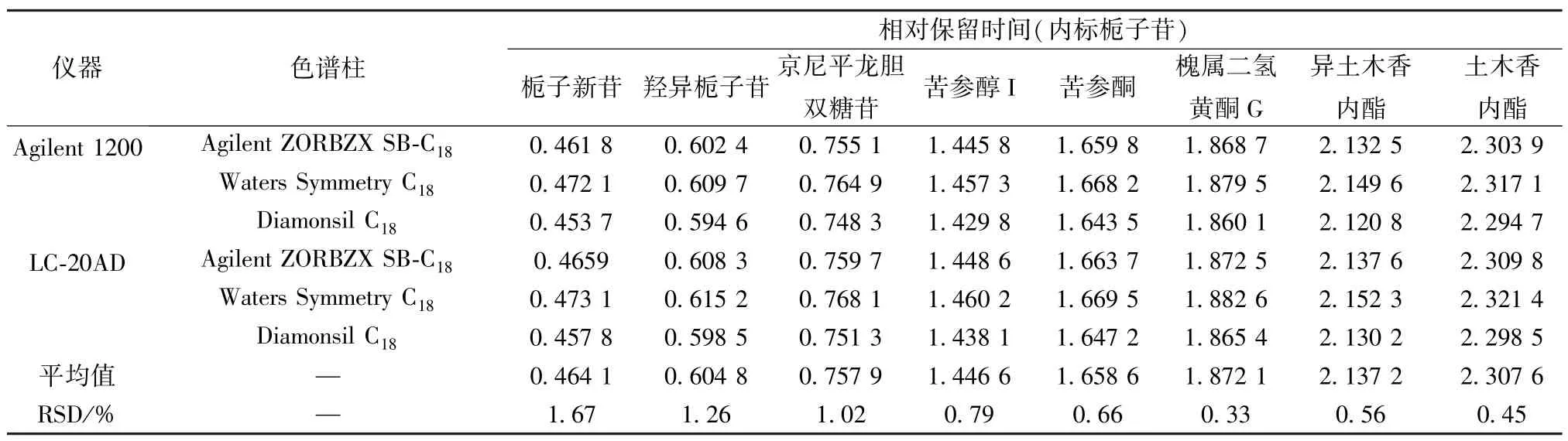
表5 各成分相对保留时间Tab.5 Relative retention time of various constituents

表6 各成分含有量测定结果(mg/g, n=3)Tab.6 Results of content determination of various constituents(mg/g, n=3)
3 讨论
3.1 指标成分筛选 在克感额日敦片中,君药栀子的主要成分为栀子新苷、羟异栀子苷、京尼平龙胆双糖苷、栀子苷等环烯醚萜,臣药苦参的主要成分为苦参醇I、苦参酮、槐属二氢黄酮G 等异戊烯基黄酮,佐药土木香的主要成分为土木香内酯、异土木香内酯等倍半萜内酯。参考中药质量标志物确定原则,本实验选取上述9 种成分作为指标进行检测。
3.2 色谱峰定位方法筛选 本实验分别采用相对保留时间法、保留时间差法定位色谱峰,发现后者在不同仪器、色谱柱下测得的RSD 明显高于前者。因此,选择相对保留时间法进行定位。
3.3 供试品溶液制备方法筛选 本实验比较了提取溶 剂(甲 醇[10⁃11,15]、70% 甲 醇[13]、95% 乙 醇、70%乙醇[12,16]),发现甲醇提取时杂质干扰较小,各成分提取充分;比较了提取方式(超声[10⁃16]、加热回流),发现加热回流提取时杂质干扰严重;比较了 提取时 间(45 min[11]、60 min[15]、90 min),发现苦参醇I、苦参酮、槐属二氢黄酮G提取60、90 min 时的效果差异不大,但明显高于45 min,可能与克感额日敦片中苦参采用细粉直接入药方式有关。最终确定,供试品溶液制备方法为甲醇超声提取60 min。
3.4 检测波长筛选 本实验采用二极管阵列检测器,在190~400 nm 范围内进行全波长扫描,发现栀子新苷、羟异栀子苷、京尼平龙胆双糖苷、栀子苷在238 nm 处有较大吸收,苦参醇I、苦参酮、槐属二氢黄酮G 在291~297 nm 处有较大吸收,异土木香内酯、土木香内酯在190~220 nm 处有较大吸收。为了避免末端吸收对检测结果的影响,结合文献[12⁃16],本实验选择220、238、295 nm,同时发现单一波长难以对克感额日敦片中9 种成分同时进行测定,故采用“2.2” 项下多波长切换模式。
4 结论
本实验首次采用一测多评法同时测定克感额日敦片中栀子新苷、羟异栀子苷、京尼平龙胆双糖苷、栀子苷、苦参醇I、苦参酮、槐属二氢黄酮G、异土木香内酯、土木香内酯的含有量,该方法简便准确,可大大降低检验成本,为该制剂全面质量控制提供新的方法和思路。
