天麻素穴位注射对癫痫模型大鼠认知功能影响及机制探讨*
2020-10-26闫禹竹崔永会焦志勤
闫禹竹,肖 飞△,崔永会,焦志勤
(1.黑龙江中医药大学附属第一医院,黑龙江 哈尔滨 150040; 2.哈尔滨市南岗区革新社区卫生服务中心,黑龙江 哈尔滨 150000; 3.哈尔滨理工大学,黑龙江 哈尔滨 150000)
癫痫是以脑神经元过度放电导致的发作性中枢神经系统功能障碍为特征的慢性脑部疾病。其中近一半的癫痫病人可伴有认知功能特别是学习记忆功能障碍[1]。因此,近年来如何治疗癫痫伴学习记忆等认知功能障碍成为神经科学的研究热点之一。本课题通过观察天麻素穴位注射对戊四氮致痫模型大鼠行为学及脑组织海马区COX-2 mRNA表达的变化,探讨天麻素穴注的抗痫及神经保护作用及可能的机制。
1 材料与方法
1.1 实验动物与分组
由黑龙江中医药大学实验动物中心提供120只健康Wistar雄性大鼠,SPF级,体质量250~325 g。采用随机数字表法将尾部标记编号的实验大鼠分为空白组、模型组、穴注组及西药组,每组各30只。
1.2 实验药物及试剂
按等效剂量比例换算方法,穴注天麻素(昆明制药集团股份有限公司,批号:H20013046,规格:0.2 g/支)成人用量:0.088 6 mL/kg,换算后实验大鼠用量:0.37 mL/kg;丙戊酸钠片(山东仁和堂有限公司,批号:H19983059,规格:0.2 g/片)放置于4 ℃环境下遮光保存;戊四氮(PTZ,美国Sigma公司,货号:Sigma-p6500)配制成戊四氮溶液(PTZ溶液,浓度:2 mg/mL);10%水合氯醛溶液;Trizol试剂(美国Invitrogen公司);PCR扩增仪(MJ Research公司)。
1.3 造模方法
除空白组外,每日上午8:30—11:30模型组、穴注组及西药组大鼠腹腔注射PTZ溶液35 mg/kg,空白组给予等剂量生理盐水腹腔注射,连续注射28 d以点燃戊四氮癫痫大鼠动物模型。每次注射治疗后,观察模型大鼠的行为学变化1 h,并根据Racine分级[2]判断评估及记录大鼠癫痫发作的级别。对实验大鼠可能发生的意外情况进行干预。在造模周期28 d内连续5 d出现Ⅳ级及以上的痫性发作,视为戊四氮癫痫大鼠造模成功,对于达不到造模标准或死亡大鼠予以剔除并补充相应数目大鼠以保证大鼠样本量恒定。
1.4 处置方法
穴注组在造模成功后,参照《实验针灸学》[3]及《大鼠穴位图谱的研制》[4],定位大鼠百会穴及大椎穴,给予标记,将天麻素溶液按0.37 mL/kg的给药剂量分别注射入模型大鼠百会穴及大椎穴,连续治疗28 d;西药组在造模成功后,给予丙戊酸钠溶液(350 mg/kg)灌胃,日1次,连续治疗28 d。
1.5 取材
Morris水迷宫及八臂迷宫试验结束后,对模型大鼠进行麻醉、固定、断头等处理,将实验大鼠的脑组织海马区迅速分离取材,将体积1 mm3大小组织块置于2.5%戊二醛固定液中前固定,保存标本,常规处理并按操作说明书以实时荧光定量PCR法检测COX-2 mRNA表达。
1.6 观察指标
1.6.1 全面强直发作-阵挛发作潜伏期和极小阵挛发作潜伏期 每次给予各组大鼠PTZ腹腔注射后,参照Racine分级,观察大鼠极小阵挛发作(MCS)潜伏期及全面性强直-阵挛发作(GTCS)潜伏期[5]。
1.6.2 Morris水迷宫试验 对各组实验大鼠进行Morris水迷宫试验检测大鼠的空间学习记忆能力。最后1次治疗结束后,每组大鼠再随机选出10只大鼠进行Morris水迷宫试验并记录实验大鼠寻找并爬上平台所需的时间以及穿越平台象限的次数。
1.6.3 八臂迷宫试验 对各组大鼠进行八臂迷宫试验检测大鼠与海马相关的工作记忆错误和参考记忆错误。治疗结束后,各组大鼠再随机选出10只大鼠进行八臂迷宫试验,并记录大鼠在八臂迷宫中的觅食情况,包括参考记忆错误次数、工作记忆错误次数、吃完食物所需总时间。
1.6.4 检测COX-2 mRNA的表达 实时荧光定量PCR法检测COX-2 mRNA在大鼠海马组织的表达。实验大鼠海马组织取材后,去RNA酶离心管中加入30 mg海马组织,同时加入Trizol试剂1 mL,剪碎、迅速匀浆、氯仿抽提、振荡混匀、离心、移入去RNA酶离心管。
1.7 统计学处理
采用SPSS13.0软件对数据进行统计分析,所有实验数据以均数±标准差表示。实验数据结果采用重复测量的多因素方差分析进行统计。P<0.05表示有统计学差异,P<0.01表示有差异显著统计学意义。
2 结果
2.1 一般情况
2.1.1 全面性强直-阵挛发作潜伏期(GTCS) 与模型组对比,穴注组及西药组大鼠GTCS均显著延长(P<0.01);穴注组与西药组对比,差异无统计学意义(P>0.05)。空白组大鼠未出现痫性发作。
2.1.2 极小阵挛发作潜伏期(MCS) 与模型组对比,穴注组及西药组大鼠MCS均显著延长(P<0.01);穴注组与西药组对比,差异无统计学意义(P>0.05)。空白组大鼠未出现痫性发作。见表1。

表1 各组戊四氮致痫大鼠全面强直发作-阵挛发作(GTCS)潜伏期和极小阵挛发作(MCS)潜伏期比较
2.2 各组Morris水迷宫试验比较
各组实验大鼠在Morris水迷宫中搜索平台游泳轨迹策略如图1所示,经训练后,空白组大鼠游泳轨迹表现为直线式有效策略;模型组大鼠游泳轨迹表现为以随机式为主,并且具极大盲目性;穴注组大鼠表现为趋向式的有效策略;西药组以边缘式为主。

图1 各组大鼠在Morris水迷宫中搜索平台游泳轨迹策略图
模型组与空白组相比,实验大鼠逃避潜伏期明显延长,差异具有统计学意义(P<0.01);模型组大鼠与空白组相比,在空间探索试验中穿越平台数明显减少,差异具有统计学意义(P<0.01);穴注组及西药组大鼠与模型组相比,逃避潜伏期时间均较模型组明显缩短,差异有统计学意义(P<0.01),穿越平台数明显增多,差异有统计学意义(P<0.01);穴注组与西药组比较差异无统计学意义(P>0.05)。见表2。

表2 Morris水迷宫试验各组大鼠逃避潜伏期与穿越平台次数比较
2.3 各组八臂迷宫试验比较
与空白组比较,模型组、穴注组、西药组数据均有差异,参考记忆错误次数、工作记忆错误次数均显著增多(P<0.01),吃完食物总时间模型组及西药组显著增多(P<0.01)、穴注组增多(P<0.05)。穴注组及西药组之间差异无统计学意义(P>0.05)。见表3。
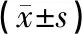
表3 各组大鼠八臂迷宫试验比较
2.4 各组COX-2 mRNA在大鼠海马组织表达比较
各组大鼠海马组织COX-2 mRNA表达水平以β-actin作内参。与空白组相比,模型组大鼠COX-2 mRNA表达水平显著升高(P<0.01),穴注组、西药组大鼠COX-2 mRNA表达水平升高(P<0.05);与模型组对比,穴注组、西药组干预后均降低COX-2 mRNA的表达水平(P<0.05);穴注组与西药组对比,大鼠海马胞浆内COX-2 mRNA表达差异无统计学意义(P>0.05)。见表4、图2。
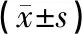
表4 各组大鼠海马组织COX-2 mRNA表达

图2 各组大鼠海马组织COX-2 mRNA表达
3 讨论
癫痫是在神经功能紊乱疾病中所占比例最高的慢性临床综合征[6],其中部分癫痫患者会伴随有不同程度的认知功能障碍以及学习记忆功能障碍,在学习记忆能力中又以视觉空间记忆能力以及长、短时记忆能力损伤最为严重[7]。研究发现在癫痫治疗方面,中药单体及复方制剂发挥着非常重要的作用[7]。天麻为兰科植物,具有熄风定惊功效。《日华子本草》云:“助阳气,补五劳七伤,通血脉,开窍。”《本经》记载:“主恶气,久服益气力,长阴肥健。”现代研究表明天麻超微粉对血管性痴呆模型大鼠学习记忆功能的降低有改善作用,可能与调节胆碱能系统促进神经递质乙酰胆碱的释放有关[8]。另有研究发现天麻对创伤性脑损伤所致血脑屏障渗漏及脑水肿均有减轻,可能通过减少神经元丢失、胶质细胞活化使神经干细胞增殖,进而改善损伤后导致的认知及运动功能障碍[9]。王氏等总结多项研究证实天麻单药具有缓解认知障碍、神经保护作用、抗阿尔兹海默病、抗氧化、抗惊厥、抗癫痫及脑保护作用[10]。穴位注射疗法是在传统毫针针刺基础上发展而来,较以往传统针刺疗法,穴注可将提纯药物采用针刺输注手段直接作用于穴位,临床上取得更为理想疗效。临床上本研究团队已应用天麻单药及复方制剂治疗癫痫及癫痫后伴认知障碍患者多年,且通过实验研究发现天麻素穴注可有效抑制痫性发作,并调控抗凋亡因子Bcl-2及凋亡因子Caspase-3的表达,进而发挥对海马神经元的保护作用[11]。
本研究水迷宫试验显示模型组大鼠潜伏期较空白组数据明显延长、穿越平台数减少,八臂迷宫试验示模型组大鼠较空白组大鼠数据参考记忆错误次数和工作记忆错误次数均显著增多、吃完食物总时间显著延长,证明造模后癫痫大鼠已经出现学习记忆能力、工作记忆、参考记忆能力下降,存在认知功能障碍的表现。穴注组和西药组与模型组实验大鼠数据进行比较,潜伏期明显缩短、穿越平台次数增加、参考记忆错误次数、工作记忆错误次数均减少、吃完食物总时间缩短,表明穴注和西药均可对癫痫大鼠认知、记忆力有一定的改善作用。目前,在AEDs治疗基础上,添加中药辅助治疗癫痫已经成为了一种研究和应用的趋势,本研究结果穴注组及西药组两组学习记忆能力数据差异无统计学意义,但穴注组数据优于西药组,提示在后续研究中关注中药不同剂量、干预治疗时长对癫痫大鼠认知功能障碍的治疗差异。
COX-2作为前列腺素E2代谢产生过程的关键酶和限速酶,前列腺素E2参与炎症、凋亡等多种病理过程,COX-2主要在中枢神经系统中表达,参与介导神经元损伤[12-13]。在癫痫发作、炎症反应发生及脑外伤刺激后,COX-2能够通过合成 PGE2进而调节细胞膜兴奋性、增强细胞膜通透性及异常兴奋性信号传导而诱发细胞的损伤[14]。研究显示应用COX-2抑制剂能明显抑制癫痫大鼠的痫性发作的发作频率及发作持续时间,并且减轻脑组织损伤[15]。本研究发现戊四氮致痫大鼠海马组织COX-2mRNA表达明显增强,由此推测,COX-2的异常表达可能参与了癫痫发病中的氧化应激损伤以及海马神经元死亡或凋亡过程,天麻素可能通过调节COX-2的异常表达,进而具有抗氧化损伤、抗凋亡的脑保护作用。
综上所述,本研究证实天麻素穴注延长戊四氮致痫大鼠GTCS潜伏期和MCS潜伏期、改善认知功能,其机制可能是通过调节 COX-2的异常表达发挥其改善大鼠认知障碍及神经保护功能,该研究结果为临床癫痫疾病的治疗及改善癫痫后认知障碍均提供了新的治疗思路。
