婴儿躯干部弥漫型先天性动静脉瘘并发新生儿持续肺动脉高压1例病例报告
2020-08-04沈晓霞马晓路
朱 枫 沈晓霞 马晓路
1 病例资料
男,因“孕检时发现胎儿背部肿块2月余”于出生1.5 h入浙江大学医学院附属儿童医院(我院)NICU。患儿系G1P1,孕39+2周因“羊水少”剖宫产娩出,羊水清,1和5 min Apgar评分均为10分。母亲孕7月时胎儿B超发现胎儿右腰背部皮下组织增厚,范围约4.3 cm×2.2 cm×0.9 cm,边界清晰,彩色多普勒血流显像可见条状血流信号进入,进一步行胎儿MRI检查示右侧腰背部皮下组织增厚,肌肉来源病变可能。生后无气促、发热、呻吟,右侧腰背部可见1个包块,右腿较左腿粗,遂转至我院急诊。
入院时体格检查:体温35.4 ℃,脉搏150·min-1,呼吸50·min-1,血压74/30 mmHg,鼻导管吸氧下SpO293%,反应可,哭声稍嘶哑,前囟平,无口吐泡沫,呼吸平稳,未闻及啰音,未见三凹征,心律齐,心音强,未闻及病理性杂音,腹软,肝脾肋下未及。右背部触及8 cm×5 cm肿块,质韧,右下肢(大腿围18 cm)较左下肢(大腿围14.5 cm)粗,右侧大腿皮温较左侧稍高。四肢肌张力未见异常,关节活动自如,生理反射可引出,四肢肢端稍凉,全身未见花斑。
家族史:父亲30岁,母亲31岁,均身体健康,孕期无特殊用药史,未述特殊家族史。
实验室和辅助检查:血气分析pH 7.3,PCO243 mmHg,PO257.4 mmHg,K+3.7 mmol·L-1,Lac 2.7 mmol·L-1,HCO3-21.8 mmol·L-1,ABE -3.8 mmol·L-1。颈胸部CT平扫加重建:右侧肩背部和腰部软组织肿块,密度尚均匀,软组织影似进入右侧胸腔,右侧胸膜明显增厚,临近骨质未见异常,两肺多发模糊片影,心影大,双膈正常,胸腔未见积液。腰骶椎增强CT:右侧背部竖脊肌区域软组织肿块,向腹腔及椎管内延伸,血管瘤可能,右侧腹壁及右侧臀部肌层较对侧增厚,右侧髂总动静脉、髂内外动静脉增粗,所见右侧大腿血管较左侧增粗,肝脏增大,强化不均匀,门静脉周围渗出,胆囊窝积液,右侧肾脏略增大,且向右前方移位,考虑肿块受压后改变可能,腹腔积液(图1)。腰背部肿块B超:背部肌层内低回声包块,累及椎管,考虑为脉管畸形,右下肢回声及血供改变,血管畸形可能。心脏B超:右心增大,重度肺动脉高压,动脉导管未闭(0.38 cm,右向左分流),卵圆孔未闭(0.30 cm,右向左分流),三尖瓣轻至中度返流,二尖瓣轻度返流。头颅CT和肝、胆、胰、脾、肾B超未见异常。血TORCH、甲状腺功能、肿瘤标志物水平未见异常。新生儿遗传代谢筛查未提示异常。

图1 腰骶椎增强CT
诊疗经过:入科后予气管插管机械通气,氢氯噻嗪及螺内酯利尿、米力农、西地那非降低肺动脉压力,并予心得安、甲泼尼龙治疗,入院第20 d行经皮右侧腰背部动静脉畸形(AVM)造影及血管栓塞术,造影显示患儿右侧明显增粗增生,右侧腰动脉由上向下依次逐渐增大,其中以右侧腰4、腰5动脉明显增粗(腰5动脉最粗),造影剂迅速回流,呈AVM表现(图2)。诊断:躯干部弥漫型的先天性动静脉瘘(CAVF),重度肺动脉高压,心功能衰竭。确认畸形血管后,经5F导管内微导管分次至腰5动脉放置3枚弹簧栓(1枚5 mm,2枚3 mm)、腰4动脉放置1枚弹簧栓(3 mm)、左侧增粗腰静脉主干放置1枚可调控弹簧栓,共栓塞3支血管(图2),术后造影显示畸形血管影明显缩小,但术后2 d复查心超,提示肺动脉高压79 mmHg,患儿肺动脉高压未见好转,加用曲前列尼尔、NO吸入,西罗莫司治疗,术后1周家属放弃治疗,患儿死亡。
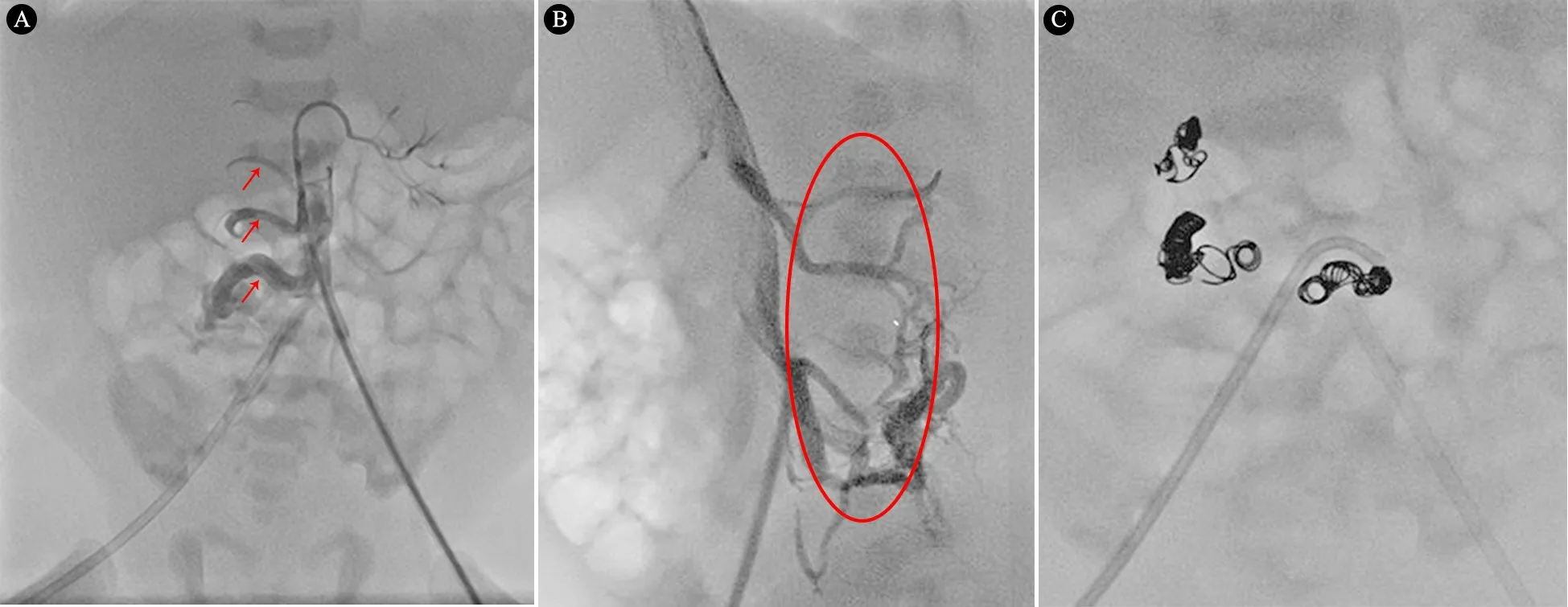
图2 经皮右侧腰背部AVM造影及血管拴塞术
2 讨论
CAVF是复杂性高流量型AVM,而非真性肿瘤[1],是由动静脉血管相通形成的异常血管团,无包膜和边界[2],血管壁增厚,管腔扩大,血管内皮细胞无增生。CAVF分局限和弥漫2种类型,可以出现在身体任何部位,以肢体常见,躯干部较罕见,国内外目前均暂无躯干部弥漫型CAVF相关报道。
弥漫型CAVF常累及整条肢体,临床表现为肢体粗长、局部皮温高、闻及杂音、浅静脉充盈或曲张、瘘支大者可扪及震颤、血管瘤等症状。局限型CAVF常表现为局部出现肿胀或伴表浅静脉曲张和海绵状血管瘤样变化、可触及震颤或搏动感、局部皮温高。儿童 CAVF有其特殊性,分流大者影响心脏功能。本文患儿临床表现为右背部包块,右下肢较左下肢粗,右侧大腿皮温较左侧稍高,生后早期即出现呼吸困难需要气管插管。患儿躯干部弥漫型CAVF大量动静脉分流导致肺循环血流增多,产生肺动脉高压,加重瘘管扩张,引起更多的动静脉分流[3]。新生儿持续性肺动脉高压(PPHN)重要的病理生理机制是肺血管循环血流增多[4]。引起PPHN的原因有很多,包括先天性肺血管发育不全、先天性心脏病、胎粪吸入综合征等,动静脉瘘是引起PPHN的罕见原因[5]。肺血流的增加也使生理性肺血管阻力下降延迟,这可能是造成PPHN的另一个原因[6]。若新生儿期出现难以解释的PPHN,且伴有高心排出量,需行相关检查是否存在CAVF或其他AVM。PPHN的治疗包括对基础疾病的支持疗法和针对PPHN的特异性治疗,治疗原则为降低肺动脉压力和提高体循环压力,逆转右向左分流。
影像检查是诊断CAVF的关键,彩色多普勒血流显像作为初检手段,可显示动静脉分流现象,还可检出较大的瘘支。动脉造影能明确病变的部位、范围和主要瘘支[7],是诊断本病的重要手段。对于局限型病变,MRA检查有很好效果。
本文患儿因CAVF引起重度肺动脉高压,予药物治疗病情无好转,只有减少异常血管的分流,才有机会解决肺动脉高压。CAVF的治疗是外科难题,经导管动脉介入栓塞术、经皮穿刺瘤腔内药物硬化治疗,和手术治疗是目前主要的治疗方法。但不论是手术还是栓塞治疗, 都难以达到根治性目的[8]。本文患儿通过血管造影,充分地观察和显示血管病变的范围,提示右侧腰动脉与左侧腰静脉相通,形成异常血管网,应用微弹簧圈是最佳选择,因为微弹簧圈具有安全、永久、容易投放等优点[9]。遂予微弹簧圈阻塞血管,以阻断异常血管的血供,达到减少异常血管血流目的。但由于患儿形成的动静脉瘘是由腰动静脉形成的异常血管团,如果完全栓塞腰动静脉血管,可能会导致截瘫等不良后果,故只阻塞了部分异常血管,虽术后血流减少,但仍有侧枝血管相通,导致患儿肺动脉高压未改善,病情未见缓解。
本文患儿血管畸形在胎儿期就已发现,由于宫内环境复杂,有羊水和子宫等干扰因素以及麻醉药的使用限制等,手术治疗很难进行,胎儿期手术对孕妇及胎儿都是高风险,目前还没有宫内手术治疗CAVF的方法。回顾文献,仅有2例经产前诊断及产前治疗的肝脏AVM存在,1例为氢化可的松应用于妊娠29周心脏衰竭的肝脏AVM胎儿,在随访中,胎儿的心衰症状有所改善,产后婴儿无心力衰竭的迹象,没有给予治疗,婴儿生后18 d再次出现心脏衰竭和肝血管流量明显增加的迹象,使用类固醇治疗,症状得到明显改善[10]。另1例为在胎儿期对类固醇和普萘洛尔治疗有反应并达到足月的肝脏AVM病例,普萘洛尔在产后继续治疗,观察到肝脏AVM在使用后3个月和4个月时有所改善[11]。CAVF属于高流量型AVM,其产前诊断对患儿疾病的治疗及预后非常重要,产前诊断明确的病例可用普萘洛尔和类固醇药物治疗。回顾文献发现在肝血管瘤[12]中,普萘洛尔和类固醇在出生后经常联合应用,关于类固醇治疗AVM疗效的研究仍存在争议,但普萘洛尔近年来的研究表明它对AVM[13]的治疗是有效的。然而,目前只有2例产前肝脏AVM用普萘洛尔和类固醇治疗的病例。如躯干部弥漫型CAVF在产前诊断明确立即予药物治疗可能会改善患儿的治疗效果。
