川牛膝不同产地药材质量综合评价研究
2020-06-17李隆云宋旭红付绍智
丁 刚,李隆云*,宋旭红,付绍智
1重庆市中药研究院;2重庆市中药良种选育与评价工程技术研究中心;3重庆市中药资源学重点实验室;4中国中医科学院中药资源中心重庆分中心,重庆 400065;5重庆三峡医药高等专科学校,重庆 404120
川牛膝又名白牛膝、甜牛膝,始载于明初兰茂的《滇南本草》。川牛膝来源于苋科植物川牛膝(CyathulaofficinalisKuan)的干燥根,为著名的川产道地药材之一,是一种重要的大宗中药材。《中国药典》(2015版,一部)有收载,其性甘,微苦,平,归肝、肾经,具有逐瘀通经、通利关节、利尿通淋等功效,在我国有较长的民间药用和临床应用历史。川牛膝的产地主要是四川、重庆、湖北和湖南,由于各地气候、地形、土壤条件等不同,所产川牛膝质量也不均一。Ma等[1]测定不同产地川牛膝中杯苋甾酮的含量有显著性差异,道地川牛膝中杯苋甾酮含量并不是最高。Zhang等[2]检测不同产地川牛膝中齐墩果酸含量差异较大,牛膝栽培品的含量均高于野生品。Geng等[3]分离测定川牛膝中阿魏酸,Liu等[4]分离纯化鉴定川牛膝的多糖。分别从不同角度研究川牛膝内在质量,为了综合开发川牛膝产品及保障用药安全,有必要对各产地川牛膝药材的质量进行全面的评价。本实验建立了同时测定川牛膝杯苋甾酮、前杯苋甾酮和齐墩果酸,3种成分的HPLC方法,对不同产地川牛膝3种成分、总灰分、水冷浸物和乙醇冷浸物进行测定,并通过系统聚类分析法、主成分分析法进行评价,通过以上研究,更加全面地评价各地川牛膝的质量,为川牛膝药材的临床使用和产品开发提供依据。
1 仪器与试药
仪器:Agilent 1260高效液相色谱仪(Agilent公司,美国;DAD检测器),UV 2600紫外分光光度计(岛津公司,日本),Milli(Q Integral 5型纯水仪(Millipoer公司,美国),BSA 124(S型电子天平(Sartorius,德国),KQ(250 DB型数控超声波清洗仪(昆山市超声仪器有限公司,中国),8(10型马弗炉(沈阳节能电炉厂,中国),XMTB数显式电热恒温水浴锅(上海跃进医疗器械有限公司,中国),G2X(9240 MBE电热鼓风干燥箱(上海博讯实业有限公司医疗设备厂,中国)。
对照品:杯苋甾酮对照品(批号:MUST-16070511,纯度:≥99%)、前杯苋甾酮对照品(批号:MUST-16072203,纯度:≥98%)购自成都曼斯特生物科技有限公司;齐墩果酸对照品(批号:TAQT-LRLA,纯度:≥93.1%)购自中国食品药品检定研究院。
试剂:甲醇(TEDIA公司,美国;色谱纯)、醋酸(TEDIA公司,美国;色谱纯),其它试剂均为分析纯。
样品产地:在全国范围内共收集样品54批,详细信息见表1。样品经重庆市中药研究院李隆云研究员鉴定为苋科植物川牛膝(CyathulaofficinalisKuan)的干燥根。

表1 川牛膝样品来源Table 1 Origin of C.officinalis Kuan
续表1(Continued Tab.1)

地区Region编号No.地点Habitat海拔Altitude(m)地区Region编号No.地点Habitat海拔Altitude(m)c-24奉节县奉节县长安乡石缙村11 740h-8湖南小沙江镇杉木坪村1 685c-25奉节县长安乡石缙村14社1 760h-9湖南小沙江镇肖家院子1 623c-26奉节县长安乡石缙村21 820贵州省zz-1贵州大方县兴隆乡狮子村5组1 925c-27奉节县长安乡石缙村17社1 830c-28巫溪县天元乡新月村1 740
2 实验方法
2.1 水分、总灰分、水冷浸物、乙醇冷浸物的检测
水分、灰分、浸出物,样品处理及检测方法按照《中华人民共和国药典》[5]中相关方法进行检测。
2.2 含量测定
2.2.1 色谱分析条件
色谱柱:XTERRA®MS-C18(150 mm × 4.6 mm,3.5 μm)。流动相:0.2%醋酸水溶液(A)-甲醇(B),梯度洗脱,0~5 min,95% A;5~10 min,95%→65% A;10~35 min,65%→55% A;35~50 min,55%→5% A;50~51 min,5%→95% A;51~60 min,95%A;流速1 mL/min,进样量10 μL,柱温为35 ℃,检测波长:杯苋甾酮、前杯苋甾酮243 nm,齐墩果酸215 nm。色谱图见图1。

图1 对照品(A,B)和川牛膝供试品(C,D)的HPLC图Fig.1 HPLC chromatograms of reference substance (A,B) and C.officinalis sample (C,D)注:1.齐墩果酸;2.杯苋甾酮;3.前杯苋甾酮。Note:1.Oleanolic acid;2.Cyasterone;3.Precyasteron.
2.2.2 混合对照品溶液的制备
精密称取对照品齐墩果酸3.21 mg、杯苋甾酮2.11 mg、前杯苋甾酮1.03 mg置10 mL容量瓶中,加甲醇溶解并稀释至刻度,摇匀;精密移取上述溶液,甲醇稀释,得齐墩果酸浓度为321 μg/mL、杯苋甾酮浓度为211 μg/mL、前杯苋甾酮浓度为103 μg/mL的对照品溶液母液。
2.2.3 供试品溶液的制备
精密称取干燥川牛膝样品粉末(过30目筛)0.5 g,置具塞锥形瓶中,加甲醇25 mL,称定质量。于25 ℃超声处理(功率400 W,频率40 kHz)60 min,冷却,用甲醇补足失重,摇匀,0.45 μm微孔滤膜滤过,取滤液即得。
2.2.4 方法学考察
2.2.4.1 线性关系考察
将梯度浓度的混合对照品溶液按“2.2.1”项下色谱条件进样检测。以各对照品峰面积(Y)为纵坐标,浓度(X,μg/mL)为横坐标,做标准曲线,齐墩果酸的线性方程为Y=2.968X-0.255,r=0.999 1;杯苋甾酮的线性方程为Y=14.04X-2.516,r=0.999 9;前杯苋甾酮的线性方程为Y=11.721X+2.256,r=0.999 4。结果表明,齐墩果酸在0.49~19.6 μg/mL、杯苋甾酮在1.45~72.5 μg/mL、前杯苋甾酮在1.24~12.38 μg/mL范围内线性关系良好。
2.2.4.2 精密度试验
取同一混合对照品溶液按“2.2.1”项下色谱条件连续进样6次,记录各成分的峰面积。结果齐墩果酸、杯苋甾酮、前杯苋甾酮面积RSD分别为2.81%、1.28%、2.07%,表明仪器精密度良好。
2.2.4.3 重复性试验
取同一来源川牛膝样品,按“2.2.3”项下方法平行制备6份供试品溶液,分别进样,记录各成分的峰面积。结果齐墩果酸、杯苋甾酮、前杯苋甾酮面积RSD分别为2.87%、1.40%、2.24%,表明本方法重现性良好。
2.2.4.4 稳定性试验
取同一供试品溶液,按“2.2.1”项下色谱条件分别在0、2、4、8、12、24 h进样,记录各成分的峰面积。结果齐墩果酸、杯苋甾酮、前杯苋甾酮峰面积RSD分别为2.11%、1.34%、1.99%,表明供试品溶液于24 h内测定结果稳定。
2.2.4.5 回收率试验
精密称取已知含量的同一来源川牛膝样品6份,每份0.25 g,分别精密添加与样品中含量相当的齐墩果酸、杯苋甾酮、前杯苋甾酮对照品,按“2.2.3”项下方法制备供试品溶液,按“2.2.1”项下色谱条件进样检测,计算得到齐墩果酸的平均加样回收率为103.31%,RSD为2.73%;杯苋甾酮的平均加样回收率为100.77%,RSD为1.75%;前杯苋甾酮的平均加样回收率为102.63%,RSD为2.75%。结果表明本方法的回收率良好。
3 结果与分析
3.1 水分、总灰分、浸出物及乙醇冷浸物的检测
川牛膝样品中水分、总灰分、浸出物及乙醇冷浸物的检测结果见表2。结果显示54批川牛膝样品的水分含量在4.08%~8.95%之间,均低于16.00%,符合药典规定;总灰分含量在2.41%~5.40%之间,均低于8.00%,符合药典规定;浸出物水冷浸含量在66.13%~81.82%之间,均大于65.00%,符合药典规定;浸出物乙醇冷浸含量在7.91%~23.94%之间,药典没有控制。
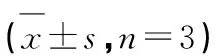
表2 川牛膝中水分、灰分、水浸出物和乙醇冷浸物测定结果Table 2 The determination of moisture,ash,water extract,95% ethanol extract in C.officinalis
续表2(Continued Tab.2)

编号No.水分Moisture(%)总灰分Total ash(%)水冷浸Water extract(%)乙醇冷浸物95% ethnaol extract(%)c-156.38±0.154.67±0.4278.83±1.4718.60±0.03c-168.40±0.384.58±0.2380.10±2.6616.53±1.20c-176.76±1.293.45±0.4674.12±1.1715.74±0.47c-186.86±1.372.41±0.2679.55±1.5621.18±1.34c-195.59±0.283.95±0.5181.17±0.4522.95±0.08c-208.05±0.544.39±0.3268.7±2.8811.41±0.56c-218.06±0.344.73±0.0376.88±2.3918.46±0.03c-226.19±0.854.77±0.5275.00±1.0219.23±1.48c-237.45±0.304.67±0.5080.76±1.4823.94±0.30c-247.77±1.434.67±0.0471.38±1.0815.55±0.37c-255.61±1.444.86±0.0779.50±1.2422.61±0.18c-265.88±0.214.58±0.6977.27±0.5016.91±0.83c-277.06±1.125.40±0.8274.32±1.0716.36±0.17c-287.47±1.254.13±0.2678.32±1.6620.14±0.25s-16.27±0.793.59±0.0678.79±1.5322.92±1.47s-25.79±0.435.06±0.0774.83±2.5617.17±0.30s-36.51±0.074.78±1.0077.84±1.7118.51±0.10s-46.74±1.124.54±0.8267.52±2.887.19±1.10s-58.25±0.724.78±0.0577.63±1.1115.91±1.31s-67.21±1.424.39±0.2877.92±1.9316.37±0.20s-77.03±0.044.87±0.1473.44±1.7116.09±0.83s-85.57±0.114.87±0.4568.72±1.8810.65±0.40s-96.65±0.513.58±0.2474.58±2.1117.82±0.46s-106.28±0.385.11±0.5077.27±2.9315.05±0.11s-117.44±1.294.52±0.0476.02±0.9115.38±0.02s-128.12±0.924.87±0.5481.82±1.0621.35±0.21s-137.14±1.394.87±0.9570.00±2.5710.16±1.66s-148.75±0.423.58±0.8276.18±1.1015.38±2.87s-158.32±0.594.79±0.0578.39±0.2819.21±0.05s-167.19±1.595.09±0.2169.16±1.6515.41±0.19h-17.22±0.813.80±0.1970.00±1.2713.14±0.52h-25.75±0.784.92±0.3579.18±0.4519.71±0.48h-37.07±1.194.82±0.4467.39±0.2312.03±0.78h-45.88±0.824.78±0.3569.16±1.0414.18±0.64h-57.06±1.194.39±0.2481.12±1.1121.75±0.74h-67.03±0.924.41±0.2472.55±0.2318.97±0.72h-77.17±0.794.87±0.7975.35±0.3316.03±0.66h-88.06±1.193.58±0.7276.66±0.4018.80±0.53h-96.19±1.224.79±0.6578.83±0.4115.97±0.56zz-16.95±0.445.16±0.2179.49±0.1119.22±1.01药典规定Pharmacopeial regulations≤16.0≤8.00≥65.0未控制Uncontrolled
3.2 含量测定
按“2.2.3”项下方法每个样品平行制备3份供试品溶液,按“2.2.1”项下色谱条件进样检测,记录色谱图。根据线性方程分别齐墩果酸、杯苋甾酮与前杯苋甾酮的百分含量,结果见表3。

表3 川牛膝中3种成分含量测定结果Table 3 Determination results of 3 components in C.officinalis
续表3(Continued Tab.3)

编号No.齐墩果酸Oleanolic acid(%)前杯苋甾酮Precyasterone(%)杯苋甾酮Cyasterone(%)PCA得分排序PCA score sorts-80.01±0.0030.017±0.0080.198±0.11351s-90.021±0.0180.011±0.0050.312±0.02713s-100.027±0.0010.011±0.0030.184±0.03115s-110.029±0.0110.023±0.0040.172±0.01028s-120.005±0.0100.027±0.0010.223±0.0438s-130.014±0.0000.027±0.0020.241±0.01845s-140.011±0.0200.015±0.0030.170±0.04541s-150.013±0.0080.014±0.0020.164±0.01720s-160.035±0.0030.022±0.0020.181±0.00533h-10.010±0.0010.010±0.0120.243±0.04146h-20.046±0.0010.012±0.0030.287±0.0232h-30.021±0.0150.015±0.0120.243±0.02139h-40.011±0.0130.014±0.0040.232±0.00738h-50.034±0.0010.025±0.0010.242±0.0083h-60.026±0.0010.023±0.0060.221±0.03121h-70.014±0.0020.009±0.0050.238±0.01318h-80.034±0.0020.019±0.0030.242±0.02711h-90.026±0.0020.019±0.0070.223±0.0239zz-10.070±0.0020.003±0.0010.581±0.0281药典规定Pharmacopeial regulations未控制Uncontrolled未控制Uncontrolled≥0.030%
由结果可知,川牛膝样品中杯苋甾酮含量在0.10%~0.58%之间,均符合药典要求。
3.3 化学模式识别
3.3.1 聚类分析
总灰分、水冷浸物、乙醇冷浸物及单个有效成分含量是评价川牛膝质量的重要指标。本研究以总灰分、水冷浸物、乙醇冷浸物、齐墩果酸、杯苋甾酮和前杯苋甾酮含量数据为变量,运用SPSS 20.0软件,以平方欧氏距离作为度量标准,对54批样品进行系统聚类分析,结果见图2,54批样品共被分为2大类。
3.3.2 主成分分析
运用SPSS 20.0软件,以川牛膝中齐墩果酸、杯苋甾酮、前杯苋甾酮、总灰分、水冷物、乙醇冷浸物的含量作为变量,以特征值和累计贡献率作为判定依据,对不同产地川牛膝进行主成分分析。根据降维结果,共挑选出3个主成分PC1、PC2、PC3,特征值分别为1.951、1.497、1.250。各成分方差贡献值分别为32.511%、24.955%、20.840%,累积贡献值达到78.306%,具有较强的代表性,可用来评价川牛膝的质量。

表4 因子载荷矩阵Table 4 Initial factor load matrix

图2 川牛膝样品聚类分析Fig.2 Cluster analysis of C.officinalis
根据各因子载荷矩阵及特征值计算得分系数,进一步得到PC1、PC2、PC3及综合得分(Y)方程式:
PC1 =-0.025ZX1+0.075 ZX2+0.272 ZX3-0.065 ZX4+0.672 ZX5+0.681 ZX6
PC2 = 0.323 ZX1-0.649 ZX2+0.675 ZX3+0.058 ZX4-0.091 ZX5-0.090 ZX6
PC3 = 0.595 ZX1+0.392 ZX2+0.036 ZX3+0.692 ZX4+0.090 ZX5-0.059 ZX6
Y= 0.415 PC1+0.319 PC2+0.266 PC3
式中:ZX1、ZX2、ZX3、ZX4、ZX5、ZX6分别为齐墩果酸、前杯苋甾酮、杯苋甾酮、总灰分、水冷浸物、乙醇冷浸物的标准化值。
利用上式计算各地川牛膝质量综合得分并按结果高低进行排序(表3),得分越高,表明川牛膝质量越好,排名越靠前。同一地域样品排名有前有后,川牛膝质量与地域没有明显关系。此外,由表4及图4可知,PC1主要反映了水冷浸物和乙醇冷浸物的信息,PC2主要反映了杯苋甾酮的信息;PC3主要反映了总灰分和齐墩果断的信息。

图3 主成分得分图Fig.3 Scores plot from principal component analysis

图4 主成分因子分析图Fig.4 Loadings plots from principal component analysis
4 讨论
本研究建立了可同时检测齐墩果酸、杯苋甾酮、前杯苋甾酮,3种成分的HPLC方法,方法学验证均符合药典中相关规定,表明该方法准确、可行。
本研究对全国各主要产地川牛膝的质量指标进行了较全面地考察。运用主成分分析方法和聚类分析法,分析总灰分、水冷浸物、乙醇冷浸物和齐墩果酸、杯苋甾酮、前杯苋甾酮含量指标数据,通过一系列算法重新组成新的互不相关的几个综合指标代替原来数据指标[6]。结果可将54批川牛膝样品分为2大类,提炼出3个主成分。2大类主要体现是浸出物与有效成分含量指标。3个主成分,第一主成分反应浸出物,体现多糖[7]对川牛膝质量的影响;第二主成分反应杯苋甾酮[8],体现有效成分对川牛膝质量的影响;第三主成分反应总灰分,体现盐类、金属氧化物含量等对川牛膝质量的影响。
重庆奉节县长安乡西曹村两个川牛膝伪品(麻牛膝),杯苋甾酮含量分别为0.086%和0.077%,与正品川牛膝杯苋甾酮含量均值0.207%有显著差异。经过田间海拔实验,川牛膝在海拔1 400 m以下,发现杯苋甾酮含量明显降低。
川牛膝质量与地域没有明显关系,因为川牛膝种植区域集中在西南高海拔山区,生长气候条件类似。药农种植技术、田间管理水平、初加工技术是导致质量差异的主因,同一个加工点,不同批次,川牛膝质量也存在差异。下一步将开展种植技术、初加工技术对川牛膝质量影响的研究。
