BiVO4/CeO2复合光催化材料的制备及其降解甲基橙废水的研究
2020-06-08王泽华杜力勤于震源梁亦欣郑宾国
王泽华 杜力勤 于震源 孙 鹏 梁亦欣 郑宾国
(1.郑州航空工业管理学院 郑州市环境功能材料重点实验室,河南 郑州 450015;2.郑州大学环境技术咨询工程有限公司,河南 郑州 450015)
随着经济的飞速发展,工业废水污染问题日益凸显。尤其是印染行业,因其产出的废水具有色度高[1](含有发色基团)、成分复杂(含有酚类、芳烃等有机物)、水质变化大[2]、可生化性差等特征[3],已成为工业废水处理中的一大“毒瘤”。目前,国内外处理印染废水以生物法为主[4],但其对印染废水中色度的去除不够理想。而光、电催化氧化技术,在难降解有机工业废水处理方面发展快速,并成为高级氧化技术领域的重点研究对象。
氧化铈 (CeO2)是一种重要的稀土氧化物功能材料,具有良好的储存和释放氧的功能[5-7]。钒酸铋是单斜白钨矿晶相,能够很好地吸收太阳光的可见光部分,在可见光范围内具有良好的光电化学活性[8]。但BiVO4的光生电子和空穴对易复合,导致BiVO4的实际光电量子产率并不高[9]。因此,可考虑把BiVO4与CeO2复合,减少光生电子和空穴对复合的几率,进而提高BiVO4的光催化性能。
本文通过把BiVO4与CeO2复合,研究其光催化降解甲基橙废水的效果,期望通过基础研究,能够在技术方面找到突破点,为当前光催化降解有机废水提供一种新思路,并在工业中得到广泛应用。
1 实验部分
1.1 实验材料
1.1.1实验仪器
双光束紫外可见分光光度计(T9CS)、X射线衍射仪(Smart Lab),扫描电子显微镜(FEI Quanta 200 FEG)、分析天平(FA2104N)、精密数显酸度计(PHS-3C)。
1.1.2实验试剂
尿素、无水乙醇、盐酸、偏钒酸铵、六水合硝酸铈、五水合硝酸铋、氢氧化钠、甲基橙、成套缓冲剂,试剂均为分析纯。
1.2 材料制备
1.2.1CeO2材料的制备
采用水热法制备CeO2。分别取配制好的0.2 mol/L的尿素溶液150 mL和0.1 mol/L的硝酸铈溶液250 mL于500 mL的烧杯中,磁力搅拌30 min。将反应后的混合物均分于100 mL聚四氟乙烯反应釜中,150 ℃恒温24 h,自然冷却至室温;过滤,然后将固体放在80 ℃恒温干燥箱里干燥12 h,得到淡黄色固体。将所得的固体在600 ℃马弗炉中煅烧4 h,得到淡黄色粉末CeO2。
1.2.2BiVO4/CeO2复合材料的制备
以偏钒酸铵、硝酸铋和CeO2为材料,用水热合成法制备BiVO4/CeO2复合材料。将0.3 mol/L的偏钒酸铵溶液和0.5 mol/L的硝酸铋溶液于100 mL烧杯中混合均匀,并调节pH为7。然后逐滴加入20 mL 0.15 mol/L的二氧化铈混合分散液,并磁力搅拌30 min;在180 ℃条件下水热12 h,并自然冷却至室温;抽滤,固体放入到真空干燥箱中,在60 ℃下干燥6 h,所得即为BiVO4/CeO2复合材料。
2 结果与讨论
2.1 BiVO4/CeO2复合材料的表征
2.1.1SEM分析
样品的SEM表征结果如图1~3所示。由图1可知,CeO2样品为梭状,分布均匀,易于负载其他物质;由图2可知,BiVO4为类葡萄状,且相互之间衔接紧凑,分散度不高;由图3可知,BiVO4/CeO2复合材料中BiVO4大都均匀的分散在CeO2的表面,但部分区域BiVO4分布过于密集,有团聚现象,这可能会对降解甲基橙产生不利影响。

图1 CeO2材料的SEM图Fig. 1 SEM image of CeO2 material

图2 BiVO4材料的SEM图Fig. 2 SEM image of BiVO4 material

图3 BiVO4/CeO2复合材料的SEM图Fig. 3 SEM image of BiVO4/CeO2 composite
2.1.2XRD分析
各材料的X射线衍射分析结果如图4所示。由图4可知,CeO2的特征衍射峰和立方氧化铈的特征峰的匹配度较高,表明所制备的CeO2属于立方晶系,且XRD图中未出现其他杂峰,其衍射峰较尖锐,说明该样品纯度较高、结构较好;BiVO4样品特征衍射峰的强度很高且峰型也很好,说明制得的BiVO4样品具有很好的结晶度;BiVO4/CeO2复合材料的衍射峰与单一CeO2和BiVO4的峰几乎吻合,且衍射峰较尖锐,半峰宽较窄,说明其复合的效果很好。

图4 CeO2、BiVO4和BiVO4/CeO2的XRD图谱Fig. 4 XRD image of CeO2 、BiVO4 and BiVO4/CeO2
2.2 BiVO4/CeO2降解甲基橙条件的优化
2.2.1pH对甲基橙降解效果的影响
分别取6瓶等体积,浓度为30 mg/L的甲基橙溶液,调节pH为1、2、3、4、5、6,然后测其吸光度;之后分别加入10 mg的BiVO4/CeO2复合材料,把锥形瓶放在恒温摇床里,在黑暗下处理1 h,再在紫外光下光照2.5 h,静置10 min左右,再测其吸光度,计算甲基橙的降解率,结果如图5所示。
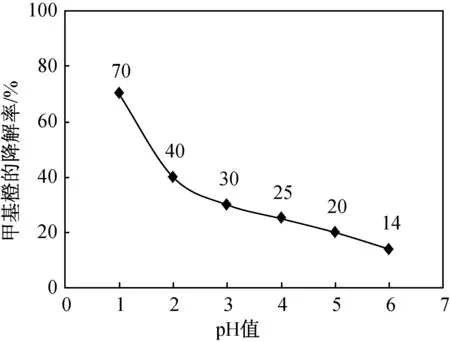
图5 甲基橙的降解率与pH的关系Fig. 5 Relationship between the degradation rate of methyl orange and pH
由图5可知,pH为1时,BiVO4/CeO2复合材料对甲基橙溶液的降解率最大,为70%。在酸性氛围中,甲基橙的降解率较高,随着pH的增大,甲基橙的降解率逐渐减小。由此可知,本实验条件下,BiVO4/CeO2复合材料对甲基橙降解的最佳pH为1。
2.2.2甲基橙初始浓度对其降解效果的影响
分别配制浓度为10 mg/L、15 mg/L、20 mg/L、25 mg/L、30 mg/L、35 mg/L的甲基橙溶液,调节pH为1,BiVO4/CeO2的投加量为10 mg,在黑暗处1 h,再紫外光照2.5 h,结果如图6所示。

图6 甲基橙降解率与其初始浓度的关系Fig. 6 Relationship between the degradation rate of methyl orange and its initial concentration
由图6可知,当甲基橙溶液的初始浓度为15 mg/L时,BiVO4/CeO2复合材料对甲基橙的降解效果最好,为80%。BiVO4/CeO2复合材料对甲基橙的降解,随着初始甲基橙浓度的增大呈先增大随后逐渐减小的趋势。
2.2.3BiVO4/CeO2投药量对降解效果的影响
设置甲基橙的初始浓度为15 mg/L, pH为1,BiVO4/CeO2的投药量分别为10 mg、15 mg、20 mg、25 mg、30 mg、35 mg,考察BiVO4/CeO2投加量对甲基橙降解效率的影响,结果如图7所示。

图7 甲基橙的降解率与BiVO4/CeO2的投药量的关系Fig. 7 Relationship between the degradation rate of methyl orange and dosage of BiVO4/CeO2
由图7可知,当BiVO4/CeO2的投药量为30 mg时,BiVO4/CeO2复合材料对甲基橙的降解率最大,为85%;随着BiVO4/CeO2复合材料投加质量的增大,甲基橙的降解率先增大后逐渐减小。
2.2.4光照时间对降解效果的影响
设置甲基橙的初始浓度为15 mg/L,调整溶液 pH为1,BiVO4/CeO2的投药量为30 mg,考察不同光照时间对甲基橙降解效率的影响,结果如图8所示。

图8 甲基橙的降解率与光照时间的关系Fig. 8 Relationship between the degradation rate of methyl orange and illumination time
由图8可知,当光照时间为180 min时,BiVO4/CeO2复合材料对甲基橙的降解率最大,为91%。随着溶液在光照时间的延长,甲基橙的降解率先逐渐升高后基本保持不变。由此可知,对甲基橙的降解来说,最佳光照时间为180 min。
3 结论
(1) 通过水热法制备CeO2,并以此为载体,采用水热法制备BiVO4/CeO2。SEM、XRD表征结果显示,CeO2呈梭状,为立方晶型;BiVO4为类葡萄球状,为单斜白钨矿晶型,BiVO4与CeO2复合的较好。
(2) BiVO4/CeO2复合材料对水中甲基橙有较强的光催化去除能力。当紫外光的照射时间为180 min,BiVO4/CeO2的投加量为1.2 g/L,pH为1,甲基橙的初始浓度为15 mg/L时,甲基橙的降解率可达到91%。
