三维镧系配位聚合物[Sm(oba)2(H2O)2]∙H2O的合成与表征
2020-04-06刘江平张芙蓉
刘江平,陈 瑛,余 浩,张芙蓉,曾 岗,蒋 兰
(1.重庆三峡医药高等专科学校公共基础部,重庆 404120;2.重庆三峡医药高等专科学校临床医学院,重庆 404120;3.重庆三峡医药高等专科学校科技处,重庆 404120)
近年来,基于过渡金属和有机配体形成超分子配合物领域的发展迅速,这类化合物巧妙融合了有机配体和金属离子,通过自组装形成有规律的网状框架,结构新颖多样,结合了高分子化合物和配位聚合物的双重特点,在荧光、磁性、催化、生物制药等多个领域具有潜在的应用价值[1-9]。作为良好的功能性材料,超分子配位聚合物的设计与构筑受多重因素影响,其中比较重要的是金属离子和配体选择[10-11]。一方面,f 区金属离子由于结构特殊、存在空轨道、配位数较高,在形成新颖的超分子拓扑结构方面备受青睐[12-14];另一方面,芳香羧酸配体由于苯环及羧基的存在使配位能力增强,配位模式多样化,在金属-有机配合物领域备受关注;另外,羧基的桥连能力很强,桥连方式也比较灵活,既有单齿桥连,也有双齿桥连。本实验合成的新型晶体结构中,羧基呈现两种不同的桥连方式,正是这种多样的桥连方式构筑了结构新颖、性能新奇的配位聚合物[15-17]。水热合成法可以改变反应物的反应性能,提高反应活性,具有较强的可调控性和可操作性,在功能材料和配合物等的制备方面发挥着独特的作用。本实验通过水热法合成了一种新型三维配位聚合物[Sm(oba)2(H2O)2]∙H2O(oba=4,4′-二羧基二苯醚),并通过X-射线单晶衍射仪对其结构进行了表征。
1 实验
1.1 试剂及仪器
试剂:Sm(NO3)3∙6H2O、4,4′-二羧基二苯醚、蒸馏水(均为分析纯,未经进一步纯化处理)。
仪器:磁力搅拌器,不锈钢反应釜,烘箱,Perkin-Elmer 2400Ⅱ型热分析仪。
1.2 [Sm(oba)2(H2O)2]∙H2O 的合成
将0.3 mmol Sm(NO3)3∙6H2O、0.5 mmol 4,4′-二羧基二苯醚溶于装有8 mL 蒸馏水的小烧杯中,搅拌均匀后转移至25 mL 聚四氟乙烯内衬的不锈钢反应釜中,设置程序升温至160 ℃,恒温4 天后,冷却并用蒸馏水洗涤,产生浅黄色块状晶体。分子式为C28H17O13Sm,元素分析计算值为C 47.25%、H 2.40%;实验值为C 47.21%、H 2.38%。
1.3 测试
单晶:使用Bruker Apex-ⅡCCD 单晶衍射仪测定,样品体积0.50 mm×0.50 mm×0.37 mm,在296(2)K下用石墨单色化的Mo-Kα 射线(λ=0.710 73 Å)作为入射辐射源,以ω-2θ 方式扫描收集衍射点,1.89°≤θ≤25.00°,共收集到13 798 个衍射点[4 943 个独立衍射点I>2σ(I)]。
红外光谱:使用Nicolet Avatar 360 型红外光谱仪测定,溴化钾压片,扫描波数4 000~400 cm-1。
TG 热分析:在热分析仪(空气气氛,升温速度10 ℃/min)上测定。
2 结果与讨论
2.1 晶体结构表征
用直接法解析晶体结构,并用全矩阵最小二乘法F2进行精修,对全部非氢原子采取各向异性热参数处理,最终偏移因子R1=0.031 6,wR2=0.083 5。晶体解析的所有计算工作均采用SHELXTL-97 程序系统完成[18]。具体晶体学数据见表1。

表1 配合物[Sm(oba)2(H2O)2]·H2O的晶体学数据
2.2 晶体结构描述
晶体结构分析表明,该配合物属单斜晶系,C2/c空间群;最小不对称单元含1 个Sm3+,两个4,4′-二羧基二苯醚配体和两个氧原子,其中Sm(Ⅲ)分别与配体oba 上的6 个O 和另外两个孤立的O 配位,为八配位构型(如图1 所示,为清晰起见,略去氢原子和结晶水)。结构中配体oba 有两种不同的配位方式:(1)羧基氧原子以桥连方式连接3 个Sm(Ⅲ),见图2a;(2)单纯的双齿配体,一个羧基上的两个O 各连一个Sm(Ⅲ),见图2b。

图1 配合物的非对称单元结构

图2 配合物中配体的两种配位方式
与配合物晶体相邻的最小不对称单元通过羧基上的O 以第一种连接方式形成三维网状超分子结构(如图3 所示),Sm—O 键长为2.353(2)~2.610(3)Å;此外,作为单纯的配体,羧基上的氢原子与桥氧间有氢键作用,可使配合物的稳定性进一步增强,具体数据如表2所示。

图3 配合物的三维结构图

表2 配合物的氢键数据
2.3 配合物的红外光谱
由图4 可以看出,位于1 691、1 602 和1 414 cm-1的强吸收峰归属于配体oba 的νas(COO)和νs(COO),表明羧基氧原子与钐离子配位[19]。3 200~3 600 cm-1的较宽吸收峰归属于O—H 的振动特征峰[20]。上述分析结果与晶体结构相吻合。

图4 配合物的红外光谱图
2.4 热性质
配合物的TG 曲线见图5。
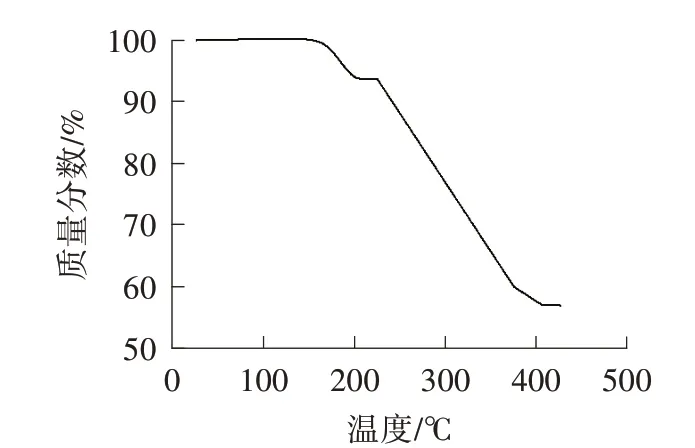
图5 配合物的TG 曲线
由图5 可知,配合物表现为两步失重:(1)155~206 ℃,失重约为6.21%(理论值7.50%),为3 分子水的失去;(2)206~406 ℃,失重约为36.88%(理论值为36.25%),相当于失去1个单纯配体oba。
3 结论
基于金属-有机配位聚合物的合成受金属离子和有机配体的影响较大,金属离子的空轨道越多,配位模式增加,配位环境更复杂;有机配体的种类、配位能力、配位模式变化也较大,对配位聚合物结构的形成产生重要影响。
