健康志愿者清醒时疼痛程度与镇痛伤害感受指数相关性研究
2020-03-30安海燕
闫 琦 安海燕 冯 艺
(北京大学人民医院麻醉和疼痛医学科,北京 100044)
目前,视觉模拟评分法 (visual analogue scale,VAS) 是评估疼痛程度的金标准,操作简便,临床应用广泛[1]。临床医师希望使用的评估方法能够及时、有效、正确、可重复、可操作性强。VAS可以很好的达到上述要求,但对于无法交流的病人以及老人、小孩,VAS的应用便有所限制。另外VAS评分很难区分心因痛和躯体痛。由于这部分特殊人群的需求,临床医师可以应用其他的一些评估方法[2,3],如疼痛行为量表(behavior pain scale, BPS)[4]、危重症病人疼痛观察工具(critical-care pain observation tool,CPOT)[5],这些量表可由医师对这些无法交流的病人的行为活动进行评估,从而判断病人目前的疼痛程度。但这些量表操作复杂,临床使用费时费力,应用并不广泛。
体温、脉搏、呼吸、血压、疼痛五大生命指征中只有描述疼痛的VAS是一个主观参数,无法客观反应病人的疼痛程度。理想的临床医学监测手段应该无创、连续、方便而且能够实时客观的反映机体生理或病理变化。是否有客观的指标能够与疼痛相对应呢?疼痛是不是可以进行客观的量化?镇痛伤害感受指数(analgesia nociception index, ANI) 或许能满足上述要求。
ANI是一个新参数,它是近10年发展起来的可用于监测镇痛程度及伤害性刺激反应程度的新型监测参数。ANI主要利用心率变异性(heart rate variability, HRV)来反映交感张力/副交感张力的平衡,从而反映疼痛水平[6,7]。在手术当中,HRV 与伤害性刺激/抗伤害性刺激平衡相关联,可作为判断麻醉中镇痛程度的可靠指标。现已有研究表明在麻醉中[8],ANI与疼痛程度有较好的相关性。而对于清醒病人而言,交感/副交感张力的平衡在一定程度上会受到心理应激的影响,因此是否可用ANI反映清醒病人的疼痛程度,尚无定论。有研究[9]尝试对术后急性疼痛病人应用ANI来评估疼痛程度,并发现ANI与VAS呈一定程度的负相关,其诊断数字评分法(numerical rating scale, NRS)是否大于3的ROC曲线下面积可达0.89。但也有研究者持不同意见,同样也是针对术后急性疼痛病人,Ledowski则发现ANI与NRS仅呈较弱的负相关[10]。
为能更进一步研究ANI用于清醒病人疼痛程度的客观评估的可能性,设计了本次针对健康清醒志愿者的疼痛试验。本文的创新性在于首次采用客观量化的疼痛模型,并采用自身对照以排除心理的影响(暗示、应激等),讨论ANI与VAS之间的相关关系,致力于寻找表明清醒病人疼痛程度的客观指标,并研究在给予有效镇痛药物后ANI的变化趋势,设计了本次试验。
方 法
1.一般资料
本试验为随机、双盲、交叉对照试验,共入组40例健康志愿者。本研究已获北京大学人民医院伦理委员会批准并已注册 (2012-15,ChiCTR-INR-16009356; http://www.chictr.org.cn/showproj.aspx?proj = 15973),并与志愿者签署知情同意书。
入组标准:①年龄1~39岁;BMI 18~25 kg/m2;②健康志愿者:生命体征正常(体温、脉率、呼吸、血压);矫正视力 > 0.8;活动耐量正常(可爬4层楼梯);③右侧前臂掌侧无感觉障碍者,无瘢痕;④自愿接受本试验并签署知情同意书。
排除标准:①局部麻醉药和/或无药物乳霜 (VE)过敏者;近期服用影响心率的药物;存在心律失常;②女性志愿者处于月经期/孕期/哺乳期;③既往肝病、肾病史;④存在焦虑状态者,焦虑自评量表(self-rating anxiety scale, SAS)提示存在焦虑;⑤患有精神、神经系统疾病者。
脱落标准:受试者中途退出。
2.材料
监测工具:ANI监测仪(ANI MetroDoloris®,法国),脑电监测仪(Wli 易飞华通,中国)。
疼痛模型:TSA-II,Medoc,0.1℃持续60 s诱发的冷痛刺激。
镇痛药物:5%复方利多卡因乳膏(LIDO,紫光药业)。
阴性对照:无利多卡因乳膏(VE,北京大学人民医院药剂科),无镇痛效果,膏体乳白色,在肉眼观察中与利多卡因乳膏无法区分。
3.研究方法
准备专门的试验室,场地要求安静。每位受试者在进入试验前进行简单查体,测量体温(35~37℃),脉搏 (60~100 bpm)、呼吸 (12~24次/分 )、血压(90 mmHg < SBP < 140 mmHg),监测心电图(无心律失常)。填写SAS量表,提示受试者目前无焦虑状态。方可进入试验流程(见图3)。
开始试验前1.5 h,用准备好的专用模具,标出涂抹乳霜的皮肤区域(见图2A),只包括区域4、2、6,采用统一模具可保证每位受试者前后两次试验为同一皮肤区域),涂抹本次测试所用乳霜(利多卡因乳霜或VE乳霜),再以3M贴膜覆盖,在3M贴膜上写明编号及涂药时间(见图2B)。
1.5 h后撕去3M贴膜,清洁前臂皮肤。按要求接好ANI仪器(MetroDoloris®)、标准生命体征监测以及WLi监测[11](在整个试验过程中WLi > 80)。嘱受试者平静呼吸。平卧10 min后开始给予冷痛刺激试验。
每位志愿者均接受两轮试验,每轮接受3次冷痛刺激,每次刺激间隔10 min。按电脑随机表安排接受涂抹无药物乳霜和利多卡因乳膏的先后顺序,第二轮试验的洗脱期为两周。进行冷痛刺激时,将TSA温度探头按顺序分别置于上图所示区域4、2、6其中之一,给予0.1℃持续60 s的冷痛刺激。请志愿者评估疼痛刺激的强度VAS,并记录刺激结束即刻的ANI、VAS、HR。间隔10 min后换下一区域,取3次的平均值作为最终值。
4.数据采集与统计学分析
本试验为观察性预实验,共招募40位健康受试者。记录受试者人口学资料,记录受试者在疼痛刺激结束即刻的ANI、AS、HR。采用SPSS 13.0统计学软件进行统计学分析,计量资料以均数±标准差() 表示,组间比较采用t检验。ANI与VAS间进行pearson相关分析。P< 0.05为差异有统计学意义。

图1 试验流程图Fig.1 Flow chart of the study

图2 (A)标出接受试验的皮肤区域4/2/6;(B)在接受试验的皮肤区域4/2/6涂抹本轮所用乳霜(利多卡因乳霜或无利多卡因乳霜),以3M贴膜覆盖1.5 hFig.2 (A) Relevant skin areas of stimuli included areas 4, 2 and 6; (B) Cream used in this trial (LIDO Cream Compound or VE Cream) was applied to the relevant skin areas (areas 4, 2 and 6) and covered with Tegaderm Film3M 1.5 h before the trial.
结 果
本试验为随机双盲交叉对照试验,共入组40例健康志愿者,人口学等一般资料见表1。所有受试者均顺利完成试验。每位志愿者均先后接受利多卡因乳膏(LIDO组)和无利多卡因乳膏(VE组)的处理,洗脱期为2周。
40例受试者先后两次接受疼痛刺激的VAS、ANI、HR数据见表2。LIDO组接受疼痛刺激时的VAS明显低于VE组,其差异具有统计学意义。而LIDO组ANI略高于VE组,HR略低于VE组,但其差异均无统计学意义。
将40例病人先后两次接受疼痛刺激的VAS与对应的ANI全部汇总,共80个VAS-ANI数据,发现VAS≤3 cm共25个,VAS > 3 cm共55个。VAS ≤ 3 cm 的 ANI为 88.5±7.3,VAS > 3 cm的ANI则如预期的那样有所降低,ANI为84.0±10.6,虽然变化幅度不大,但二者间的差异具有统计学意义(P= 0.014,见表3)。
表1 人口学资料(n = 40,)Table 1 Demographic data (n = 40,)
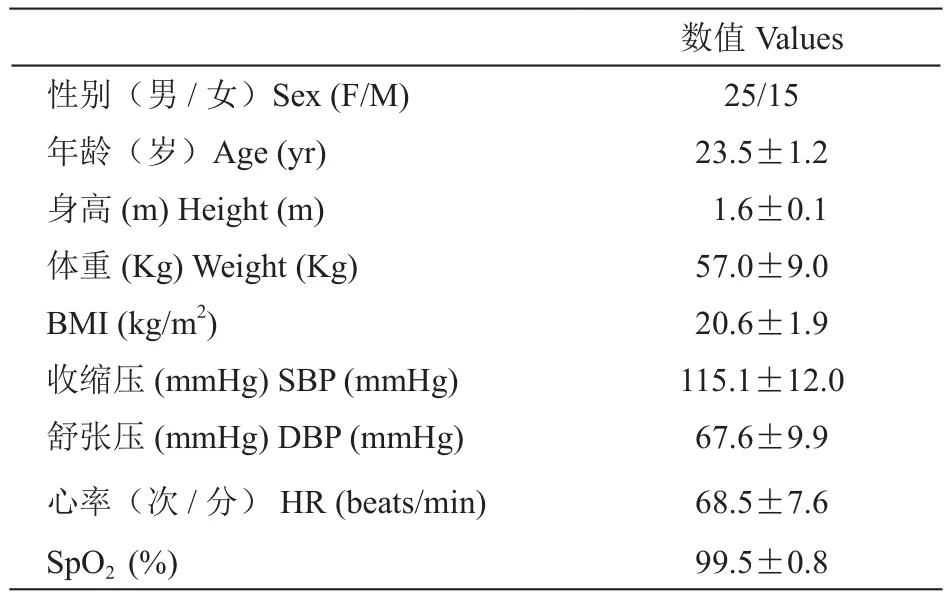
表1 人口学资料(n = 40,)Table 1 Demographic data (n = 40,)
数值Values性别(男/女)Sex (F/M) 25/15年龄(岁)Age (yr) 23.5±1.2身高 (m) Height (m) 1.6±0.1体重 (Kg) Weight (Kg) 57.0±9.0 BMI (kg/m2) 20.6±1.9收缩压(mmHg) SBP (mmHg) 115.1±12.0舒张压(mmHg) DBP (mmHg) 67.6±9.9心率(次/分) HR (beats/min) 68.5±7.6 SpO2 (%) 99.5±0.8
考虑受试者可能存在对利多卡因乳膏的镇痛效果不敏感的情况,剔除了涂抹LIDO与涂抹VE时的VAS变化≤2 cm的受试者数据(11位),再对剩余29位受试者的VAS-ANI数据进行分析(见表4),发现LIDO组接受疼痛刺激时的VAS明显低于VE组,其差异具有统计学意义,且LIDO组ANI略高于VE组,其差异也具有统计学意义(P< 0.05)。
将ANI与对应的VAS进行相关性分析,发现ANI与VAS存在一定的负相关,相关系数-0.267(P= 0.017,见图3)。
为判断应用ANI鉴别VAS > 3 cm的诊断能力,做ROC曲线(见图4A),其ROC曲线下面积即AUC为0.603,仅具有较低的诊断意义。
为判断应用ANI鉴别VAS > 6 cm的诊断能力,做ROC曲线(见图4B),其ROC曲线下面积即AUC为0.673,提示ANI判别重度疼痛的能力好于其判别轻度疼痛的能力。
讨 论
ANI 监测仪通过对心率变异性进行分析,提供取值范围介于0~100 的ANI 数值,实时连续地反映机体的伤害性刺激/抗伤害性刺激平衡。
心率变异性(heart rate variability, HRV)并不是一个新概念,它是指在观察或测定时间内窦性心律时,心电活动的R-R 间期随时间而发生的持续性变化。研究显示,HRV体现了交感神经、迷走神经和体液因素对心血管系统调节的结果,反应了神经体液因素与窦房结相互作用的平衡关系。对HRV的定量分析方法主要是频域法,通过将心率变异信号进行傅里叶转换,得到功率谱图。HRV的频谱主要包括超低频(ULF < 0.003 Hz),极低频(VLF 0.003~0.004 Hz),低频 (LF 0.04~0.15 Hz)和高频(HF 0.15~0.50 Hz)。HRV中高频部分HF的变化仅受到副交感神经张力变化的影响。与HRV相比,HF变化与镇痛伤害性平衡状态更具相关性[12]。
也正是基于这一点,Logier R等研发了PhysioDolorisTM ANI监测仪[13],通过计算机分析HRV中的HF成分,计算副交感神经系统反射弧的能量,从而提供实时连续的“镇痛与伤害性刺激指数”ANI,反映机体的伤害性刺激/抗伤害性刺激平衡。
最初,ANI是用于手术麻醉中的镇痛程度的监测,并且ANI在镇痛监测和应激水平监测方面已经取得了广泛的临床验证[14]。2012年,Jeanne等[8]观察到,在全麻下行腹腔镜胆囊切除术的病人中,切皮及气腹时,ANI明显下降,这是ANI用于全麻中镇痛程度监测的典型例子。ANI目前主要用于麻醉病人,一般认为,术中ANI维持在50~70可以认为镇痛充分。在麻醉状态下,ANI对伤害刺激的快速反应和相关性已得到广泛认可,但对清醒受试者是否有效报道很少。2012年,ANI的应用延伸至清醒病人,Le Guen等[15]研究了ANI在临产妇女中的应用,发现VAS与ANI呈显著负相关,宫缩时ANI相较宫缩间期平均下降9.3±1.8。由此,启发了人们将ANI用于清醒者疼痛程度评估的尝试。Le Guen的研究中,观察的是一类特殊人群-产妇,宫缩痛属于内脏痛。2015年,Gall[16]等研究了ANI对于儿童术后疼痛评估的能力,发现在手术组与非手术组的ANI值分别为52 (16)和75 (17),也说明ANI的降低预示着疼痛的存在。但遗憾的是在成人术后疼痛模型中, ANI的应用存在争议[9,10,23]。
表2 LIDO组与VE组的疼痛指标比较()Table 2 Comparation of pain index between group LIDO and VE ()

表2 LIDO组与VE组的疼痛指标比较()Table 2 Comparation of pain index between group LIDO and VE ()
*P < 0.05,与 LIDO 组相比;*P < 0.05, compared with group LIDO.
Group VAS ANI HR (beats/min)LIDO 2.6±1.5 87.3±8.2 66.6±6.8 VE 6.0±1.0* 83.5±11.1 68.1±9.6 P< 0.001 0.059 0.334
表3 VAS≤3 cm与VAS > 3 cm的ANI数值比较 ()Table 3 Comparison of ANI between VAS≤3 cm and VAS > 3 cm ()
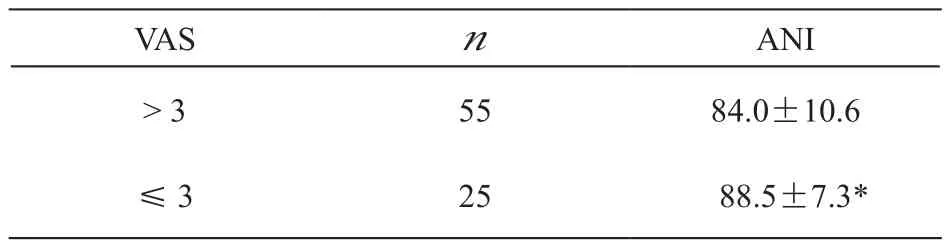
表3 VAS≤3 cm与VAS > 3 cm的ANI数值比较 ()Table 3 Comparison of ANI between VAS≤3 cm and VAS > 3 cm ()
VAS n ANI> 3 55 84.0±10.6≤3 25 88.5±7.3*
表4 剩余29位受试者的VAS和ANI疼痛指标比较()Table 4 Comparation of pain index between VAS and ANI in the remaining 29 subjects ()

表4 剩余29位受试者的VAS和ANI疼痛指标比较()Table 4 Comparation of pain index between VAS and ANI in the remaining 29 subjects ()
*P < 0.05,与 LIDO 组相比;*P < 0.05, compared with group LIDO.
Group VAS ANI LIDO 2.0±1.2 88.6±7.5 VE 6.2±1.0* 84.1±10.5*P< 0.001 0.042
在本试验中,希望通过制作一个统一的疼痛模型,给受试者一个客观上来讲可以量化的程度相同的疼痛刺激,并监测病人接受疼痛刺激时的ANI,期望能够由此发现评估疼痛的客观参数。

图3 VAS与ANI相关性Fig.3 Correlation between ANI and VAS
在本试验中,这个统一的疼痛模型采用的是冷痛(0.1℃持续60 s)。Price等[17]使用了45~51℃持续5 s的温度刺激, Harkins 等[18]使用了43~51℃持续5 s的温度刺激,Gallez等[19]在其试验中使用了47.5~48.7℃来模拟伤害性刺激,Zacny等[20]使用了2℃持续180 s的冷痛刺激。TSA-II主要用于感觉定量测定及痛阈测定,并能够提供痛阈上刺激。Olofsen等[21]、Yosipovitch等[22]使用TSA-II产生合适的疼痛刺激进行相关研究,这些刺激被证明对人体无不可逆损害,可安全使用。
在正式试验开始前,进行了一个预实验,用以判断0.1℃持续60 s冷痛的有效性。参与预实验的5个受试者接受该冷痛刺激后NRS均≥4(见表5),说明该疼痛模型有效且能够提供中度左右的疼痛。
当然也考虑过使用热痛(48℃,持续8 s),其所造成的疼痛程度较冷痛更为强烈。参与预实验的5个受试者接受该热痛刺激后NRS评分均≥6(见表6)。但受试者的耐受性较差,不能很好的配合试验,有可能增加研究中的脱落率。因此,本试验放弃采用热痛模型。
在本试验中,所有病人未给予任何镇静药,实验全程受试者保持安静清醒状态。
本研究设计的优点在于:选择健康受试者,可以规避疾病因素的影响,特别是手术后炎症反应的影响,可以避免麻醉药物的影响;采用的疼痛模型单一;使用自身对照,可避免心理暗示作用,使系统误差降至最低。

图4 (A) ANI预测VAS > 3 cm的ROC曲线;(B) ANI预测VAS > 6 cm的ROC曲线Fig.4 (A) ANI predicting ROC curve of VAS > 3 cm; (B) ANI predicting ROC curve of VAS > 6 cm

表5 冷痛模型预实验Table 5 Preliminary experiment of cold pressor model

表6 热痛模型预实验Table 6 Preliminary experiment of heat pain model
本试验的结果显示,ANI与VAS存在一定的相关性,相关系数-0.267,相关性并不高。该结果与Boselli[23]等的研究并不一致。考虑原因可能有:本试验所采用的疼痛模型与术后急性疼痛相比,疼痛程度较轻,持续时间短,但考虑到受试者的耐受性,不能延长疼痛时间,可能并未对病人的副交感神经张力产生改变,或者其改变的程度并不足以被仪器监测;ANI可能对内脏痛较敏感,而对单纯体表疼痛不敏感;与ANI监测仪自身局限相关,尽管已经在试验时向受试者说明保持规律的自主呼吸,但仍有可能出现不规律的呼吸动作(咳嗽、讲话),呼吸频率过低(RR < 9次/分),影响ANI数值的可靠性。
综上所述,对于清醒健康志愿者,ANI与试验冷痛的VAS评分呈一定程度的负相关,但仍不足以用于清醒病人的疼痛监测。
