柚皮素标准物质的研制及不确定度评定
2020-03-19刘金涛董家吏焦必宁苏学素
刘金涛,李 玲,董家吏,焦必宁,苏学素*
(1.西南大学 化学化工学院,重庆 400715;2.中国农业科学院/西南大学柑橘研究所,农业农村部柑橘产业质量安全风险评估实验室,重庆 400712)
图1 柚皮素的分子结构
标准物质具有一种或多种足够均匀和准确的特性值、高精确度和溯源性,可用来校准测量装置,评价测量方法或给材料赋值,是测试分析技术的保障、量值传递和量值溯源的基础[1]。
柚皮素(Naringenin)属于二氢黄酮类化合物,是柚皮苷的苷元,主要存在于柑橘类水果、蔬菜、坚果及其他植物中[2],其分子式为C15H12O5,分子结构见图1。病理学研究表明,柚皮素具有抗菌消炎、抗癌、抗肿瘤、改善糖尿病、预防老年痴呆症等多种生理功能[3-5],可被开发应用于食品和药品行业。目前,我国尚无市售柚皮素纯度标准物质,研制柚皮素标准物质能够保证柚皮素检测结果的准确性、可比性和溯源性。质量平衡法可直接溯源到国际单位制(SI)中的质量(kg),是一种潜在的基准方法,被世界卫生组织和欧洲药典推荐为药品标准物质定值方法[6-7]。差示扫描量热法(DSC)具备试样用量少、操作简单、无需分离杂质、能测定物质的绝对纯度等优点,适合于高纯度化工医药产品的测定,是美国药典推荐的药品纯度检验及生产质量控制方面的首选方法[8]。本研究同时采用以上两种方法对柚皮素标准物质进行定值分析,其中质量平衡法包括液相色谱法测定主成分的含量,以及水分、无机杂质和残留溶剂的分析。根据标准物质研制的相关要求和技术规范,对柚皮素标准物质进行均匀性检验、稳定性考察及不确定度评价[9]。
1 实验部分
1.1 仪器与试剂
600 MHz核磁共振谱仪(瑞士Bruck公司);紫外可见近红外光谱仪(日立有限公司);HP1200高效液相色谱仪,VWD检测器(美国Agilent公司);RE-52AA旋转蒸发器(上海亚荣生化仪器厂);XC841远红外鼓风干燥箱(吴江市新成烘箱制造厂);ZF-1三用紫外分析仪(上海力辰科技有限公司);DL32型卡尔费休水分测定仪,XS205十万分之一分析天平(瑞士梅特勒公司);DSC60-Plus(日本岛津公司);Agilent5110ICP-OES,Agilent 6890N气相色谱仪,Agilent G1888顶空进样器(美国Agilent公司);Y101超纯水仪(美国Millipore公司)。
柚皮素样品(上海源叶生物有限公司,纯度98.5%);甲醇、乙腈、乙酸乙酯、丙酮、正己烷、氯仿、二氯甲烷、无水乙醇(色谱纯,美国Merck公司);C18硅胶(美国Sigma公司);液体水分含量标准物质(GBWE130654)。
1.2 标准物质的制备
将150 g反相C18硅胶在甲醇中浸泡12 h,摇匀装入内径40 mm的层析柱中,以洗脱剂水-甲醇(65∶35,体积比)平衡层析柱。称取300 mg柚皮素样品,用3.9 mL甲醇溶解后加入2.1 mL超纯水,摇匀,用滴管缓慢滴入层析柱中,加入洗脱剂水-甲醇(65∶35)洗脱,并用20 mL玻璃试管收集洗脱液,随后用毛细管吸取少量洗脱液在硅胶板上点样,将可在紫外灯下显色的洗脱液合并,旋蒸除去溶剂,即得到标准物质样品。经液相检测,样品纯度从98.89%提高到99.85%。重复上述操作,将得到的柚皮素标准物质样品混合均匀,于105 ℃烘箱中干燥6 h,分装到棕色样品瓶中,每个单元包装量为20 mg,共制备120瓶。
1.3 实验条件
1.3.1 液相色谱分析条件通过优化色谱柱种类(XDB-C18、SB-C18和XBridge-C18)、流动相比例(V水相∶V有机相=60∶40、65∶35、70∶30)以及样品质量浓度(100、300、500、700、1 000 mg/L),得到液相色谱定值条件为:Agilent1200液相色谱仪;Agilent XDB-C18色谱柱(4.6 mm×250 mm,5 μm);流动相:0.2%乙酸水溶液-乙腈(70∶30);流速:1 mL/min;进样量:5 μL;样品质量浓度:700 mg/L;检测波长:290 nm。
1.3.2 水分测定条件将样品于105 ℃烘箱中干燥6 h后进行水分测定。环境条件为温度:25 ℃,湿度:23%。开启卡尔费休水分仪,待仪器稳定后开始测定。用微量注射器吸取30 μL液体水分含量标准物质对仪器进行校准。每次准确称取10 mg样品,迅速加入滴定池内,输入称样质量,读取水分值。
1.3.3 残留溶剂测定条件色谱柱:DB-624(0.32 mm×1.8 μm,30 m),载气:氢气,流速:40 mL/min,空气流速:400 mL/min,检测器温度:260 ℃;程序升温条件:初始温度保持5 min,以7 ℃/min的速率升温至60 ℃,再以15 ℃/min的速率升温至190 ℃。
顶空进样器条件:进样量:1 mL;恒温炉温度:90 ℃;样品流路温度:105 ℃;传输线温度:120 ℃。
1.3.4 无机杂质测定条件ICP-OES仪器工作参数:射频功率:1 300 W;等离子体流速:4 L/min;辅助气流速(Ar):5 L/min;观察高度:7.8 mm;蠕动泵转速:30 r/min;检测时间20 s。
1.3.5 DSC测定条件准确称取4~6 mg样品于铝坩埚中,用卷边器密封,置于DSC仪中。参比:空的40 μL标准铝坩埚;N2流速:50 mL/min;程序升温:20~230 ℃,10 ℃/min;230~260 ℃,1 ℃/min;纯度分析软件:TA acquisition。
1.4 均匀性检验与稳定性考察
根据标准物质研制的技术规范,从分装好的120瓶样品中,随机抽取15瓶进行编号,每个样品平行测定3次。用甲醇溶解,配成质量浓度为700 mg/L的溶液,采用高效液相色谱法进行纯度检测,测得数据采用方差分析法(F检验法)进行统计检验。
采用线性拟合法对柚皮素标准物质进行长期和短期稳定性考察。长期稳定性考察:将样品保存在4 ℃条件下,用液相色谱法在第0、1、2、4、6月进行检测,每次抽取2个样品单元,每个单元重复测定3次。短期稳定性考察:取3组样品(每组5瓶)分别在20、40、60 ℃条件下保存,于第1、3、5、7、9 d取样进行检测,采用趋势分析(t检验法)对数据进行分析。
2 结果与讨论
2.1 原料定性分析
在红外光谱仪上测定柚皮素的红外光谱,3 279 cm-1处有强而宽的吸收峰,为羟基的伸缩振动峰,由氢键缔合后的羟基引起;1 633 cm-1处的强吸收为羰基的伸缩振动峰;1 518、1 497、1 463 cm-1处为苯环骨架的伸缩振动峰。样品的红外谱图(图2A)与标准红外谱图(图2B)吸收峰一致。
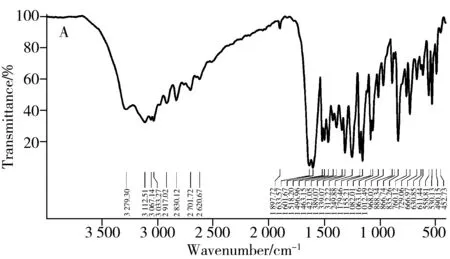

图2 柚皮素样品红外光谱(A)与柚皮素标准红外光谱(B)
测定柚皮素样品的核磁共振氢谱,其化学位移及对应的质子数为:12.15(1H,s,Ar-OH),10.76(1H,s,Ar-OH),9.57(1H,s,Ar-OH),7.32(2H,dd,J=8.5,4.9 Hz,H-2*,H-6*),6.80(2H,d,J=1.2 Hz,H-6,H-8),5.89(2H,m,H-3*,H-5*),5.43(1H,m,H-2),3.23(1H,m,H-3),2.88-2.61(1H,m,H-3)。样品的核磁氢谱与标准核磁氢谱相同(图3)。因此可以确认样品为柚皮素。
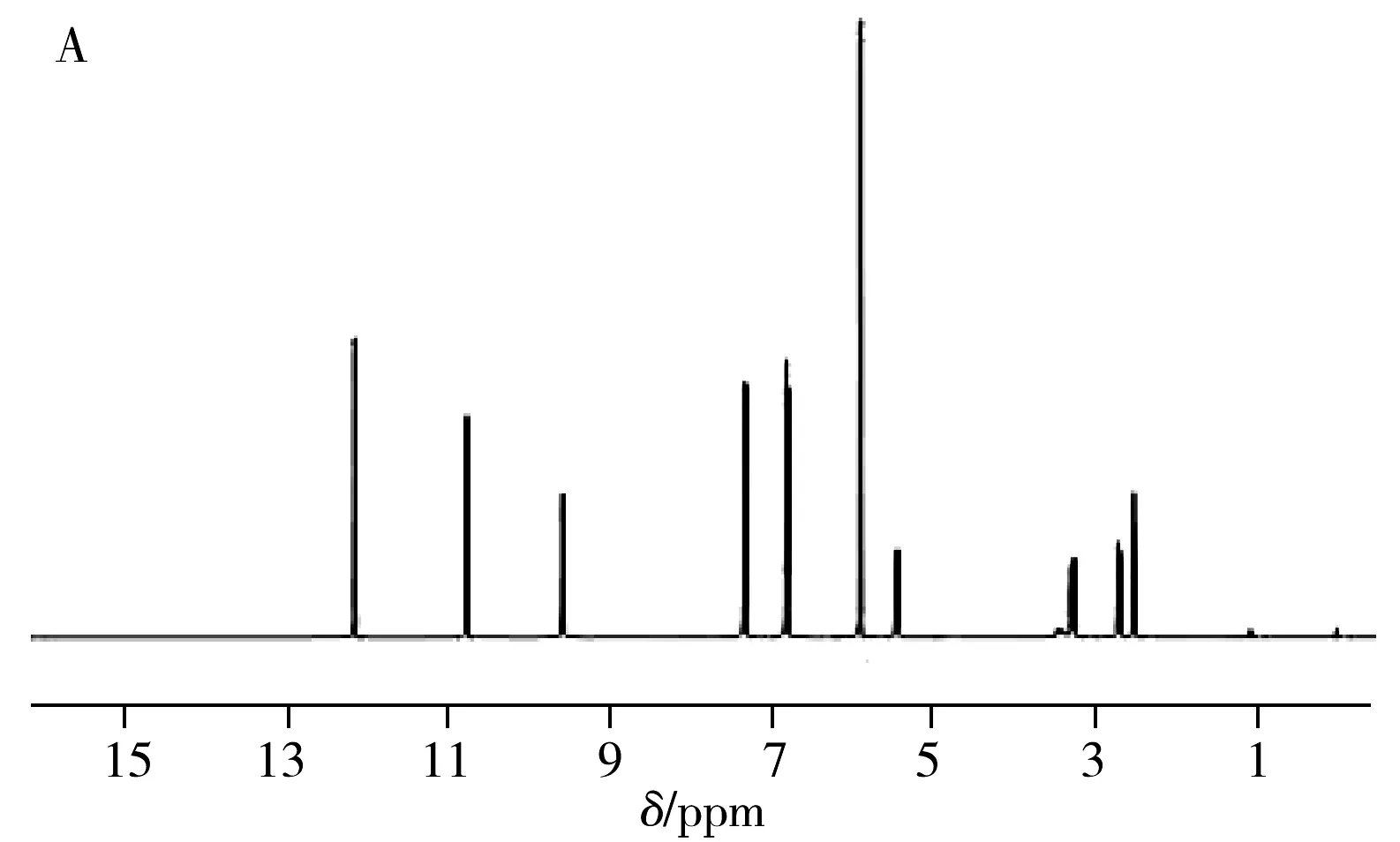
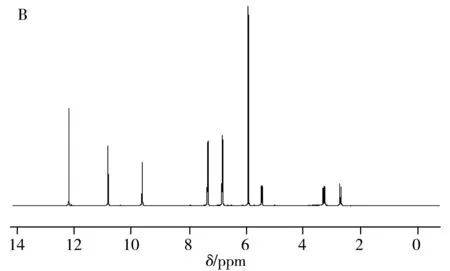
图3 柚皮素样品核磁氢谱(A)与柚皮素标准核磁氢谱(B)
2.2 纯度定值
为了提高定值准确度,同时采用质量平衡法和差示扫描量热法两种不同原理的方法对柚皮素标准物质进行定值分析。
2.2.1 质量平衡法质量平衡法又叫杂质扣除法,指通过测定所有杂质的含量从而得到样品的纯度[10]。由于液相色谱面积归一化法测定纯度值的局限性,样品中的水分、无机杂质和残留溶剂均无法检出[11]。因此分别采用卡尔费休库伦法、等离子体原子吸收光谱法和顶空气相色谱法测定样品中相关杂质的含量,并对结果进行校正。
纯度计算公式为:PMB=(1-Xmoi-Xele-Xvola)·P0
(1)
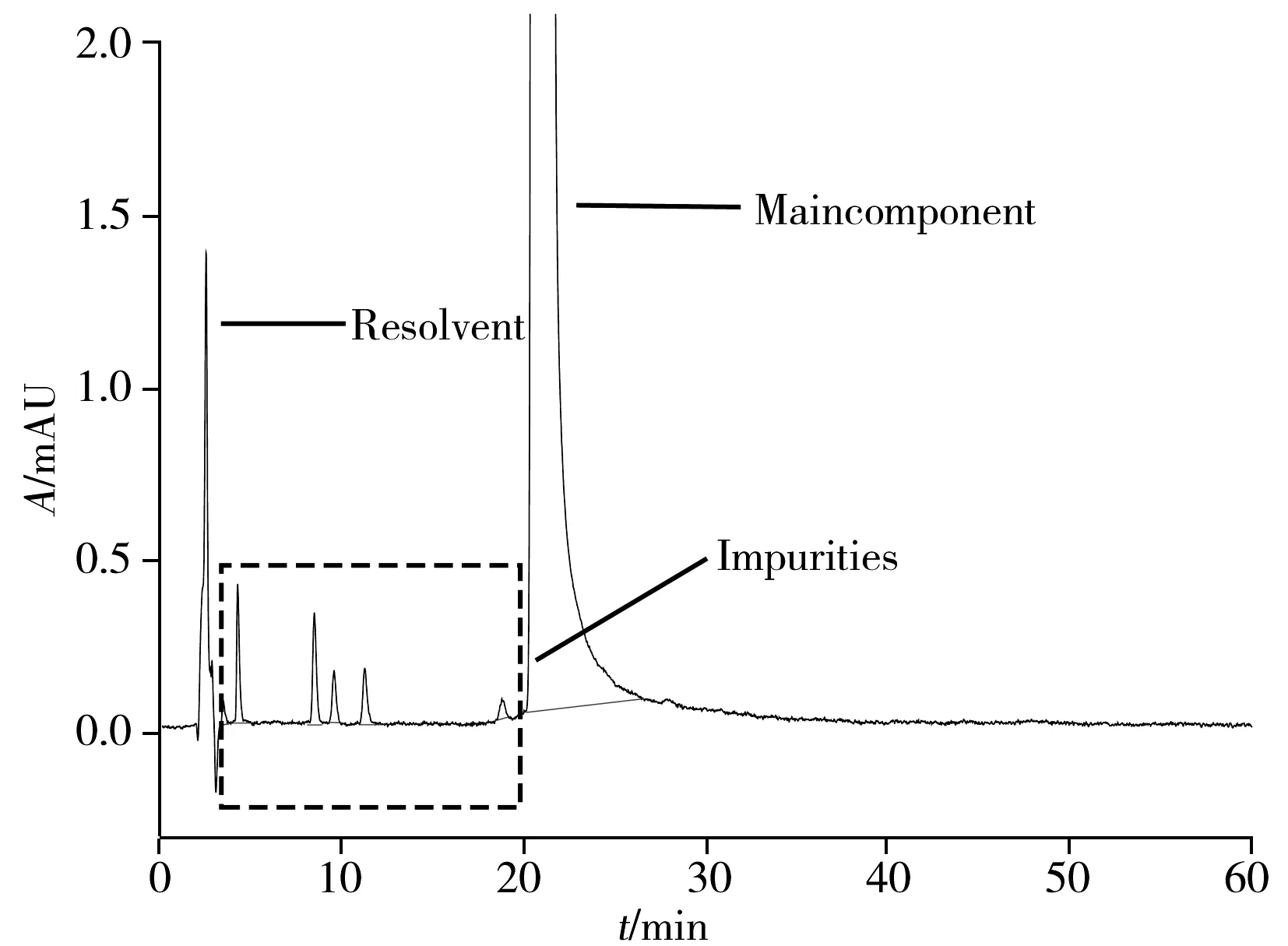
图4 柚皮素标准物质液相定值色谱图

图5 柚皮素标准物质的DSC图谱
式中:PMB为质量平衡法定值结果;P0为主成分含量;Xmoi为水分含量;Xele为无机杂质含量;Xvola为残留溶剂含量。
(1)主成分的测定:采用液相色谱法测定柚皮素主成分的含量,重复测定7次,主成分测定结果的平均值为99.85%,液相定值色谱图如图4所示。
(2)水分、残留溶剂和无机杂质的测定:样品在105 ℃干燥6 h后采用卡尔费休库伦法测定水分值,残留溶剂含量采用顶空气相色谱法测定,无机杂质含量采用ICP-OES法测定,测定结果如表1所示。结果显示,柚皮素标准物质水分含量为0.655 1%,无机杂质含量为0.004 27%,残留溶剂含量为0.042 57%。质量平衡法得到的柚皮素标准物质的纯度值为99.14%。
2.2.2 DSC法DSC法测定样品的纯度以范德霍夫熔点下降理论为依据,由于柚皮素含有杂质,其熔点有所降低,熔点的降低值与杂质的摩尔分数之间符合范德霍夫方程[12-14]:
(2)
式中,T0为纯样品的熔化温度;TS为实际样品的熔化温度;R为气体常数;ΔHf为纯样品的摩尔熔化焓;F为熔化了的样品分数;x为杂质摩尔分数。

表1 柚皮素标准物质定值结果
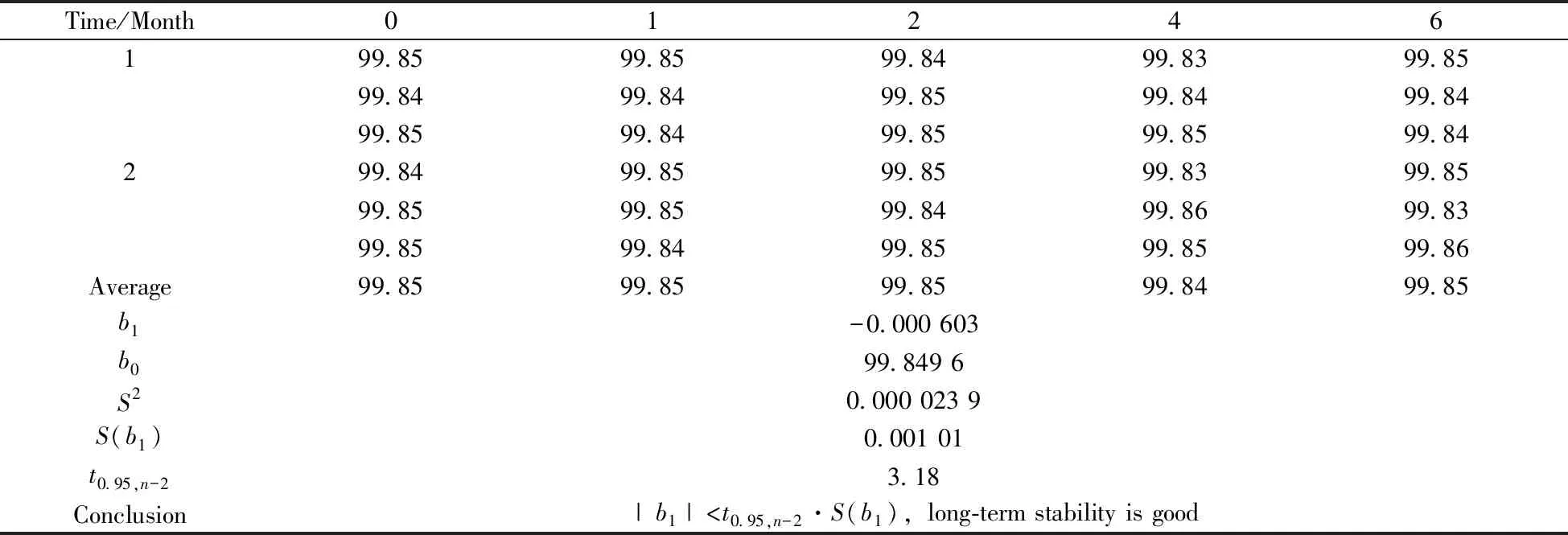
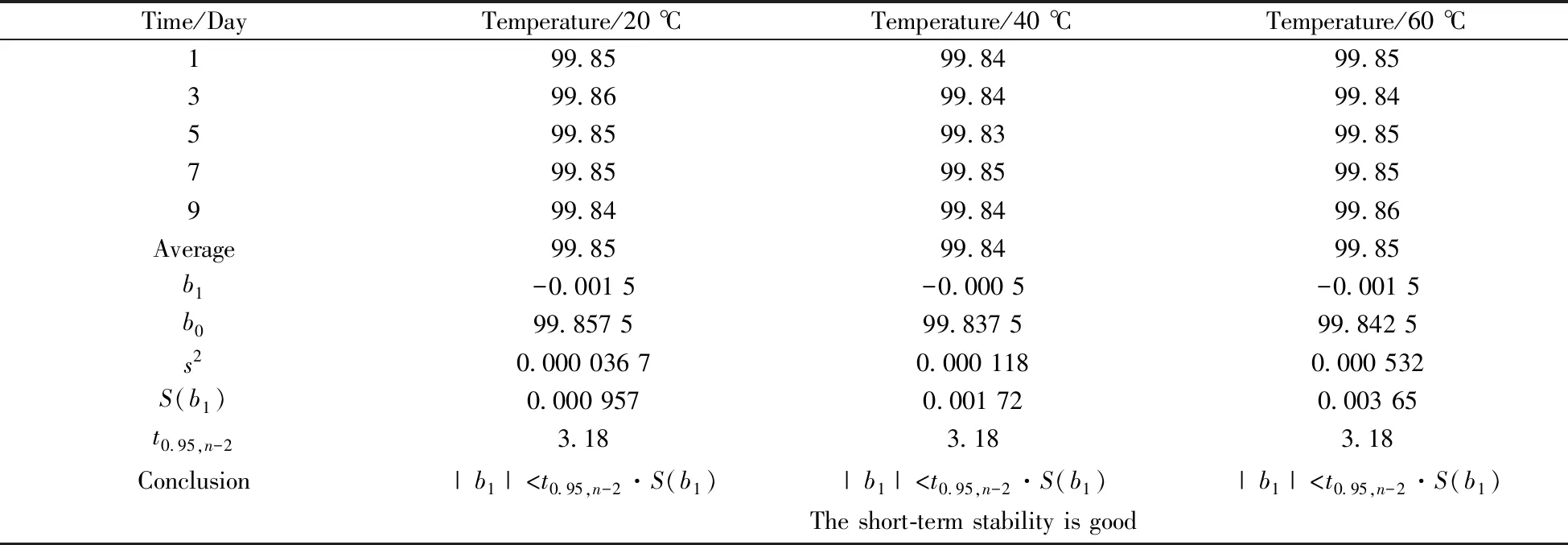
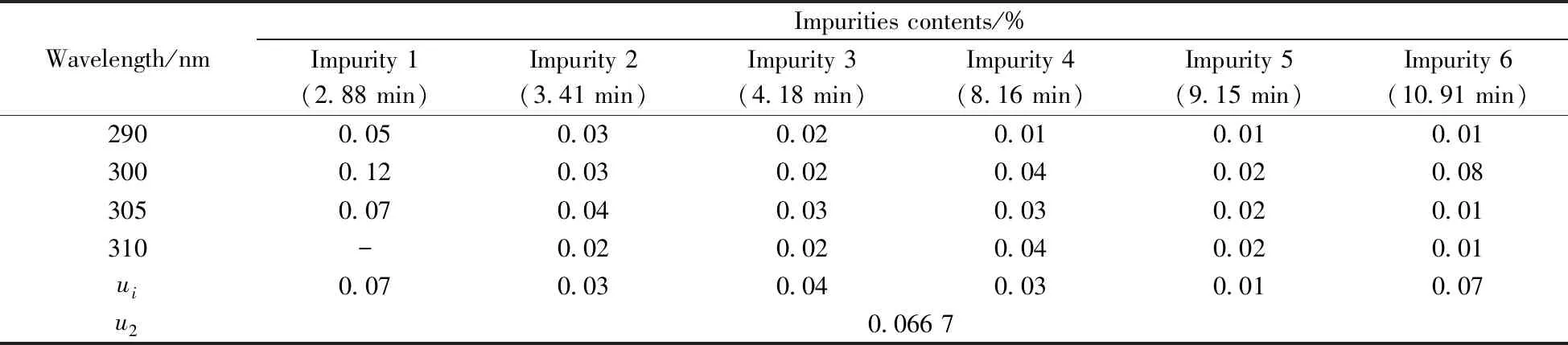
柚皮素的DSC测定曲线如图5所示,DSC法得到的柚皮素标准物质纯度值为99.16%(表1)。将质量平衡法和DSC法测得的两组数据进行等精度检验,t(0.80) 高效液相色谱法均匀性检验结果见表2,经计算F=2.01,查临界值表F0.05(14,30)=2.04。F 表2 柚皮素标准物质均匀性检验结果 2.4.1 长期稳定性检验结果通过高效液相色谱法对柚皮素标准物质进行长期稳定性检验,结果见表3。采用线性拟合法进行分析。以x代表时间,y代表纯度值,拟合成一条直线,设时间对纯度值的方程为y=b0+b1x,采用t检验法来检验斜率b1的显著性,从而评估长期稳定性。当|b1|>t0.95,n-2·S(b1)时,斜率被认为在统计学上是显著的,其中S(b1)是斜率的不确定度,t0.95,n-2是95%置信度,n-2自由度下的临界t值。经计算|b1| 表3 柚皮素标准物质长期稳定性检验结果 2.4.2 短期稳定性检验结果短期稳定性数据的处理方式与长期稳定性一样,采用t检验法来检验斜率b1的显著性,从而评估短期稳定性。经计算在20、40、60 ℃下的|b1|均小于t0.95,n-2·S(b1)(表4),表明在模拟运输条件下柚皮素标准物质9 d稳定性良好。 表4 柚皮素标准物质短期稳定性检验结果 根据《JJF1342-2012 标准物质定值的通用原则及统计学原理》[15],标准物质总的不确定度包括以下3个方面:(1)样品均匀性引入的不确定度uH;(2)样品稳定性引入的不确定度us(包括长期稳定性不确定度ults和短期稳定性不确定度usts);(3)样品定值引入的不确定度uchar。标准物质的合成不确定度为: (3) 2.5.1 均匀性引入的不确定度 2.5.2 稳定性引入的不确定度 2.5.3 定值引入的不确定度 (1)质量平衡法定值引入的不确定度: 质量平衡法定值的不确定度uMB计算公式如下: (4) 其中:uMB、u(P0)、u(Xmoi)、u(Xele)、u(Xvola)分别为质量平衡法定值不确定度、液相色谱法测定主成分的不确定度、水分测定不确定度、无机杂质测定不确定度和残留溶剂测定不确定度。 液相色谱法测定的不确定度主要由两部分组成。分别为:(1)测定结果的重复性引入的不确定度u1,由多次测量的标准偏差计算;式中,Bimax为在6个检测波长下杂质成分i的最大百分比含量;Bi定值λ为定值波长下的杂质成分i的百分比含量。(2)主成分和杂质最大响应波长差异引入的不确定度u2。 (5) 表5 不同波长下主成分和杂质的响应 (续表5) Wavelength/nmImpurities contents/%Impurity 1(2.88 min)Impurity 2(3.41 min)Impurity 3(4.18 min)Impurity 4(8.16 min)Impurity 5(9.15 min)Impurity 6(10.91 min)2900.050.030.020.010.010.013000.120.030.020.040.020.083050.070.040.030.030.020.01310-0.020.020.040.020.01ui0.070.030.040.030.010.07u20.066 7 液相色谱法的合成不确定度为: (6) 无机杂质和残留溶剂的含量很少,因此主要考虑测量重复性引入的不确定度。无机杂质测定的不确定度u(Xele)为0.000 4%,残留溶剂测定的不确定度u(Xvola)为0.001 0%。 因此,质量平衡法的标准不确定度: (7) (2)差示扫描量热法引入的不确定度: DSC法定值引入的不确定度uDSC分为A类不确定度和B类不确定度。A类不确定度由测量的重复性引起,用测量结果的标准偏差来计算。B类不确定度是仪器设备或测量条件等影响因素引入的不确定度。将ΔHf=Q·M/m代入公式(2)可得: (8) 式中:x表示杂质的摩尔分数;R为气体常数;T0和TS分别表示纯样品和实际样品的熔化温度;ΔHf表示摩尔熔化焓;Q为样品热焓;m为样品质量;M为样品摩尔质量;F为熔化了的样品分数。 DSC法测量中的B类不确定度由以下公式计算: (9) 式中,u(x)为杂质含量测定的偏差,u(Q)为铟标准物质的热焓测定值与实际值的偏差,u(F)为熔融峰面积计算的偏差,u(TS)为铟标准物质熔点不确定度,u(m)为天平称量和检定的不确定度。 2.5.4 标准物质的合成及扩展不确定度下表所示为标准物质定值过程中各不确定度的分量,将其合并得到标准物质的总不确定度。 ParametersValue/%均匀性不确定度uH0.004 3长期稳定性不确定度ults0.006 1短期稳定性不确定度usts0.037 3质量平衡法定值不确定度uMB0.069 0差示扫描量热法定值不确定度uDSC0.040 3 标准物质的合成不确定度: (10) 扩展不确定度为:U=uC×k≈0.2%(k=2)。 本文以反相硅胶柱层析法纯化得到柚皮素纯度标准物质,采用质量平衡法和差示扫描量热法进行定值分析。定值结果不确定度较低,表明质量平衡法和DSC法作为纯度定值方法具有很高的准确性。柚皮素纯度标准物质水分含量较高,可能由于烘箱干澡法效果不理想,可尝试同时使用真空冷冻干燥。另外,采用卡尔费休法测定微量水分时,称样量的选择要保证测量结果的均匀性。通过高效液相色谱法进行均匀性检验和稳定性考察,研制的柚皮素纯度标准物质均匀性、稳定性良好,纯度值为99.2%,扩展不确定度U=0.2%(k=2),有效期为6个月。该标准物质对于柚皮素样品分析检测结果的准确性、量值溯源和量值传递具有重大意义。2.3 均匀性检验结果

2.4 稳定性检验结果
2.5 不确定度评定
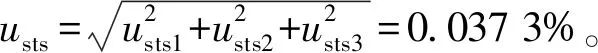

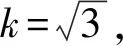

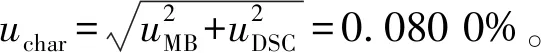

3 结 论
