普通高中化学课程中“σ键与π键”的教材分析及教学建议
2020-03-18储开桂
储开桂
摘要:“σ键与π键”是高中化学《物质结构与性质》模块部分的重要内容,通过对不同版本教材中相关内容的对比分析,提出适当的教学建议。
关键词:共价键;σ键与π键;教材分析;教学建议
文章编号:1008-0546(2020)03-0081-03
中图分类号:G632.41
文献标识码:B
doi: 10.3969/j.issn.1008-0546.2020.03.022
一、课程标准中“σ键与π键”的教学要求
《普通高中化学课程标准(实验)》和《普通高中化学课程标准(2017年版)》都对高中学生学习共价键有明确的要求:认识原子间通过原子轨道重叠形成共价键,知道根据原子轨道重叠方式,共价键可以分为“σ键与π键”等类型。从共价键键参数(键能、键长、键角)描述键的强弱和分子的空间结构。学好“σ键与π键”有助于学生认识和理解共价键的特征和本质,也是学生后续学习《物质结构与性质》和《有机化学基础》两个模块知识的必备学科基础知识。
二、“σ键与π键”的教材分析
《物质结构与性质》模块中大部分学习内容比较抽象,旨在让学生体会物质构成的奥秘,并用所学物质结构的知识增强一些解决化学问题的能力。现行高中教材江苏凤凰教育出版社(以下简称苏教版)和人民教育出版社(以下简称人教版)围绕“σ键与π键”的编排精选案例、采用丰富生动的图像呈现“σ键与π键”的形成过程、选择不同层次的问题解决内容帮助学生理解和掌握“σ键与π键”,但两本教材呈现方式上有明显差异,中学化学教师在教学过程中应根据学生已有的认知水平灵活处理教材,“用好”高中化学教材而不是“教好”高中化学教材。
1.苏教版教材中“σ键与π键”的编排特点
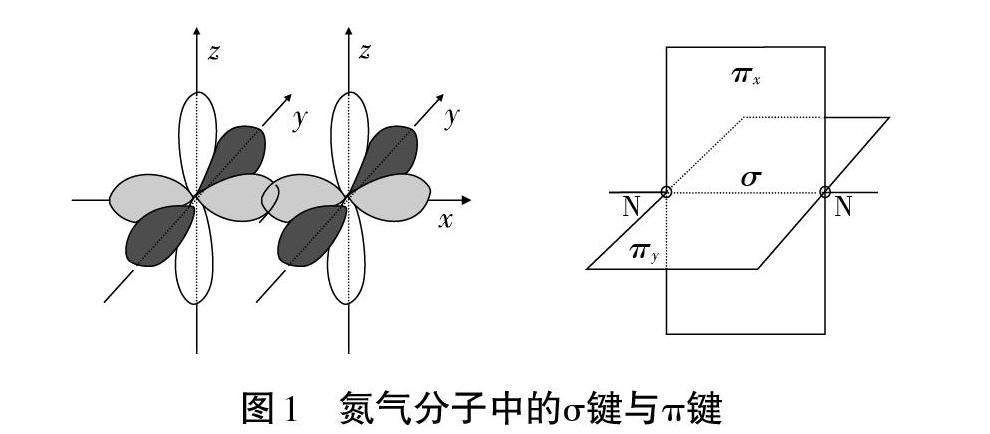
苏教版教材在介绍“σ键与π键”概念时选择的例子是氮气分子。其优点在于氮气分子是一个典型的既含有σ又含有π键的分子,同时基于学生对氮原子的原子轨道及原子核外电子排布已经有了充分的认识和理解,在教学过程中借助于氮气分子的结构模型,引导学生分析和发现氮原子结合成分子的过程,很容易理解原子轨道重叠方式的不同(“头碰头”、“肩并肩”)会形成两种不同的类型的化学键即“σ键与π键”。
教材在介绍“σ键与π键”概念及差异的基础上设置了“问题解决”,引导学生运用“σ键与π键”的有关知识,从结构的角度深入讨论在必修2中所学的乙烷、乙烯和乙炔分子中的化学键的成键情况,让学生学会从“σ键与π键”的稳定性差异的角度分析乙烷、乙烯和乙炔三种物质特征反应的差异,与必修2学过的知识相关联。
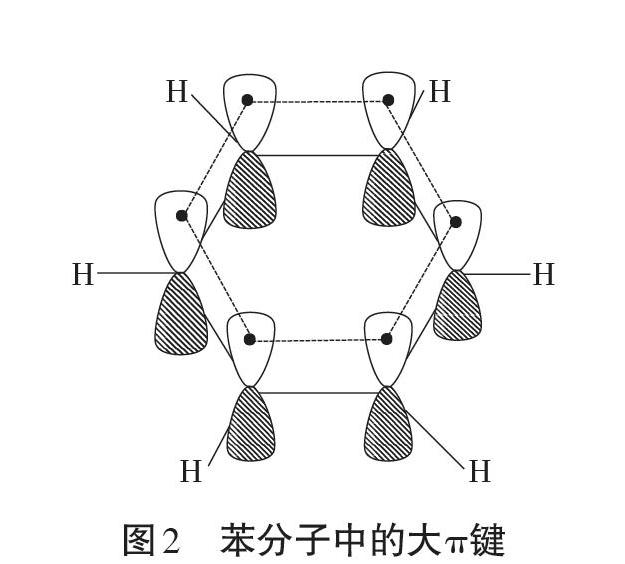
教材最后在“拓展视野”栏目中选择了苯,分析了苯分子中的σ键与大π键,一方面是对必修2教材中苯分子结构和性质的呼应,让学生逐步形成结构决定性质的化学学科思想;另一方面是对π键相关知识的延伸(离域π键),为后面的学习打好铺垫。
虽然苏教版教材在介绍“σ键与π键”概念时选择了典型的例子氮气分子,但也正是这个典型的例子给学生的学习带来了困惑。困惑在于学生很难理解同样都存在π键,为什么乙烯、乙炔中的π键不牢固而氮气分子中的π键反而特别稳定,教材上对此差异并未提供很好的解释和说明,不利于学生的认知发展。
2.人教版教材中“σ键与π键”编排特点
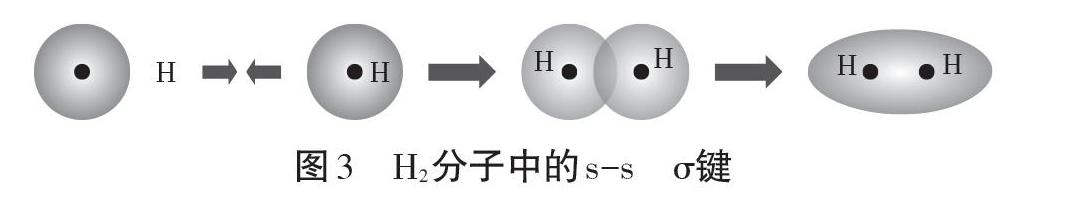
人教版教材在介绍“σ键与π键”概念时更加着重基础,循序渐进引导学生学习。先从最简单的H2分子人手,从1s轨道与1s轨道的重叠过程分析得出σ键的特征(轴对称)。σ键可以绕两原子核连线为轴自由旋转。
然后再以学生熟悉的HCl分子和Cl2分子为例介绍了s-pσ键和p-pσ键的形成,这样有充足的例子让学生更充分认识σ键的形成,加深对通过原子轨道重叠形成化学键本质的认识。
在介绍p-pσ键形成的基础上引入了p电子与p电子除了以“头碰头”的形式成键还可以以“肩并肩”的形式成键即π键。通过图像对比了“σ键与π键”的差别,π键不能绕原子核连线自由旋转,π键的特征表现为“镜像对称”。
从原子轨道重叠程度不同分析得出π键不如σ键牢固,比较容易断裂。教材同样以乙烷乙烯为例,从化学键形成的不同角度说明它们性质的差异。从正文内容的编排角度,人教版的编排更符合学生的认知规律,学生更容易理解和接受。
与苏教版教材的设置相比,人教版教材对于氮气分子中氮氮三键的处理更合理一些。首先是教材是在介绍了“σ键与π键”的概念和特征之后让学生尝试去分析氮气中的成键情况,这更符合学生的认知规律,也有利于学生巩固对该节知识的掌握和应用,问题的设置并没有要求学生去探讨氮气分子中“σ键与π键”的稳定性差异,在普通高中的学习过程中让学生了解氮氮三键的牢固性比了解“σ键与π键”的稳定性差异更有价值和教学意义。值得肯定的是,为了化解学生的困惑,人教版教材在课后习题P36第5题中通过给出N-N、N=N、N=N键能之比为1:2.17:4.90,而C-C、C=C、C≡C键能之比为1:1.77:2.34,引导学生得出氮气稳定而碳碳双键和碳碳三建不稳定的结论。这种基于数据证据的结论获取正是新课程所提倡的教学目标导向,也能帮助学生消除这个部分学习可能产生的疑虑,巧妙回避了“σ键与π键”谁更稳定的问题。
三、教学建议
基于中学化学的教学要求,需要让学生弄清“σ键与π键”的差异源于原子轨道的重叠方式的差异,在这个方面选取氮气还是氯气并无本质区别,但如若要求从化学键形成的本质差异去分析“σ键与π键”的稳定性要注意选择不同的例子会带来截然不同的教学效果。当然作为教师自身,应该尝试理清这其中的差异。一线教师需要搞清“σ键与π键”的稳定性是有复杂性的。
σ键的成键方式为电子云“头碰头”重叠,π键的成键方式为电子云“肩并肩”重叠。从价键理论的角度,共价键的强度与键能及键长有关,共价键键长越短,键能越大。例如,碳碳单键的键能为356kj/mol,碳碳双键的键能为615kj/mol,由此可推出碳碳σ键键能为356kj/mol,碳碳π键键能为259kj/mol。通常情况,“头碰頭”相比“肩并肩”电子云具有更好的重叠,因此碳碳σ键比碳碳π键更稳定。这一结论也与碳碳共价键键能的实验测定结果相符合。
然而,从“乙烯及乙烷分别通人溴水,乙烯可以使溴水变色”说明碳碳σ键比碳碳π键更稳定是不全面的。反例:光照条件下乙烯与乙烷分别与溴蒸汽混合,乙烷体系中可检测到一溴甲烷这一碳碳σ键断裂的产物,而乙烯体系中很难检测到1,2一二溴乙烷这一碳碳π键断裂的产物。通过相同的逻辑得出“碳碳σ键不如碳碳π键稳定”這一结论显然是矛盾的。其原因在于“共价键的强度”为热力学概念,而化学反应的发生为热力学与动力学共同作用的结果。水溶液这一反应条件更有利于乙烯的亲电加成反应,光照这一条件更有利于乙烷的自由基反应。因此,化学反应的发生与否与共价键的强度并无直接关系。只有特殊情况下,才能通过化学反应判断共价键的强度,例如由于氢卤共价键强度的递减,相同浓度HCl、HBr、HI水溶液的酸性递增(HF水溶液存在分子间氢键不在此讨论)。
碳碳σ键比碳碳π键更稳定,然而,σ键并不始终比π键更稳定。例如,氮氮单键的键能为159kj/mol,氮氮双键的键能为419kj/mol。由此可得,氮氮σ键的键能为159kj/mol,氮氮π键的键能为260kJ/mol。这一现象的解释需要通过分子轨道理论,两个氮原子原子轨道线性组合构成氮气分子的分子轨道。随后通过对其分子轨道能量进行计算可得氮气分子能级图如图6。每个氮原子的2p轨道上各有3个成单电子,6个2p轨道组合形成3个成键轨道和3个反键轨道,其中两个π2p成键轨道的能量要比σ2p成键轨道的能量低,所以在氮气分子中的π2p键反而比σ2p键更稳定。用分子轨道理论分析氮分子还可以发现其2p轨道上的电子全部填充在成键轨道上,这也更好地解释了氮气的稳定性。
通过对教材的对比分析,期望能对广大同行的教学起到一点帮助,也希望中学教科书的编写专家能多采纳广大一线教师的建议,为更好地开展中学化学教学而共同努力。
参考文献
[1] 曹锡章,宋天佑,王杏乔.无机化学(第三版)[M].北京:高等教育出版社,177,2003
[2]人民教育出版社.普通高中课程标准实验教科书选修3[M].北京:人民教育出版社,2009
[3]王祖浩,普通高中课程标准实验教科书(物质结构与性质)[M].南京:江苏凤凰教育出版社,2006
[4] 中华人民共和国教育部制订.普通高中化学课程标准(实验稿),人民教育出版社,2003
[5] 中华人民共和国教育部制订.普通高中化学课程标准(2017版),人民教育出版社,2018
