浅析《绝命毒师》中的化学原理
2020-03-02周泓宇
周泓宇
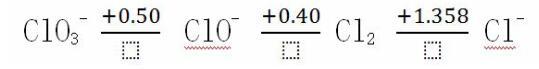
摘 要:《绝命毒师》这部作品十分优秀,在严谨的科学理论基础上延伸了许多艺术产物,本文将从三处作品中的基本化学反应现象原理为基础,从更深的层面来探究反应原理背后的一些历史、产物和用途。
关键词:歧化反应;氟化氢;雷酸汞
主人公沃特?怀特(Walter White),又名老白是一名中学化学教师,在一次体检后突然得知身患肺癌且已步入晚期,时间所剩无几的他决定在生命最后的时光中为家庭做些贡献,于是他走上了一条违法犯罪不归且悲惨的路……此部作品中充满了大量的且几近乎完美的化学反应,挑选几处进行一些更深入的探究。
一、使用磷化氢(PH3)化解危机
一次在荒野里房车中的货物交易,买家看到了老白技术的高超,想要得到他的制作技术,于是借着环境优势威胁他交出技术,手无寸铁的老白深知自己在劫难逃,交出或是不交都会招致灾祸,便只能设法自救。在加热浓NaOH溶液的时候,他缓缓拿起了装有白磷(P4)的容器,在将其倒入了热液刹那,他利用剧烈反应发出的眩光冲了出去,顶住车门后,他复杂的神情解释了他听到的哀嚎……
白磷与热NaOH溶液的剧烈反应,产生了剧毒的PH3气体,反应如下:
P4+3NaOH+3H2O 3NaH2PO2+PH3↑
纯净的PH3气体是无色无味的,其微溶于水,易溶于乙醇,吸入PH3急性中毒症状十分严重,这种系统毒剂会引发身体系统的功能严重紊乱以及死亡,哪怕是吸入一点也会产生一些症状,这也是为什么患有肺癌的老白不慎吸入一丁点后带上了防毒面具的缘故。至于产生的火光,其原因一是可能上述反应进行时,产生了微量的P2H4(联膦),而空气中含痕量P2H4可自燃,PH3浓度达到一定程度时可发生爆炸,二是PH3作为易燃气体,其与空气混合物爆炸下限为1.79%(26 g/m3),浓度达到后遇到加热的明火产生爆炸。
分析上述的反应式,可以看出P元素在反应中有一部分被还原,一部分被氧化,一个标准的歧化反应,那如何判断歧化反应呢?其一就是运用元素电势图进行判断,一般具有多种化合价的元素不同价离子或者单质之间的元素电势并不相同,在酸性或是碱性的环境中反应便会依据kθ的大小确定反应物的产物趋势,接下来拿氯(Cl)元素的来进行分析:
碱性介质中Cl的电势如下:
可知Cl2可发生歧化反应,产物可能是ClO-和Cl-,也可能是ClO3-和Cl-,对于反应:
Cl2+2OH-=ClO-+Cl-+H2O
Eθ=Eθ(Cl2/Cl-)-Eθ(ClO-/Cl2)=1.358-0.40=0.958(V)
根据lgKθ=nEθ/0.0592 可算出反应的平衡常数 K1θ=1.7×1016
而对于Cl2的另一歧化反应:
Cl2+6OH-=ClO3-+5Cl-+3H2O
Eθ=Eθ(Cl2/Cl-)-Eθ(ClO3-/Cl2)=1.358-0.48=0.878(V)
K2θ=2.6×1074
由K1 二、错误的使用了含有氢氟酸(HF)的酸液去销毁证据 老白和搭档在一次事故后,需要销毁一些证据,于是老白配置了一些含有HF的酸液,并安排他的搭档也是他曾经的学生去处理证据,老白特意叮嘱了搭档要找一个塑料容器进行溶,这位昔日不学无术的学生显然不明白这句话的重要性,偷懒的他使用了浴池当作容器以至于二楼楼板塌下,两人功亏一篑。 之前有提到,使用的酸液里含有HF,这种酸的水溶液浓度很高的情况下,会快速对SiO2或者含有SiO2的物质产生腐蚀,瓷质浴缸、楼板(混凝土制成)中恰恰少不了SiO2以及其化合物,HF的接触使得它们的结构迅速破坏,最后导致大面积的破坏,反应式如下: SiO2+4HF = 2H2O+SiF4↑ SiF4+2HF = H2[SiF6] 因此,HF不能象其他常见酸一样使用玻璃制品保存,只能使用塑料容器进行存放,四氟乙烯制品效果最好,这也是为什么老白坚持要使用塑料容器的原因。 酸液中含有HF的原因又是为何?因为HF对生物组织具有极强的腐蚀性,人体皮肤与HF接触后,F-会溶解细胞膜,不断解离而渗透到深层组织,造成各层组织液化坏死。当接触到代人体的牙齿时,牙齿的表层物质(Ca5[PO4]3F)并不溶于单纯的弱酸HF中,为了彻底的处理证据,因此酸液中应该还有强酸,诸如HCl和H2SO4等,反應式如下: Ca5[PO4]3F + 5H2SO4 = 3H3PO4 + 5CaSO4 + HF↑ Ca5[PO4]3F + 10HCl = 5CaCl2 + 3H3PO4 + HF↑ 当然,HF的存在意义并非于此,它是一种机器重要的化工原料,用来蚀刻玻璃制品、去除硅表面的氧化物、做烷基化反应的催化剂,在芯片行业中来蚀刻“电路”等,这些用途都是与它的特殊性质分不开的,举一个它在半导体行业中的完美应用方式。众所周知,今天的世界可以说是一片片半导体芯片堆积起来的世界,半导体芯片的巨大用途目前来看是其他事物所无法比拟的,一片片的芯片是如何生产的呢?首先把柱形的纯硅(99.9999%)切片,在切片上涂抹一层光敏树脂(遇紫外线发生性状改变而溶于水),然后用紫外线照射一面雕刻好部分集成电路的透镜(只有电路部分可以透过紫外线),之后对切片用纯净水进行清洗,性状改变部分的树脂被清洗掉,再使用含有HF、HNO3的混合溶液蚀刻切片,进行一层的电路蚀刻,之后重复这个几个步骤,就可以雕刻出一层层的电路。蚀刻电路的原理就是先利用HNO3把Si氧化为SiO2,然后HF溶解SiO2,为了控制反应速率,蚀刻液中往往加入醋酸(CH3COOH)来控制反应速度。 三、巧用雷酸汞(Hg(CNO)2)彰显身手 老白的帮手在一次纠纷中遭到了竞争对手的恶意报复,于是为了彰显自己的能力,老白决定找到竞争对手进行一次实力上的谈判,重病在身的他自然不可能用蛮力去征服,于是他把Hg(CNO)2结晶成为冰块状固体,外观酷似他们的产品,轻而易举的带着“产品”进入了谈判地点后,使用一小块Hg(CNO)2爆炸的威力震慑了对手,赢得了谈判最后的胜利。 老白制作的Hg(CNO)2是块状的,而一般Hg(CNO)2的粗制品为灰色至暗褐色晶体或粉末,精制品为白色光泽的针状结晶,这应该是对晶体结晶技术深有造诣的老白运用了特殊的结晶方式制成的。Hg(CNO)2的化学性质极其不稳定,在干燥时,其对振动、撞击和摩擦极为敏感,很容易被火星和火焰引起爆炸,高纯度的Hg(CNO)2热分解可以在低至100°C的温度下开始,尽管随着温度的升高它的分解速率要高得多,其反应式如下: Hg(CNO)2 = 2CO↑+ N2↑+ Hg↑ 也有文献提到分解反应可能会产生二氧化碳气体,氮气以及相对稳定的汞盐的混合物,其反应式如下: 4 Hg(CNO)2 = 2CO2↑+ N2↑+ HgO + 3Hg(OCN)CN 此反应产生大量的热量和气体,因此产生的能量十分巨大。 Hg(CNO)2可以通过将汞溶解在硝酸中并向该溶液中添加乙醇制得,这种制备方法是由爱德华?查尔斯?霍华德于1800 年首次发明的,人们发现了Hg(CNO)2的性质后迟迟未使用这种危险的物质,但自18S世纪20年代开始,它被用作小型铜制帽盖的起火成分,迅速取代火石成为点燃枪口装火器中黑色粉末装药的一种方法,后来在19世纪后期和大多数20世纪,Hg(CNO)2或KClO3被广泛使用在引物的自包含的步枪和手枪子弹。有趣的是,人们使用了很久Hg(CNO)2,但是它的晶体结构直到2007年才得以确定。
