PCV中吸气流速对OLV患者呼吸功能及炎症因子的影响
2020-01-03秦新磊殷姜文樊世文张成超代志刚
秦新磊 殷姜文 樊世文 张成超 张 钰 代志刚
石河子大学医学院第一附属医院麻醉科(石河子 832008)
单肺通气(one lung ventilation,OLV)技术常用于胸科手术,便于术者的操作、有效实施双肺隔离[1]。大量临床研究均证实单肺通气是诱发围术期急性肺损伤(acute lung injury,ALI)、急性呼吸窘迫(acute respiratory distress syndrome,ARDS)的危险因素[2- 3]。近年来,压力控制通气(pressure-controlled ventilation,PCV)被证实较容量控制通气(volume-controlled ventilation,VCV)更利于单肺通气下的肺保护[4- 5]。本研究拟进一步探索在压力控制通气模式下,调节吸气流速,观察对单肺通气患者呼吸功能及炎症因子的影响,为临床麻醉中吸气流速的设置及优化提供参考与依据。
1 资料与方法
1.1 一般资料
本研究方案通过石河子大学医学院第一附属医院伦理委员会批准(审批号:2018- 109- 01)并通过中国临床试验中心注册(注册号:ChiCTR 1800018051)。充分告知患者及其家属研究目的情况下,签署知情同意书。本研究样本选择2018年9 月—2019 年8 月于我院择期行单侧肺病损切除术的单肺通气全麻患者75 例。纳入标准:性别不限,年龄29~65岁。ASA Ⅰ或Ⅱ级,18
1.2 分组、随机、盲法
分组:将患者随机分为三组,吸气流速30 L/min (A组,n=25);吸气流速50 L/min (B组,n=25);吸气流速70 L/min (C组,n= 25)。随机方法: 采用随机数字表法。盲法:麻醉分组,麻醉实施、数据记录、术后随访均有独立的研究员负责。
1.3 通气方法
入室后监测BP、HR、SPO2、ECG、BIS。行右侧颈内静脉穿刺置管建立中心静脉压监测,局麻下桡动脉穿刺置管建立有创动脉血压监测及供动脉采血。通过外周静脉给予咪达唑仑0.03 mg/kg,枸橼酸舒芬太尼0.5 μg/kg,苯磺顺阿曲库铵0.2 mg/kg,丙泊酚1.5 mg/kg 麻醉诱导。根据患者性别以及身高体质量选择Fr35~39双腔支气管导管,经口明视下行双腔支气管插管。经纤维支气管镜检查双腔管位置,定位良好后固定导管。接麻醉机行控制机械通气,PCV模式。呼吸参数:按照潮气量(VT)=8 mL/kg调整压力值,潮气量计算使用预测体质量,男性为50+0.91(身高cm- 152.4),女性为45.5+0.91(身高cm- 152.4),呼吸频率(RR)12~14次/min,吸呼比值(I:E)=1:2,吸入氧浓度(FiO2)为100%,氧流量2 L/min,呼气末正压通气(PEEP)=0 cmH2O,控制呼气末二氧化碳分压(PETCO2)30~45 mmHg。侧卧位后再次应用纤支镜定位双腔支气管导管的位置。单肺通气后,先行容量控制通气,按照VT=6 mL/kg记录气道平台压(Pplat),以此压力值为基础设置PCV中的Ppinsp,A组调整吸气流速为30 L/min,B组调整吸气流速为50 L/min,C组调整吸气流速为70 L/min,RR 12~14次/min,其余参数保持不变。麻醉维持给予丙泊酚4~12 mg/(kg·h-1)、盐酸瑞芬太尼0.1~0.3 μg/(kg·h-1)和苯磺顺阿曲库铵0.1~0.15 mg/(kg·h-1)静脉泵注。术中维持血流动力学稳定,麻醉深度监测BIS值维持在40~60之间。关胸前恢复双肺通气,缝皮前停用瑞芬太尼。术毕符合拔管指征后拔除气管导管,并予自控静脉镇痛。
1.4 观察指标
主要观察指标:分别于插管后单肺通气开始前(T0)、单肺通气30 min(T1)、单肺通气60 min(T2)、单肺通气120 min(T3),记录心率(HR)、收缩压(SBP)、舒张压(DBP)、中心静脉压(CVP)、潮气量(VT)、气道峰压(Ppeak)、气道平台压(Pplat)、呼气末二氧化碳分压(PETCO2)并抽取动脉血及中心静脉血行血气分析,记录动脉血氧饱和度(SaO2)、动脉血氧分压(PaO2)、动脉血二氧化碳分压(PaCO2)、中心静脉血氧分压(PcvO2)、中心静脉血氧饱和度(ScvO2)及血红蛋白含量(HB),最终计算潮气量增加量(ΔVT,实测VT与6 mL/kg的VT差值)、肺动态顺应性(Cdyn)、死腔率(VD/VT)、氧合指数(PaO2/FiO2)和肺内分流率(Qs/Qt)。
次要观察指标:分别于T0、T1、T2、T3四个时刻抽取中心静脉血5 mL, 2000 r/min 离心20 min,取1 mL血清于- 80 ℃冰箱保存待测。采用酶联免疫吸附法(ELISA)检测分析IL- 6、IL- 8、TNF-α和sICAM- 1。
1.5 术后肺部并发症的发生情况
采用墨尔本评估量表观察术后3天肺部并发症的发生率。墨尔本评估量表总计8项观察指标:胸片检查示肺实变或肺不张;血液中白细胞升高(>11.2 × 106/mL),并排除预防性使用抗感染药物,术后额外给予抗感染药物;体温>38℃;痰液微生物学检查显示有感染表现;脓痰状态不同于术前;无吸氧状态下SPO2<90%;专科医生明确诊断患有肺炎;ICU停留时间延长(肺部及食管手术超过1或2天或再次送往ICU)。上述8项观察指标中,出现 ≥ 4项为阳性者,可定义为发生了肺部并发症。
根据柏林定义判定术后ARDS的发生情况;呼吸困难急性发作超过1周或更短;双肺模糊不清与肺水肿一致;最低PEEP 5 cm H2O(或持续气道正压)条件下,动脉氧分压与吸入氧分数(PaO2/FiO2)的比值小于300 mmHg;医生通过获得的信息进行的最佳评估,发现用心力衰竭或液体超负荷不能完全做出解释。当患者满足上述条件,则定义为发生了ARDS。
1.6 统计方法
采用SPSS 22.0 统计软件进行数据分析。采用Kolmogorov- Smirnov检验进行数据正态性检验。计量资料呈正态性分布采用均数±标准差,非正态分布性资料采用中位数;分类变量采用数字和百分比表示。采用重复测量方差比较三组间不同时间点动脉血相关指标、呼吸功能相关指标的差异;采用χ2检验比较三组间分类资料的差异性(肺部并发症、ARDS发生率)。P<0.05认为差异有统计学意义。
2 结 果
2.1 一般情况
共75例入组,A组25例,B组25例,C组25例,3组患者性别、年龄、身高、体质量、ASA分级、术前肺功能、手术时长、麻醉时间、单肺时间、丙泊酚用量、瑞芬太尼用量之间比较,差异无统计学意义(P>0.05),见表1。
2.2 血流动力学
三组患者的HR、SBP、DBP和CVP比较,差异无统计学意义(P>0.05),见表2。
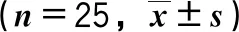
表1 三组患者术前一般资料、手术时间和单肺通气时间、药物使用
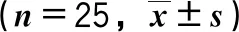
表2 三组患者各时点生命体征的比较
2.3 呼吸力学
与A组比较,B组、C组ΔVT均升高(P<0.05),B组与C组差异无统计学意义;三组Ppeak差异无统计学意义;与A组比较,B组、C组PEEP均增大(P<0.05),B组与C组差异无统计学意义(见表3)。
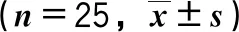
表3 三组患者各时点呼吸力学的比较
2.4 血气分析
与A组比较,T1-T3时B组、C组PaCO2降低(P<0.05),B组与C组差异无统计学意义;与T0时比较,T1-T3时三组PaO2、SVO2均降低(P<0.05);三组PH、SO2和HB差异均无统计学意义(P>0.05)(见表4)。
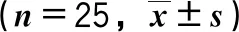
表4 三组患者各时点血气分析的比较
2.5 呼吸功能
与A组比较,T1-T3时B组、C组VD/VT减少(P>0.05);与A组比较,T1-T3时B组、C组Cdyn增大(P<0.05);与T0相比,T1-T3时三组Qs/Qt增加(P<0.05);与T0相比,T1-T3时三组PaO2/FiO2降低(P<0.05)(表5)。
表5 三组患者各时点呼吸功能的比较
2.6 炎症因子
与T0相比,T1-T3时三组IL- 6、IL- 8、TNF-α和sICAM- 1的浓度增多(P<0.05),但A组、B组低于C组(P<0.05)(见表6)。
表6 三组患者各时点炎症因子的比较
2.7 术中事件及术后并发症
A组有3例(12%)患者出现肺部并发症,2例(8%)患者发生ARDS;B组有2例(8%)患者出现肺部并发症,3例(12%)患者发生ARDS;C组有4例(16%)患者出现肺部并发症,4例(16%)患者发生ARDS,见表7。

表7 术后3天并发症 [n=25,n(%)]
3 讨 论
在OLV期间,由于肺内异常分流,患者容易出现低氧血症,发生率约为5%。VCV和PCV是OLV常使用的两种通气方式,VCV确保了稳定和精确的通气量,但较高的Ppeak可能导致气压伤和不均匀的气体分布。PCV可产生具有减速吸气流速模式的方形压力波形,导致吸入气均匀的弥散分布于肺组织,可避免局部过度扩张,具有降低气道压和降低肺内分流的优点,从而减少VILI的发生风险[6- 7]。与VCV相比在同等的Ppeak下PCV可以增加VT,有研究表明,在腹部或胸部大手术期间,在正常肺中,高VT的机械通气不会在3小时内增加肺部或全身的炎症反应[8]。课题组在前期研究的基础上,采取与VCV压力相同的个体化PCV模式。
本研究发现,在OLV后增加吸气流速后ΔVT量增加。我们分析原因:PCV模式受减速吸气流速和吸气时间的影响,增加吸气流速后,压力迅速达到预设压力值,吸气中后期,气流仍持续进入,VT增加。
增加吸气流速后降低了PaCO2,但对PH、PaO2、SO2、SVO2无明显影响,增大了肺动态顺应性,减少了死腔率,但对氧合和肺内分流改善不明显,与Kim SH等[9]建议VT为10~12 mL/kg以防止OLV期间VT在8 mL/kg以下的肺不张,OLV期间的高VT可以改善氧合的结果一致。分析其原因,增加吸气流速增加的部分潮气量所增加的气体交换的空间有限,CO2的弥散大于O2,因此氧合改善不明显。
IL- 6广泛被作为外科损伤和呼吸机致肺损伤的标志物[10- 11],炎症因子的激活及其在OLV过程中的级联反应是导致肺损伤的主要机制,TNF-α由肺泡巨噬细胞产生,通过释放炎症因子促进炎症反应[12]如IL- 6,导致肺组织损伤[13]。在机械通气诱导的炎症反应中,TNF-α和IL- 6的水平与肺损伤程度[13- 14]有关。sICAM- 1广泛存在于气管、支气管上皮细胞、平滑肌黏膜下,正常情况下不表达,当组织受到刺激或损伤时sICAM- 1表达有不同程度的上调[15]。本研究表明,TNF-α、IL- 6、IL- 8和sICAM- 1水平与A组、B组相比,C组更高。我们分析原因:根据压力波形图观察,C组达到预设压力时间较A、B组更短,肺泡短时间快速增大,气管及肺泡表面受到的气流较大,多种因素的影响下,造成肺上皮与内皮间屏障的遭到破坏。据报道,根据墨尔本评估量至少出现四项所确定的术后肺部并发症的发生率在胸外科中约为13%[16]到14.5%[17]。在本研究中A、B、C三组的术后肺部并发症的发生率分别为12%、8%、16%;术后肺部并发症或ARDS的发生率为20%、20%、32%;然而三组差异并无统计学意义。虽然上述数据表明C组炎症因子增加,但其是否能造成术后肺部并发症仍需进一步研究。
本研究仍存在一定的局限性。例如:样本量相对较小;患者接受了多种类型的手术;在血样中只检查了一小部分炎症因子,这可能构成系统偏倚。可进一步研究支气管肺泡灌洗液标本。三组的单肺通气过程中使用了高FiO2。这可能会使患者受到氧化应激肺损伤。我们没有纳入在OLV期间可能出现的内源性PEEP(PEEPi)的影响。虽然在TLV期间不发生PEEPi,但在OLV[18]期间可以出现2~6 cm H2O PEEPi,并且这个范围可以影响外部应用PEEP的效果。本研究是没有通过调节外部的PEEP来改变驱动压(ΔP),在对ARDS患者的回顾性研究中,每个单位的ΔP(1 cm H2O)与主要发病率的风险增加3.4%[19]。
综上所述,在PCV模式下通过增加吸气流速能增加VT,减少死腔率,促进CO2的交换,并且改善肺动态顺应性,但并不能很好的改善氧合及肺内分流。吸气流速50 mL/L在较小炎症反应的情况下达到上述改善呼吸功能和呼吸力学,可推荐应用于进行OLV患者。
