非肥胖型非酒精性脂肪性肝病患者胰岛素抵抗及胰岛β细胞功能的研究*
2020-01-03周夫黄春梅李素芬苏彩霞韦钰蘅陈燕玲黄志玲
周夫 黄春梅 李素芬 苏彩霞 韦钰蘅 陈燕玲 黄志玲
非酒精性脂肪性肝病(nonalcoholic fatty liver disease,NAFLD)是指除外酒精和其他明确的损肝因素所致的肝细胞内脂肪过度沉积,是一组获得性代谢应激相关性肝病[1]。NAFLD 已经成为最常见的慢性肝病,与肥胖的流行密切相关[2]。肥胖的存在,使胰岛素抵抗成为NAFLD 患者中普遍存在的现象,胰岛素抵抗被认为是NAFLD 的一个典型特征,NAFLD 是胰岛素抵抗和代谢综合征的一种肝脏表现[3-4]。然而,NAFLD 却并非总是发生于肥胖患者,文献[5]揭示,中国非肥胖人群的NAFLD 患病率为10.8%。流行病学调查观察到非肥胖NAFLD 患者亦存在胰岛素抵抗现象[6]。
胰岛素抵抗及胰岛β 细胞功能障碍是2 型糖尿病的重要病理生理机制[7]。NAFLD 是2 型糖尿病的危险因素。部分NAFLD 患者发展为2 型糖尿病,表明患者可能存在胰岛素抵抗和/或胰岛β 细胞功能缺陷。目前国内尚鲜见有关非肥胖的NAFLD 患者胰岛素抵抗及胰岛β 细胞功能的对照性随访研究。本研究通过对非肥胖NAFLD 患者及健康对照者进行18 个月随访,观察胰岛素抵抗指数、胰岛功能指数、早相胰岛素分泌指数的变化程度,旨在为2 型糖尿病的防治提供理论依据及新思路,现报道如下。
1 资料与方法
1.1 一般资料 选择2018 年1-6 月在南海区第四人民医院内分泌代谢科及体检中心就诊的非肥胖的患者32 例为NAFLD 组。诊断标准:《非酒精性脂肪性肝病防治指南(2018 年更新版)》中的超声诊断标准[8]。纳入标准:符合NAFLD 诊断标准;BMI 18.5~28 kg/m2。排除标准:其他原因导致的肝病;合并糖耐量减低或糖尿病;一级亲属罹患2 型糖尿病;依从性差,拒绝随访。另选取同期于本院体检的与病例组年龄、性别、暴饮暴食、少运动、吸烟相匹配的32 例健康人为对照组。本研究获得南海区第四人民医院伦理委员会批准,研究对象在参加试验前均已了解研究全过程,签署知情同意书。
1.2 方法 人体指标测量:受试者清晨排空膀胱后,固定专人使用同一测量工具测量并记录身高、体重,计算体重指数(BMI)=体重(kg)/身高2(m2)。生化指标测量、口服葡萄糖耐量试验(OGTT)及胰岛素释放试验(IRT):所有受试者夜间禁食12 h,次日清晨6:00-8:00 空腹采集肘静脉血立即送检,检测空腹血糖(FPG)、空腹胰岛素(fasting insulin,FINS)。空腹状态下行75 g OGTT 及IRT,检测糖负荷后30 min 血糖(PG30min)和胰岛素(INS30min)水平,计算稳态模型评估胰岛素抵抗指数(HOMA-IR)、稳态模型评估胰岛β 细胞功能指数(HOMA-β)与早相胰岛素分泌指数(ΔI30/ΔG30)。血糖采用葡萄糖氧化酶法检测,胰岛素采用化学发光法检测,HOMA-IR=FPG×FINS/22.5;HOMA-β=20×FINS/[(FPG-3.5)];ΔI30/ΔG30=(INS30min-FINS)/(PG30min-FPG)。随访18 个月后重复进行OGTT 及IRT,检测FPG、FINS、PG30min、INS30min,并比较HOMA-IR、HOMA-β 及ΔI30/ΔG30变化程度。
1.3 统计学处理 采用SPSS 17 软件对所得数据进行统计分析,应用Kolmogrov-Smirnov 检验方法检验各变量正态分布情况。符合正态分布的计量资料用()表示,组间比较采用独立样本t 检验,组内比较采用配对t 检验;不符合正态分布的计量资料用M(P25,P75)表示,组间比较采用Mann-Whitney U 检验,组内比较采用Wilcoxon 检验,计数资料以率(%)表示,比较采用χ2检验。以P<0.05 为差异有统计学意义
2 结果
2.1 两组基线资料比较 两组性别、年龄、暴饮暴食者比例、少运动者比例及吸烟者比例比较,差异均无统计学意义(P>0.05),具有可比性,见表1。
2.2 两组随访前BMI、血糖及胰岛素情况比较NAFLD 组BMI、FPG、FINS、PG30min及INS30min均高于对照组,差异均有统计学意义(P<0.05),见表2。
2.3 两组随访前后胰岛素抵抗及胰岛β 细胞功能比较 随访前后,NAFLD 组HOMA-IR 与ΔI30/ΔG30均高于对照组,差异均有统计学意义(P<0.05),而两组HOMA-β 比较,差异无统计学意义(P>0.05)。NAFLD 组随访前后HOMA-IR、HOMA-β 及ΔI30/ΔG30) 比较,差异均无统计学意义(P>0.05)。对照组随访前后HOMA-IR、HOMA-β 及ΔI30/ΔG30比较,差异均无统计学意义(P>0.05)。见表3。
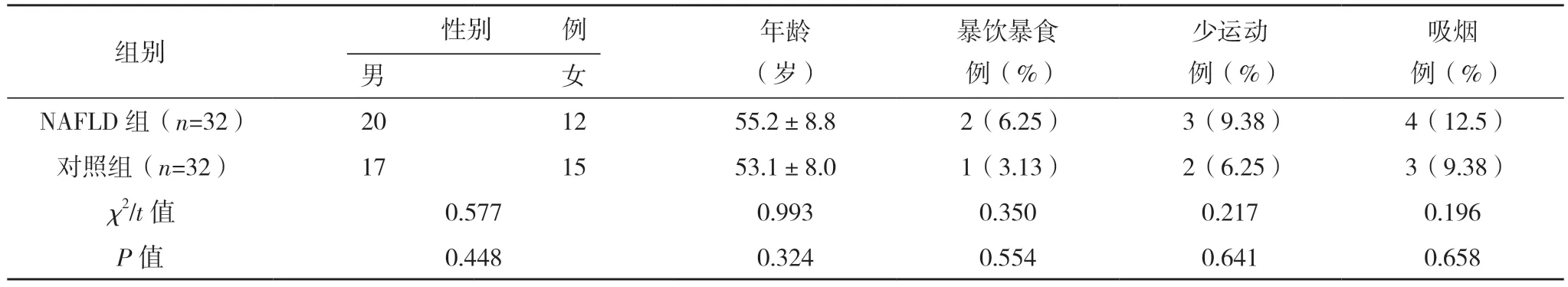
表1 两组基线资料比较
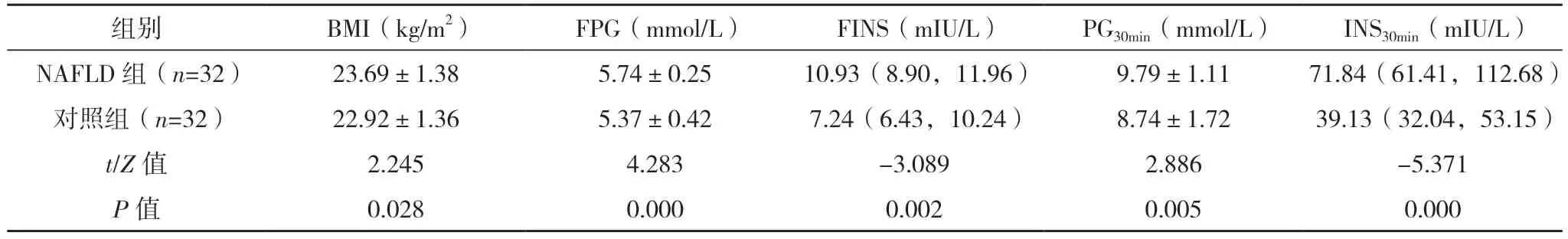
表2 两组随访前BMI、血糖及胰岛素情况比较
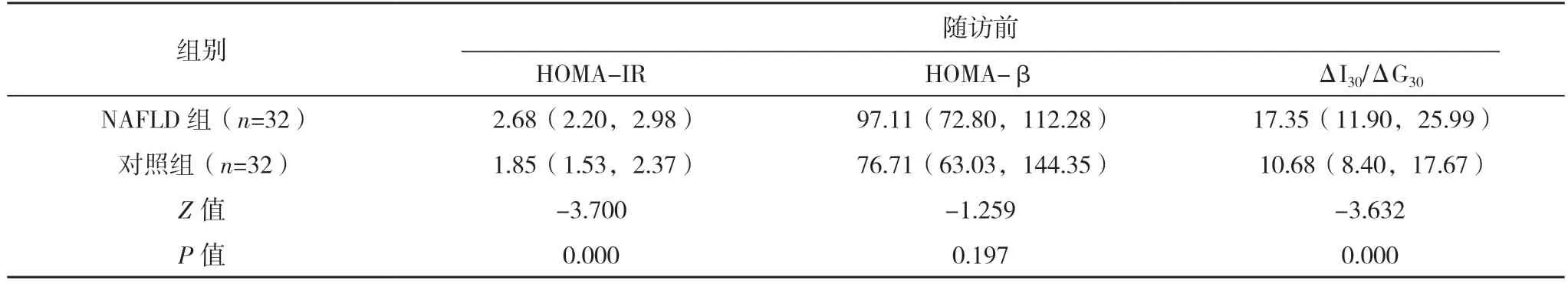
表3 两组随访前后胰岛素抵抗及胰岛β细胞功能比较[M(P25,P75)]
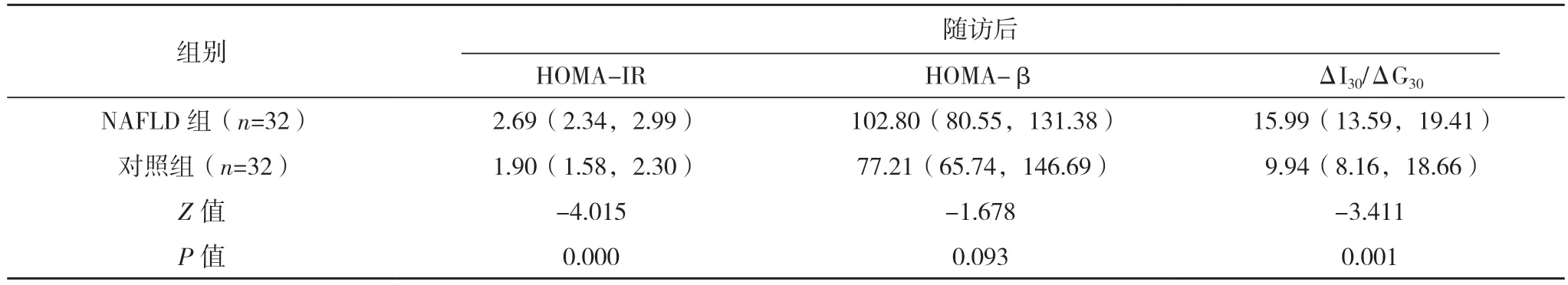
表3(续)
3 讨论
肝脏是人体能量代谢的中枢[9]。肝脏脂肪沉积与代谢异常的关系越来越密切,当前对NAFLD的关注已从肝病意义扩展到代谢意义。最近,国际专家共识小组提出用“代谢相关性脂肪性肝病(metabolic associated fatty liver disease,MAFLD)”来代替NAFLD[10-11]。
不健康的饮食、久坐不动以及吸烟等生活方式是导致NAFLD 大流行的主要原因,也是胰岛素抵抗的危险因素[12-14]。为控制选择性偏倚,本研究选取的两组在年龄、性别、生活习惯(如饮食、运动、吸烟)各个重要人群特征上均给予相应的匹配,具有可比性。本研究发现,非肥胖NAFLD 患者BMI、FPG、FINS、PG30min、INS30min、HOMA-IR、ΔI30/ΔG30均高于正常人群,与魏晨敏等[15]研究相似。随访前后,NAFLD 组HOMA-IR 与ΔI30/ΔG30均高于对照组(P<0.05),提示NAFLD 的病理生理机制类似于2 型糖尿病前期;尽管是非肥胖人群,但NAFLD 患者BMI 高于正常人群。文献[16]显示,BMI 增加是NAFLD 发病的危险因素。肝脏内脂肪的沉积可能是导致非肥胖NAFLD 患者发生胰岛素抵抗的原因。文献[17]指出,虽然体脂的绝对数量对胰岛素敏感性有影响,但是腹腔内脂肪与胰岛素抵抗的联系更密切,并且血糖、胰岛素与胰岛素抵抗的联系均强于总脂肪和胰岛素抵抗的联系。胰岛素抵抗既是NAFLD 发病的核心机制,亦是2 型糖尿病发病的核心机制。胰岛素抵抗要早于2 型糖尿病的发病而出现,而且长期存在[17]。胰岛素抵抗最早前兆为餐后高胰岛素血症,继而空腹高胰岛素血症,最后为高血糖[18]。多数研究认为胰岛素抵抗较胰岛素分泌缺陷更早发生,当胰岛素分泌不足时才发生糖尿病[18]。两组HOMA-β 比较,差异无统计学意义(P>0.05),说明非肥胖NAFLD 患者稳态模型下胰岛β 细胞功能尚未受损,可能与疾病早期相关。
本研究显示,随访期内胰岛素抵抗及胰岛功能的变化进展缓慢。随访18 个月后,非肥胖NAFLD患者与正常人群的HOMA-IR、HOMA-β 以及ΔI30/ΔG30均无显著变化。文献[19]指出,胰岛素抵抗在2 型糖尿病病程开始就已进入平台期,且有报道显示,β 细胞功能在糖尿病发病前13 年内保持稳定[20]。
本研究的局限性:(1)受单中心研究、非肥胖NAFLD 发病率不高、排除标准多等诸多因素影响,本研究纳入样本量过少;(2)样本量过少,可致偏倚较大以及混杂因素难以控制;(3)随访时间过短,难以准确、客观反映胰岛素抵抗及胰岛功能发展的过程。期待加大样本量,延长随访时间加以验证。
综上所述,本研究表明非肥胖型NAFLD 患者存在胰岛素抵抗,稳态模型下胰岛β 细胞功能尚未受损,早相胰岛素分泌功能增强。短期内胰岛素抵抗及胰岛功能的变化进展缓慢。
