不同分子量辛烯基琥珀酸蜡质玉米淀粉酯的制备及其性能
2019-11-28,,*
,,*
(1.浙江师范大学化学与生命科学学院,浙江金华 321000;2.浙江省农业科学院食品科学研究所,浙江省果蔬保鲜与加工技术研究重点实验室,农业农村部果品产后处理重点实验室,浙江杭州 310021)
淀粉作为最重要的农业加工品之一,被广泛应用于食品、制药和轻纺化工等多个领域,但天然淀粉包括蜡质玉米淀粉在内,因性能局限性难以直接满足各领域的需求[1]。辛烯基琥珀酸淀粉酯(octenyl succinic anhydride modified starch,简称OSAS),是淀粉与辛烯基琥珀酸酐(OSA)经酯化反应得到的改性产物,具有油水两亲的乳化性质,是近几年国内外变性淀粉研究与开发的热点之一[2-4]。OSAS具有安全无毒、生物相溶性好、体内可降解等优点[5],在食品工业中常用作乳化剂[6-8]、稳定剂[9]和微胶囊壁材[10]等。
淀粉与OSA发生酯化反应,生成的OSAS大多属于高黏度型[11],可适用于工业生产应用中一些高黏度需求的产品,如在调和色拉油中作为增稠稳定剂等。但是,对于一些黏度要求低的产品,如微胶囊类制品,就需要OSAS在保持原有优良性能的基础上具有更低的黏度[12]。因此,为了满足这些产品的生产与应用需求,需将制得的高黏度OSAS进行降解,或者将天然淀粉原料先降解处理再进行酯化[13-16]。本文采用水相法制备淀粉酯,再通过β-淀粉酶对其降解,将OSAS大分子降解成不同相对分子质量的小片段,通过物性分析和结构表征,探究其分子量与理化性质间的相互关系,以期为OSAS在工业生产中的更广泛应用及蜡质玉米淀粉深加工提供一定的理论参考。
1 材料与方法
1.1 材料与仪器
蜡质玉米淀粉 甘肃昆仑生化有限责任公司;辛烯基琥珀酸酐OSA(纯度≥99.5%) 山东济南浩化实业有限责任公司;葡聚糖系列标准品(分子量分别为13050、21400、41100、84400、133800和200000 Da) 中国药品生物制品检定所;中温β-淀粉酶(酶活70万U/mL) 上海源叶生物科技有限公司;无水乙醇、盐酸和氢氧化钠 分析纯,上海国药集团化学试剂有限公司。
ZHW-02C型全温振荡培养箱 太仓市华美生化仪器厂;SCIENTZ-18N型冷冻干燥机 宁波新芝生物科技股份有限公司;UV-1800型紫外分光光度计 日本岛津公司;R/S plus型黏度计 BROOKFIELD美国博勒飞公司;LXJ-ⅡB型离心机 上海安亭科学仪器厂;TM3000型台式扫描电子显微镜 日本日立公司;Agilent 1100型高效液相色谱仪(G1362A示差折光检测) 安捷伦科技有限公司;XMTD-8222型电热恒温水浴锅 上海精宏实验设备有限公司;DHG-9146A型电热恒温鼓风干燥箱 上海精宏实验室备有限公司; BS200S-WE1型电子天平 余姚金诺电子天平仪器有限公司;VERTEX 70型傅里叶红外光谱仪 BRUKER德国布鲁克公司;FE20型pH计 梅特勒-托利多仪器(上海)有限公司;SHZ-D型循环水真空泵 杭州明远仪器有限公司。
1.2 实验方法
1.2.1 辛烯基琥珀酸蜡质玉米淀粉酯(OSAS)制备 称取100 g蜡质玉米淀粉置于去离子水中,配制成质量分数为35%的乳液,然后用质量分数2% NaOH(溶液)将乳液pH调至8.5,滴加无水乙醇稀释5倍的OSA溶液3 g,控制2 h内加完,于恒温35 ℃水浴中反应3 h(反应过程中pH保持8.5恒定)。反应结束,用质量分数为2%盐酸将混合物pH调至6.5后,将混合物过滤,得滤饼,滤饼再用去离子水和95%乙醇反复洗涤3次后,置于50 ℃烘箱中平衡24 h,粉碎过100目筛,备用。
1.2.2 OSAS酶解 称取10 g OSAS(干基)溶于去离子水中,配置成质量分数为35%乳液,用质量分数为2%盐酸将乳液pH调至5.0。沸水浴搅拌充分糊化1 h,冷却至55 ℃后,分别加入质量分数为0、0.5%、1.0%、1.5%、2.0%(占干OSAS质量百分分数)的β-淀粉酶,于55 ℃、120 r/min振荡培养箱中酶解2 h。酶解结束后,沸水浴中加热30 min灭酶,冷冻干燥得到酶解OSAS。
1.2.3 OSAS分子量测定 样品分子量由凝胶渗透色谱法(GPC)测定[17]。色谱条件为:Agilent 1100型高效液相色谱系统,采用TSK G3000 PWxl凝胶柱(300×7.8 mm,7 μm),流动相为超纯水,过0.22 μm膜并超声脱气,进样量20 μL,流速1.0 mL/min,检测器温度50 ℃,柱温70 ℃。称取15 mg酶解样品于5 mL超纯水中,沸水浴充分溶解,趁热过0.22 μm膜进行分子量分布测定。
1.2.4 黏度测定 准确称取 1.0 g样品(绝干)置于100 mL去离子水中,适当搅拌配制成乳液,倒入200 mL高脚烧杯中于常温进行表观黏度的测定,使用一号转子,速度选择40 r/min。
1.2.5 糊透明度测定 准确称取0.5 g样品(绝干)置于50 mL去离子水中,沸水浴加热糊化并保温 20 min,冷却至室温后以蒸馏水为空白,使用分光光度计在200~800 nm波长范围内进行全波段扫描,选择650 nm处得到的透光率来衡量样品糊透明度。
1.2.6 凝沉性测定 准确称取 0.5 g样品置于50 mL 去离子水中,沸水浴中加热糊化并保温20 min,冷却至室温后精确量取25 mL样品糊液置于具塞比色管中,常温放置观察分层情况。每隔24 h测定并计算上清液的高度与体积,并按以下公式计算凝沉性(retrogradation property,简称RP,%):
式中,V1为样品糊液体积,mL;V2为上清液体积,mL。
1.2.7 膨胀度测定 准确称取3.0 g样置于150 mL去离子水中,30 ℃恒温水浴30 min且4000 r/min离心30 min[18]。弃去上清液,称量沉积物质量,按公式计算膨胀度(swelling degree,简称SD,%):
式中,m1为样品干基质量,g;m2为离心后沉积物质量,g。
1.2.8 FT-IR分析 红外光谱仪的波长范围设定为400~4000 cm-1。分析前,干燥处理好的样品需与适量KBr混合研磨均匀后进行压片处理。
1.2.9 SEM分析 将样品均匀地撒在有胶性物质的样品台上进行镀金处理,于扫描电子显微镜样品室中观察样品形貌并拍照。放大倍数为1800倍和5000倍。
1.3 数据处理
所有实验均重复3次,采用Excel 2010和SPSS 17.0软件进行数据处理与分析,不同试验组数据间差异显著范围均取小于0.05(P<0.05)。
2 结果与分析
2.1 加酶量对OSAS分子量的影响
表1给出了不同分子质量葡聚糖标品所对应的保留时间。图1给出了酶添加量与OSAS分子量对应关系。高分子量辛烯基琥珀酸玉米淀粉酯标记为L-OSAS(β-淀粉酶添加量为0),较大分子量辛烯基琥珀酸玉米淀粉酯标记为Lr-OSAS(β-淀粉酶添加量0.5%),中分子量辛烯基琥珀酸玉米淀粉酯标记为M-OSAS(β-淀粉酶添加量1.0%),较小分子量辛烯基琥珀酸玉米淀粉酯标记为Sr-OSAS(β-淀粉酶添加量1.5%),小分子量辛烯基琥珀酸玉米淀粉酯标记为S-OSAS(β-淀粉酶添加量2.0%)。

表1 不同分子质量葡聚糖标准品保留时间Table 1 Retention time of glucan standardsat different molecular weights

图1 加酶量对OSAS分子量的影响Fig.1 Effect of amount of enzymeson the molecular weight of OSAS注:不同字母表示差异显著(P<0.05)。图3、图5同。
以葡聚糖标准品体积排阻色谱图中的保留时间tR为横坐标,lgMt为纵坐标进行作图,从而得到OSAS的相对分子质量标准曲线:y=-0.3977x+9.7452,R2=0.9952。由图1可以看出,经不同加酶量酶解处理后得到5种OSAS样品,其分子量在1.0×104~2.0×105Da范围内呈梯度变化,随加酶量的增加OSAS分子量显著下降(P<0.05)。
2.2 分子量对 OSAS物理性质的影响
2.2.1 分子量对OSAS黏度的影响 OSAS加热糊化时黏度增大,搅拌困难,加入β-淀粉酶后黏度明显下降,图2为不同分子量OSAS的黏度测定结果。

图2 不同分子量对OSAS黏度的影响Fig.2 Effects of different molecular weightson the viscosity of OSAS
图2表明,随着分子量的减小,OSAS的黏度在0.0035~0.0010 Pa·s呈现逐渐下降的趋势,尤其Lr-OSAS比L-OSAS黏度下降明显,说明酶解这一处理方法能明显降低OSAS的黏度。其实质是β-淀粉酶酶解切断了淀粉间部分相互作用的糖苷键,导致淀粉链的平均长度减短[12]。
2.2.2 分子量对OSAS糊透明度的影响 不同分子量OSAS糊透明度的测定结果见图3。淀粉颗粒糊化后,其透光度越好,透明度就越高。
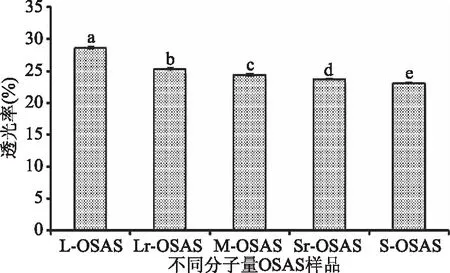
图3 不同分子量对OSAS糊透明度的影响Fig.3 Effects of different molecular weightson the transparency of OSAS pastes
淀粉糊化时分子进行重新排列,其相互缔合程度是影响淀粉糊透明度的重要因素。如果分子间或分子内的缔合作用较大,则会引起光的折射,使透光度减弱,即透明度下降;淀粉中支链淀粉含量越高,分子间缔合作用越小,越不易发生分子间聚合,则其透明度越高[18-19]。图3数据显示,随着OSAS分子量的降低,即随其支链淀粉含量的降低,透光率从L-OSAS的28.6%减小至 S-OSAS的23.1%,5种样品的糊透明度显著降低。
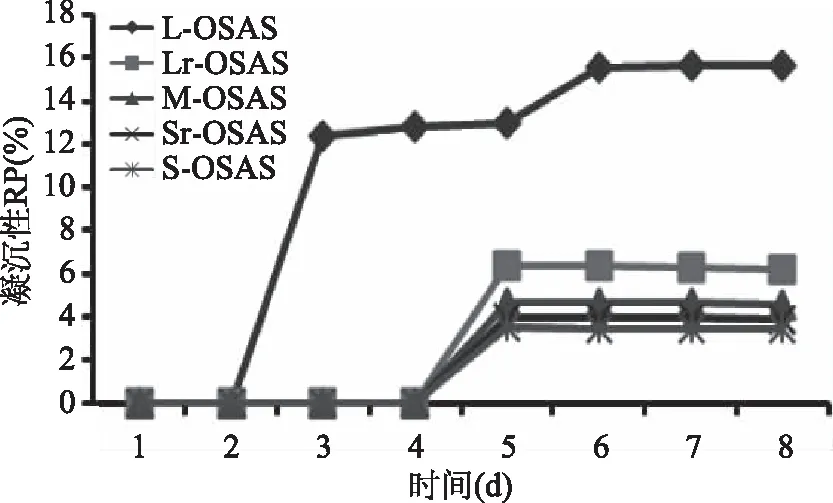
图4 不同分子量对OSAS凝沉性的影响Fig.4 Effects of different molecular weightson the retrogradation property of OSAS
2.2.3 分子量对OSAS凝沉性的影响 由图4可知,Lr-OSAS、M-OSAS、Sr-OSAS、S-OSAS的凝沉性均明显低于L-OSAS。淀粉颗粒加热糊化后,因水分子和热作用,原本有序的淀粉分子会变得杂乱无序;淀粉糊静置降温后,因分子势能的作用,高能态的无序状态将逐步趋于低能态的有序化,淀粉糊的凝沉是淀粉分子从无序状态到有序重排的老化过程[20]。在β-淀粉酶作用下,淀粉链间糖苷键被破坏,导致淀粉平均链长减短,且生成更多短链,分子势能降低。因此,酶解处理后,分子量的减小会较大程度地削弱淀粉糊的老化作用,凝沉性降低。
2.2.4 分子量对OSAS膨胀度的影响 玉米淀粉颗粒浸入水中会吸水进行有限的可逆膨胀,而膨胀度的大小能够间接地表示淀粉内部键结合的程度。不同分子量OSAS膨胀度测定结果如图5所示。

图5 不同分子量对OSAS膨胀度的影响Fig.5 Effects of different molecular weightson swelling degree of OSAS
由图5可以看出,Lr-OSAS、M-OSAS、Sr-OSAS、S-OSAS的膨胀度均小于L-OSAS,且其膨胀度随着分子量的降低也在2.4~2.1范围内下降。有研究曾发现淀粉的膨胀主要是支链淀粉的特性,而直链淀粉起到稀释剂的作用,其含量增加不利于淀粉的膨胀[18-21]。OSAS在β-淀粉酶酶解处理过程中,支链淀粉分子会部分降解,导致直链淀粉含量增大、支链淀粉含量降低,因此膨胀度减小。
2.3 分子量对 OSAS结构性质的影响
2.3.1 分子量对OSAS的 FT-IR影响 由图6可以看出,在全部样品FT-IR特征光谱区域内,925、1080和1155 cm-1等处都有非常明显的因C-O键伸缩和振动而产生的吸收峰,1649 cm-1处是因烯醇式C=O键伸缩振动产生的特征峰,2922 cm-1处是因C-H键伸缩振动产生的特征峰,3390 cm-1处是一个O-H键的伸缩振动的较大特征峰。与蜡质玉米原淀粉光谱比较,5种OSAS的光谱中,均分别在1735 cm-1处出现新的特征峰,原因是OSA与淀粉发生酯化反应,经酯化变性处理后的淀粉引入了新的酯键与葡萄糖上羟基相连,因而检测到酯羰基的特征峰[22-23]。
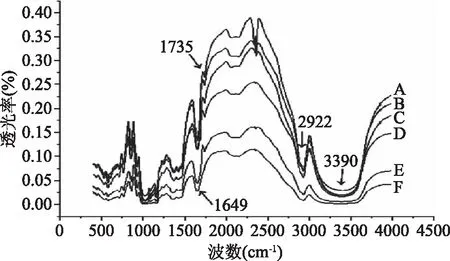
图6 不同分子量OSAS的 FT-IR光谱Fig.6 FT-IR spectra of OSASwith different molecular weights 注A:Lr-OSAS;B:M-OSAS;C:Sr-OSAS;D:S-OSAS;E:L-OSAS;F:蜡质玉米淀粉。
另外,除波数 1735 cm-1外,蜡质玉米原淀粉与5种OSAS样品的FT-IR吸收光谱基本相同;除特征峰吸收强度因样品分子量的不同而差异明显外,5种OSAS样品的光谱图基本相同。综上所述,蜡质玉米原淀粉和OSA发生了取代反应,生成的OSAS中除引入OSA外,酯化变性和酶法降解处理未引入其他成分[24]。
2.3.2 不同分子量OSAS 的SEM分析 由图7可见,蜡质玉米淀粉颗粒表面光滑,而L-OSAS颗粒表面明显因凹陷而粗糙,但并未产生明显裂痕,说明OSA基团与蜡质玉米淀粉分子酯化作用主要发生在淀粉颗粒的表面[24-25]。而M-OSAS图中,其颗粒由规则的椭球形改变为不规则状,推测是由于β-淀粉酶酶解作用导致。

图7 不同分子量OSAS的SEM照片Fig.7 SEM photos of OSAS with different molecular weights 注:A1和A2分别为蜡质玉米淀粉1800倍和5000倍放大;B1和B2为L-OSAS1800倍和5000倍放大;C1和C2为M-OSAS1800倍和5000倍放大。
3 结论
采用水相法制备得到辛烯基琥珀酸蜡质玉米淀粉酯(OSAS),利用中温β-淀粉酶酶解处理,得到5种不同相对分子质量的OSAS,经凝胶渗透色谱法测得其分子量在1.0×104~2×105Da范围内呈梯度减小。物理性质测定结果表明,OSAS的黏度、糊透明度、凝沉性和膨胀度均随其分子量减小而降低;结构表征结果表明,OSA基团与蜡质玉米淀粉分子酯化作用主要发生在淀粉颗粒的表面,酶解处理不会引入其他基团。本研究初步探究了OSAS分子量与其理化性质间的相互关系,能够为其更广泛应用提供一定的理论参考。
