超高效液相色谱法同时测定复方丹参方中4种成分及其在大鼠体内药动学研究*
2019-10-30贾田芊黄喆崔春利李兴欢任丽唐志书史亚军孙静
贾田芊,黄喆,崔春利,李兴欢,任丽,唐志书,史亚军,孙静
(1.陕西中医药大学药学院,咸阳 712046;2.西安高新医院放射科,西安 710075)
复方丹参方是活血化瘀、理气止痛的经典方剂,该方由丹参、三七、冰片组成,用于胸中憋闷、心绞痛,是治疗心血管病最常用的中成药[1-3]。目前临床应用剂型有片剂、滴丸剂、颗粒剂、口服液、胶囊剂和气雾剂等十余种。复方丹参方主要成分[3-5]有来自丹参的丹酚酸类,如丹酚酸B、丹参素、原儿茶醛等和丹参酮类,如丹参酮ⅡA、丹参酮及隐丹参酮等;来自三七中皂苷类,如人参皂苷Rg1、Rb1及三七皂苷R1等和黄酮类;另有来自冰片的龙脑类。
近年来,对复方丹参方质量及复方中有效成分的药动学[4-8]研究较多,常以方中丹参或三七为指标进行研究,鲜有将丹参、三七中主要有效成分于同一指纹图谱中展现出来。在前人研究的基础上,笔者建立超高效液相色谱(UPLC)法在同一色谱条件下快速、方便检测复方丹参方中丹参、三七中主要有效成分,并进行整合药动学研究。本实验在同一色谱条件下对大鼠血浆中丹酚酸B、人参皂苷Rg1、三七皂苷R1、丹参酮ⅡA 的药动学特征进行研究,并运用复方丹参片与复方丹参滴丸45 min时在体内的吸收情况来验证该色谱条件及处理方法的可行性,根据4种成分在体内的吸收量可为药材、制剂的质量研究提供新的依据,为复方丹参方体内指纹图谱的建立提供参考。
1 材料
1.1动物 雄性SPF级SD大鼠,体质量(200±20) g,均来自成都达硕实验动物有限公司,实验动物生产许可证号:SCXK(川)2015-030。大鼠饲养室温度保持20~25 ℃,相对湿度50%~65%,并在封闭饲养室采用光照定时装置,提供适当(光照12 h、黑暗12 h或光照14 h、黑暗10 h)昼夜光变化周期。
1.2仪器 Waters I-class超高效液相色谱仪(美国Waters公司),双波长紫外检测器(美国Waters公司),U-3000高效液相色谱仪(美国赛默飞世尔公司),486紫外检测器(美国赛默飞世尔公司),KH-400KDE高功率数控超声波清洗器(昆明市超声仪器有限公司),MS205DU电子天平(北京赛多利斯仪器系统有限公司,感量:0.1 mg),EYELA MG-2200氮吹仪(上海赛默生物科技发展有限公司),Allegra64R冷冻离心机(美国贝克曼库尔特有限公司),SK-2涡旋振荡器(上海奥然科贸有限公司)。
1.3试药 三七皂苷R1(批号:110745-201318,含量:95%)、人参皂苷Rb1(批号:110704-201424 含量:94%)、人参皂苷Rg1(批号:110703-201530,含量:92%);丹参酮ⅡA(批号:110766-201520 ,含量:99%)、丹酚酸B(批号:111562-201514,含量:94% )均来自中国食品药品检定研究院。复方丹参片(广州白云山制药股份有限公司,批号:20160821)、复方丹参滴丸(天士力制药集团股份有限公司,批号:20160511);丹参(批号:20160721)、三七(批号:20160507)、冰片均购于陕西兴盛德药业有限责任公司,均由陕西中医药大学药学院胡本祥教授鉴定,分别为丹参、三七、冰片药材。甲醇、乙腈为色谱纯,磷酸、盐酸为分析纯,水为娃哈哈纯净水。
2 方法与结果
2.1色谱条件 色谱柱Waters Acquity UPLC C18(50 mm×2.6 mm,1.7 μm);流动相为0.02%磷酸(A)和含0.02%磷酸的80%乙腈(B ),梯度洗脱;柱温:40 ℃;流速:0.42 mL·min-1;检测波长:203 nm;进样量:3 μL;流动相梯度:0~0.8 min,90% (A)~80%(B),4~10 min 75%(A)~25%(B),10 min 95%(B)。
2.2复方丹参方提取物的制备 精密称取丹参450 g、三七150 g、冰片7.5 g,丹参饮片加乙醇回流1.5 h,滤过,得滤液一;药渣加50%乙醇回流1.5 h,滤过,得滤液二;药渣加水煎煮2 h,滤过,得滤液三;三七粗粉加70%乙醇回流1.5 h,滤过,得滤液四;滤渣加水煎煮2 h,滤过,得滤液五;合并滤液一、二、三、四、五,减压干燥为粉末,加入冰片研匀备用。
2.3对照品溶液的制备 分别取丹酚酸B、人参皂苷Rg1、三七皂苷R1、丹参酮ⅡA 对照品适量,精密称定,加甲醇制成每毫升含丹酚酸B 60 μg、人参皂苷Rg1 0.2 mg、三七皂苷R1 0.05 mg及丹参酮ⅡA 40 μg的混标溶液及单标溶液,即得。
2.4给药与血浆采集 大鼠适应性饲养1周,实验前禁食不禁水12 h,复方丹参方提取物按照“2.2”项方法制备,按10 g·kg-1提取物(丹酚酸B:598 mg·kg-1,丹参酮ⅡA:110 mg·kg-1,三七皂苷R1:121 mg·kg-1,人参皂苷Rg1:300 mg·kg-1,冰片:500 mg·kg-1)溶于羧甲基纤维素钠中灌胃,每组平行灌胃大鼠12只,每个采血点(5,10,15,30,45,60,90,120,240,360,480,600 min)对应1只大鼠进行眼眶采血,平行5组,采血液4 mL于肝素抗凝离心管中,后进行离心,取血浆800 μL,-20 ℃保存。
2.5血浆中丹酚酸B、人参皂苷Rg1、三七皂苷R1、丹参酮ⅡA测定样品处理 取血浆800 μL,加入乙腈2.5 mL,涡旋震荡10 min,15 000 r·min-1离心(r=9.5 cm)10 min,吸取上清液,37 ℃氮气吹干,加70%甲醇200 μL复溶,15 000 r·min-1离心10 min,取上清液,备用。
2.6方法学考察
2.6.1专属性考察 取大鼠空白血浆,加入含丹酚酸B 60 μg·mL-1、人参皂苷Rg1 0.2 μg·mL-1、三七皂苷R1 0.05 μg·mL-1、丹参酮ⅡA 40 μg·mL-1的混合对照品300 μL,按“2.5”项处理,按“2.1”项进行检测,色谱图见图1,结果可见4种成分与相邻成分的分离度良好,大鼠体内内源性物质不影响所选指标的检测,该方法专属性良好。

A.混合标准品;B.空白血浆;C.空白血浆加混合对照品;D.给药后45 min血浆样品;1.丹酚酸B;2.三七皂苷R1;3.人参皂苷Rg1;4.丹参酮ⅡA
图1 大鼠血浆HPLC色谱图
A. mixed standard; B. blank plasma; C. blank plasma spiked with mixed standard; D. plasma sample from a patient 45 min after medication;1.salvianolic acid B;2.notoginsenoside R1;3.ginsenoside Rgl;4.tanshinone ⅡA
Fig.1HPLCchromatogramofplasmasamplefromrats
2.6.2线性范围考察 取4种成分储备液适量,用甲醇逐级稀释,加入空白大鼠血浆,使其混标中丹酚酸B、人参皂苷Rg1、三七皂苷R1、丹参酮ⅡA制得20,50,100,300,500,800,1000 ng·mL-1质控样品。将上述质控样品按“2.3”项方法处理,按“2.1”项条件下测定,以被测物质的峰面积(Y)对其在血浆中的浓度(X)进行回归分析,所得4种成分的标准曲线方程、线性范围、相关系数及检测限和定量限见表1。表明丹酚酸B、人参皂苷Rg1、三七皂苷R1、丹参酮ⅡA在线性范围内相关性良好。
2.6.3精密度与准确度 取空白血浆,加入混合对照品制成高、中、低浓度质量控制样品,按“2.5”项方法处理,每个浓度连续进样5次,连续5 d,通过标准曲线计算含量,计算日内与日间精密度及准确度,结果见表2。结果表明Waters I-class超高效液相色谱仪的精密度良好。
表1 血浆中4种成分标准曲线和线性范围
Tab.1Standardcurveandlinearityrangeoffourcomponentsinplasma

成分回归方程线性范围/(ng·mL-1)相关系数(r)检测线定量限(ng·mL-1)三七皂苷R1Y=7.99X+25.520~10000.990 03.2010.92人参皂苷Rg1Y=545.76X-557420~10000.995 14.5913.35丹酚酸BY=83.12X-30120~10000.991 05.1016.22丹参酮ⅡAY=2496.92X+76420~10000.990 12.516.90
2.6.4基质效应与提取回收率 首先,按照对照品的配制方法分别配制高、中、低浓度对照品溶液,按“2.1”项条件下测定并记录4种成分的峰面积A1、B1、C1、D1,每个浓度点平行测定5次。其次,取空白血浆按照“2.5”项方法处理后加入上述4种成分高、中、低浓度对照品溶液,测得4种成分峰面积分别为A2、B2、C2、D2,每个浓度点平行测定5次。然后,按照样品处理方法直接测定高、中、低浓度的4种成分的对照品溶液,测定4种成分的峰面积分别为A3、B3、C3、D3,每个浓度点平行测定5次。最终,基质效应为峰面积A2、B2、C2、D2与峰面积A1、B1、C1、D1之比,高、中、低浓度平均基质效应分别为三七皂苷R1:102.5%,110.3%,108.1%;人参皂苷Rg1:97.8%,95.9%,100.6%;丹酚酸B:99.2%,96.2%,94.8%,丹参酮ⅡA:101.2%,105.1%,101.8%;提取回收率为A3、B3、C3、D3与A2、B2、C2、D2之比,高、中、低浓度平均提取回收率分别为三七皂苷R1:88.3%,86.1%,81.9%;人参皂苷Rg1:91.3%,89.9%,87.2%;丹酚酸B:93.7%,90.3%,91.2%;丹参酮ⅡA:101.2%,103.1%,102.5%。结果说明,基质效应不影响4种成分测定且回收率结果良好。
表2 大鼠血浆中4个指标成分日内和日间精密度及准确度测定结果
Tab.2Inter-andintra-dayprecisionandaccuracyoffourmakercomponentsinratplasmang·mL-1,n=5

成分加入量日内平均测得量精密度(RSD)准确度(RE)%日间平均测得量精密度(RSD)准确度(RE)%三七皂苷R12019.144.09-4.3019.115.34-4.4510094.285.32-5.7294.176.31-5.831000948.906.03-5.11948.106.23-5.20人参皂苷Rg12018.775.21-6.1318.588.11-7.1210096.304.21-3.7096.675.34-3.331000955.006.50-4.50948.317.32-5.17丹酚酸B2019.116.66-4.4718.966.99-5.19100103.495.673.49102.228.232.221000946.914.21-5.31940.403.13-5.96丹参酮ⅡA2018.666.50-6.6618.586.68-7.0910095.895.06-4.1194.795.55-5.211000956.914.67-4.31938.115.01-6.19
2.6.5稳定性实验 精密吸取血浆200 μL,加入高、中、低浓度丹酚酸B、人参皂苷Rg1、三七皂苷R1、丹参酮ⅡA对照品溶液,按照“2.5”项方法进行处理,制成高、中、低浓度质控样品,在5种条件下进行处理: ①放于室温中6 h;②冻融3次;③-20 ℃储存30 d;④-80 ℃储存30 d;⑤血浆处理后4 ℃存放2,8,12 h,结果可得4种成分的RSD<6.2%,表明血浆样品在5种条件下稳定性良好。
2.7血浆的药动学研究 将血浆样品按“2.4”项方法采集,按“2.5”项方法处理,按“2.1”项条件下测定,记录4种成分的峰面积,代入回归方程中,计算4种成分随时间变化体内吸收浓度。所得数据用DAS软件进行非房室模型拟合,计算药动学参数。得出各被测成分平均血药浓度-时间曲线,见图2,主要药动学参数见表3。
2.8复方丹参片与复方丹参滴丸中4种成分45 min时体内含量测定 将复方丹参片与复方丹参滴丸分别研成粉末,用羧甲基纤维素钠制成混悬液,按两种取药量方式进行给药,①取等量复方丹参片与复方丹参滴丸各0.6 g;②按照复方丹参片与滴丸日服用量,取高(片剂:9片、滴丸:30丸)、中(片剂:6片、滴丸:20丸)、低(片剂:3片、滴丸:10丸)剂量进行灌胃,根据权重可得在45 min时4种成分吸收峰均较佳,故以此图谱为标准图谱进行45 min时灌胃复方丹参片与复方丹参滴完体内含量计算。按照“2.4”项采血,按照“2.5”项处理方法,按照“2.1”项色谱条件进行含量测定,结果见表4。通过同时测定复方丹参片与复方丹参滴丸中4种有效成分含量,进一步运用复方丹参片与复方丹参滴丸来验证该色谱条件及处理方法的可行性,并为两种复方丹参方制剂的质量检测提供依据,为复方丹参片与复方丹参滴丸有效成分在大鼠体内含量特征提供参考。
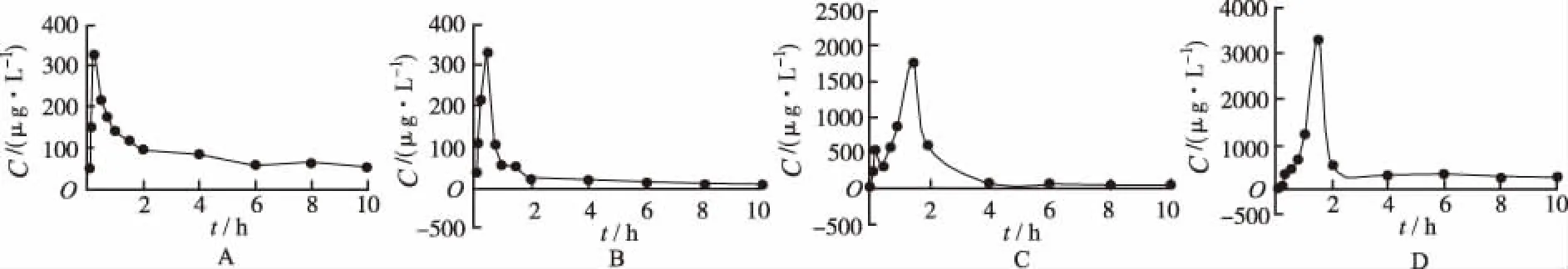
图2 大鼠灌胃给予复方丹参方后三七皂苷R1 (A)、人参皂苷Rg1 (B)、丹酚酸B (C)、丹参酮ⅡA(D)在血浆中药物浓度-时间曲线(n=5)
Fig.2Meanplasmaconcentration-timeprofileofnotoginsenosideR1(A)、ginsenosideRg1(B)、salvianolicacidB(C)andtanshinoneⅡA(D)inratplasmaafteroraladministrationofcompoundDanshenpreparation(n=5)
表3 大鼠灌胃给予复方丹参方后4种成分在血浆中主要药动学参数
Tab.3MainplasmapharmacokineticsoffourcomponentsinratplasmaafteroraladministrationofcompoundDanshenpreparation


成分AUC(0-t)AUC(0-∞)(μg·h·L-1)tmax/hCmax/(μg·L-1)MRT(0-t)/ht1/2z/hVz/(L·kg-1)Cl/L/(h·kg-1)丹酚酸B2 848.7±1 021.33 574.3±577.71.5±01 784.0±322.32.3±0.58.8±0.72 122.6±578.3167.3±45.1人参皂苷Rg11 957.6±981.52 297.2±832.50.5±0.11 811.0±452.62.5±0.24.7±1.3887.9±302.5130.6±56.7三七皂苷R1886.5±311.81 615.4±409.10.3±0330.0±112.73.9±0.49.1±1.2986.6±541.274.9±70.1丹参酮ⅡA5 459.9±2011.616 161.7±1769.91.5±03 300.0±1223.63.5±0.125.9±1.5255.1±77.56.8±4.2
表4 复方丹参片与复方丹参滴丸中4种成分在大鼠体内45 min时含量
Tab.4ContentoffourcomponentsofcompoundDanshentabletsandcompoundDanshendrippingpillsinRatsafter45mintreatment

剂型给药量成分测得量/ngRSD/%片剂0.6 g三七皂苷R115.195.15丹酚酸B75.036.11人参皂苷Rg122.114.31丹参酮ⅡA47.743.883片三七皂苷R128.226.87丹酚酸B39.433.77人参皂苷Rg1200.125.13丹参酮ⅡA60.143.326片三七皂苷R138.326.23丹酚酸B78.335.16人参皂苷Rg1423.993.45丹参酮ⅡA93.323.679片三七皂苷R169.137.11丹酚酸B769.584.81人参皂苷Rg1130.333.99丹参酮ⅡA171.035.11剂型给药量成分测得量/ngRSD/%滴丸0.6 g三七皂苷R131.195.14丹酚酸B23.944.53人参皂苷Rg147.004.21丹参酮ⅡA0.000.0010丸三七皂苷R145.555.17丹酚酸B38.004.32人参皂苷Rg154.423.88丹参酮ⅡA0.000.0020丸三七皂苷R176.755.74丹酚酸B69.323.88人参皂苷Rg191.667.66丹参酮ⅡA0.000.0030丸三七皂苷R192.745.78丹酚酸B154.185.12人参皂苷Rg1111.534.79丹参酮ⅡA0.000.00
3 讨论
3.1指标成分的选择 中药复方是指在辨证审因决定治法以后,选择合适的药物酌定用量,按照组成原则妥善配伍而成的一组药物。其所含化学成分复杂,如何选择控制指标为其难点,本实验参考《中华人民共和国药典》[1]及文献[9-14],丹参药材中主要含有水溶性成分和脂溶性成分,故选择水溶性成分中丹酚酸B和脂溶性成分中丹参酮ⅡA为指标;三七中主要成分为皂苷类,最终选择三七皂苷R1、人参皂苷Rg1作为指标成分,所选指标成分不仅代表性强,同时科学合理,将复方丹参方中丹参、三七主要有效成分于同一色谱条件下展现出来。
3.2色谱条件的选择 将所含发色团、助色团不同的4种成分于同一波长下检测出来,首先将丹酚酸B、人参皂苷Rg1、三七皂苷R1、丹参酮ⅡA进行全波长扫描,丹酚酸B在280 nm、丹参酮ⅡA在270 nm、三七皂苷R1在203 nm处有最大吸收,因三七中皂苷发色团与助色团较少,只能在低波长处检测出来,因203 nm处存在末端吸收,通过不断的调整流动相比例,使得检测成分吸收峰与末端吸收峰分离度大于1.5,最终以末端吸收203 nm进行色谱条件的探索,同时实验运用超高效液相色谱仪,将此图谱于10 min内展现出来,分析时间短,分离度好,有利于药品检测机构高效的检测送检样品,节省人力、物力。其次,参考相关文献及《中华人民共和国药典》,通过调整流动相比例,比较流动相为0.02%磷酸水-含0.02%磷酸的80%乙腈、甲醇-水、醋酸甲醇-醋酸水、水-乙腈、醋酸水-乙腈时所得色谱图中峰数、峰型、峰高、峰面积,最终选择0.02%磷酸水-含0.02%磷酸的80%乙腈为流动相进行检测。同时进行柱温考察,当25,30,35,40 ℃时,最终选择40 ℃为检测柱温。以此色谱条件为基础,测定4种成分在大鼠血浆中药动学过程,同时在采血45 min处比较复方丹参片与复方丹参滴丸主要有效成分在大鼠体内吸收情况。
3.3血浆处理方法的选择 在对采血量的选择过程中,参考文献[4-8]选择血浆200 μL进行研究,在检测过程中发现大鼠血浆中药物的含量较小,对药动学过程会产生影响,同一只大鼠进行多次采血,结果未测出其中2种成分,本实验后采取一只动物一个点进行研究,实验购买同一批大鼠,饲养环境相同,严格控制大鼠的一致性,最终采取大鼠血浆800 μL进行研究,提高药动学研究过程中检测的稳定性。在对血浆处理方法选择时,依照简单、方便的原则选择甲醇、10%三氯乙酸、乙腈对血浆进行一步沉淀处理,甲醇处理所得色谱图末端吸收严重,故不选用;10%三氯醋酸处理所得色谱图中丹酚酸B回收率低,同时色谱图中出现非检测成分的较大吸收峰,影响所选成分的检测,故不选;乙腈处理所得色谱图中丹酚酸B、人参皂苷Rg1、三七皂苷R1、丹参酮ⅡA回收率良好,故选择乙腈对其进行沉淀蛋白。
3.4血浆药动学参数 根据药动学结果,得出4种成分在给药后10 min内均能检测出来,药物吸收较快。丹参酮ⅡA的血浆浓度-时间曲线下面积(AUC)大于其他成分AUC,且丹参酮ⅡA的给药剂量小于其他成分给药剂量,原因可能丹酚酸B为亲脂性成分,其余均为亲水性成分,亲水性物质[13]经细胞旁路过肠膜,由于旁路细胞占肠上皮细胞总表面积小于0.1%,上皮细胞之间的紧密连接限制了药物吸收,所以亲水性化合物的吸收较差。三七皂苷R1在体内吸收相比于其他三种成分最快,达峰时间为0.29 h,人参皂苷Rg1的AUC是三七皂苷R1的3倍,最大吸收浓度为7倍,由此可见人参皂苷Rg1给药后口服吸收优于三七皂苷R1。
本实验同时测定大鼠体内4种成分的药动学过程,节省实验及分析时间,10 min内快速将4种成分在同一图谱中检测出来,能说明复方丹参方中主要有效成分整体的含量在体内的变化过程,从而为进一步探索提高复方丹参方主要成分整体在体内的吸收提供方法与依据。
