超声造影灌注时相分析在监控肝硬化结节演变和恶变中的临床价值
2019-10-17韩莹莹翟凌云沙红芳徐祥勇崔建巍
虞 梅,梅 琪,韩莹莹,翟凌云,沙红芳,徐祥勇,倪 娟,崔建巍,丁 红
1.上海市徐汇区大华医院超声影像科,上海 200237;
2.复旦大学附属中山医院超声科,上海 200032
原发性肝癌多在慢性肝炎、肝硬化的基础上发生,一般认为,肝细胞癌(hepatocellular carcinoma,HCC)的发生、发展经由肝硬化结节(cirrhotic nodule,CN)、低度异型增生结节(dysplastic nodule,DN)、高度DN等一系列过程,最终演变为HCC。病理学上的DN在组织和细胞结构上与正常肝细胞存在异型,但尚未达到HCC的诊断标准,目前被认为属于癌前病变[1]。肝内异常结节和准确诊断HCC的影像学方法是提高肝癌检出率的重要手段。本研究探讨超声造影下肝内CN、DN和微小HCC的血流动力学灌注特征,为临床早期诊断HCC、及时干预和治疗、改善患者预后奠定基础。
1 资料和方法
1.1 研究对象
2007年3月—2017年12月于复旦大学附属中山医院就诊随访的符合慢性乙肝诊断标准的患者9 550例,每3~6个月随访常规彩超,每3个月随访肝脏相关血生化指标及肿瘤标志物。选择具备完整资料的肝硬化伴肝内结节的392例患者共551枚结节作为跟踪随访对象。其中男性235例,女性157例,年龄11~85岁,平均(54.7±12.8)岁,平均随访次数(12.7±14.9)次,随访时间24~121个月,平均(51.3±45.1)个月。
选择标准:① 肝硬化伴肝内异常结节;② 肝硬化不伴有结节,但有肝癌家族史或相关肿瘤标志物异常;③ 定期随访5次以上,资料完整并明确诊断者。
排除标准:① 肝肿瘤直径大于2 cm,或伴有门静脉癌栓的晚期肿瘤患者;② 转移性肝癌患者;③ 失访或资料不全者。
1.2 仪器及方法
使用Siemens Sequoia 512和S2000、Philips iU22及GE LOGIQ E9彩色超声仪,腹部凸阵探头,频率1~5 MHz。造影剂为声诺维,59 mg六氟化硫气体,用5 mL 0.9%的NaCl溶液配制成微泡混悬液。每次根据每例患者的体质量抽取相定量的微泡混悬液1.5~2.5 mL经外周静脉团注,随后推注5 mL 0.9%的NaCl溶液。实时动态视频的形式储存造影全过程,并定性及定量地分析造影增强方式。
1.3 图像分析
超声造影时相定义:以开始注射造影剂后第8~30 s为动脉期,31~120 s为门静脉期,121~ 360 s为延迟期[2]。
诊断标准:参照国际超声造影临床应用指南对肝内结节进行定性诊断。同时,采用德国TomTec公司提供的Sonoliver定量分析软件,分别选择病灶区和邻近肝实质的造影灌注时相和病灶的灌注模式,自动分析两者的时间-强度曲线(time-intensity curve,TIC)和拟合曲线,直观地显示病灶灌注廓清的模式。平均渡越时间是指注射造影剂后感兴趣区从灌注到廓清的时间,即从开始注射造影剂到TIC下降至强度值一半的时间。
1.4 统计学处理
采用SPSS 20.0统计软件进行分析,定量资料由不同数据类型选取对应的t检验,定量数据以表示。P<0.05为差异有统计学意义。
2 结 果
本组551枚定期随访的肝内结节中,最终诊断微小HCC 55枚,DN 19枚,CN 477枚。其中55枚HCC均经手术后病理学检查或穿刺活检病理学检查证实为HCC;19枚DN中,经手术病理学诊断15枚,穿刺活检病理学诊断4枚;477枚CN中,经手术病理学诊断7枚,穿刺活检病理学诊断6枚,其余结节由增强CT/MRI的典型增强表现而提示诊断,即动脉期、门脉期和延迟期均为等增强,并符合临床特征:肿瘤指标正常,随访2年以上无明显变化。
2.1 灰阶声像图特征
肝内551枚结节的灰阶声像图表现见表1。其中低回声346枚(62.8%),高回声188枚(34.1%),等回声17枚(3.1%)。不同病灶的大小及出现3种回声的百分率差异无统计学意义(P>0.05)。

表 1 CN、DN和HCC的声像图特征比较Tab. 1 Ultrasound patterns of CN, DN and HCC[n (%)]
2.2 超声造影特征
肝内CN、DN和微小HCC的超声造影特征见表2。55枚HCC中,动脉期高增强46枚,病灶与肝实质同步增强7枚,门脉期呈等增强40枚,延迟期低增强48枚。对照国际超声造影指南的诊断标准,符合典型HCC诊断标准的病灶有47枚(85.5%)。
由表2可见,CN的造影特征以等-等-等的增强方式最多见,占89.5%(427/477);DN的造影特征以低-等-等的增强方式最多见(图1),占52.6%(10/19);微小HCC的造影特征则以高-等-等和高-等-低的增强方式最多见(图2),占85.5%(47/55)。
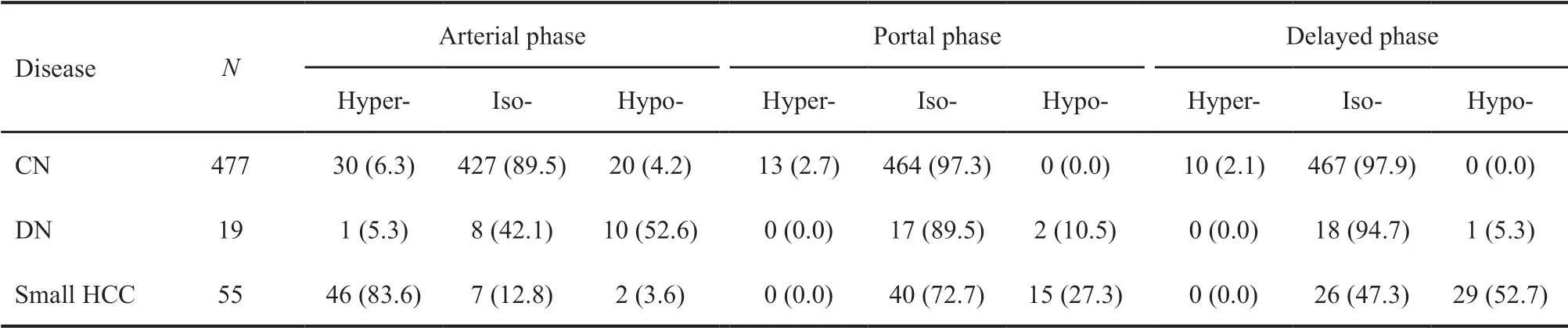
表 2 CN、DN和微小HCC的超声造影表现Tab. 2 Contrast-enhanced ultrasound of CN, DN and small HCC[n (%)]
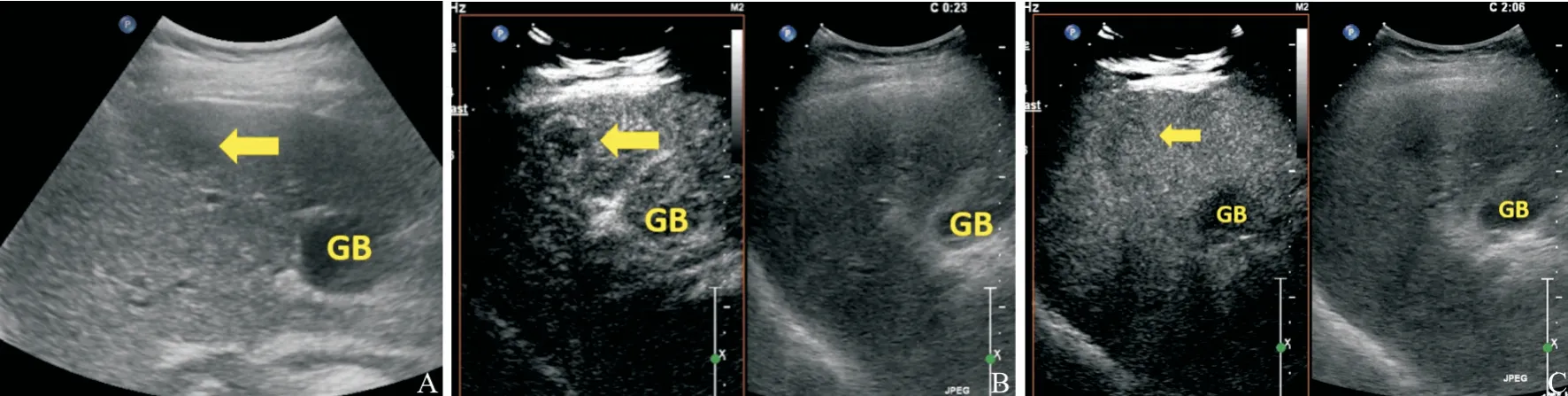
图 1 DN超声造影图像Fig. 1 Contrast-enhanced ultrasound of DN

图 2 CN演变为HCC的超声影像Fig. 2 Ultrasound images of evolution process from CN to HCC
2.3 超声造影灌注参数特征
肝内DN和HCC的超声造影灌注参数见表3。 经统计,DN和HCC在开始增强时间、达峰时间、开始消退时间和平均渡越时间参数的差异有统计学意义(P<0.05);两组肝实质的平均渡越时间差异无统计学意义。
2.4 超声造影诊断肝内结节的准确性评估
若以肝内结节的造影剂开始增强时间及消退时间与周围肝实质一致为肝硬化良性CN;若灌注时相为造影剂开始增强晚于周围肝组织,消退时间与周围肝组织一致为DN;若灌注时相为造影剂开始增强时间早于周围肝组织,消退时间早于或与肝实质同步,或造影剂与肝实质同步增强而早于肝实质消退,即为HCC,则本组超声造影诊断正确的病灶数分别为445、15和47枚,准确率分别为93.3%、78.9%和85.5%。
表 3 肝内DN与微小HCC的超声造影血流灌注参数比较Tab. 3 Comparison of perfusion parameters of DN and small HCC on contrast-enhanced ultrasound
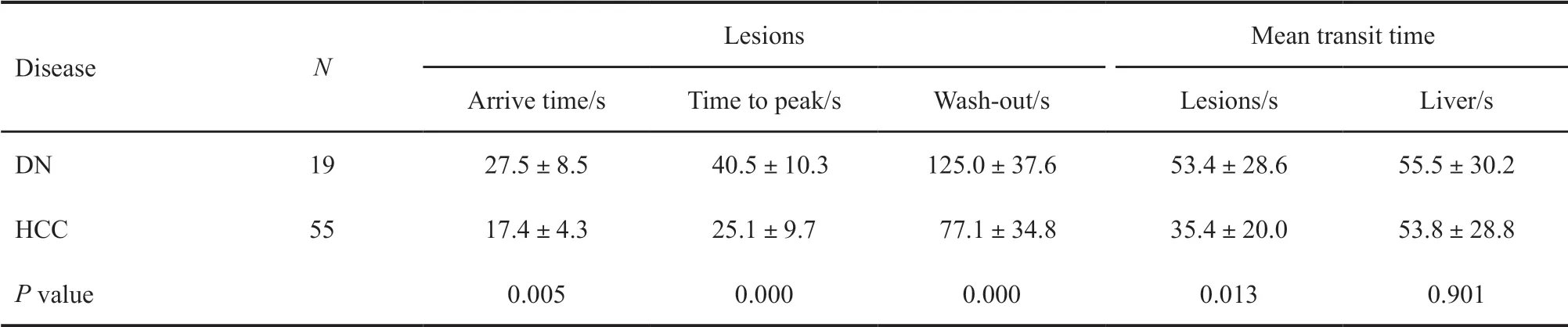
表 3 肝内DN与微小HCC的超声造影血流灌注参数比较Tab. 3 Comparison of perfusion parameters of DN and small HCC on contrast-enhanced ultrasound
There was statistical difference of arrive time, time to peak, wash-out and mean transit time between DN and small HCC (P<0.05)
Disease N Lesions Mean transit time Arrive time/s Time to peak/s Wash-out/s Lesions/s Liver/s DN 19 27.5±8.5 40.5±10.3 125.0±37.6 53.4±28.6 55.5±30.2 HCC 55 17.4±4.3 25.1±9.7 77.1±34.8 35.4±20.0 53.8±28.8 P value 0.005 0.000 0.000 0.013 0.901
3 讨 论
超声检查因其普及率高、无创价廉等优势而成为临床上慢性肝病患者筛查和定期随访的常用影像学手段。但肝硬化患者常合并不同性质的肝内结节,由于肝区回声增粗且不均匀,肝实质背景结构异常,CN及其他良恶性小病灶声像图不典型,常规彩色多普勒超声难以显示小病灶的血流信号,这些因素导致常规超声鉴别诊断肝内结节良恶性的准确率较低[3]。
从肝硬化发展至HCC的过程中,最早的CN是在肝细胞破坏后,肝组织反应性增生而形成,结节与周围肝硬化组织的血流动力学无明显差异;随着病变进展,出现了主要由门静脉供血、少量肝动脉供血的低度DN;进一步向高度异型增生结节转变时,结节内肝动脉供血逐渐增加,门静脉供血逐渐减少;最终发展为HCC结节时,通常由肝动脉和门静脉双重供血,且以肝动脉供血为主[3-5]。这些血流动力学的变化,常规超声很难显示;超声造影则具有良好的血流灌注显像功能,能实时动态地观察病灶与肝实质的血流灌注时相和灌注模式的变化规律,显著提高超声鉴别诊断肝内结节良恶性的准确率[2-5]。
本组病例中,477枚CN来自325例患者,其中13枚硬化结节病灶因患者同时存在肝癌病灶而行手术切除。超声造影显示,10例动脉期高增强、门脉期和延迟期高/等增强,其余结节在超声造影的3个时相均呈等增强,即与肝实质同步增强和同步减退。这些增强特征与其病理学检查显示的硬化结节虽然组织结构不同于正常肝组织,但功能及血供与周围正常肝组织类似,并以门静脉及少量动脉供血为主,故造影时表现为始终与周围肝实质同步增强。
据报道,随着肝硬化病程的进展,结节内正常肝动脉血流逐渐减少,肿瘤新生动脉血流逐渐增多,DN以不断减少的肝动脉血流为特征,门静脉血供可保留直至癌变阶段[6-7]。多数研究认为,CT增强扫描以动脉期至延迟期三期呈等密度及低密度多见[8]。本组19枚DN中,10枚动脉期呈低增强,门脉期或延迟期呈等回声,符合DN的血流动力学表现。其余9枚DN结节中,8枚动脉期和门脉期均为等增强,3枚延迟期减退;另1枚动脉期高增强,门脉期和延迟期未减退。按照肝肿瘤超声造影应用指南,这两种增强方式均符合肝硬化时HCC的诊断标准,导致4枚DN术前超声造影误诊为HCC。国内学者对33例不典型增生结节的超声造影研究也报道了8例(24.3%)呈动脉期高增强和延迟期低增强的类似结果[9],这部分结节的超声造影表现难与HCC鉴别,必要时需进行特异性造影剂如普美显增强MRI或穿刺活检以明确诊断。
典型HCC的超声造影特征为动脉期高增强,门脉期或延迟期呈低增强,即病灶的动脉血供明显增多和门脉血供明显减少。本组29枚(52.7%)HCC病灶呈现该种增强方式,与DN的造影表现明显不同,容易鉴别诊断。其余26例微小HCC的增强类型包括三期分别呈高-等-等、等-等-低和等-低-低的方式,即动脉期高增强、门脉期及延迟期等增强,或动脉期增强不明显、门脉期等增强、延迟期低增强,或动脉期增强不明显、门脉期及延迟期低增强,尤其在肉眼观察时有歧义的可能。超声造影定量分析通过获取病灶区与肝实质的造影剂灌注TIC,可相对精确地分析病灶的血流灌注特征。DN的TIC形态表现也较为多样,本组以曲线上升支低于正常肝脏组织、下降支与周围肝组织一致最为多见,其余的形式包括曲线上升支略快于正常肝组织、下降支略平缓,或基本与肝实质同步上升和下降等形式,不同于典型HCC的曲线形态。表2的定量参数则更客观地显示了DN与HCC的灌注特征,两者的开始增强时间、达峰时间、开始消退时间和渡越时间参数差异均有统计学意义(P<0.05),而两者的肝组织渡越时间差异并无统计学意义(P>0.05)。可见,超声造影定量分析的灌注参数有助于DN和HCC的鉴别诊断。TIC量化了超声造影揭示的病灶内血流灌注特征,是反映病灶内血流分布的客观指标,可为肝硬化背景下DN与微小HCC的鉴别诊断提供重要依据,对指导治疗和判断预后至关重要[10-11]。
当然,本组DN和HCC的造影灌注特征有部分重叠,这也是导致术前超声造影误诊的主要原因。进一步分析超声造影显示动脉期高增强的1例DN,病理学检查显示病灶的大部分区域呈肝细胞异型以外,局部可见异常增生的新生血管,与正常结构的汇管区同时存在。而分析HCC中呈动脉期等增强、消退相对较晚的9个病灶,7例为高分化型HCC合并脂肪变性,2例为透明细胞型,因高分化HCC病灶内可见类门静脉样血窦,造影剂由类门静脉血窦持续进入病灶导致消退相对较晚,类似的结果也有报道[12-13]。而林满霞等[9]报道的33例不典型增生结节中18例(54.6%)出现动脉期高增强,9例(27.3%)呈延迟期低增强,与本研究结果不同。世界超声医学与生物学联合会颁布的最新指南指出,延迟期消退呈低增强是肝恶性肿瘤的特征,因此,DN造影后门脉期和延迟期无明显消退可与延迟期主要呈低增强的典型HCC区分开。
总之,超声造影可动态显示肝硬化时不同结节的血流灌注特征,CN以三期等增强为特征;DN以动脉期低或等增强、门脉期和延迟期未见消退为特征;微小HCC以动脉期高增强、门脉期或延迟期低增强为特征。TIC显示DN平均渡越时间较HCC明显延长,超声造影可客观地反映肝内CN、DN及典型HCC的不同血流灌注方式。
