呋喃唑酮代谢物直接竞争化学发光检测方法的建立
2019-10-12古丽斯坦斌2富昕纯周晓龙
安 静 古丽斯坦 宋 斌2 姜 娜 富昕纯 周晓龙
(1.新疆农业科学院农业质量与检测技术研究所,乌鲁木齐 830091;2.中国农业科学院上海兽医研究所,上海 200241)
呋喃唑酮(Furazolidone)属于硝基呋喃类药物,具有良好的抗菌作用,主要用于水生动物的细菌性疾病防治,曾被广泛用于水产动物养殖[1]。虽然呋喃唑酮在动物体内的半衰期极短,但呋喃唑酮代谢物3-氨基-2-唑烷基酮(AOZ)能够与体内的蛋白质结合,并以结合物的形式长期存在机体内[2]。相关研究表明AOZ蛋白结合物在胃部等酸性环境易被释放,从而对动物机体造成致癌、致畸、致突变等毒害作用[3]。鉴于上述风险,1995年,欧盟禁止呋喃唑酮在畜禽、水产动物食品中使用[4];2002年,韩国《食品公典》中规定猪肉中不得检出呋喃唑酮,同年我国颁布禁止使用硝基呋喃类抗生素的禁令,残留限量为1μg/kg[5]。但是,由于硝基呋喃类药物价格低廉、抗菌效果良好,在水生动物养殖中仍被违规使用,严重影响食品安全质量和对外水产品的贸易出口,提示了加强呋喃唑酮等硝基呋喃类药物的食品安全监管、提升呋喃唑酮残留检测水平的现实需求。
目前,呋喃唑酮代谢物残留检测的方法主要有HPLC、酶联免疫吸附法等,其中HPLC检测结果精准可靠,但操作流程繁琐、技术要求高,而酶联免疫吸附法操作简便、检测快捷,且具有较高的特异性和灵敏性[6-8]。本研究通过建立AOZ-CLIA方法,可在短时间内完成AOZ残留检测,并联合HPLC同时检测新疆罗非鱼样品,展现出较好的准确性和可靠性,适用于基层大规模水产品中呋喃唑酮代谢物残留检测。
1 材料与方法
1.1 主要试剂
AOZ购自Witega公司;AOZ单克隆抗体由上海兽医研究所提供;N-羟基琥珀酰亚胺购自Aldrich公司,辣根过氧化物(HRP)购自上海雪满生物科技有限公司;N,N’-二环己基碳二亚胺(DCC)、N,N’-二甲基甲酰胺(DMF)、对醛基苯甲酸和对醛基苯甲醛均购自北京博时立华生物科技有限公司;化学发光底液购自Biopanda公司。
1.2 酶标记物CPAOZ-HRP制备
1.2.1CPAOZ合成
将DMF滴加至400μL浓度为0.04g/mL的对醛基苯甲酸溶液,待对醛基苯甲酸完全溶解后,加入0.025gAOZ,室温反应3h,有黄色沉淀生成后,抽滤水洗3次,烘干得到CPAOZ。
1.2.2CPAOZ-HRP制备
将2.5mgCPAOZ溶于0.25mLDMF,分别加入1.80mgNHS,3.0mgDCC,充分混匀,制备成混合A液;将2.0mgHRP溶于1mL碳酸盐缓冲液,制备成混合B液。取0.2mL混合A液加入混合B液,室温搅拌3h,置于4℃过夜反应,而后用PBS透析3d。透析完毕,加入等体积的甘油保存液,保存于-20℃。
1.3 酶标记物的鉴定
使用220~500nm紫外光扫描检测CPAOZ、HRP和CPZAO-HRP,测定最大吸收波长的吸光度,比较3个物质特征吸收峰,判断酶标记物是否偶联成功。
1.4 AOZ-CLIA方法建立
1.4.1最佳抗体包被浓度和酶标记物浓度的测定
将AOZ抗体和酶标记物梯度稀释,AOZ抗体分别纵向包被化学发光板,酶标记物横向加入,37℃反应2h,洗涤3次后,加入化学发光滴液,采用发光检测仪检测,读取化学发光值(CPS),选择CPS在1X106的抗体包被浓度和酶标记物浓度为最佳浓度。
1.4.2检测步骤
采用最佳抗体包被浓度的AOZ抗体包被化学发光板,用10g/L明胶溶液封闭,洗涤后,加入50μL NPAOZ(AOZ的对硝基苯甲醛衍生物)标准液或备测溶液,然后加入50uLHRP,震荡混匀,37℃反应2h,洗涤3次,加入化学发光底液,检测读取CPS。
1.4.3特异性测定
将AOZ和其他硝基呋喃类药物代谢标志物AMOZ、SEM、AHD,以及其他水产品养殖中禁用药物作为竞争抑制物,进行直接竞争CLIA,测定各竞争抑制物的IC50,计算各竞争物对AOZ单克隆抗体的交叉反应率(反应率计算公式:AOZ的IC50/抑制物的IC50×100%)。
1.4.4最低检出限测定
运用CLIA法测定20个空白样品(20μL PBS+20μL酶标物)和20个空白罗非鱼样品提取液。计算空白样品和空白罗非鱼样品的CPS平均值和标准差。运用公式Z=X-3SD,根据标准曲线计算Z值对应的4-NPAOZ浓度,即为最低检出限。
1.4.5回收试验
取HPLC检测的阴性样品作为空白样品,在罗非鱼肉空白样品中添加AOZ至终浓度0.5、1、2μg/kg,每个浓度设5个平行。采用CLIA法测定样品中AOZ浓度,并计算回收率和变异系数。回收率公式=(实测浓度平均值/添加浓度)×100%,变异系数=(实测浓度偏差/实测浓度平均值)× 100%。
1.5 市售样品检测
采集新疆某市5个农贸市场的罗非鱼样品15份。用AOZ-CLIA法、HPLC检测15份市售样品和2份阴性、6份阳性对照,每个样品重复2次,检测结果取平均值,分析两种方法的相关性。
2 结果
2.1 酶标记物鉴定
220~500nm紫外光扫描检测CPAOZ、HRP和CPZAO-HRP,CPAOZ最大吸收波长为275nm,HRP最大吸收波长分别为262nm和403nm,CPZAO-HRP最大吸收波长分别为290nm和403nm,结果显示酶标记物偶联成功(图1)。
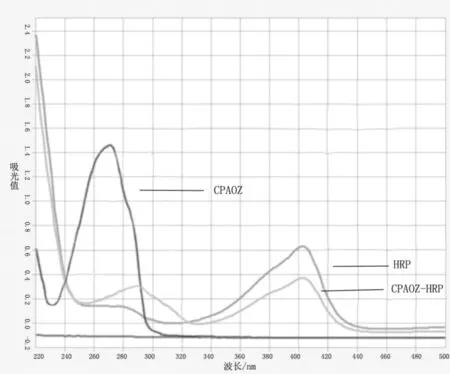
图1 CPAOZ、HRP和CPAOZ-HRP紫外扫描图
2.2 AOZ-CLIA方法的建立和优化
2.2.1最佳抗体包被浓度和酶标记物浓度的确定
通过棋盘法选择1x106CPS值附近的抗体包被浓度和酶标记物为最佳浓度,分别为1∶6000和1∶64000。详见表1。

表1 不同抗体包被浓度和酶标记物浓度下的CPS值(n× 106)
2.2.2CLISA标准曲线的建立
NPAOZ在线性范围0.0527~8.5ng/mL之间,相对吸光值与NPAOZ浓度的对数值呈线性关系,回归方程为y=-0.249x+0.325,R2=0.995,IC50为0.235ng/mL(图2)。

图2 NPAOZ-CLIA标准曲线
2.2.3特异性测定
AOZ单克隆抗体与NPAOZ、AOZ交叉反应率分别为100%和0.21%,与同类抗生素、同类抗生素代谢物未发生交叉反应,表明AOZ抗体特异性较高。详见表2。
2.2.4最低检出限测定
根据20个空白样品和20个空白罗非鱼样品的平均值X和标准差SD,计算4-NPAOZ标准溶液的最低检出限为0.0509ug/kg。详见表3。

表2 AOZ单克隆抗体与硝基呋喃类抗生素、水产品中常用禁药的交叉反应率
表3 最低检出限测定结果

样品类型CPS值1234567891011121314151617181920XSD空白样品297890301525295408297100289659305407298152289965298715304892285962297108310107298526301472285979302651287571285475302560296806.27020.27空白罗非鱼样品265085274320299857283512243107256715271205263217249878295137269580276940289659271852276565265840281952274560281259279813273502.6513676.197
2.2.5样品添加回收试验
AOZ的添加范围分别为0.5μg/kg、1μg/kg和2μg/kg ,用CLIA方法测定AOZ回收率在87.2%~95.0%,检测值的变异系数≤10%。详见表4。
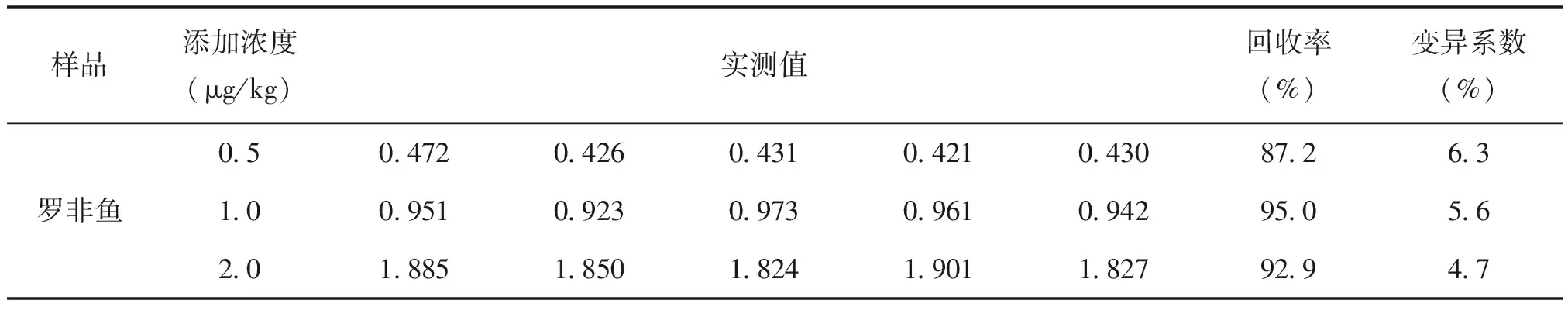
表4 添加回收率和变异系数
2.3 实际样品检测
2份阴性对照和15份市售样品的AOZ-CLIA、HPLC检测值均小于0.02ng/g;6份阳性对照检测结果见表5。绘制阳性对照的HPLC和AOZ-CLIA标准曲线,两种方法呈线性相关y= -0.872x+0.429,R2=0.996,结果见图3。
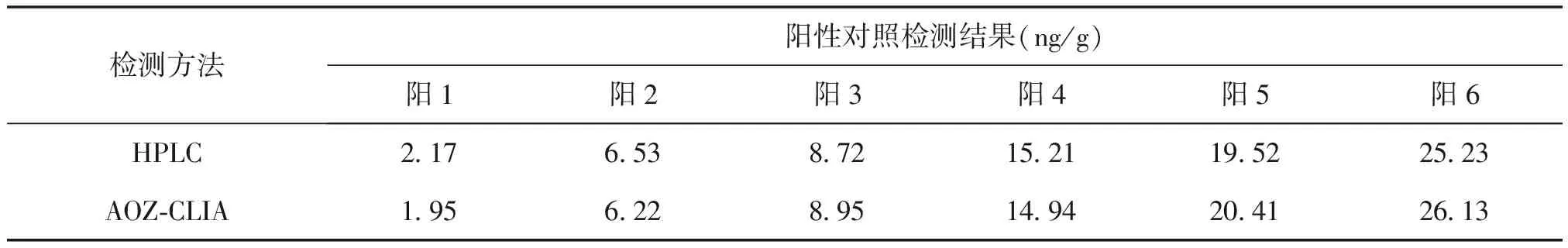
表5 实际样品检测结果

图3 AOZ-CLIA和HPLC检测结果相关性分析
3 讨论
AOZ是小分子半抗原,不具有免疫原性,需要与大分子蛋白载体偶联合成人工抗原,才能获得免疫原性,进而诱导机体免疫应答[9]。AOZ和AMOZ、SEM等硝基呋喃类药物代谢产物的分子质量较小,且分子空间结构简单,如果直接偶联大分子蛋白质,很难获得特异性高的抗体,因此在偶联过程中,需要对半抗原进行衍生修饰[10,11],本研究借鉴王民燕等研究[12],选择醛基苯甲酸作为衍生剂,一方面是其可以与代谢物和大分子蛋白载体结合,另一方面其具有的苯环结构可提高单抗制备的成功率。此外,为了有效提升酶标记物与免疫原的结合,降低两者偶联过程中的结构差异,实验先将AOZ与对醛基苯甲酸进行反应,生成CPAOZ,并引入羧基,再通过与HRP偶联生成酶标记物CPAOZ-HRP,紫外光谱鉴定表明酶标记物偶联成功。
基于单克隆抗体的免疫学方法,一般具有特异性强、效价高的特点[13]。本实验采用自制备AOZ单克隆抗体建立CLIA检测方法,结果显示AOZ单抗与硝基呋喃类其他药物及其代谢产物无交叉反应,表明了CLIA方法具有较高的特异性。与此同时,本实验建立的AOZ直接竞争CLIA检测方法展现出较高的灵敏度,其IC50为0.235ng/mL,且CLIA方法在检测罗非鱼样品的最低检出限为0.0509ug/kg,比我国硝基呋喃类药物代谢物限定值,以及欧盟规定的最大残留量(1ug/kg)均低,表明了该检测方法可以满足我国和欧盟的检测要求
目前,采用免疫学原理进行药物残留检测的方法主要有两种[14],一种是直接竞争法,其首先将特异性抗体吸附于固相载体,而后加入酶标记物和待测样品,通过底物显色,定量分析待测样本中的靶药物含量,该方法的优点是操作简单、步骤少,检测时间短。另一种是间接竞争法,通过靶药物的完全抗原吸附于固相载体,加入经前处理的待测样品和抗靶药物的单克隆抗体,而后加入酶标二抗,再与底物显色反应,测定待测样品中的靶药物含量,该方法相较于第一种方法,其灵敏度更高,但操作较为繁琐、检测时间较长。本研究建立的CLIA方法属直接竞争法,其灵敏度虽然要低于间接竞争法,但该方法的最低检出限仍低于我国和欧盟的最大残留量。
本研究运用AOZ-CLIA法和HPLC法对新疆市售的罗非鱼样本进行检测,结果显示所有市售样品均未检出超标样本,且两种方法的检测结果呈线性相关。HPLC法作为药物残留检测的金标准,其检测结果精准可靠[15,16],而本研究建立的AOZ-CLIA法与HPLC法检测结果高度相关,表明前者具有极高的准确度。此外,15份新疆市售罗非鱼样本均符合呋喃唑酮类药物的限量要求,表明近年来新疆通过行政监管、市场监督和监测常态化,有效限制了水产行业对呋喃唑酮类药物的使用。
综上所述,AOZ-CLIA灵敏度高、特异性强,且操作简便,用时较短,适合于监测现场和大批量样本的初筛检测,值得基层推广应用。
