盐酸N-叔丁基羟胺的合成及表征
2019-09-13代本才刘长春
李 锐,代本才,刘长春
(1.河南中帅医药科技股份有限公司,河南 郑州 450001;2.河南省科学院化学研究所有限公司,河南 郑州 450002)
N-烃基取代羟胺是羟胺的一类重要的衍生物,其结构相当于 H2N-OH 分子N上的一个或两个氢原子被烃基所取代。该类化合物在精细化工合成、染料合成、农药合成、药物合成、核废料处理、清洁能源及高分子材料等方面用途广泛,随着化学工业的快速发展,其用途也不断扩展。如N,N-二乙基羟胺(DEHA)具有优良的还原能力,是一种重要的游离基抑制剂,在共轭烯烃生产阻聚、橡胶生产端聚抑制、不饱和油类和树脂抗氧化、环境光化学烟雾抑制、换热设备缓蚀等方面有着重要的应用[1];N ,N-二甲基羟胺(DMHAN)可以作为有机无盐还原剂应用于核电站乏燃料后处理[2-3];N-异丙基羟胺(IPHA)还原性良好,常被用作阻聚剂、除氧剂等[4-5];N-甲基羟胺可作为 1,3-偶极环加成反应试剂、N-甲基化反应试剂和生物酶反应中电子转移的载体,以及核废料处理和回收等[6]; N-(2-甲基苯基)羟胺是一种高效、低毒、对使用者和环境均安全友好的新型广谱Strobin杀菌剂等[7]。
N-(叔丁基)羟胺(N-(tert-Butyl) hydroxylamine),分子式:C4H11NO,分子量89.14,CAS No.: 16649-50-6,由于特别容易氧化变质,通常做成盐酸盐储存,即盐酸N-(叔丁基)羟胺(N-(tert-Butyl) hydroxylamine hydrochloride,分子式: C4H11NO.HCl,分子量125.6,CAS No.:57497-39-9)。近年来的研究发现,除常见的工业应用外, N-叔丁基羟胺作为抗氧化剂,还能清除细胞内的活性氧,延缓与活性氧有关的细胞衰老和凋亡,其可能机制是作为线粒体抗氧化剂,清除了活性氧。可应用于逆转与年龄相关衰老及退化,如延缓人体肺成细胞衰老,避免人体视网膜病变而导致的视力损伤等生物医药领域[8-10]。
目前,N-叔丁基羟胺及其盐的合成主要采用硝基、亚硝基和肟衍生物的还原,这几种方法普遍存在还原深度难以控制、副产物多、成本高等缺点,因此目前市场上 N-叔丁基羟胺及其盐价格昂贵,产量很低,严重限制了该类化合物的广泛应用[11-12]。本文以叔丁胺为起始原料,经过缩合、氧化、水解、成盐制备得到了N-叔丁基羟胺盐酸盐。相关化合物通过NMR、HRMS、IR、UV等进行了结构表征,并利用TG-DSC和PXRD技术研究了目标化合物的晶型特征。路线所用苯甲醛可以反复回收利用,操作简单,成本低,利于工业化生产。合成路线如下:
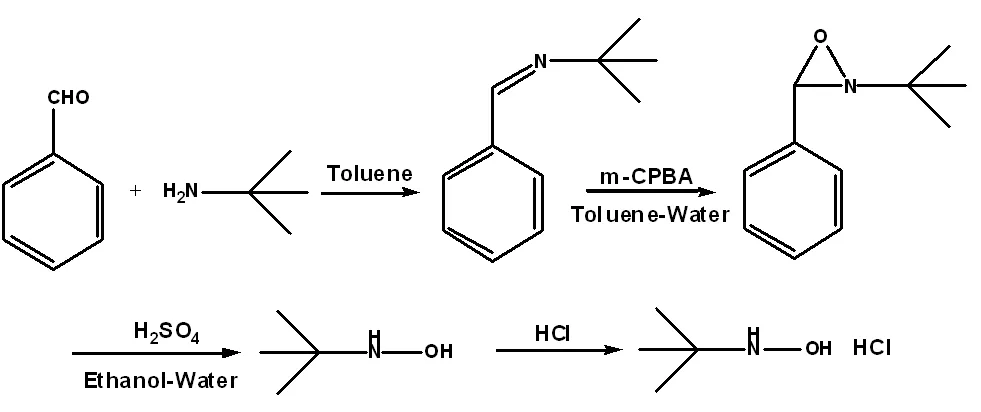
图1 N-叔丁基羟胺盐酸盐合成Fig.1 Synthesis of N-(tert-Butyl) hydroxylamine hydrochloride
1 实验部分
1.1 主要仪器与试剂
Bruker Tensor-27 红外光谱仪(德国 bruker 公司);Bruker AVANCE III 400超导核磁共振仪(德国 bruker 公司),Micromass Q-TOF液-质联用仪(美国Waters公司),NETZSCH STA 409 PC/PG 热分析仪(德国NETZSCH公司),Panalytical X'Pert PRO X-射线衍射仪(荷兰PANalytical公司),安捷伦8453型紫外-可见分光光度计(美国Agilent公司),MP430全自动视频熔点仪(济南海能仪器股份有限公司);DF-101S集热式恒温磁力搅拌器(巩义宇翔仪器有限公司),RE-52C旋转蒸发仪(巩义宇翔仪器有限公司),DZF真空干燥箱(北京科伟永兴仪器有限公司)。
叔丁胺为化学纯试剂(国药集团化学试剂有限公司),苯甲醛(天津市科密欧化学试剂有限公司)、甲苯(国药集团化学试剂有限公司)、碳酸钠(天津市光复精细化工研究所)、乙醇(天津市光复精细化工研究所)、98%浓硫酸(开封芳晶化学试剂有限公司)、乙酸乙酯(烟台市双双化工有限公司)、冰醋酸(烟台市双双化工有限公司)、无水乙醚(国药集团化学试剂有限公司)均为分析纯试剂,间氯过氧苯甲酸(上海阿拉丁生化科技股份有限公司)含量为85%,氯化氢乙醇(山东西亚化学工业有限公司)含量为30%,水为纯化水。
1.2 目标化合物的合成
1.2.1 N-亚苄基-叔丁胺的合成
在带有磁力搅拌和分水器的1L三口烧瓶中,加入苯甲醛85.0g(0.8mol),叔丁胺64.7g(0.88mol),甲苯500mL,控制温度120~130℃油浴加热回流8h。反应结束后降温至50℃以下,减压蒸馏除去甲苯和过量的叔丁胺,浓缩残余物为黄色油状物,称重123.0g,产率为95.4%。
1.2.2 2-叔丁基-3-苯基氧杂氮丙啶的合成
在带有磁力搅拌和恒压滴液漏斗的2L三口烧瓶中,加入N-亚苄基-叔丁胺120.0g(0.75mol),甲苯400mL,80.0g碳酸钠(0.75mol)溶于500mL水配成的溶液,常温搅拌15min。将162.7g(0.79mol)间氯过氧苯甲酸溶于500mL甲苯和250mL乙醇的混合溶液中。控制反应体系0~10℃条件下,向反应体系滴加间氯过氧苯甲酸的甲苯-乙醇溶液,40min滴毕,继续0~10℃保温反应1h,静置,分出水相,有机相分别用饱和碳酸钠溶液和水洗涤一次,无水硫酸钠干燥,抽滤,滤液减压蒸馏,浓缩残余物为黄色油状物,称重118.0g,产率88.8%。
1.2.3 N-叔丁基羟胺的合成
在带有磁力搅拌的2L三口烧瓶中,加入2-叔丁基-3-苯基氧杂氮丙啶115.0g(0.65mol),乙醇450mL,96.0g浓硫酸(0.98mol)溶于450mL水配成的溶液,20~25℃搅拌反应48h。减压蒸馏,浓缩除去乙醇,浓缩残余物加入450mL水及500mL乙酸乙酯萃取,静置,分出有机相,水相再用500mL乙酸乙酯萃取一次,合并有机相,减压蒸馏,浓缩除去乙酸乙酯,有机相回收得到苯甲醛,可循环使用。水相滴加45%的氢氧化钠水溶液调节pH值约8,加入乙酸乙酯500mL萃取两次,静置,分出有机相,无水硫酸钠干燥,抽滤,滤液减压蒸馏除去乙酸乙酯,浓缩残余物为淡黄色油状物,称重50.0g,产率86.3%。
1.2.4 盐酸N-叔丁基羟胺的合成
在带有磁力搅拌和恒压滴液漏斗的1L三口烧瓶中,加入N-叔丁基羟胺44.6g(0.50mol), 500mL无水乙醇,20~25℃下滴加30%的氯化氢-乙醇溶液75.0g,30min滴毕,继续保温20~25℃搅拌30min,20~25℃下滴加250mL无水乙醚,慢慢析出白色结晶沉淀,继续保温结晶4h,抽滤, 45℃减压干燥8h,得白色结晶,称重56.5g,产率90.0%。
2 化合物的结构表征及目标产物的晶型表征
利用熔点仪、超导核磁共振仪、液-质联用仪、红外光谱仪、紫外-可见分光光度计等对四种化合物进行结构表征,并用差热分析仪和X-射线衍射仪表征了目标化合物盐酸N-叔丁基羟胺的晶型。
2.1 N-亚苄基-叔丁胺的结构表征
淡黄色油状物,1H-NMR(CDCl3,400MHz),δ(ppm):1.29(s,9H),7.37(m,3H),7.73(s,2H),8.26(s,1H)。13C-NMR(CDCl3,400MHz),δ(ppm):29.6,57.1,127.8,128.4,130.0,137.1,155.0。HRMS(ESI+):m/z: calcd for C11H15N, M+:161,[M+-15]:146。
2.2 2-叔丁基-3-苯基氧杂氮丙啶的结构表征
淡黄色油状物,1H-NMR(CDCl3,400MHz),δ (ppm):1.17(s,9H),4.68(s,1H),7.33~7.46(m,5H)。13C-NMR(CDCl3,400MHz), (ppm):25.2,58.3,73.5,127.4,128.3,129.6,133.2,135.5。HRMS(ESI+):m/z: calcd for C11H15NO,M+:177。
2.3 N-叔丁基羟胺的结构表征
淡黄色油状物,1H-NMR(CDCl3,400MHz), δ (ppm):1.26(s,9H),6.15(br,NH-OH)。13-C NMR(CDCl3,400MHz), (ppm):23.16, 58.56。HRMS(ESI+):m/z: calcd for C4H11NO:89.0844,[M+H]+:90.0917。
2.4 目标产物盐酸N-叔丁基羟胺的全面结构表征及解析
盐酸N-叔丁基羟胺样品为白色结晶粉末,测定其熔点为183.2~185.8℃。将其配制成水溶液,测定其紫外吸收光谱,结果水溶液中在200~400nm范围内无明显吸收峰,与分子中无共轭发色基团相符。

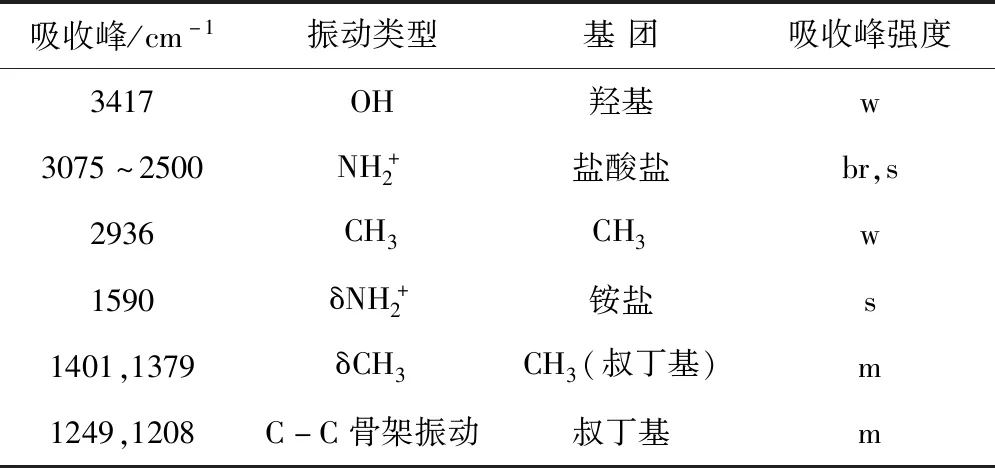
表1 盐酸N-叔丁基羟胺盐红外光谱数据Table 1 Infrared Spectrum Data of N-(tert-Butyl) hydroxylamine hydrochloride
样品的核磁共振氢谱数据为:1H-NMR(DMSO-d6,400MHz), (ppm):1.26(s,9H),10.73(br,N-OH),11.33(br,NH,HCl),解析如下:1H-NMR谱给出3组峰,其积分比(由低场至高场)为2∶1∶9,共12个质子,与盐酸N-叔丁基羟胺盐分子结构中质子个数相符。结合H-HCOSY谱, 11.33(2H,br)的宽峰,相当于2个质子,结合其化学位移值归属为分子中成盐的NH与HCl的质子,在H-H COSY谱上与之耦合的 10.73(1H,br)宽峰归属为分子中-OH的质子, 1.26(9H,s)的单峰归属为分子中叔丁甲基上的质子。
样品的核磁共振碳谱数据为:13C- NMR(CDCl3,400MHz), (ppm):23.17, 58.57,解析如下:13C- NMR谱上有2个峰,对应于分子中的4个C(3个CH3的碳峰部分重叠),由HSQC谱可知其中有1个连接氢的碳峰。根据DEPT135、DEPT90谱可知,化学位移为 58.57的峰为季碳(1个), 23.17的峰为伯碳(1个)。结合H-HCOSY、HSQC、HMBC谱,分别归属谱峰如下: 58.571(季C)化学位移和HMBC谱上的相关峰可归属其为分子中与N相连的季碳。 23.169(伯C)化学位移和HSQC谱上的相关峰归属其为与季碳相连的三个甲基C,它与季碳共同构成分子中的叔丁基。
样品的高分辨质谱数据为:HRMS(ESI+):m/z: calcd for C4H11NO:89.0844,[M+H]+:90.0917,解析如下:高分辨质谱图表明样品的准分子离子峰[M+H]+为90.0917,推断其分子量为89.0844,与N-叔丁基羟胺的理论精确分子量89.0841相比,误差小于5ppm,元素匹配结果表明其元素组成为C4H11NO,与N-叔丁基羟胺的结构一致,表明其元素组成正确。
2.5 盐酸N-叔丁基羟胺的晶型表征
利用差热-热重(DSC-TG)分析和粉末X-射线衍射(PXRD)技术对制备的盐酸N-叔丁基羟胺样品进行了晶型表征,DSC-TG和PXRD图见下图2和图3。DSC-TG分析以Al2O3为参比物,Ar=60mL/min,升温速率6℃/min,升温范围30~220℃,样品量5.475mg。DSC-TG图表明样品熔融分解,其Onset值为183.2℃,Peak值为185.8℃,样品中不含结晶水,也非溶剂化物。
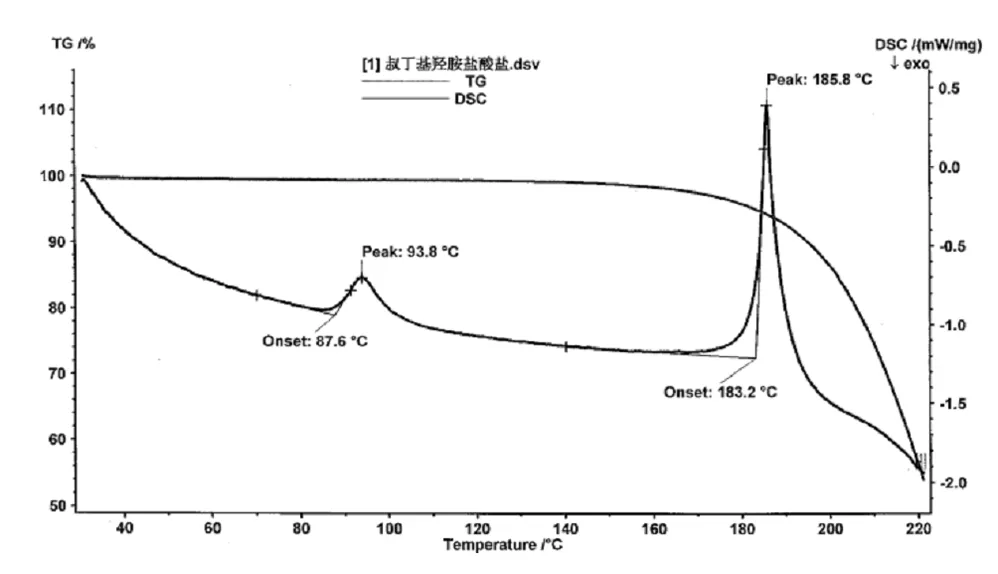
图2 盐酸N-叔丁基羟胺TG-DSC图Fig.2 TG-DSC Curves of N-(tert-Butyl) hydroxylamine hydrochloride
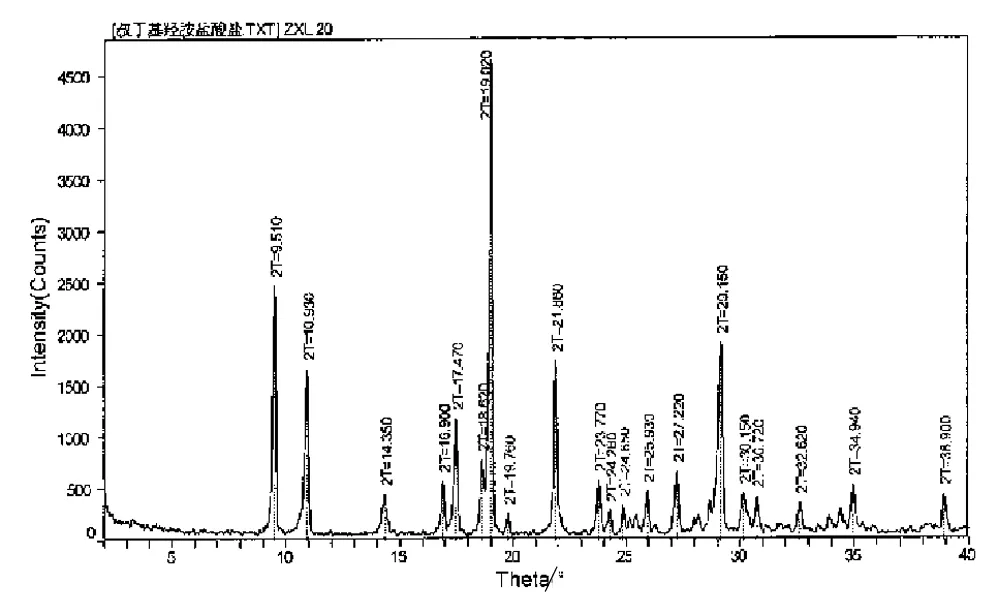
图3 盐酸N-叔丁基羟胺PXRD图Fig.3 PXRD of N-(tert-Butyl) hydroxylamine hydrochloride
查阅相关文献,未见关于盐酸N-叔丁基羟胺的多晶型报道,所制备样品的粉末X-射线衍射具有如图3特征衍射峰(Cu靶,40kV,40mA靶),结果表明,样品的结晶度较高,X射线在衍射角为9.510°、10.930°、17.470°、19.020°、21.860°、29.150°时衍射强度较高,最高衍射峰在19.020°,样品为结晶度较高的粉末,相关特征衍射数据和特征X-射线粉末衍射图可用于指导纯晶型样品的鉴别、纯度分析和质量控制,保证制备过程中的晶型稳定性,从而保持相对稳定的理化特性。
3 结论
以叔丁胺为起始原料,经缩合、氧化、水解、成盐合成了一种重要的N-烷基取代羟胺生物N-叔丁基羟胺盐酸盐,反应总产率65.8%。利用NMR、HRMS、IR、UV等测试技术对相关化合物行全面结构表征,并利用DSC-TG、PXRD对目标产物进行了晶型表征。合成工艺所用苯甲醛可以反复回收利用,操作简单,成本低,利于工业化生产。
