面筋蛋白粒子-黄原胶Pickering乳液的制备及其表征
2019-09-06谢安琪邓苏梦左白露朱雨晴邹立强
谢安琪,邓苏梦,左白露,周 伟,朱雨晴,邹立强,*,刘 伟
(1.南昌大学食品学院,食品科学与技术国家重点实验室,江西 南昌 330047;2.中国热带农业科学院农产品加工研究所,农业农村部热带作物产品加工重点实验室,广东 湛江 524001)
20世纪初,Ramsden[1]发现胶体尺寸的固体颗粒也可以形成稳定的乳状液,Pickering对这种乳状液体系展开了系统的研究工作,因而此类由胶体颗粒稳定的乳液被称为Pickering乳液[2-3]。Pickering乳液在食品、药学、造纸、化妆品等领域有着十分重要的应用价值和广阔的应用前景。固态胶体颗粒稳定乳液或泡沫的机理被归结为空间位阻效应。与表面活性剂以及天然的高聚物等稳定的乳液相比,Pickering乳液具有较大的优势[4],如:1)减少表面活性剂的用量,降低成本;2)天然物质替代无机高分子物质类型的表面活性剂,减少表面活性剂对人体带来的毒害;3)环境友好;4)改变体系的pH值、离子强度、温度,乳液依然具有较好的稳定性。近10 a对Pickering乳液的研究重新成为热点,但是单独由固体粒子稳定的Pickering乳液在其制备、贮藏和最终应用过程中,随着外界环境(pH值、粒子浓度、离子强度、电荷等)的变化,Pickering乳液会发生如乳析、絮凝和相转变等不稳定现象。因此,Pickering乳液的稳定性可通过粒子修饰[5]、多组分协同稳定[6-7]、调节环境因素等方法进行调节[8-9]。
蛋白质粒子是常用于稳定Pickering乳液的粒子,主要包括麦醇溶蛋白、玉米醇溶蛋白、大豆蛋白等。单独蛋白粒子稳定的乳液容易出现乳析[10-11],从而导致乳液的稳定性发生变化。采用蛋白纳米粒子和多糖协同改善乳液黏度,可使乳液达到一个稳定的状态。常用的多糖有壳聚糖[12]、甜菜果胶[13]。多糖添加至食品乳液体系中可提高连续相黏度、提供理想的质构特性、减缓液滴运动,从而抑制乳液乳析或沉降的发生,达到稳定乳液的目的。多糖在中等浓度时,会引起乳液絮凝,此时液滴絮凝增加粒子有效体积的作用(促进乳析)大于提高连续相黏度的作用(抑制乳析),从而引起体系乳析,导致乳液分层;多糖在浓度足够高时会形成三维网络结构,抑制乳液液滴的运动,从而减少体系液滴之间的絮凝或聚集作用;多糖在更高的浓度下,由于高黏或者凝胶网络结构的形成,液滴运动受阻,乳析得到抑制[14]。因此,多糖对乳液的稳定性的影响很复杂,依赖于体系的各项特性。
小麦面筋蛋白(俗称谷朊粉)是小麦天然蛋白质的重要组成部分,为小麦淀粉生产的副产物。面筋中蛋白质主要以单体或通过二硫键形成的寡聚体、多聚体的形式存在[15]。小麦面筋蛋白是营养丰富、物廉价美的植物性蛋白,具有乳化性、凝胶性、黏弹延伸性和成膜性等特点,其独特的理化性质使其具有广阔的应用空间。但由于小麦面筋蛋白自身独特的氨基酸组成,含有较多不带电荷的氨基酸和疏水性氨基酸,使其溶解度较低,不能满足食品加工的要求,在实际生产和生活中的应用受到限制[16]。因此,研究开发小麦面筋蛋白新的应用领域,提高其经济价值显得尤为重要。
黄原胶的相对分子质量(Mr)分布范围在2×106~2×107之间,分布范围取决于链之间的相互作用,几个单链间会形成聚合物[17]。黄原胶的三糖侧链和主链紧密连接,形成单股螺旋、双螺旋或者三螺旋的刚性结构[18],这样的黄原胶因其分子的特殊结构和胶体性质,从而具有多种功能。其一,黄原胶具有耐高温、抗酶解、耐碱和耐酸等特性,具有较高的稳定性,可作为稳定剂[19];其二,黄原胶兼具亲水性和亲油性,在水中可形成较稳定的水油动态平衡体系,具有良好的悬浮性和乳化性[20];其三,黄原胶无毒、无刺激性和不致敏性,可广泛应用于药品和食品领域。黄原胶的存在可显著增加乳状液分散相的黏度[21],有助于乳液形成凝胶网络结构,减缓由于重力或布朗运动造成的不稳定现象的发生,并且赋予产品理想的质构特征,因此黄原胶已经广泛应用于提高乳液的稳定性。但是,黄原胶在食品Pickering乳液中的应用较少,且黄原胶对蛋白质稳定的Pickering乳液的影响尚无相关研究。本实验室前期采用pH循环法制备了200~300 nm的面筋蛋白纳米颗粒,并发现pH 4.0的面筋蛋白纳米颗粒具有较好的贮藏稳定性,可作为Pickering乳液的乳化剂,但由面筋蛋白单独稳定的Pickering乳液在贮藏7 d后出现很明显的乳析现象。为进一步提高Pickering乳液的稳定性,本研究制备了面筋蛋白纳米粒子和黄原胶协同稳定的食品级Pickering乳液,研究蛋白与多糖的添加顺序及多糖浓度对乳液稳定性的影响,探究面筋蛋白纳米粒子与黄原胶协同稳定的食品级Pickering乳液的结构及物理化学特性,以期为改善Pickering乳液的稳定性和加工特性提供一定的理论支持与技术指导。
1 材料与方法
1.1 材料与试剂
小麦面筋蛋白粉(粗蛋白86%) 鹤壁市天龙面业集团有限公司;黄原胶、Keltrol T Plus 上海阿泽雷斯国际贸易有限公司;玉米油 益海嘉里粮食食品公司;其他试剂均为分析纯。
1.2 仪器与设备
M-110动态高压微射流 美国Microfluidic公司;Delta320 pH计 梅特勒-托利多仪器(上海)有限公司;D-37520高速冷冻离心 德国Thermo Electron公司;MS3000马尔文激光衍射粒度仪 英国Malvern仪器有限公司;XW-80A旋涡混匀器 上海精科实业有限公司;X85-2S恒温磁力搅拌 上海梅颖浦仪器仪表制造有限公司;ULTRA TURRAX®T18 digital高速分散机德国IKA公司;MCR302流变仪 上海安东帕有限公司;Carl Zeiss LSM710激光共聚焦显微镜 德国卡尔·蔡司股份公司。
1.3 方法
1.3.1 Pickering乳液的制备
乳液制备参考Shao Yun等[21]的方法并略修改。主要通过高速分散机在13 000 r/min分散3 min,采用0.1 mol/L HCl或0.1 mol/L NaOH溶液调节乳液的pH值。最终乳液油水体积比为4∶6,黄原胶质量分数为0%、0.1%、0.2%、0.3%、0.4%、0.5%和1%。
乳液0的制备方法:面筋蛋白纳米粒子溶液与玉米油按照体积比6∶4混合,用分散机在13 000 r/min条件下分散3 min;乳液1(mixed-wheat gluten-xanthan gum,M-WGXG)的制备方法:将一定量的玉米油和面筋蛋白纳米粒子溶液按4∶6的比例用分散机分散,然后加入不同质量的黄原胶进行二次乳化后即得乳液1,乳液中黄原胶质量分数分别为0%、0.1%、0.2%、0.3%、0.4%、0.5%和1%;乳液2(mixed-wheat gluten/xanthan gum,M-WG/XG)的制备方法:将面筋蛋白纳米粒子溶液与不同质量的黄原胶混合,混合溶液的pH值调至4.0,形成面筋蛋白/黄原胶复合物,再将玉米油与混合溶液按4∶6的比例加入用分散机乳化得乳液2,乳液中黄原胶质量分数分别为0%、0.1%、0.2%、0.3%、0.4%、0.5%和1%;乳液3(mixedxanthan gum-wheat gluten,M-XG-WG)的制备方法:玉米油和不同质量的黄原胶溶液按4∶6的比例混合分散,再加入一定量的面筋蛋白纳米粒子溶液进行二次乳化得乳液3,乳液中黄原胶质量分数分别为0%、0.1%、0.2%、0.3%、0.4%、0.5%和1%。
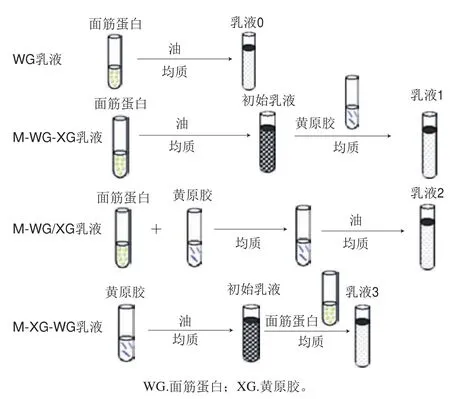
图1 乳液制备方式示意图Fig. 1 Schematic representation of emulsion preparation methods
1.3.2 Pickering乳液粒径的测量
参考Shao Yun等[21]方法测量Pickering乳液的粒径,采用马尔文激光衍射粒度仪测定面筋蛋白纳米粒子与黄原胶协同稳定的食品级Pickering乳液的粒径大小。用蒸馏水作为分散介质,设置分析条件为:粒子折射率1.456,粒子吸收率0.100,分散剂吸收率1.33,激光遮光度为10%~15%。粒径的大小用加权平均体积直径(d4,3)表示,如式(1)所示:

式中:di为液滴直径;ni为颗粒的数目。每个样品重复测定3 次,结果取平均值。
1.3.3 Pickering乳液电位的测量
参考Zhu Xuefeng等[22]的方法并略作修改测量乳液的电位,将面筋蛋白纳米粒子与黄原胶协同稳定的Pickering乳液用相应pH值的水溶液稀释适当的倍数,采用激光纳米粒度分析仪测定Zeta电位。测试参数为温度23 ℃,液体黏度0.933 cP,折光率1.333,激光波长635 nm,外部光纤角度18.9 deg,散射角度14.063 6 deg。每个样品重复测定3 次,结果取平均值。
1.3.4 Pickering乳液的微观结构
乳液的微观结构使用激光共聚焦显微镜观察,参考课题组实验室前期研究的方法[23],样品染色的方法为:取2 mL乳液样品加入100 μL 0.1%尼罗红染料和100 μL 0.1%尼罗蓝染料,使用旋涡仪混匀,染料和乳液全程避光放置。将乳液样品固定于激光共聚焦显微镜载物台上,用40 倍物镜观察初调聚焦平面。激发波长为488 nm和633 nm,并采集荧光图像,使用ZEN 2009 Light Edition软件对图像进行处理。
1.3.5 Pickering乳液的流变性质
乳液流变学性质的测量参考Pi Guilu等[24]的方法,并适当修改。控制乳液的pH值、油含量以及蛋白纳米粒子的含量,制备不同添加顺序所得的乳液。使用MCR302安东帕流变仪对乳液的流变学特性进行测定,所用夹具为平板夹具(pp-50圆盘),测试时平板间距为1 mm,测试温度为(25±0.1)℃。吸取适量样品于平板上,剪切速率范围为1~1 000 s-1,测定其表观黏度的变化曲线。然后对乳液进行动态频率扫描0.01~50 Hz,记录其储能模量(G’)和损耗模量(G”)随频率变化趋势。
1.3.6 Pickering乳液的贮藏稳定性
乳液的乳析指数可以间接提供乳液液滴发生聚集程度的信息,乳析指数越大,则乳液液滴移动越快,因此液滴聚集程度越大[25]。乳液的乳析指数主要依靠视觉观察监控,乳析指数越小,乳液稳定性越好。取20 mL新鲜乳液置于带有刻度的密闭试管中。分别在1、3、5、7 d和30 d记录乳液总体积和乳析相体积,乳液的乳析指数[26]计算如式(2)所示:

式中:He为乳析相体积;Ht为乳液总体积。
1.3.7 Pickering乳液的离子稳定性
乳液离子稳定性的测量参考Zhang Zipei等[27]方法并稍作修改。取一定质量的NaCl配制成溶液备用,分别加入不同量的NaCl与乳液混合,使得乳液中NaCl最终浓度分别为0、40、80、160、320、640 mmol/L和1 000 mmol/L,取每个离子浓度的样品10 mL分装于试管中,观察其乳析稳定性,测其粒径分布Zeta电位,每个样品重复测量3 次,取平均值。
1.4 数据分析
采用Origin 8.0软件绘图,并用SPSS 17.0软件处理数据,进行显著性分析,P<0.05,差异显著。
2 结果与分析
2.1 不同质量分数黄原胶稳定Pickering乳液的贮藏稳定性
贮藏稳定性是乳液非常关键的品质参数,在某种程度上决定了产品最终能否被使用。乳析是乳液聚并或聚集的先兆,最终会造成乳液的相分离,严重影响乳液产品的感官和理化性质。贮藏稳定性主要通过乳析指数评定。
由表1可得出,面筋蛋白单独稳定的Pickering乳液在贮藏5 d时,没出现乳析现象,而在第7天则出现了很明显的乳析现象。加有低质量分数黄原胶(<0.2%)的Pickering乳液的乳析现象较明显,贮藏1 d即可观察到乳液出现分层现象。加入较高质量分数的黄原胶(>0.2%)后,乳液的贮藏稳定性有所提高。由表1可知,黄原胶质量分数越大,乳液的稳定性越好。当黄原胶质量分数为0.2%时,乳液仍有乳析现象,这表明低质量分数多糖的添加促进了乳液的聚集,这可能是电荷中和以及桥联絮凝所致[28],阴离子多糖的加入降低了液滴表面的电荷,从而降低了液滴之间的静电斥力而导致乳液聚集;同时,当低质量分数多糖无法完全包裹在乳液液滴表面而出现两个或多个液滴吸附一个多糖分子时,会出现液滴桥联絮凝[29]的现象;当黄原胶质量分数大于等于0.3%时,乳液于4 ℃贮存30 d仍无乳析现象,说明乳液的稳定性较好。这可能是由于高质量分数多糖增加了液滴表面的电荷,从而增加了液滴之间的静电排斥力而减少乳液液滴聚集;当黄原胶质量分数为1.0%时,乳液在贮藏30 d后出现析油现象,这说明高质量分数的黄原胶使得液滴之间的相互作用增强,油滴泄露。故黄原胶的最适合质量分数为0.3%。
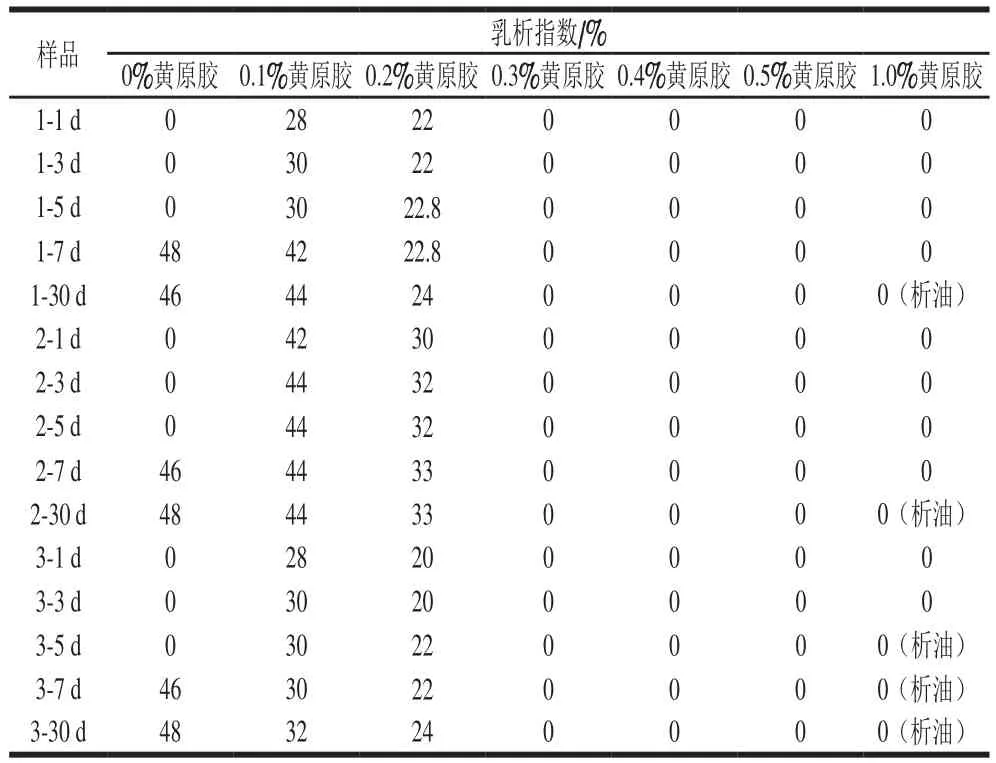
表1 黄原胶质量分数对Pickering乳液乳析指数的影响Table 1 Effect of xanthan gum concentration on emulsion creaming index
2.2 Pickering乳液的粒径与电位

表2 乳液的粒径和Zeta电位Table 2 Particle size and zeta potential of emulsions
表2显示面筋蛋白和0.3%黄原胶的不同加入顺序所制备的Pickering乳液的平均粒径(d4,3)和Zeta电位。由面筋蛋白纳米粒单独稳定的Pickering乳液的平均粒径为(10.88±0.283)μm,加入黄原胶协同稳定的Pickering乳液的平均粒径增大,且蛋白和多糖不同的加入顺序的粒径存在差异。乳液M-WG-XG和乳液M-XG-WG具有较小的平均粒径,而M-WG/XG则显示出较大的平均粒径。这可能是由于在pH 4.0时WG与XG形成不溶性复合物,然后WG/XG不溶性复合物组装成较大的颗粒并吸附至油滴表面,因此乳液M-WG/XG显示出较大的平均粒径。黄原胶的加入增大了乳液的净电荷,乳液液滴之间的斥力增加,减少了乳液之间的絮凝,乳液的稳定性增加。蛋白和多糖的不同添加顺序制备的Pickering乳液的Zeta电位无明显变化,说明加入顺序对液滴的电位影响不大。
2.3 不同乳化方法制备的Pickering乳液的微观结构
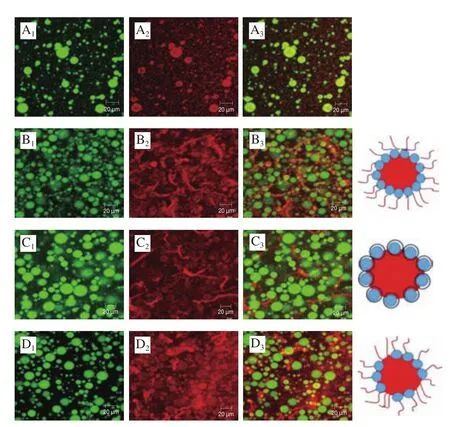
图2 乳液WG(A)、M-WG-XG(B)、M-WG/XG(C)和M-XG-WG(D)的共聚焦显微镜图Fig. 2 Confocal micrographs of emulsions WG (A), M-WG-XG (B),M-WG/XG (C), and M-XG-WG (D)
图2 显示了pH 4时,4 种乳液的共聚焦显微镜图,蛋白用0.1%尼罗蓝染色,油相用0.1%尼罗红染色,将蛋白的信号设置为红色,油相的信号设置为绿色。由图2B~D均可清楚地看出红色面筋蛋白颗粒包裹绿色油滴,说明3 种乳液形成的都是由颗粒稳定的Pickering乳液。由图2A可知,单独的面筋蛋白纳米粒子稳定的乳液界面层一般呈单层结构,由图2B可以看出,乳液M-WGXG液滴分布均匀,界面层呈现出多层结构。多层粒子堆砌形成厚的界面层,液滴之间形成桥连,粒径增大。由图2C可知,乳液M-WG/XG的液滴最大,此结果与表2所得的粒径数据一致。粒子的多层堆积和黄原胶与面筋蛋白的静电相互作用有很大关系。由面筋蛋白纳米粒子单独稳定的Pickering乳液粒径较小,而其他3 个加入黄原胶的乳液油滴粒径都大于由面筋蛋白纳米粒子单独稳定的Pickering乳液,此结果和粒度仪所测乳液粒径所得结果一致。乳液M-WG-XG和乳液M-XG-WG的液滴较小且液滴分布较为均匀,这可能是由于蛋白和多糖在油-水界面上形成了稳定的界面层,黄原胶液滴充满于液面上的粒子和油滴之间,形成液桥,使得界面膜封闭。与乳液M-WG-XG和M-XG-WG相比,乳液M-WG/XG的粒径最大,这可能是因为面筋蛋白和黄原胶复合改变了粒子油水界面的润湿性,从而使得乳液液滴变大。乳化方式对乳液的微观结构有所影响,共聚焦显微镜图中乳液液滴大小变化与粒径测得结果一致。
2.4 制备方法对Pickering乳液流变性质的影响
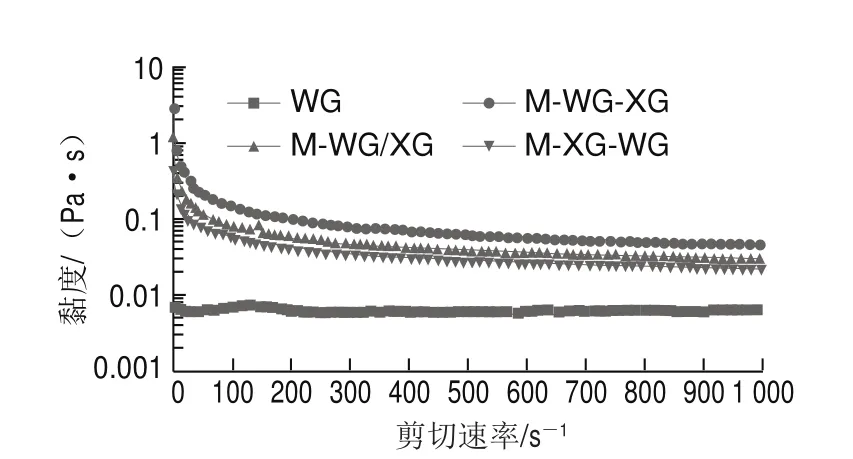
图3 剪切速率对乳液表观黏度的影响Fig. 3 Effect of shear rate on apparent viscosity of emulsions
通过静态和动态振荡测量模式研究4 种不同方式制备的Pickering乳液的流变性能。由图3可以看出,随着剪切速率的增加(0.1~1 000 s-1),由面筋蛋白纳米粒单独稳定的乳液(WG)的黏度保持不变,WG表现出近乎牛顿流体的行为。而由面筋蛋白纳米粒与黄原胶协同稳定的Pickering乳液都具有剪切变稀行为。正如预期一样,黄原胶的加入使得乳液形成了凝胶,而且从图3可知,不同乳化顺序形成的Pickering乳液的黏度大小不同,M-WG-XG>M-WG/XG>M-XG-WG>WG,图2亦可以看出黄原胶的加入增加了相邻液滴之间的絮凝桥连,形成网络结构,从而使得乳液具有较高的黏度[30]。
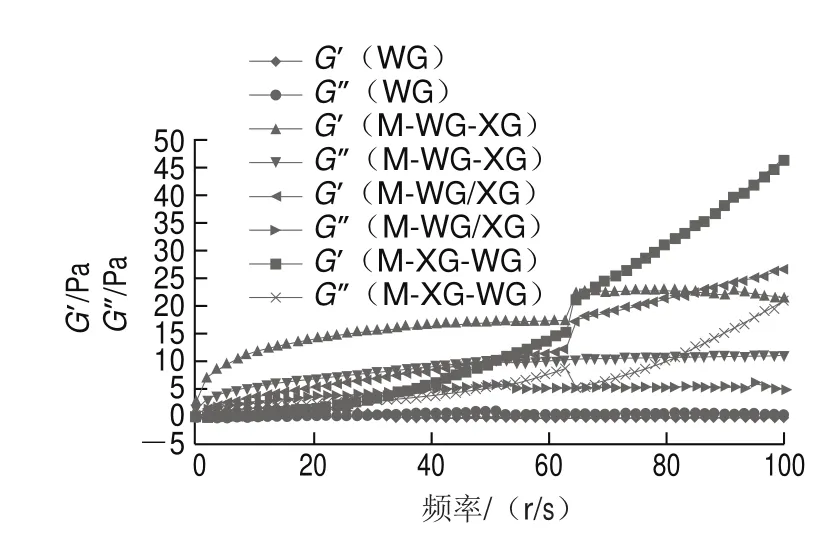
图4 频率对乳液G’和G”的影响Fig. 4 Effect of frequency on emulsion storage modulus (G’) and loss modulus (G”)
乳液的微观结构和流动性之间的关系可通过频率扫描[31]表示。图4显示,在整个频率扫描范围内,加有黄原胶的乳液的G’都大于G”,说明在此状态下的3 个乳液都为凝胶状结构的乳液,而且具有以弹性为主的凝胶性质。M-WG-XG的G’和G”在振幅小于70 r/d内都比M-WG/XG和M-XG-MG的值更高,说明在此范围内,第1种乳化方法能更好地增强乳液的黏弹性。
2.5 4 种方法制备的Pickering乳液的离子稳定性

表3 NaCl浓度对Pickering乳液平均粒径的影响Table 3 Effect of NaCl concentration on mean particle size of Pickering emulsions

图5 NaCl浓度对乳液WG(a)、M-WG-XG(b)、M-WG/XG(b)和M-XG-WG(d)的影响Fig. 5 Effect of NaCl concentration on visual appearance of emulsions WG (a), M-WG-XG (b), M-WG/XG (c), and M-XG-WG (d)
由图5可知,加入NaCl溶液后,WG的粒径有较明显的增加,而且有明显的乳析现象,说明WG的离子稳定性较差。黄原胶的加入提高了Pickering乳液的离子稳定性。在低NaCl浓度(≤160 mmol/L)时,M-WG/XG的粒径没有明显增加,外观亦没有出现明显的分层。这可能是由于WG与XG形成了带负电荷的保护层,抑制了乳液的聚集。而当NaCl浓度增加时,M-WG/XG的粒径增大,乳液出现分层现象。这可能归因于界面的结构、厚度和组成随着盐浓度的增加而改变[32]。M-WG-XG在所有离子浓度范围内,粒径变化幅度不大,实物图没有出现分层现象,这说明M-WG-XG具有较好的离子稳定性。这可能是由于M-WG-XG乳液具有较强的凝胶强度,所以体系内部空间位阻较大。M-WG-XG的粒径略微增加,表明生物聚合物形成了稳定的双界面膜。乳液M-XG-WG在离子浓度大于320 mmol/L时,出现分层现象,乳液的粒径也出现较大的增长,导致乳液不稳定。乳液的离子稳定性:M-WG-XG>M-XG-WG>M-WG/XG>WG。
3 结 论
本实验通过黄原胶与面筋蛋白纳米粒协同作用,制备出稳定性较好的Pickering乳液并对其理化性质进行了研究。结果表明:1)低质量分数黄原胶会促进乳析,当黄原胶质量分数低于0.2%时,乳液会出现乳析现象;随着黄原胶质量分数的升高,乳液稳定性增强;当黄原胶质量分数不小于0.3%时,贮存30 d乳液稳定性依然较好;当黄原胶质量分数为1%时,贮存30 d乳液出现析油的现象。因此,黄原胶的最适质量分数为0.3%。2)面筋蛋白和黄原胶的乳化顺序对Pickering乳液的稳定性也存在一定的影响,粒径电位分析发现,M-WG-XG和M-XGMG具有较小的平均粒径,分别为(21.40±0.314)μm与(23.91±0.402)μm,而M-WG/XG显示出较大的平均粒径,为(33.40±0.292)μm。黄原胶的加入增大了乳液液滴的净电荷,增强了液滴之间的静电斥力,乳液的稳定性增加。蛋白和多糖的不同加入顺序所制备的Pickering乳液的Zeta电位无明显变化。3)利用激光共聚焦显微镜和流变仪研究了乳液的界面结构及乳液的聚集行为,共聚焦显微镜图中乳液液滴大小变化与粒径测得一致。流变结果表明,黄原胶的加入增大了乳液的黏度,4 种乳液的黏度变化为:M-WG-XG>M-WG/XG>M-XG-WG>WG。频率扫描显示,M-WG-XG的G’和G”都比M-WG/XG和M-XG-MG的值更高,说明第1种乳化方法能够更好地增强乳液的黏弹性,即M-WG-XG的稳定性和流变性能最佳。4)黄原胶可以改善乳液的离子稳定性,不同乳化方式得到乳液的离子稳定性为:M-WG-XG>M-XG-WG>M-WG/XG>WG。
