鸡粒细胞巨噬细胞集落刺激因子-猪干扰素α1融合基因在大肠埃希菌中的可溶性表达及其生物学活性研究
2019-07-30何志远张文昌王明丽
胡 涛,何志远,张文昌,赵 俊,王明丽*
(1.安徽医科大学微生物学教研室,安徽合肥230032;2.安徽九川生物科技有限公司,安徽芜湖241000)
细胞因子是人与动物在抵御外界病原微生物侵入和感染的长期过程中产生的一类免疫因子,在传染病的防治中起重要作用[1],其中干扰素(Interferon,IFN)是一种由病毒或其它IFN诱生剂刺激机体后产生的一种小分子蛋白质,具有广谱抗病毒、抗细胞分裂增殖和免疫调节作用,在机体固有免疫及适应性免疫中发挥重要作用。自1986年Lefevre等[2]首次克隆出猪IFNα1(PoIFNα1)基因以来,国内外学者对重组PoIFNα1抗猪病毒性感染及对猪病毒性疾病的治疗进行了一系列体内外实验研究[3-4]。粒细胞巨噬细胞集落刺激因子(GM-CSF)是一种细胞因子,主要由淋巴细胞、内皮细胞、成纤维细胞、肥大细胞和巨噬细胞等产生,该细胞因子在机体免疫应答中发挥着重要的作用,其不仅能够活化巨噬细胞、树突状细胞以及单核细胞等免疫细胞,还能够促进造血干细胞的增殖分化[5]。
本研究采用RT-PCR方法从鸡、猪肝脏细胞总RNA中扩增鸡 GM-CSF(ChGM-CSF)和 PoIFNα1基因,通过柔性linker将ChGM-CSF与PoIFNα1基因连接,构建了pET-GM-CSF-PoIFNα1/BL21基因工程菌;并对诱导表达出的重组蛋白(rChGM-CSF-PoIFNα1)进行相应活性检测和鉴定。
1 材料与方法
1.1 主要实验材料 猪睾丸上皮细胞(ST cells)、水疱性口炎病毒(VSV)、E.coliDH5α菌株、BL21(DE3)菌株和pET-32a载体均由安徽医科大学微生物学教研室保存。实验用鸡(雌雄兼用)和猪(断奶仔猪)购自安徽省合肥市周谷堆农贸批发市场,取其肝脏组织保存于本实验室;限制性内切酶BamHⅠ和HindⅢ、T4 DNA连接酶、IPTG、质粒提取试剂盒、DNA回收试剂盒、DNA Marker、TaqDNA聚合酶、pMD18-T载体均购自TaKaRa公司;IFN-α活性测定国家标准品购自中国食品药品检定研究院(批号:07/01,效价:11 000 IU/支);羊抗鼠IgG-HRP和鼠抗重组PoIFNα1单克隆抗体(MAb)购自英国Abcam公司;小鼠抗鸡GM-CSF多克隆抗体(PAb)购自Bio-Rad公司;四氮唑蓝(MTT)美国Biotrin公司;二甲基亚砜(DMSO)购自美国Sigma公司;Lowry法蛋白浓度测定试剂盒(货号:PC0030)购自索莱宝科技有限公司。EtEraserTMSE安全型内毒素去除试剂盒购自厦门鲎试剂生物科技股份有限公司。
1.2 引物的设计与合成 根据GenBank中ChGM-CSF(AJ621740/EU939770.1)与 PoIFN-α1(NM_214393.1)两种目的基因序列,应用Oligo软件设计两对引物。扩增ChGM-CSF基因引物序列为:5'-GCGGGATCCATGTTAGCGCAGC-3'/5'-ACCACCA CCAGAACCACCACCACCAATGCAATCTTTTTCTTC CG-3',扩增片段大小为 432 bp。PoIFN-α1:5'-GGT GGTTCTGGTGGTGGTGGTTCTATGGCTGTGCCTG C-3'/5'-CCGAAGCTTAGTGCGCGTGTTG-3',扩增片段大小为501 bp。在扩增鸡GM-CSF的上游和下游引物中分别引入BamHⅠ酶切位点和Linker序列,在PoIFN-α1的上游和下游引物中分别引入互补的Linker序列和HindⅢ酶切位点。引物由深圳华大基因股份有限公司合成。
1.3 目的基因的扩增及重组表达质粒的构建 分别从鸡和猪肝脏组织中提取其基因组总RNA,反转录获得ChGM-CSF和PoIFN-α1的目的基因cDNA,并以各自cDNA为模板,PCR扩增获得相应目的基因。PCR反应条件:95℃3 min;95℃1 min、59℃30 s、72℃10 min,共 30个循环;72℃ 10 min。经1%琼脂糖凝胶电泳检测并回收各自基因片段,克隆至pMD18-T载体,阳性重组质粒由深圳华大基因股份有限公司测序鉴定,正确的阳性重组质粒命名为pMD-ChGM-CSF和pMD-PoIFNα1。
利用重叠PCR通过linker连接重组鸡ChGMCSF与PoIFNα1,将获得的融合目的基因ChGMCSF-PoIFNα1克隆至pET-32a表达载体中,重组质粒转化E.coliBL21(DE3)菌株,挑取单菌落进行该重组质粒的PCR、双酶切及测序鉴定,重组菌命名为 pET-ChGM-CSF-PoIFNα1/BL21。
1.4 重组蛋白 rChGM-CSF-PoIFNα1的诱导表达、纯化与检测 将pET-ChGM-CSF-PoIFNα1/BL21基因工程菌在LB培养基中扩大培养3 h后,测其OD600nm值在0.6~0.8时,加入终浓度为0.5 mmol/L IPTG,32℃诱导表达5 h,收集菌体,PBS重悬菌体沉淀,4℃超声破碎细菌沉淀,12 000 r/min离心15 min。分别取沉淀和上清及裂解前菌体经SDSPAGE电泳检测。
将表达的rChGM-CSF-PoIFNα1粗制品采用镍离子亲和层析柱纯化,采用EtEraserTMSE安全型内毒素去除试剂盒对纯化后的该重组蛋白去除内毒素。将纯化后的重组蛋白溶液分别以小鼠抗鸡GM-CSF PAb(1∶2 000)和小鼠抗重组 PoIFNα1 MAb(1∶2 000)为一抗,羊抗鼠 IgG-HRP(1∶15 000)为二抗,经western blot鉴定纯化的重组蛋白与两种特异性抗体的反应性。
1.5 rChGM-CSF-PoIFNα1刺激鸡淋巴细胞增殖活性的检测 将纯化的rChGM-CSF-PoIFNα1溶液采用Lowry法测定蛋白含量,利用RPMI1640培养液将其稀释成13个浓度梯度,分别为600 μg/mL、300 μg/mL、 150 μg/mL、 75 μg/mL、 37.5 μg/mL、18.75 μg/mL、9.38 μg/mL、4.69 μg/mL、2.34 μg/mL、1.17 μg/mL、0.58 μg/mL、0.29 μg/mL 和 0.155 μg/mL;备用。无菌采集鸡血2 mL,置于无菌15 mL离心管中,加入同体积的PBS稀释。按照《中华人民共和国药典》2015版通则3526“重组人粒细胞巨噬细胞刺激因子生物学活性测定法”[6],以鸡外周血淋巴细胞/MTT比色法检测不同样品中蛋白含量及外周血淋巴细胞刺激指数值(SI),分析ChGM-CSF的生物学活性。
1.6 rChGM-CSF-PoIFNα1抗病毒活性的测定按照《中华人民共和国药典》2015版通则3523“干扰素生物学活性测定法”以及本实验已建立的检测方法[7-8],采用ST细胞/VSV猪干扰素抗病毒活性和比活性测定系统,以细胞病变抑制法及以不同稀释度的IFN-α标准品作为对照,检测原液中rChGMCSF-PoIFNα1抗病毒活性。
2 结果
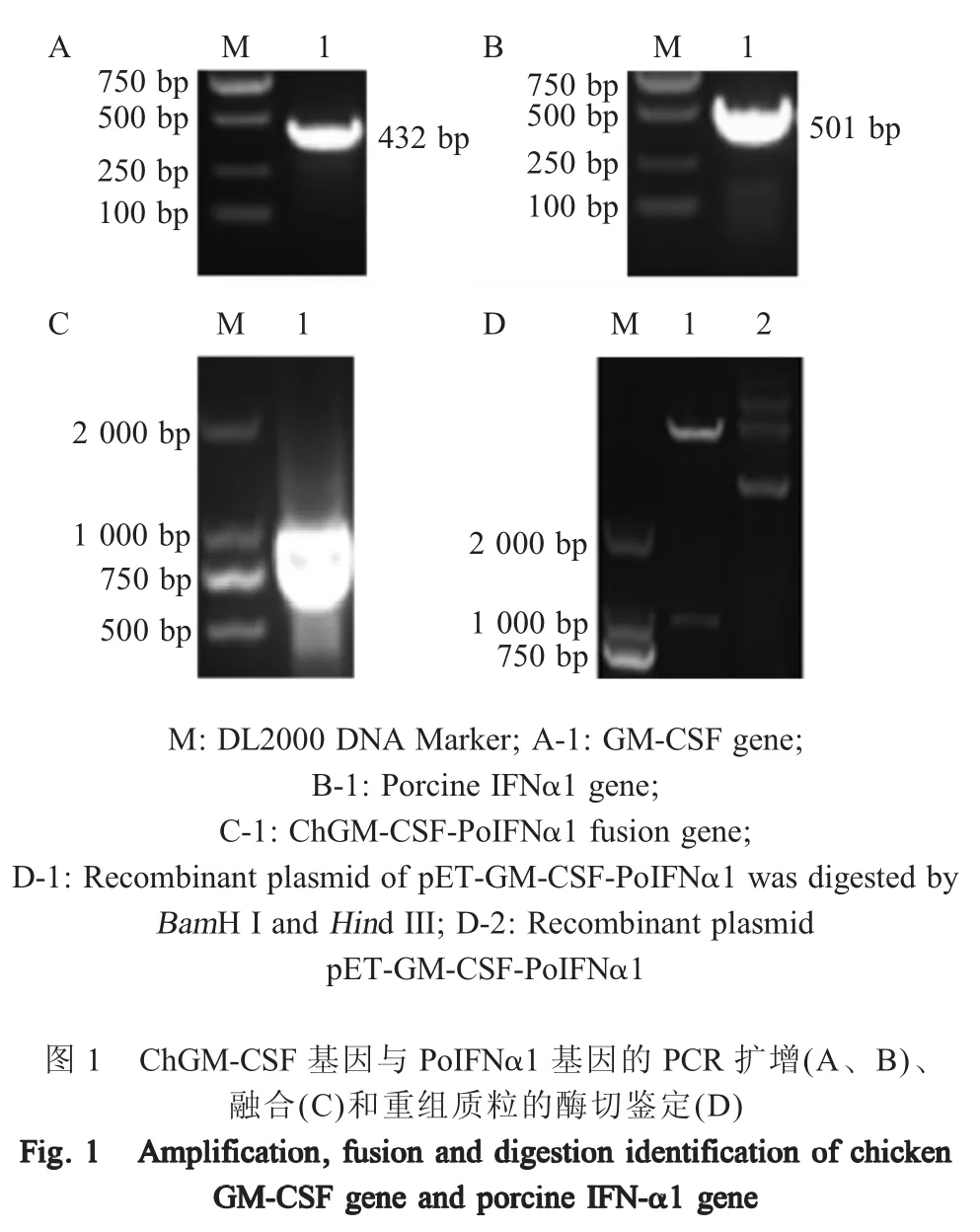
2.1 目的基因的PCR扩增 分别从鸡和猪肝脏组织样品中提取总RNA,经RT-PCR扩增后,产物经琼脂糖凝胶电泳检测。结果显示,在约400 bp和500 bp处出现特异条带,大小与预期相符(图1A、图1B),初步表明,已分别扩增获得了ChGM-CSF和PoIFNα1目的基因。利用重叠延伸PCR技术连接目的基因,扩增产物经琼脂糖凝胶电泳检测,在约1 000 bp处出现明显特异性条带(图1C)。融合PCR产物测序和NCBI Blast在线软件比对分析结果进一步表明,ChGM-CSF和PoIFNα1融合基因正确构建。
2.2 pET-ChGM-CSF-PoIFNα1重组表达载体的构建与鉴定 重组表达载体pET-ChGM-CSF-PoIFNα1经双酶切和质粒测序鉴定。结果显示,重组质粒 pET-ChGM-CSF-PoIFNα1经BamHⅠ和HindⅢ双酶切后在约1 000 bp处可见目的条带,与预期相符(图1D)。重组质粒测序结果与GenBank中ChGMCSF基因和PoIFNα1基因序列一致,表明包含该两个融合基因的重组表达载体构建正确。
2.3 rChGM-CSF-PoIFNα1的诱导表达与鉴定将pET-GM-CSF-PoIFNα1/BL21基因工程菌诱导表达后经SDS-PAGE电泳检测,结果显示,在55 ku左右处出现目的蛋白条带,与预期相符(图2)。同时该结果显示,该目的蛋白条带表达量约占菌体总蛋白的35%,且主要以可溶性表达形式存在于细胞破碎上清中。将该蛋白通过镍离子亲和层析纯化后采用SDS-PAGE检测其纯化效果,结果显示,该目的蛋白纯度约为90%,纯化效果较好。
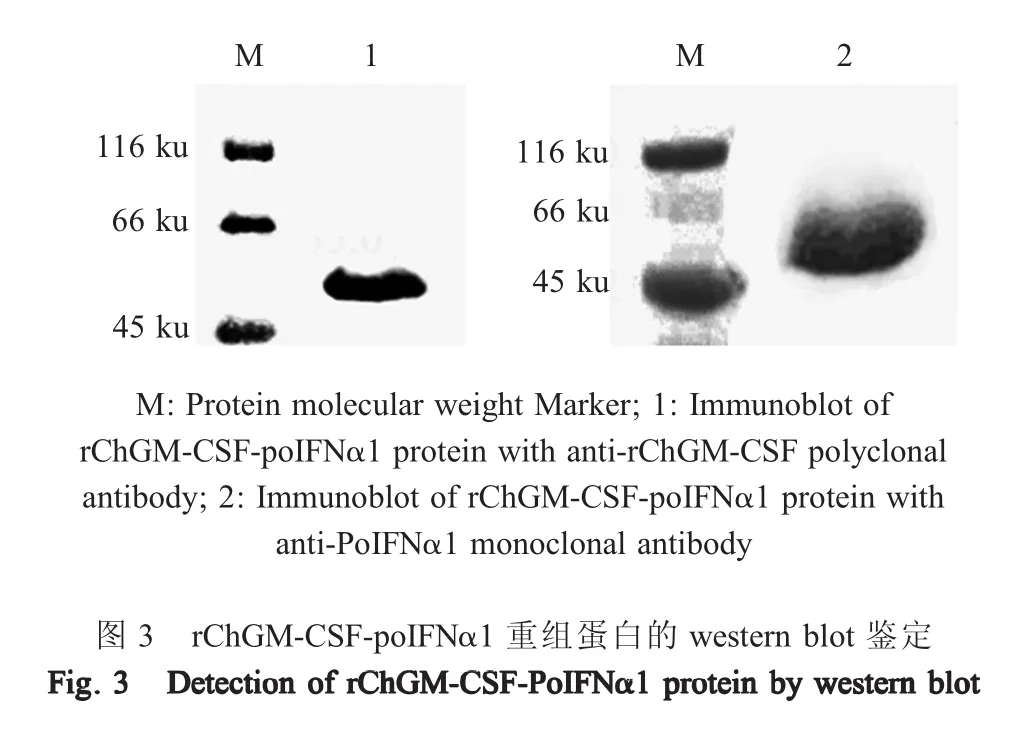
2.4 重组蛋白的反应原性鉴定 分别利用小鼠抗ChGM-CSF PAb(1∶2 000)和小鼠抗重组 PoIFNα1 MAb(1∶2 000)为一抗,对收集的纯化后重组蛋白进行western blot鉴定。结果显示,该重组蛋白可被两种特异性抗体分别识别(图3)。表明该融合蛋白具有与ChGM-CSF和PoIFNα1特异性抗体的双重反应原性。

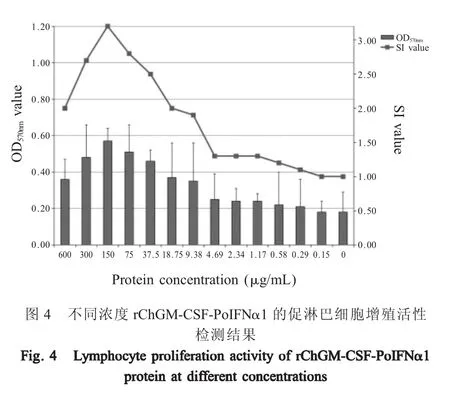
2.5 rChGM-CSF-PoIFNα1对鸡淋巴细胞增殖活性的检测结果 以RPMI 1640培养基作为稀释液,将纯化后去除内毒素检测合格的rChGM-CSF-PoIFNα1(1.2 mg/mL)稀释为13个不同浓度的样本,采用MTT法检测rChGM-CSF-PoIFNα1刺激鸡外周血淋巴细胞的增殖效果(酶标仪测量OD570nm值)。结果显示,当 rChGM-CSF-PoIFNα1 浓度为 150 μg/mL时,鸡外周血淋巴细胞的SI值达到最大值为3.2(图4)。表明该重组融合蛋白具有明显促鸡淋巴细胞增殖的活性。
2.6 rChGM-CSF-PoIFNα1抗病毒活性检测结果采用细胞病变抑制法测定纯化后的rChGM-CSFPoIFNα1抗病毒活性。其中rChGM-GSF-PoIFNα1纯化后原液先稀释成0.1 μg/mL后开始依次做2倍倍比稀释,共做10个稀释度,同时设立上下复孔;而非融合rPoIFNα1对照蛋白先稀释成10 ng/mL,再2倍倍比稀释,设立上下复孔,共做10个稀释度。结果显示,rChGM-CSF-PoIFNα1原液比活性达到1.1×106IU/mg,比非融合 rPoIFNα1对照蛋白的效价(3.7×107IU/mL)低 97%(图 5)。表明 rChGM-CSFPoIFNα1可以明显抑制VSV引起ST细胞病变的效应。
3 讨论
近年来,由于动物传染病致病病原种类多、变异快,一旦发病,往往呈现传播性强、危害性大及具人畜共患性特征等特点;而有些传统疫苗免疫效果较差,又缺少特异性治疗药物,这给动物传染病的预防、控制和治疗造成了极大困难。细胞因子虽已被广泛地应用在动物传染病的临床预防和治疗中并取得了一定成绩,但因其品种繁多,效力较短暂需要反复用药,并有相对种属特异性等的限制,在临床实际应用中缺乏实用性。再者产品自身缺少统一的质控标准和监控手段等,使得细胞因子在动物传染病预防和治疗方面的应用存在许多障碍。因此,研发动物抗感染及预防用生物制品时,应考虑长效性、多功能性和无种属特异性的通用型制剂是临床兽医期待的产品。

本研究将鸡和猪编码不同的细胞因子基因连接出具有不同种属蛋白质的rChGM-CSF-PoIFNα1,并在大肠埃希工程菌中高效表达了该种新的可溶性重组蛋白。该蛋白分子量(约为55 ku)较大,同时具有较强的体外抗病毒活性和促进鸡淋巴细胞增殖的活性。Western blot结果显示,该融合蛋白具有与ChGM-CSF多抗和rPoIFN MAb的双重反应原性。采用ST细胞/VSV病毒猪干扰素抗病毒活性和比活性测定系统检测rChGM-CSF-PoIFNα1的效价,以不同稀释度IFN-α标准品作为对照。所测数据分析可知,两者均具有明显抗病毒的效应,该试验测得rChGM-CSF-PoIFNα1的抗病毒效价为1.4×106IU/mL,比活性为1.1×106IU/mg。提示 rChGM-CSF不干扰rPoIFNα1的抗病毒效应。但与 rPoIFNα1相比,rChGM-CSF-PoIFNα1的比活性降低了97%左右。造成比活性降低的原因一方面可能由于连接的rChGM-CSF相对分子质量高达32 ku,是rPoIFNα1相对分子质量的1倍左右;另一方面由于连接rChGM-CSF分子后,rPoIFNα1分子的空间结构发生了变化,使之与PoIFNα1受体的结合产生了空间位阻[9]。近年研究显示,GM-CSF作为疫苗佐剂已在临床广泛使用,有效地增强了疫苗的免疫效力[10]。本研究采用MTT法对rChGM-CSF-PoIFNα1促鸡淋巴细胞增殖活性检测结果显示,当rChGM-CSF-PoIFNα1蛋白浓度为150 μg/mL时,外周血淋巴细胞的SI值达到最大值为3.2;表明该重组融合蛋白具有促鸡淋巴细胞增殖的活性,提示该融合蛋白可能具有一定的免疫增强效力。因此,下一步要解决的另一问题是将该融合蛋白作为鸡或猪用疫苗佐剂进行研究,为探索细胞因子增强疫苗免疫效力及其相关的机制的研究奠定基础。
