空腹与餐后条件下非洛地平缓释片在健康人体内的药代动力学比较研究
2019-06-05吴正宇李相鸿周理想梁大虎赵亚男
吴正宇,李相鸿,周理想,梁大虎,赵亚男,3
(1.皖南医学院,安徽 芜湖 241002;2.皖南医学院第一附属医院弋矶山医院,安徽 芜湖 241001;3.安徽医健领航医药科技有限公司,安徽 合肥 230031)
高血压是世界上最常见的慢性疾病,也是心脑血管疾病、肾脏疾病和死亡最重要的危险因素,控制高血压对心脑血管疾病的预防和管理至关重要,非洛地平(Felodipine,FLDP)是一种二氢吡啶类钙通道阻滞剂,常用于治疗高血压和稳定型心绞痛[1-2]。非洛地平是BCS(生物药剂学分类系统)Ⅱ类药物,具有高渗透性、低溶解性的特点,制作成缓释制剂具有优良的长效释放特性,可减少病人服药频率[3-4]。非洛地平血浆浓度曲线会伴随食物摄取受到强烈的影响,有研究发现薄荷醇、柚汁、葡萄汁、咖啡等会影响非洛地平的药动学特征[5-6]。与食物一起摄入后,在胃近端混合不均匀会对药物吸收产生影响,导致非洛地平的血浆峰值药物浓度增加[7-8]。本试验采用液相色谱串联质谱(LC-MS/MS)法检测人血浆中非洛地平的浓度,研究了空腹及餐后条件下非洛地平缓释制剂的药动学,比较了空腹与餐后条件下吸收与代谢特征,评价了进食对非洛地平药代动力学参数的影响。
1 材料与方法
1.1 仪器 UPLC20-AD超快速液相系统(岛津公司);AB Sciex Triple QuadTM AB SCIEX 5500 质谱(美国应用生物系统公司)。
1.2 试剂与试药 非洛地平对照品(待测物,批号:100717-201403)来源中国食品药品检定研究院;非洛地平-d5对照品(内标物,批号:1037-147A1)来源于TLC Pharmaceutical Standards;甲醇(色谱纯,Merck公司),乙酸铵(分析纯,Sigma公司)试验用水为自制超纯水,非洛地平缓释片(Plendil,depottabletter)(规格:5 mg/片,阿斯利康(瑞典)制药有限公司,批号:YCEN)。
1.3 给药方法及血浆样品采集 本试验为随机开放试验,共纳入受试者72名,其中36名受试者被随机分至空腹组,在空腹条件下服用非洛地平缓释制剂,男女均有,年龄为(28.3±6.1)岁,体重为(65.7±8.9)kg,服药前禁食10 h过夜;另外36名受试者被随机分至餐后组,在餐后条件下服用非洛地平缓释制剂,男女均有,年龄为(29.5±6.15)岁,体重为(63.94±7.22)kg,禁食10 h过夜,服药前半小时给予高脂餐。给药前(0 h)及给药后1、2、2.5、3、3.5、4、4.5、5、6、8、12、24、36、48、60 h取静脉血4 mL,置抗凝管中,4 000 rpm离心5 min,取血浆于-70~-20 ℃冰箱储存,用于血药浓度检测。非洛地平对光较敏感,样品处理过程中应注意避光(黄光下操作)。试验经过皖南医学院弋矶山医院伦理委员会批准,试验地点为皖南医学院弋矶山医院Ⅰ期临床试验病房。试验前所有受试者均签署知情同意书。
1.4 色谱及质谱条件 使用LC-MS/MS法检测血浆样品中的血药浓度。色谱柱:Luna C8色谱柱(5 μm,50 mm×2.0 mm),C18预柱(4 mm×2.0 mm);流动相:A 10 mmol·L-1乙酸铵水溶液,B甲醇;流速:0.6 mL·min-1,进样时间:4.5 min;进样量:5 μL,流动相洗脱流程见表1。离子源:电喷雾离子化(ESI)源,离子源喷雾电压(IS):5 000 V;离子源温度(TEM):500 ℃,气帘气(CUR):20 psi;碰撞气(CAD):9 unit;离子源气体1(GS1):50 psi,离子源气体2(GS2):50 psi;检测方式:多反应监测模式(MRM);监测离子:338.1~384.3(非洛地平),338.1~389.3(内标物,非洛地平-d5);碰撞电压(CE):非洛地平与非洛地平-d5均为15 eV。

表1 流动相洗脱程序
1.5 溶液配制 非洛地平标准储备液:精密称取非洛地平对照品,用适量甲醇溶解,配制成浓度为1.00 mg·mL-1的非洛地平储备液A,移取0.02 mL 非洛地平储备液A加到19.98 mL甲醇中,混合均匀,配制成浓度为1.00 μg·mL-1的非洛地平储备液B,移取1.00 mL非洛地平储备液B加到9.00 mL甲醇中,混合均匀,配制成浓度为0.100 μg·mL-1的非洛地平储备液C。非洛地平对照品工作液:分别取非洛地平储备液A 0.02 mL,非洛地平储备液B 5.00、4.50、4.00、2.50、2.00 mL,非洛地平储备液C 5.00、2.50、0.50、0.30、0.20、0.10 mL,均添加甲醇至10 mL,配制成浓度为2 000、500、400、450、250、200、50.0、25.0、5.00、3.00、2.00、1.00 ng·mL-1的非洛地平对照品工作液。
非洛地平-d5(内标)标准储备液:精密称取非洛地平-d5对照品,同上操作,制备成浓度为1.00 mg·mL-1的内标储备液A,浓度为1.00 μg·ml-1的内标储备液B,浓度为0.100 μg·mL-1的内标储备液C。非洛地平-d5工作液:与非洛地平工作液进行同样操作,配制成浓度为2 000、500、400、450、250、200、50.0、25.0、5.00、3.00、2.00、1.00 ng·mL-1的非洛地平-d5工作液。
1.6 血浆样品预处理 向固相萃取板 (C18E,25 mg )每个孔内加入0.8 mL甲醇溶液与0.8 mL 超纯水,取500 μL样品(空白样品和内标空白样品加500 μL空白人血浆)至96孔板(Plate-1)中;分别加入10 μL甲醇∶水(1∶1),混合均匀,将样品转移至预处理的固相萃取板中,减压抽干;向每个孔内加入0.8 mL超纯水,减压抽干,再加入0.8 mL超纯水,减压抽干;加入0.25 mL甲醇溶液,减压抽干,将洗脱液均收集于新的96孔板(Plate-2)中,提交LC-MS/MS分析。
1.7 药动学参数的计算 AUC0~t为0到相应时间的血药浓度-时间曲线下面积,AUC0~∞为0到时间为无穷大的血药浓度-时间曲线下面积,Cmax为最大血药浓度,Tmax为达到最大血药浓度时的时间,t1/2为消除半衰期,Vz为表观分布容积,Cl为血浆清除率,ct为相应时间的血药浓度。其中Cmax、Tmax、ct为实测值。使用Phoenix WinNolinon 6.4软件,采用非房室模型计算药动学参数。
1.8 累计吸收百分数的计算 使用Phoenix WinNolinon 6.4软件拟合血药浓度-时间数据,采用赤池(AIC)法判定房室模型,选用AIC最小的房室模型,依据房室模型判定结果选择Wagner-Nelson法或Loo-Riegelman法计算各采血点时非洛地平的累计吸收百分数(Fa)。
1.9 统计分析 数据采用SAS 9.4软件进行统计分析,Cmax与AUC经过对数转换后进行分析,对于正态分布的资料采用两样本t检验,对于非正态分布资料采用秩和检验。P小于0.05时认为差异具有统计学意义。
2 结果
2.1 血浆样品检测方法学验证结果 本法测定时,非洛地平及非洛地平-d5的保留时间分别约为2.07、2.24 min。血浆中非洛地平、内标峰形良好,出峰位置无杂峰干扰测定。在浓度为0.02、0.04、0.1、0.5、1.0、5.0、9.0、10.0 ng·mL-1范围内待测物浓度与待测物与内标物的峰面积比具有很好的线性关系,本方法测定非洛地平的标准的曲线方程为Y=0.547X+0.004 68(r=0.998 6);Y为待测物与内标物的峰面积比,X为待测物浓度。配制浓度为0.6、4、8 ng·mL-1的血浆样品,每个浓度进行6个样本分析,每天测定一批,连续5 d,批间精密度分别为3.70%、0.99%、1.93%,批内精密度分别为2.31%、2.42%、3.57%;批间准确度分别为105.47%、106.20%、105.78%,批内准确度分别为105.75%、105.29%、106.35%;提取回收率分别为88.89%±5.43%、87.56%±5.54%、84.6%±3.21%。血浆样品在室温放置24 h、-4 ℃冷藏48 h、-20 ℃与-70 ℃冰箱冷冻保存后冷冻-解冻循环5次、-20 ℃与-70 ℃冰箱放置33 d、全血离心分离前基质中室温和冰水浴2 h、血浆处理后提取物-4 ℃冷藏314 h后均稳定。
2.2 药代动力学结果 药代动力学结果如表2所示。空腹组有两名受试者中途无理由退出,34名受试者数据纳入药动学参数计算。Cmax、AUC0~60、AUC0~∞与Vz的t值分别为9.61、5.64、5.15、4.15,P值均小于0.05,差异具有统计学意义,认为餐后条件下Cmax、AUC0~60、AUC0~∞显著高于空腹条件下,而餐后组Vz显著小于空腹条件下。Tmax与t1/2秩和检验的Z值分别为-0.52和-1.84,P值均大于0.05,差异无统计学意义,认为进食不会对药物的t1/2与Tmax产生影响。Cl秩和检验的Z值为4.459 5,P值小于0.05,差异具有统计学意义,认为餐后组Cl显著小于空腹组。血药浓度时间曲线图见图1。

表2 空腹与餐后条件下口服5 mg非洛地平缓释片后药动学参数
注:采用双侧t检验,餐后组与空腹组相比,aP<0.05;采用秩和检验,餐后组与空腹组相比,bP>0.05
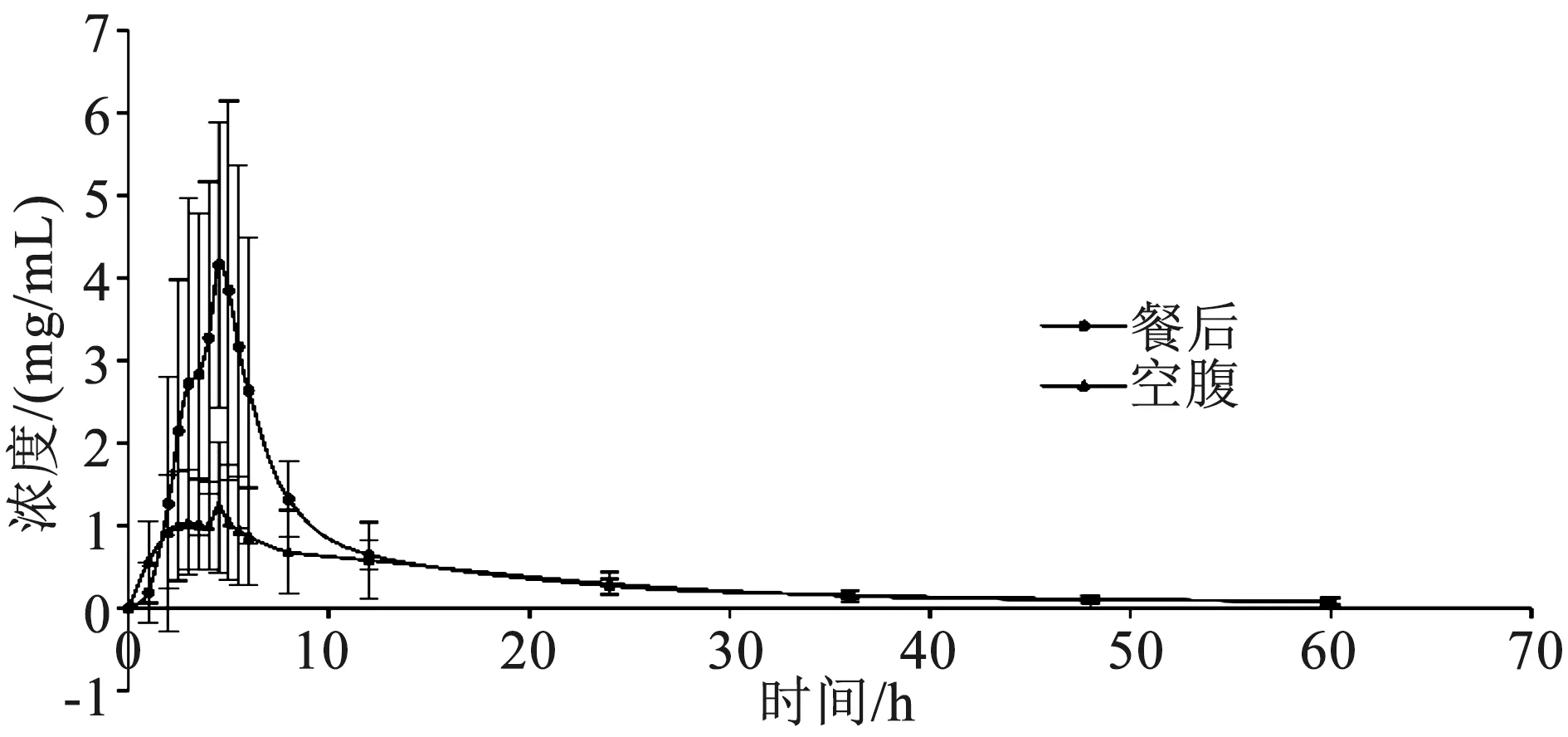
图1 受试者在空腹或餐后条件下服用非洛地平缓释片后血药浓度-时间曲线图
2.3 药物累计吸收百分数 权重取1/c2,一室模型与二室模型的AIC分别为-44.24、-45.66,因此采用二室模型,选择Loo-Riegelman法计算Fa。
(1)
t时周边室药物浓度:
(2)
k10为药物消除速率常数;(Xp)t为t时周边室的药量,(Xp)t(n-1)为上一个时间点时周边室的药量;Vc为周边室的分布容积,k12为药物从中央室向周边室转运的一级速率常数;k21为药物从周边室向中央室转运的一级速率常数;Δc为与上一时间点血药浓度差值,Δt为与上一时间点时间差值。
其中k10、k12与k21来源于edgar等[9]的研究,k10=0.626,k12=0.727,k21=0.554。
空腹于餐后条件下非洛地平累计吸收曲线见图2。
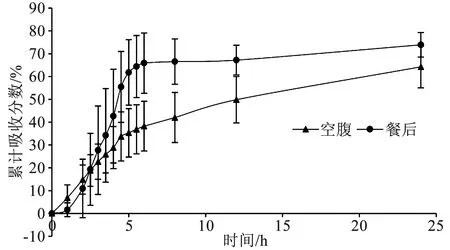
图2 受试者在空腹或餐后条件下服用非洛地平缓释片后24 h内非洛地平累计吸收百分数-时间曲线图
在空腹与餐后条件下,药物在24 h均未被完全吸收,餐后组药物吸收速度与量远大于空腹组。空腹组与餐后组在开始时药物吸收均较快,空腹组在给药5 h后吸收放缓,但直到24 h依然在持续吸收。餐后条件下在6 h前有较快的吸收,但6 h之后吸收累计吸收百分数基本稳定,很少再有吸收。进食对非洛地平缓释片的吸收特征有显著影响。
3 讨论
本试验采用LC-MS/MS法测定人血浆中非洛地平的浓度,相比于文献[10-12]使用的高效液相色谱法、荧光光度法、紫外分光光度法等,具有更好的专属性与灵敏度,定量下限达到了0.02 ng·mL-1,可以更精确的测定清除末期的血药浓度,使药动学参数计算更为准确。文献[13-14]保留时间均大于5 min,时间较长;但是本方法血浆样品处理较为繁杂,需要改进。
在选择受试者时,由于非洛地平会具有导致牙龈出血的风险[15],因而排除了牙龈炎的患者,试验过程中有部分受试者出现了轻度的牙龈炎症状。相关文献报道了非洛地平在空腹状态下的药动学参数,当采样时间为72 h时t1/2大约在20 h左右[16-17],与本试验结果相近,也有文献[18-19]报告t1/2在14 h左右,这可能与计算消除速率常数时的时间点不在消除末期,过迟或过早可能会导致计算结果偏大或偏小。将相关文献[5-6,16-20]结果经剂量校正到与本试验剂量相同后,空腹组Cmax均值在1.5 h·ng·mL-1左右、AUC0~t均值在19 h·ng·mL-1左右、AUC0~∞均值在21 h·ng·mL-1左右,本试验结果与它们接近。有研究报道[17]非洛地平的血药浓度-时间曲线下面积与CYP3A5*3 和 BCRPC421A 基因多态性有关,本试验由于条件限制未能进行验证;从药代动力学结果还发现空腹组Cmax、AUC0~t与AUC0~∞的变异系数均在52%以上,而餐后组仅Cmax的变异系数在47%,AUC0~t与AUC0~∞的变异系数均小于33%。由空腹状态与餐后状态的Cmax、AUC0~t与AUC0~∞统计检验结果可知餐后组药物吸收程度要显著大于空腹组。柯晓丹[19]等人报道了空腹与餐后条件下AUC0~∞无显著性差异,这个结果与本研究有所不同。以上结果表明餐后条件下人体对非洛地平缓释片的吸收速度与程度均较大,可能是由于餐后条件下分泌的胃酸与胆汁使药物得到更好的溶解。
由于人体节律,我们使用累计吸收百分数-时间曲线观察了24 h内药物的吸收状况。结果较为直观。从药物的吸收过程来看,在24 h内药物未被完全吸收。24 h后多数受试者的药物可能已排出体外,且本试验中未研究静脉给药的药代动力学特征,相关参数参考了他人的研究。以上原因可能会导致计算结果与实际情况出现偏差,因此本试验药物吸收过程结果不能完全代表非洛地平缓释片的吸收特征,可在比较空腹与餐后条件下人体对非洛地平吸收差异时作为参考。结果表明餐后状态下服药会使非洛地平的吸收速度与程度大幅度增加,与有关报道[21]相比结论一致,且本试验人数远大于该研究的8人,试验结果更加可信。在服药开始一段时间,空腹条件与餐后条件下药物的吸收速度均较快,给药6 h后,餐后组药物吸收基本停止,而空腹组则在给药5 h后呈现出持续而缓慢的吸收。
食物增加了非洛地平缓释片的吸收速度与程度,空腹与餐后条件下非洛地平缓释片在健康人体内的药代动力学特征有较大的差异。
