FH检测在直肠恶性肿瘤早期筛查中的诊断价值
2019-05-06马茜黄晓明郭亚苹高记华高策戚文月郭虹君
马茜,黄晓明,郭亚苹,高记华,高策,戚文月,郭虹君
0 引言
直肠恶性肿瘤(rectal cancer)是消化道一种常见恶性肿瘤,其发病率排中国肿瘤发病率第四位,死亡率居第五位[1]。近年来由于城市化的加剧及居民饮食结构的改变,我国直肠恶性肿瘤的发病率逐年升高,严重威胁人民的生命健康。由于其早期无明显症状,极易漏诊,待发现时多处于中晚期,预后不良,因此早发现、早诊断、早治疗可有效提高直肠癌的5年生存率和治愈率[2]。
目前我国直肠恶性肿瘤筛查方式主要包括:直肠指诊、电子结肠镜检查、肿瘤标志物基因检测、大便潜血试验、粪便-DNA检测等。这些检查手段各有优劣,其中直肠指诊经济、便捷,但对于直肠中上段病变的漏诊率较大,只适用于病变部位较低的直肠恶性肿瘤中晚期患者,特异性及敏感度均较低。电子结肠镜检查适用于高危人群,精确度及费用均较高,但其为侵入性检查,且受肠道准备情况、医者操作技术等影响较大,易并发肠道穿孔、出血等[3];肿瘤标志物基因检测属于广谱性肿瘤标志物,常用于胃肠道恶性肿瘤的诊断、判断预后、检测疗效、肿瘤复发等[4],费用较高,检测时间长;大便潜血试验特异性及敏感度相对较低;粪便-DNA检测特异性高但敏感度低,价格高,在我国经济贫困地区仍难以推广。
因此,本研究以病理组织学诊断为金标准,以电子结肠镜检查为辅助,将300例受试者分别进行直肠上皮细胞稳定性细胞游离亚铁原卟啉,即细胞内游离血红素(cell free ferrous protoporphyrin,FH)检测、癌胚抗原(CEA)检测、糖类抗原19-9(CA19-9)检测,并进行对比分析,评价直肠上皮细胞稳定性FH检测诊断直肠恶性肿瘤的临床意义。
1 资料与方法
1.1 研究对象
研究对象来源于2017年9月—2018年3月在河北省中医院肛肠科就诊及住院的患者。所有患者均行肛门指诊及结直肠镜检查,发现异常者行组织病理学及影像学检查,按照中华医学会消化病学分会《中国结直肠癌预防共识意见》[5]及《中国结直肠癌诊疗规范(2017 版)》[6]制定诊断依据及纳入、排除标准进行筛选。筛选出300例,其中男性173例,女性127例,年龄17~89 岁,平均(53.44±14.36)岁。结合患者病史,经电子结肠镜、组织病理学及影像学检查初次确诊为直肠肿瘤患者38例,年龄36~87岁,平均年龄(58.97±11.49)岁;确诊为直肠恶性肿瘤术后患者46例,包括44例未复发患者及2例复发患者(后并入直肠肿瘤组),年龄45~85岁,平均年龄(60.65±10.04)岁;结直肠息肉患者17例,年龄65~79岁,平均年龄(71.53±5.68)岁;结直肠炎患者49例,年龄17~80岁,平均年龄(51.86±14.11)岁。余患者共150人,其中肛窦炎患者24例;痔疮患者45例;肛瘘患者15例;肛周脓肿患者6例;肛裂患者25例;便秘患者32例;肛门及结直肠黑变病患者1例;骶前囊肿患者2例。所有患者签署知情同意书,且通过医院医学伦理委员会审查批准。
1.2 纳入标准及排除标准
1.2.1 纳入标准 (1)符合西医诊断标准;(2)所有病例均为我院就诊及住院患者;(3)所有患者均进行病史询问、体格检查、肛门指检、血常规、结直肠镜检查;上述检查异常者自愿行病理学检查、腹部彩超、全身淋巴结彩超、上腹部CT+下腹部CT+盆腔MR扫描等以协助诊断;(4)被检人员依从性良好、自愿参加,并签订知情同意书。
1.2.2 排除标准 (1)有精神病疾患者;(2)有自主意识但不愿意接受此项筛查者;(3)病情危重,无法进行相关检查的患者。
1.3 FH检测
1.3.1 直肠黏膜细胞稳定性FH检测试剂(医用型单人份)
1.3.1.1 试剂来源 本产品来自于由青岛东孚美伦生物科技有限公司(备案号:鲁青械备20140008号生产备案号:鲁青食药监械生产备20160025号)。检测。方法严格按照FH试剂盒的操作步骤进行。
1.3.1.2 样本收集及要求 准备好一次性手套、液体石蜡油、一次性肛门镜、直肠黏膜细胞稳定性FH检测试剂,检查并确认本试剂包装完好;采样部位在取样前不得清洗、上药、搔刮;嘱患者取膝胸位或侧卧位,用液体石蜡润滑一次性肛门镜后,将其置入肛管齿状线处,持采样拭子,在齿状线附近轻柔的擦拭获取直肠黏膜渗液,充分蘸取后,将取样器头部放入C试剂(样本瓶)内充分搅动,使所采集标本与C试剂充分混匀,静置约10 s后,当即检验。
1.3.1.3 检测。方法(1)将A试剂滴管管口两翼部顺时针旋转折断,把试剂准确滴入测试池;(2)将已空置的A滴管在C试剂内吸取样本液不少于1 ml滴入测试池;(3)旋转折断B试剂滴管,将试剂准确滴入测试池;(4)操作完毕后,120 s内将测试池的显色与比色板进行比对,获得检测结果。
1.3.1.4 观察指标判定标准 阴性:试剂不变色;弱阳性:试剂呈淡蓝色或淡绿色;阳性:试剂呈淡绿色或蓝色;强阳性:试剂呈深蓝色。总阳性率=(弱阳性+阳性+强阳性)/总人数×100%。
1.3.1.5 注意事项 若显示池内标本先显示上述某种颜色,后转为深黄色或棕红色,表明样本内混有血液,应按照先出现的颜色进行结果判读(深黄色或棕红色是混有血液的征象)。
1.3.2 肿瘤标志物(CEA)检测
1.3.2.1 检测过程 被检测患者无需限制饮食,血液样本用一次性专用血液样本采集管抽取全血,送检验科检验。
1.3.2.2 判定标准 阴性:CEA 测定结果≤3.40 ng/L;阳性:CEA 测定结果>3.40 ng/L。
1.3.3 糖类抗原19-9(CA19-9)检测
1.3.3.1 检测过程 同1.3.2.1
1.3.3.2 判定标准 阴性:CA19-9测定结果≤27.00 ng/L;阳性:CA19-9测定结果>27.00 ng/L。
1.4 统计学方法
采用 SPSS21.0统计学软件进行数据分析,计量资料用均数±标准差(±s)表示,两组间比较采用t检验;计数资料用率表示,组间比较采用χ2检验,多样本比较采用秩和检验,等级分布比较采用秩和检验,P<0.05为差异有统计学意义。
2 结果
2.1 FH检测结果
直肠恶性肿瘤术后患者46例(此46例患者在本次检测前已行直肠恶性肿瘤切除术),FH检测10例阳性,后经病理学检查已确诊2例为肿瘤复发,此2例并入直肠恶性肿瘤组,故直肠恶性肿瘤术后未复发患者44例中,FH检测8例阳性,阳性率18.18%;此44例患者术后均进行化疗,且定期复查上腹部CT+下腹部CT+盆腔核磁,取造瘘口(造瘘患者)附近组织或直肠吻合口(保肛患者)附近组织送病理,未见肿瘤,定期随访(2月为一周期)未见异常,仍继续随访。最终确诊为直肠恶性肿瘤患者40例,(2例术后复发患者及38例首次发现肿瘤患者),FH 检测38例阳性,阳性率95%,此40例直肠癌患者经病理学检查确诊早期直肠癌有30例,FH阳性28例,阳性率93.33%。中晚期10例,FH阳性10例,阳性率100%。由此可见,直肠黏膜细胞稳定性FH检测结果有较高的敏感度。结直肠息肉患者17例,FH检测4例阳性,阳性率23.53%,经病理学检查腺瘤样息肉12例,其中2例绒毛状腺瘤,2例绒毛状管状腺瘤,8例管状腺瘤,癌前病变检出率33.33%,见表1。
2.2 CEA和CA19-9检测与FH检测结果比较
300例入组患者,分别进行FH、肿瘤标志物癌胚抗原(CEA)及糖类抗原19-9(CA19-9)测定,结果见表2~4。
由表1~3可得出FH检测直肠恶性肿瘤具有较CEA、CA19-9更高的阳性率。可以认为FH检测与CEA、CA19-9检测直肠恶性肿瘤受试者中检出率有差别。
由表4得出FH检测直肠恶性肿瘤术后未复发患者阳性率低于CEA,与CA19-9持平,可以认为FH检测与CEA检测此组患者有差异,FH检测与CA19-9检测此组患者检出率无差别。
2.3 三种检测。方法临床常用评价指标
以所有受试者的病理检查诊断结果为金标准,以电子结肠镜检查为辅助,将三种。方法的检测结果分别计算出敏感度、特异性、假阴性率(漏诊率)、假阳性率(误诊率)、阴性似然比(LR-)、阳性似然比(LR+)、诊断指数(DI)、Youden指数、粗符合率(CA)、阴性预测值(PV-)、阳性预测值(PV+)等指标,见表5~6。
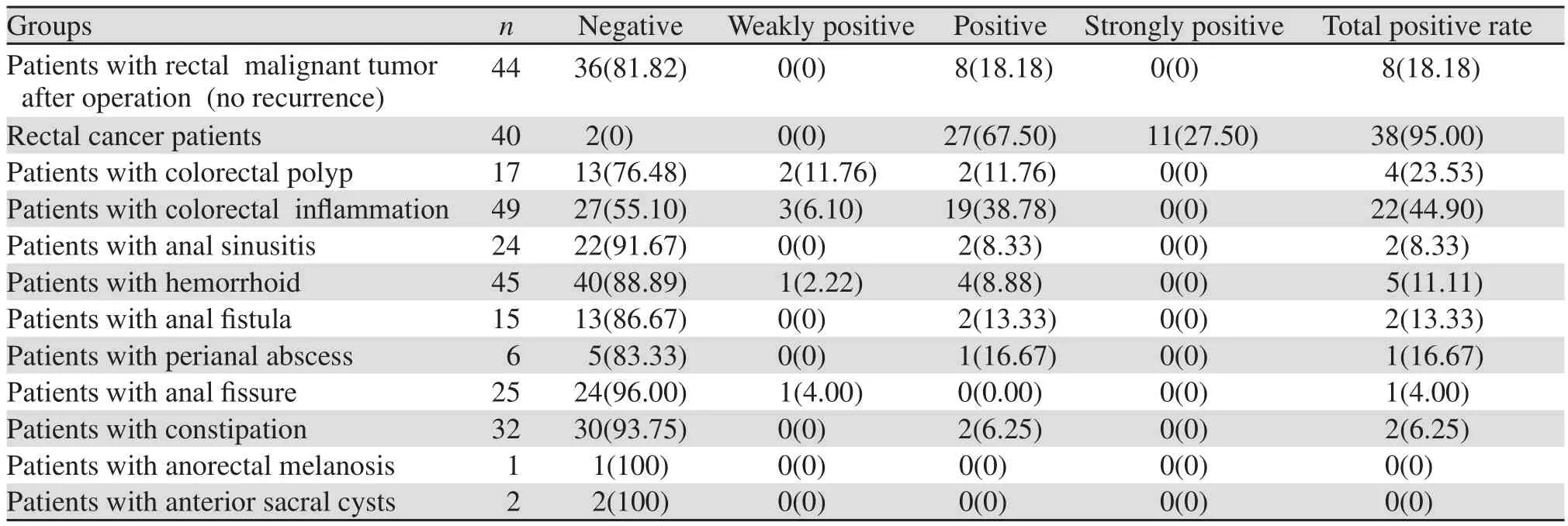
表1 300例受检者的FH检测结果 (n(%))Table1 FH test results of 300 subjects (n(%))
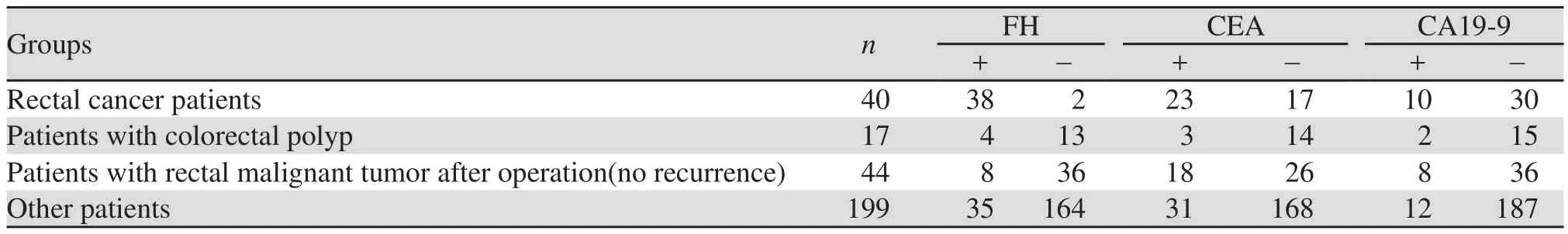
表2 300例受检者三种。方法检测结果 (n)Table2 Three detection methods of 300 subjects (n)
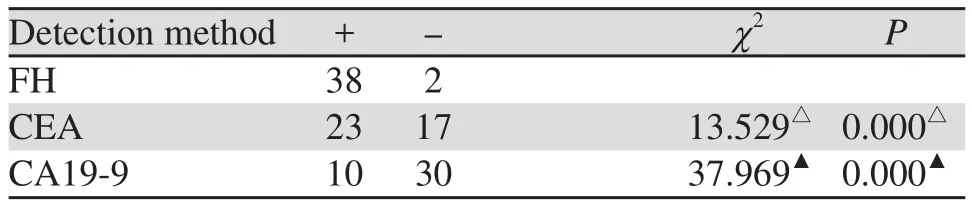
表3 肿瘤患者CEA、CA19-9检测分别与FH检测结果比较 (n)Table3 Comparison of test results between CEA, CA19-9 and FH in tumor patients (n)
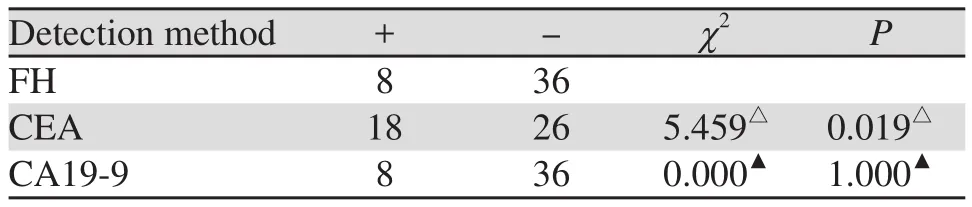
表4 肿瘤术后(未复发)患者CEA、CA19-9检测分别与FH检测结果比较 (n)Table4 comparison of CEA, CEA and ca19-9 test results with FH test results in the patients of postoperative tumor(no recurrence) (n)
通过表5~6可直观的看出,三种检测。方法在直肠恶性肿瘤筛查中FH检测的敏感度、阳性似然比、诊断指数、约登指数、阴性预测值、阳性预测值均高于CEA和CA19-9检测,假阴性率和阴性似然比低于两者。CA19-9检测的特异性、假阴性率、阴性似然比、粗符合率最高,敏感度,假阳性率、诊断指数、约登指数及阴性预测值最低。CEA检测则假阳性率最高,特异性、阳性似然比、阳性预测值最低。
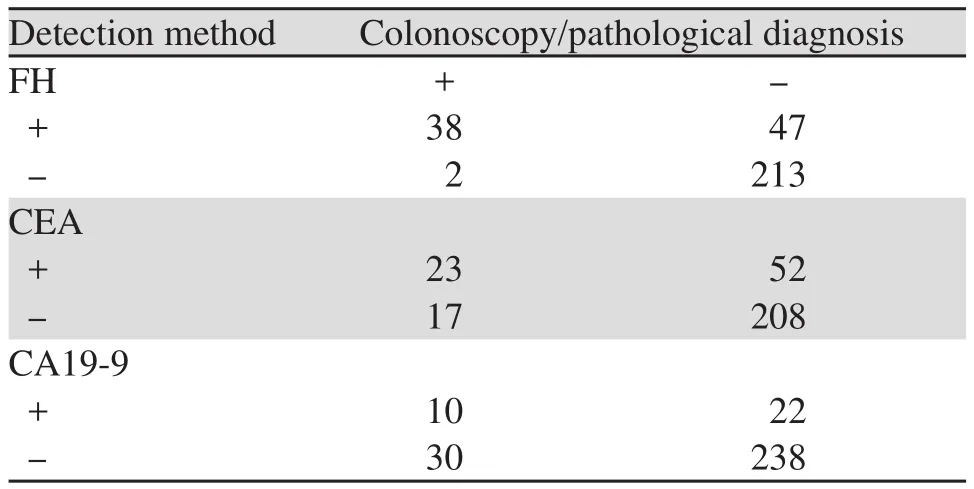
表5 直肠肿瘤、非肿瘤三种。方法检测结果 (n)Table5 Detection of rectal tumors and non-tumor results by three methods (n)
3 讨论
CEA和CA19-9是消化道恶性肿瘤应用较为广泛的标志物,无显著脏器特异性,且在肿瘤早期诊断中CA19-9的敏感度较低,部分直肠恶性肿瘤患者未能被检出,但某些非癌性因素如糖尿病、结肠炎、肝炎等因素也会导致CEA、CA19-9轻度升高,会存在一定的假阳性率。
肠道未见肿瘤、息肉的非肿瘤术后患者,FH仍检出部分阳性患者,可能是由于此类患者因炎症性肠病、混合痔出血、或肛瘘分泌脓液等原因致使收集的直肠脱落细胞结构不稳定,易出现假阳性率。
广泛存在于细胞内的亚铁血红素参与多种酶的构成[7],生理状态下,其通常以结合蛋白的形式发挥作用[8],在致癌因子的作用下,抑癌基因(尤以是抑癌基因p53为主)发生突变或缺失,细胞内稳定结构被破坏,能量代谢紊乱,细胞内蛋白构象发生改变,使某类亲脂性物质进入含亚铁原卟啉蛋白的疏水核内,导致亚铁原卟啉脱落为游离状态,称之为FH物质。游离的FH物质作为一种可氧化损伤细胞的活性基团,结构极不稳定,会夺取邻近的组织(脂肪、蛋白质及DNA等)的电子,以稳定自己的状态,而被夺取电子的组织结构则形成自由基,去夺取新的的电子,似多诺米骨牌效应,随着细胞的损伤加重导致细胞稳态失衡,使细胞增生加速、凋亡减少、分化降低,最终恶变,促进溶酶体水解酶溢出引起细胞自溶加重,FH物质渗出增多,并且其渗出量与上皮细胞的恶性程度成正比[9]。综上所述,FH物质可作为癌前病变标志物对高危患者进行早期筛查[10-12]。
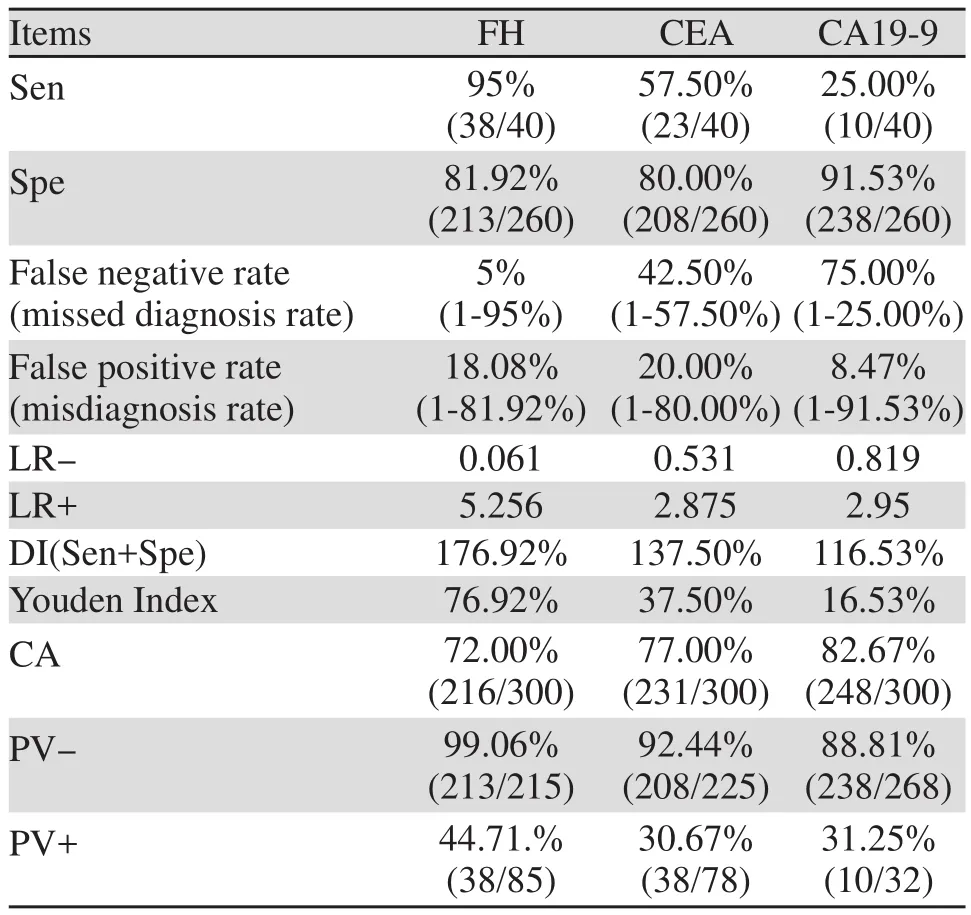
表6 直肠恶性肿瘤三种检测。方法与病理学检测结果比较Table6 Comparison between three detection methods results for rectal malignancy and pathological detection results
FH检测主要是通过FH与特定物质的氧化还原反应使直肠上皮细胞染色,根据着色的深浅分析患者病变程度[13]。它具有较高的敏感度,即使在早期肿瘤患者中也有较高的阳性率,阳性患者会提高警惕并在短时间内通过病理学检查以确诊,符合早发现、早诊断、早治疗的原则,癌前病变及早期肿瘤患者经积极治疗可有效提高直肠癌的5年生存率和治愈率。是自检型产品,检测结果可根据目测比色法[14]即查即得,简单易行,经济实用,具有临床可行性。在贫困、偏远地区及基层医院有较高的使用价值,可扩大直肠恶性肿瘤的筛查规模,降低直肠恶性肿瘤的患病率及死亡率,为我国直肠恶性肿瘤的筛查手段提供了新的思路。
