促性腺激素释放激素激动剂对激素受体阴性年轻乳腺癌辅助化疗患者卵巢功能的影响及抗苗勒氏管激素检测的价值
2019-04-24姚宝国陈万贞尹海庆
张 珂,姚宝国,苏 莉,陈万贞,尹海庆
(1.河南宏力医院检验科,河南 新乡 453400;2.宁夏回族自治区人民医院肿瘤内科,宁夏银川,750021;3.宁夏回族自治区人民医院甲乳外科,宁夏 银川,750021;4.河南宏力医院肿瘤内科,河南 新乡 453400)
乳腺癌已成为全球女性最常见的恶性肿瘤之一,发病率高居女性恶性肿瘤的首位,并且发病率逐渐递增[1],我国女性乳腺癌20岁之前处于较低水平,此后随年龄迅速上升,于55岁年龄段达到高峰,40岁以下年龄段患者占14.55%[2]。其中有部分年轻患者在确诊乳腺癌时尚未生育,而且随着我国二胎政策的放开,年轻乳腺癌患者卵巢功能的保护以及生育权的问题越来越受到关注,激素受体(hormone receptor,HR)阳性早期乳腺癌患者卵巢功能抑制剂使用已得到公认[3],但HR阴性患者是否应用尚缺乏有力证据,国外研究[4]报道(gonadotropin-releasing hormone,GnRH)激动剂能够保护化疗患者的卵巢功能,但大样本的随机对照研究相对较少且尚存争议。既往研究[5- 6]证实,抗苗勒氏管激素(anti-Mullerian hormone,AMH)是评价卵巢功能的良好指标,但AMH能否成为评价化疗后卵巢功能损害的指标尚缺乏有效的证据。本研究主要探讨GnRH激动剂对HR阴性年轻乳腺癌辅助化疗患者卵巢功能的影响以及AMH对化疗后卵巢储备功能的评价作用。
1 资料与方法
1.1 一般资料选择2013年1月至2015年1月在我院就诊的行术后辅助化疗的HR阴性年轻乳腺癌患者60例,随机均分为戈舍瑞林联合化疗组、化疗组,每组30例,同时选择同年龄健康女性30例作为对照组。入组标准:年龄20~40岁;手术后标本经免疫组化确诊为HR阴性;既往无卵巢疾病及手术史;无长期应用激素病史;无严重脏器疾病;ECOG评分0~1分;无其他化疗相关禁忌;签署知情同意书,并建议冷冻卵子、受精卵、卵巢组织;对照组为同年龄月经规则的女性,无卵巢疾病及激素类药物使用史。该研究已通过医院伦理委员会批准。戈舍瑞林联合化疗组中位年龄35(21~40)岁,化疗组中位年龄34(20~39)岁,对照组中位年龄35(20~40)岁。戈舍瑞林联合化疗组人表皮生长因子-2(HER-2)过表达患者18例,三阴性患者12例;化疗组HER-2过表达患者19例,三阴性患者11例。戈舍瑞林联合化疗组Ⅰ期患者6例,Ⅱ期患者18例,Ⅲ期患者6例;化疗组Ⅰ期患者5例,Ⅱ期患者19例,Ⅲ期患者6例。3组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法戈舍瑞林联合化疗组及化疗组选择AC-T或AC-TH方案化疗。AC-T方案具体用药:多柔比星60 mg·m-2+环磷酰胺600 mg·m-2,21 d为1周期,治疗4周期;4周期后序贯多西他赛100 mg·m-2, 21 d为1周期,治疗4周期;共8周期。AC-TH方案具体用药:多柔比星60 mg·m-2+环磷酰胺600 mg·m-2,21 d为1周期,治疗4周期;4周期后序贯多西他赛100 mg·m-2,同时联合曲妥珠单抗首次剂量8 mg·kg-1后改为6 mg·kg-1,21 d为1周期,治疗4周期,曲妥珠单抗完成1 a治疗。戈舍瑞林联合化疗组:除了化疗外,于化疗前2周第1次应用戈舍瑞林3.6 mg,后续每28 d应用1次戈舍瑞林3.6 mg,化疗结束后再次应用1次戈舍瑞林。化疗组行常规化疗,方案同戈舍瑞林联合化疗组。
1.3 检测方法对照组于月经第3天上午抽取外周静脉血,戈舍瑞林联合化疗组与化疗组于化疗前月经第3天上午抽取外周静脉血,化疗后若未闭经于月经第3天上午抽取外周静脉血,若已闭经则于化疗结束第3天抽取外周静脉血,化疗后1 a若未闭经于月经第3天上午抽取外周静脉血,若已闭经则于1 a时抽取外周静脉血。采用化学发光法检测雌二醇(E2)、促卵泡激素(FSH)、AMH,均采用美国Beckman Coulter公司DXI800全自动化学发光仪检测,试剂盒均购自美国Beckman Coulter公司。E2正常值:24~114 ng·L-1,FSH正常值:3.85~8.87 IU·L-1,AMH正常值:1.0~5.0 μg·L-1。

2 结果
2.1 戈舍瑞林联合化疗组和化疗组闭经情况比较戈舍瑞林联合化疗组30例患者有29例闭经,化疗组21例患者闭经,差异有统计学意义(P<0.05)。戈舍瑞林联合化疗组、化疗组1 a月经恢复率分别为96.6%、66.7%,差异有统计学意义(P<0.05)。
2.2 3组E2、FSH、AMH水平比较戈舍瑞林联合化疗组、化疗组和对照组E2、FSH、AMH水平治疗前比较差异均无统计学意义(P均>0.05)。戈舍瑞林联合化疗组、化疗组治疗结束时,E2、FSH高于对照组,AMH低于对照组,差异均有统计学意义(P均<0.05)。未闭经HR阴性年轻乳腺癌患者E2、FSH高于对照组,但差异无统计学意义(P>0.05);而AMH低于对照组,差异有统计学意义(P<0.05)。戈舍瑞林联合化疗组、化疗组治疗结束1 a后E2、FSH水平与对照组比较差异均无统计学意义(P均>0.05);而AMH仍低于对照组,差异均有统计学意义(P均<0.05)。戈舍瑞林联合化疗组和化疗组E2、FSH水平比较差异均无统计学意义(P均>0.05);戈舍瑞林联合化疗组AMH高于化疗组,差异有统计学意义(P<0.05)。见表1、2。

表1 3组不同时间点E2、FSH、AMH水平比较
注:与对照组比较,1)P<0.05;与化疗组比较,2)P<0.05
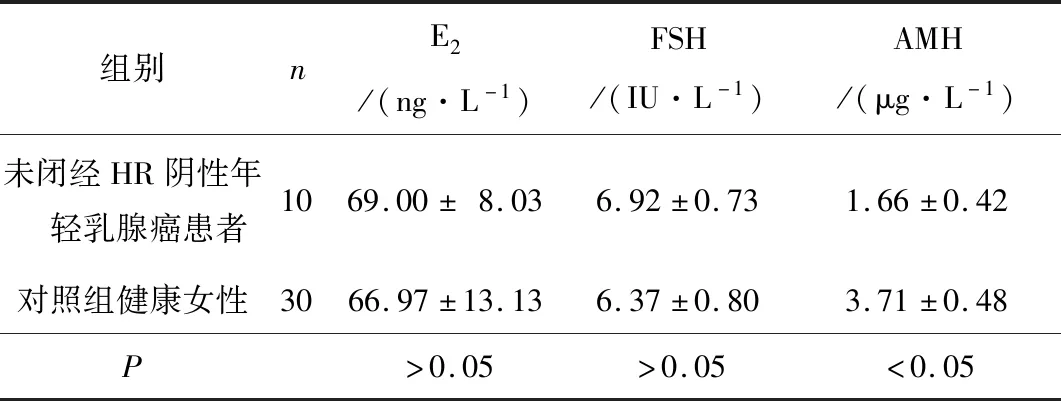
表2 未闭经HR阴性年轻乳腺癌患者与对照组健康女性E2、FSH、AMH水平比较
3 讨论
以往认为,基于治疗恶性肿瘤的需求,牺牲一部分正常功能是可以接受的,但随着肿瘤早期发现手段的丰富与精准诊治的实施,肿瘤患者治疗后长期存活成为可能,因而生活质量受到越来越多的关注[7]。卵巢是女性的重要器官,随着我国二胎政策的放开,如何避免各种医源性因素导致的卵巢功能过早衰竭以及保护生育能力成为丞待解决的问题[8]。
卵巢功能的衰退大部分情况下可以通过雌孕激素的补充加以弥补[9],但雌、孕激素的增高与乳腺癌有密切关系[10],如何在治疗乳腺癌的同时保护卵巢功能,尤其是年轻乳腺癌的生育能力,对我国年轻女性患者显得尤为重要。美国临床肿瘤学会、欧洲肿瘤内科学会的指南明确卵母细胞以及胚胎的冷冻保存是肿瘤患者生育保护的标准策略,GnRH激动剂用于卵巢功能保护的研究已有一段时间,但仍存争议[11-12],病例数较多的Ⅲ期随机对照研究较少,因此,是否在化疗中普遍采用GnRH相关药物保护卵巢功能存在争议。
有研究[4]显示,GnRH激动剂戈舍瑞林与化疗联合用于绝经前期、可手术切除的、HR阴性的乳腺癌患者,可在一定程度上抑制卵巢功能衰竭,减少了过早停经,更改善了生育前景。也有研究[13]显示,在化疗期间使用促黄体生成激素释放激素激动剂暂时性抑制卵巢功能,可使早期绝经前乳腺癌患者早发性卵巢功能衰竭的发生率减低17%,可以有效保护卵巢功能。本研究亦显示应用戈舍瑞林后月经恢复率明显高于单纯化疗,与上述研究结果一致,但上述研究大部分入组患者为HR阳性患者,后续需要内分泌治疗,故可能对结果产生影响。并且本研究尚缺少2 a卵巢早衰率以及后期妊娠率的进一步观察数据。
GnRH激动剂保护卵巢的机制尚不是很明确,可能的机制[14]有:GnRH激动剂能抑制下丘脑-垂体-性腺轴,阻止原始卵泡发育,在化疗过程中起到保护作用;低促性腺激素状态可以减少对化疗高度敏感的始基卵泡数目;低雌激素状态可以降低卵巢血供,从而减少化疗药物的浓度;GnRH激动剂直接作用于卵巢,激活GnRH受体;GnRH激动剂能上调性腺内抗细胞凋亡分子的表达,而其可以对性腺起到保护作用;GnRH激动剂可能有保护卵巢的生殖干细胞的作用。
AMH主要由窦前和窦状卵泡颗粒细胞以及次级卵泡产生,其水平与卵泡数目具有密切的关联性,月经规律的正常女性患者AMH水平波动很小,不受周期影响,近年来很多研究[15-16]表明AMH相较于FSH、E2等能够更好反映卵巢储备功能。有研究[6]显示AMH能够更早、更好反映卵巢储备功能的下降,本研究与其结果一致,但上述研究治疗前激素水平与对照组存在差异,并且月经恢复时间明显高于本研究,考虑可能与上述研究入组多为HR阳性患者有关,因为此类患者需接受内分泌药物治疗数年。
综上所述,GnRH激动剂对HR阴性年轻乳腺癌辅助化疗患者卵巢功能具有保护作用,AMH对化疗后卵巢储备功能的评价可能优于E2、FSH。但本研究为小样本研究,且未对2 a卵巢早衰率以及后期的妊娠率进一步研究,下一步将继续随访并扩大样本量。
