肾细胞癌立体定向体部放疗的研究进展
2019-04-18综述审校
综述 审校
肾细胞癌(renal cell carcinoma,RCC)是最常见的肾脏恶性肿瘤,其发病率正在逐年增加[1],全世界患者有超过14万例/年死于RCC[2]。部分和根治性肾切除术是非转移性RCC 的标准治疗方法,但对部分因高龄及临床并发症而丧失手术机会的患者,立体定向体部放疗(stereotactic body radiation therapy,SBRT)作为一种非侵入性治疗方式,可能比其他侵入性替代治疗更有优势。SBRT 对原发性和转移性RCC 有较好的局部控制(local control,LC)率,不良反应较为轻微,可控制肿瘤进展并延长无法手术患者的生存期。本文分析SBRT的放射生物学特征、不良反应和安全性,并对SBRT应用于原发性和转移性RCC的研究进展进行综述。
1 SBRT计划和实施要点
SBRT 采用现代影像技术,正确发现靶区及精确定位,将较多非共面的、动态或静态的射线束空间聚焦,形成高度适形、梯度陡峭的剂量分布,在较少的次数内(1~10次)对肿瘤给予高剂量的照射(通常单次剂量>8.0~20.0 Gy),彻底杀死肿瘤细胞,对周围正常组织的损伤亦较小。SBRT利用图像引导放疗(im⁃age-guided radiation therapy,IGRT)功能的直线加速器和复杂的放疗计划软件,执行增强CT/MRI/PET 等多模式的图像配准和高精度的放疗剂量分布。因器官在治疗过程中的运动(如呼吸、肠胃蠕动)和分次治疗间的位移误差(如治疗摆位误差、肿瘤缩小等),实施IGRT技术可使目标病灶获得精准治疗。
SBRT需通过控制呼吸动度的呼吸门控技术和靶区定位技术等,实现靶区的准确照射,如利用腹压来减少呼吸动度、根据患者呼吸的特定时相进行门控治疗、主动呼吸控制、植入金标追踪肿瘤技术、采用四维CT测量和治疗整个肿瘤移动范围等技术。
2 SBRT的放射生物学特征
2.1 放疗敏感性遵循的量-效原则
RCC传统上被认为是一种放疗抵抗性肿瘤,Ning等[3]研究显示,RCC 细胞株A498 和Caki-1 为放疗敏感性细胞株,放疗敏感性指标a/β 比值较低,分别为2.6和6.9。该研究还发现,当a/β比值较小时,大剂量分割放疗遵循量-效原则,即提高剂量可提高疗效的生物学特征,同时还能降低周围正常组织的长期毒副反应,并证明单次高剂量照射可使细胞死亡率增加。另有研究显示[4],根据危险器官的耐受性及毒副反应,SBRT 剂量可分割为30~40 Gy/3~5 次。上述研究结果为增加肿瘤照射剂量,从而提高LC 提供了依据。肿瘤细胞的存活与增值直接依赖于血液供应,而SBRT被证实直接作用于肿瘤血管。单次高剂量SBRT 造成的血管内皮损伤和随之造成的肿瘤微环境紊乱可能极大阻碍放疗损伤的修复[5]。
2.2 SBRT的远隔效应
放疗的远隔效应,被认为是由于局部放疗引起系统免疫效应,从而控制未经照射的肿瘤负荷。一项单臂可行性研究中[6],对RCC 患者的原发病灶行SBRT,与未经处理的RCC 患者相比,行SBRT 后RCC患者原发病灶和转移病灶中的钙网蛋白、肿瘤相关抗原(TAA)表达增加,增殖性T 细胞百分比更高,提供了RCC 行SBRT 治疗后免疫调节的证据。Xie 等[7]报道1例转移性RCC患者同时对原发病灶行SBRT和PD-1 抑制剂pembrolizumab 治疗,治疗后仅2.2 个月转移病灶就获得完全缓解。该报道表明晚期RCC可能受益于局部行SBRT 联合PD-1 抑制剂治疗,为晚期RCC 患者进行SBRT 联合生物免疫治疗提供了参考。Van de Walle 等[8]对1例转移性RCC患者的颈部转移病灶行姑息性常规放疗,在治疗后的几个月内发现未对肺转移瘤和皮下结节行放疗但却发生肿瘤消退的现象,这种远隔效应的发生机制有待进一步研究。
3 SBRT应用RCC治疗的现状
3.1 SBRT对转移性RCC的治疗
因相当数量的转移性RCC患者不能行手术治疗,替代疗法如SBRT成为关注的焦点。常规放疗后癌细胞再增殖起始时间多在3~5周后,SBRT的高剂量低分割照射多在1~2周内完成治疗,可避免癌细胞的加速再增殖,有利于提高LC。多项回顾性研究结果显示,SBRT对转移性RCC 治疗具有高的LC 率、总生存(overall survival,OS),并且不良反应较轻(表1)[9-15]。

表1 SBRT对转移性RCC患者的治疗
3.2 SBRT对原发性RCC的治疗
多项回顾性和前瞻性研究分析了SBRT对不能手术的原发性RCC患者的影响,结果显示治疗后LC率高且不良反应轻(表2)[16-26]。Siva等[27]对223例原发性RCC患者行SBRT后显示,4年LC率、癌症特异性生存率和OS率分别为97.8%、91.9%和70.7%。Ⅰ级或Ⅱ级不良反应发生率为35.6%,Ⅲ级或Ⅳ级不良反应发生率仅为1.3%。Siva等[28]在2012年对3项前瞻性和7项回顾性研究中的126例不能手术的原发性RCC患者分析发现,行SBRT后平均LC率高达93.9%(84%~100%),不良反应较轻,Ⅰ~Ⅱ级轻微不良事件的平均发生率为21.4%(0~93%),Ⅲ级及以上重度不良事件发生率为3.8%(0~19%),结果表明SBRT对原发性RCC有较高的LC率和较轻的不良反应。对于RCC,SBRT作为一项非侵入性治疗方式可能比射频消融或冷冻消融等侵入性治疗方式更有优势。
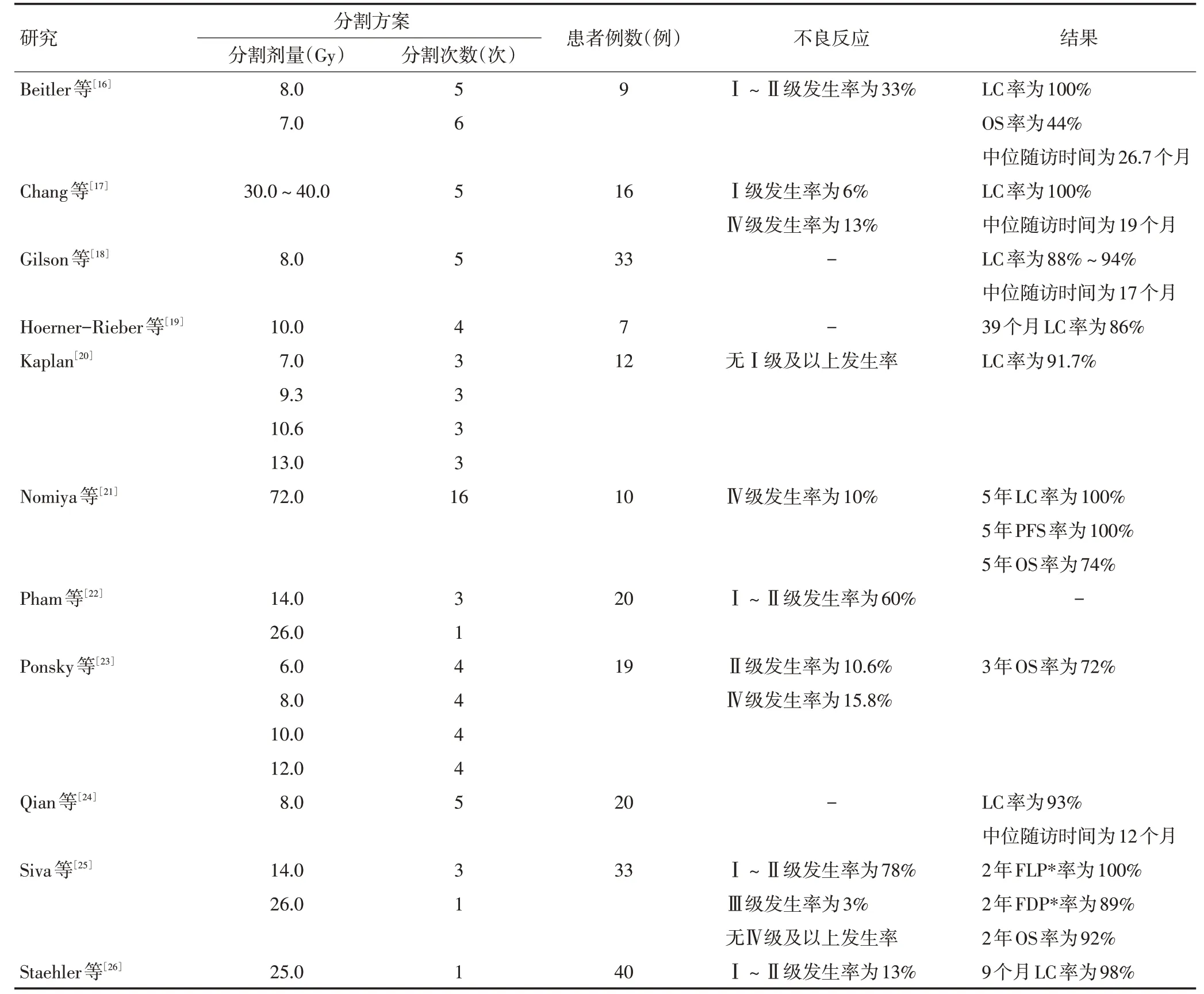
表2 SBRT对原发性RCC患者的治疗
3.3 SBRT应用于RCC的临床试验设计
对于不能手术的RCC 患者,SBRT 是一项非侵入性、方便、精准且使疗效增益的治疗手段。目前,因临床预后数据有限,设计一项大规模、多机构合作,行单独以及联合SBRT 在RCC 患者中的临床试验是非常重要的。该临床试验设计应收集完善的临床数据、制定合理的分割剂量、监测患者的预后及不良反应等,以证实SBRT 的长期安全性,并应制定一系列充分评估肾脏功能的方法,如实验室检查、生物标记物、定量的影像学检查和(或)常规细胞学检查;获得SBRT 对生存质量的影响,及与其他治疗方式相比的SBRT成本-效益数据。
4 结语
目前,手术作为RCC 标准治疗方式有较好的LC率和临床预后,虽低分割高剂量SBRT可提高RCC患者的LC率、OS率、PFS率,并且不良反应发生率低,但SBRT能否替代手术治疗还需进一步的随机对照临床试验。对RCC 的SBRT 剂量分割以及预后评估方式尚无统一指南,进一步评估SBRT在RCC中的治疗方案和长期安全性亟需进行更多的前瞻性试验。
