二氟磷酸锂的制备与性能研究
2019-04-12王永勤叶家铭王建萍
王永勤,叶家铭,王建萍
(多氟多化工股份有限公司,河南焦作454006)
锂离子电池作为一种新型的绿色能源,因其工作电压高、环保无污染、质量轻、无记忆效应等优点而广泛应用于多个领域,如移动电源、手机、笔记本电脑、电动汽车等[1-4]。同时,随着国家对新能源汽车产业的大力扶持,锂离子电池的市场需求量也越来越大。二氟磷酸锂(LiPO2F2)作为电解液添加剂,能够先于电解液在电极表面进行氧化还原反应,生成一层稳定致密的保护膜,避免电解液在正极材料表面的持续分解,从而提升锂电池的循环性能[5-6]。而且,和常用的电解质六氟磷酸锂(LiPF6)相比,LiPO2F2对水分比较稳定,生产环境要求不苛刻,存储条件要求低,易于工业化生产[7]。 因此,LiPO2F2受到了众多研究者的关注。现有的LiPO2F2制备工艺主要有:1)LiPF6和水反应制备LiPO2F2,但是这种工艺的副产物较多,导致产品纯度不高,而且对过程控制要求高;2)以二氟磷酸酐和氟化锂为原料制备 LiPO2F2,但是,该工艺的原料二氟磷酸酐价格昂贵,不利于工业化生产;3)以磷酸酐和氟化锂为原料制备LiPO2F2,该工艺的产物为LiPO2F2和LiPF6的混合物,产物提纯困难。因此,急需开发一种反应条件温和,易于工业化生产的 LiPO2F2合成工艺[8-10]。本文以 LiPF6和Li2CO3为原料,进行LiPO2F2的制备工艺研究。主要研究了反应温度、反应时间、反应物物质的量比和LiPO2F2浓度(指的是提纯过程中LiPO2F2浓度,下同)对产品纯度的影响,并对产品进行结构表征和性能检测。
1 实验部分
1.1 主要仪器与试剂
主要仪器:DF-101S集热式恒温磁力搅拌器;SHZ-D(Ⅲ)水循环真空泵;DLSB-10L低温冷却液循环泵。
主要试剂:六氟磷酸锂(纯度为99.99%);碳酸锂(纯度为 99.99%);碳酸二甲酯(DMC,分析纯);乙二醇二甲醚(DME,分析纯)。
1.2 实验原理
工艺所涉及的反应方程式如下:

1.3 实验方法
1)制备过程:氮气气氛下,在PFA(全氟烷氧基树脂)烧瓶中加入提纯后的300 mL碳酸二甲酯溶剂和2 mol高纯碳酸锂固体,搅拌均匀,转速设置为200 r/min。PFA烧瓶上面安装有PFA冷凝管,后续连接有硅油干燥器。加热至60℃,在溶液中缓慢加入2 mol六氟磷酸锂,投料过程中时刻注意反应状态,以防反应过于剧烈。搅拌反应,反应完全后,过滤除去副产物氟化锂,然后减压蒸馏、过滤,得到LiPO2F2粗品。
2)提纯过程:室温下,将LiPO2F2粗品溶解在DME溶剂中,LiPO2F2的浓度为1 mol/L,用孔径为1 μm的微滤膜进行膜过滤,滤液在-20℃冷却结晶,过滤,滤饼放在-0.1 MPa、60℃的真空干燥箱中干燥12 h,即得精制后的LiPO2F2产品。
1.4 产品检测
1)纯度:按照差量法对LiPO2F2产品的纯度进行检测。首先分析LiPO2F2产品中阳离子、阴离子、游离酸、水分、不溶物含量,然后用100%减去上述杂质含量得到LiPO2F2主含量。杂质含量测定方法:阳离子 Na+、Mg2+、K+、Ca2+、Cr3+、Fe3+、Ni2+、Cu2+、Pb2+采用电感耦合等离子体发射光谱仪(ICP-OES)测定;阴离子采用离子色谱法测定;游离酸(以HF计)采用微量滴定管测定;水分采用831水分测定仪在手套箱中测定;不溶物采用玻璃砂坩埚、电烘箱测定。
2)结构:采用Bruker AV 400型核磁共振仪对LiPO2F2产品的微观结构进行表征。
3)电化学性能:在氩气手套箱中,将碳酸乙烯酯(EC)、碳酸二乙酯(DEC)、碳酸甲乙酯(EMC)按照质量比为1∶2∶1配制电解液,并加入六氟磷酸锂(浓度为1.25 mol/L),得到标准电解液;然后,向标准电解液中加入质量分数为1%的LiPO2F2产品,作为对比电解液。分别对标准电解液和对比电解液进行线性伏安检测分析。同时,将这两种电解液分别制成软包电池,并对两种软包电池的室温(25℃)和高温(45℃)循环性能进行检测分析。
2 结果与讨论
2.1 工艺参数分析
2.1.1 反应时间对产品纯度的影响
在只改变反应时间,其他实验参数都保持不变的条件下,按照1.3所述的实验方法进行实验,以探索反应时间对产品纯度的影响。实验结果见图1。由图1可知,随着反应时间的延长,产品纯度呈现出先升高后降低的趋势。当反应时间为6 h时,产品纯度达到最大。继续延长反应时间,产品纯度出现了下降的现象,这是由于反应体系中存在微量的水分,随着反应时间的延长,产品与水分发生了副反应,从而导致产品纯度下降。因此,本实验设定反应时间为6 h。

图1 反应时间对产品纯度的影响
2.1.2 反应温度对产品纯度的影响
在只改变反应温度,其他实验参数都保持不变的条件下,按照1.3所述的实验方法进行实验,以探索反应温度对产品纯度的影响。实验结果如图2所示。由图2可知,随着反应温度的升高,产品纯度呈现出先升高后降低的趋势。当反应温度小于60℃时,产品纯度随着反应温度的升高,呈现出明显的上升趋势。说明,在该温度段,反应温度对产品纯度的影响比较大;反应温度越高,产品纯度越高。当反应温度高于60℃时,随着反应温度的升高,产品纯度呈现出下降的趋势。这是因为,当温度大于60℃时,外界提供的热量与反应体系中释放的大量热量混合在一起,使得反应体系的局部温度过高,导致部分原料六氟磷酸锂发生了分解反应,生成的氟化锂引入到成品中,从而导致了产品纯度的下降。因此,本实验设定反应温度为60℃。
2.1.3 反应物物质的量比对产品纯度的影响
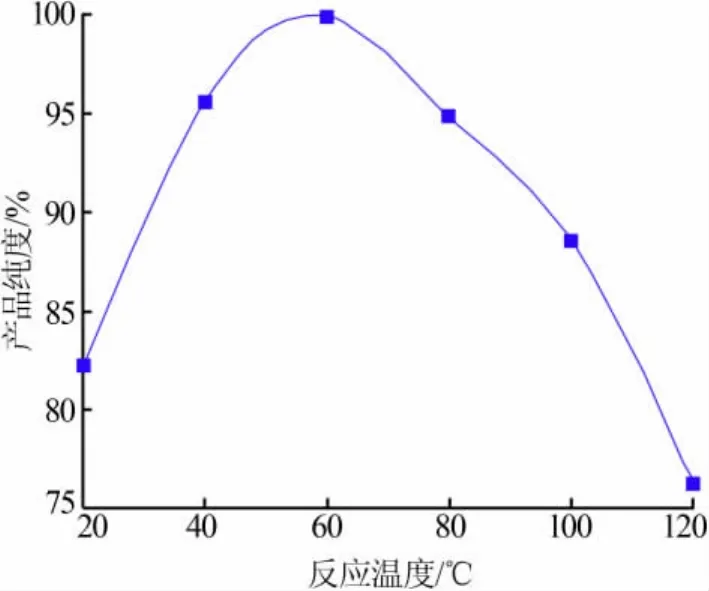
图2 反应温度对产品纯度的影响
在只改变反应物物质的量比,其他实验参数都保持不变的条件下,按照1.3所述的实验方法进行实验,以探索反应物物质的量比对产品纯度的影响。实验结果如图3所示。由图3可知,当n(Li2CO3)/n(LiPF6)小于 2,即 LiPF6过量时,产品纯度随着n(Li2CO3)/n(LiPF6)的增大而增大。这是因为当 LiPF6过量时,过量的LiPF6会分解产生氟化锂,使得少量氟化锂引入到最终产品中,导致产品纯度降低。当n(Li2CO3)/n(LiPF6)大于 2,即 Li2CO3过量时,产品纯度随着 n(Li2CO3)/n(LiPF6)的增大而降低。 原因是:当Li2CO3过量时,在提纯过程中,会有少量的Li2CO3溶解在溶剂中,并引入到最终的产品中,从而导致产品纯度出现下降的趋势。因此,本文将n(LiPF6)/n(Li2CO3)设定为 1∶2。

图3 n(Li2CO3)/n(LiPF6)对产品纯度的影响
2.1.4 LiPO2F2浓度对产品纯度和收率的影响

图4 LiPO2F2浓度对产品纯度和收率的影响
在只改变LiPO2F2浓度,其他实验参数都保持不变的条件下,按照1.3所述的实验方法进行实验,以探索LiPO2F2浓度对产品纯度和收率的影响。实验结果如图4所示。由图4可知,随着LiPO2F2浓度的逐渐减小,产品纯度逐渐增大,收率逐渐降低。当LiPO2F2浓度小于1mol/L时,产品纯度基本保持不变,约为99.91%,而产品收率由53.67%降低至36.82%。这是因为,随着LiPO2F2浓度的逐渐减小,LiPO2F2粗品中的杂质在提纯溶剂中溶解的越多,使得最终产品的纯度升高;但是,提纯溶剂中溶解的LiPO2F2产品也越来越多,导致产品收率降低。因此,本文综合考虑产品纯度和经济效益,最终将LiPO2F2浓度确定为1 mol/L。
2.1.5 正交实验设计及结果分析
为了探索反应时间 、 反应温度 、n (LiPF6)/n(Li2CO3)和LiPO2F2浓度之间的相互作用,本文按照L18(37)正交表进行正交试验。正交实验设计如表1所示。正交实验结果如表2所示。

表1 正交实验设计

表2 正交实验结果
由表2 可知,反应温度和 n(LiPF6)/n(Li2CO3)对产品纯度的影响比较大,反应时间、LiPO2F2浓度对产品纯度的影响较小。因此,综合考虑产品和经济效益,本实验的最佳实验参数设定为A1B2C2D1。
2.1.6 验证实验
为了进一步验证实验参数的重复性和再现性,根据正交实验的讨论结果,在反应温度为60℃、反应时间为 5 h、n(LiPF6)/n(Li2CO3)为 1∶2 和 LiPO2F2浓度为0.95 mol/L的实验条件下,进行了5组重复实验,实验结果见表3。由表3可知,在此实验条件下,可制备出纯度为99.95%的产品,产品收率约为55.64%。

表3 实验结果
2.2 核磁表征
对产品LiPO2F2进行19FNMR谱图分析,检测结果如图5所示。由图5可知,LiPO2F2的19FNMR谱图中有两个吸收峰,没有出现其他杂峰,说明在LiPO2F2产品结构中的F元素有且只有一种化学环境,不含有其他杂质。而且,其所对应的化学位移为-7.9×10-5,和文献[11]的检测结果相吻合。因此,本文所制备的产品LiPO2F2结构单一,纯度大于99.9%。

图5 产品LiPO2F2的19F NMR谱图
2.3 LiPO2F2对电池性能的影响
为了进一步探索LiPO2F2对电池性能的影响,本实验配制了两种具有对比性的电解液:1.25 mol/L LiPF6/EC+DEC+EC(质量比为 1∶2∶1)的标准电解液;向标准电解液中加入质量分数为1%的LiPO2F2(自制,纯度为99.95%),配制成对比电解液。在手套箱中,分别将这两种电解液注入LiNi0.6Co0.2Mn0.2O2/C全电池中,并在室温(25℃)和高温(45℃)下进行1C充放电循环性能测试。室温下,添加有1%LiPO2F2的电池循环300周,容量保持率为84.23%,容量仅衰减了15.77%,远远小于未添加LiPO2F2的电池(容量保持率为 70.56%,容量衰减了29.44%),说明将LiPO2F2添加在锂电池的电解液中,可以有效提高锂电池的室温循环性能。高温下,添加有1%LiPO2F2的电池循环200周,容量保持率为88.27%,容量仅衰减了11.73%,小于未添加LiPO2F2的电池体系(容量保持率为80.82%,容量衰减了19.18%)。其原因可能为:在充放电过程中,LiPO2F2能在电极表面形成一种致密的表面膜,抑制电解液的分解和电极材料的溶解,从而提高锂电池的循环性能。
3 结论
1)以LiPF6和Li2CO3为原料,通过反应和提纯两个步骤来制备LiPO2F2产品。最佳工艺参数为:反应温度为 60 ℃、反应时间为 5 h、n(LiPF6)/n(Li2CO3)为1∶2 和 LiPO2F2浓度为 0.95 mol/L。2)所制备的LiPO2F2产品纯度约为99.95%,收率约为55.64%。3)所制备的LiPO2F2产品可以显著提升锂电池在室温和高温(45℃)下的循环性能。
