替考拉宁药代动力学指导重症G+菌感染患者个体化用药的临床分析
2019-03-06杨丽莎朱忠立祝国芸黎俊雅李福祥
杨丽莎 刘 畅 胡 健 朱忠立 徐 伟 祝国芸 黎俊雅 李福祥,
革兰氏阳性菌感染,特别是耐药G+菌感染,在细菌感染中所占比例仍居高不下,糖肽类抗生素是目前首选治疗方案[1]。随着万古霉素广泛使用,逐渐出现耐药现象,且万古霉素存在肾毒性,使治疗颇为棘手。替考拉宁具高蛋白结合率,半衰期长,多种给药途径,药物不良反应发生率较低,与氨基糖苷类及碳青霉烯类抗生素有协同作用,对于某些感染如血液系统肿瘤等疾病的疗效甚至更优等特点,逐渐得到重视[2-4]。越来越多证据显示,临床使用替考拉宁需足量、个体化给药[5]。为此,欧洲药品委员会替考拉宁负荷剂量推荐为6~12 mg/kg q12 h×3剂,维持剂量为6~12 mg/kg qd,且要求3~5 d后血药谷浓度达到15~40 mg/L才能显著提高临床疗效并减少药物不良反应。国内注射用替考拉宁说明书推荐剂量远不足欧洲,推荐G+感染患者成人剂量400 mg q 12 h×3剂,此后200 mg qd,推荐重症感染患者目标谷浓度仅为10 mg/L。2016年7月我国《替考拉宁临床应用剂量专家共识》中推荐治疗一般感染时AUC0-24/MIC≥125,治疗重症感染时AUC0-24/MIC≥345才能达到较好的疗效[6]。本文拟通过对照试验,展现药代动力学指导下个体化用药的优势,探讨浓度与主要影响因素间的关系,为临床给药提供一定的参考。
对象与方法法
一、实验对象
选取2016年12月至2017年12月西部战区总医院(成都军区)重症G+感染患者80例。经西部战区总医院伦理委员会批准,家属或患者签署知情同意后,用随机数字表法将患者分为标准组和优化组,每组各40例。纳入标准:①符合2014年《中国严重脓毒症/脓毒性休克治疗指南》诊断标准,经病原学培养确诊为G+菌感染的危重症患者;②年龄大于18岁,性别不限制 ;③治疗时间大于72 h;④给药方式为静脉滴注[7]。 排除标准:机器无法检测或非静脉用药。
高效液相色谱仪HP1100(美国惠普公司,机号:DE91608294);Agilent ZOBAX XDB-C18色谱柱(250 mm×4.6 mm,5 μm);替考拉宁标准品(中国食品药品指定研究院,批号:130374-201002);哌拉西林钠对照品(梯希爱(上海)化成工业发展有限公司, 批号:5C8OB-NE);MIC检测: Vitek 2 Compact (梅里埃公司);注射用替考拉宁(他格适,赛诺菲安万特公司,200 mg/支,批号:J20090077)。
二、实验方法
1. HPLC血样测定: 流动相 0.01 mol/l NaH2PO4(pH=2.1)-乙腈(75︰25), 等梯度洗脱,流速 1.0 ml/min,进样量0.020 ml,柱温25 ℃;于3、6剂前0.5 h、第4剂前0.5 h及第4剂后5 min,0.5、2、6、12、24 h,采集对侧前臂静脉全血3~5 ml。以离心半径8 cm,3 000 r/min,离心10 min,提取血浆样本,准确吸取血浆样本0.40 ml,加入0.05 ml哌拉西林。加入乙腈0.600 ml。剧烈震荡20 s,以离心半径8 cm,12 000 r/min,离心5 min。取上清液0.600 ml于离心管,加入氯仿0.400 ml,剧烈震荡20 s,以离心半径8 cm,12 000 r/min 离心5 min。取上清液于样品瓶中,直至检测;用标准品配置高,中,低不同浓度的质控品各5份,测量其测定限及绘制标准曲线,并计算精密度及回收率。
2. 给药方案: 标准组 按药品说明书给药,负荷剂量400 mg q 12 h×3剂,维持剂量400 mg qd;优化组 按中国专家共识方案给药,体重计算(10 mg/kg)。维持剂量的调整根据个体第3、5剂谷浓度,AUC0-24/MIC,半衰期。①加量在第3剂给药后12 h,谷浓度水平:3.5~5 mg/L,追加一剂400 mg;5~8 mg/L,追加一剂200 mg;>8 mg/L继续原方案;②加量在第5剂后12 h:AUC0-24/MIC<345,追加一剂200 mg;AUC0-24/MIC<125,追加一剂400 mg;③谷浓度>60 mg/L,或半衰期>144 h,减量一半或延长输注间隔。
3. 检测指标: 第3、6剂谷浓度,计算AUC0-24/MIC,肌酐清除率(Cockcroft-Gault),第1、4天WBC、CRP变化、治疗前后肝肾功能、血小板计数、病原菌情况等。
4. 疗效判定标准: 参照卫生部《抗菌药物临床研究指导原则》疗效评定为治愈、显效、改善、无效4级[8]。细菌学按清除和未清除评定。
5. 安全性评价: 急性肾损伤:Ccr升高到基线的26.5 μmol/L;较基线升高50%;尿量小于0.5 ml/(kg·h),持续>6 h。满足任一条即可。肝损伤:AST或ALT≥3倍正常值上限,或AST或ALT≥替考拉宁第1天治疗开始前的异常值的3倍。
三、统计学方法

结 果
一、HPLC法的质控结果
以血清中替考拉宁的总浓度为X轴,以替考拉宁及哌拉西林钠峰面积比值(A替/A哌)为Y轴作图,采用最小二乘法进行线性回归,方程式:Y=14.316X+2.881,r2=0.9999,在3.5~100 μg/ml范围内线性关系良好,见图1。

图1 替考拉宁标准曲线
替考拉宁中定量成分TA2-2的回收率均≥80%,准确度高,精密度变异系数均≤15%,重复性及再现性好,见表1。

表1 方法回收率和精密度(n=5)
二、人口统计学特征
两组患者在性别、年龄、身高、白蛋白水平等一般资料无显著差异(P>0.05)。在治疗时间上优化组更短,P<0.05,见表2。
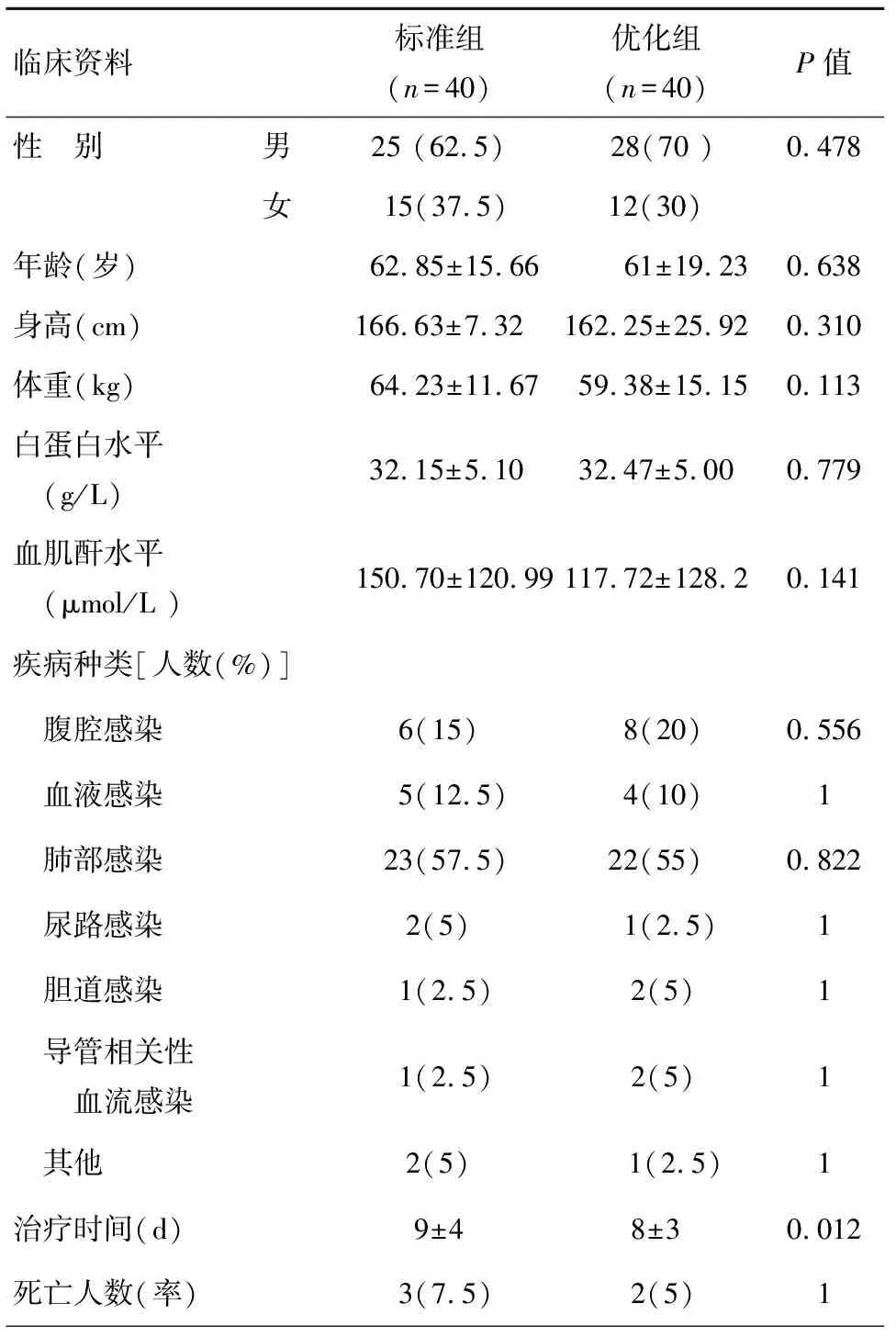
表2 两组患者人口统计学特征比较[n(%)]
三、PK/PD相关参数
优化组第6剂谷浓度及目标谷浓度达标率高于标准组,P<0.05 ,第3剂谷浓度及目标谷浓度达标率无显著差异,P>0.05,见表3。从分布情况看,两组患者第3剂谷浓度及标准组第6剂谷浓度大多<10 mg/L,优化组第6剂谷浓度集中在10~15 mg/L,图2。
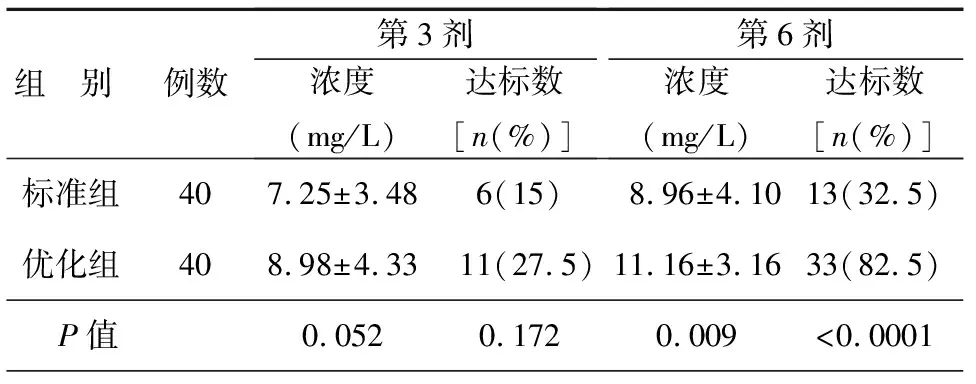
表3 两组患者第3、6剂谷浓度及目标谷浓度达标情况比较
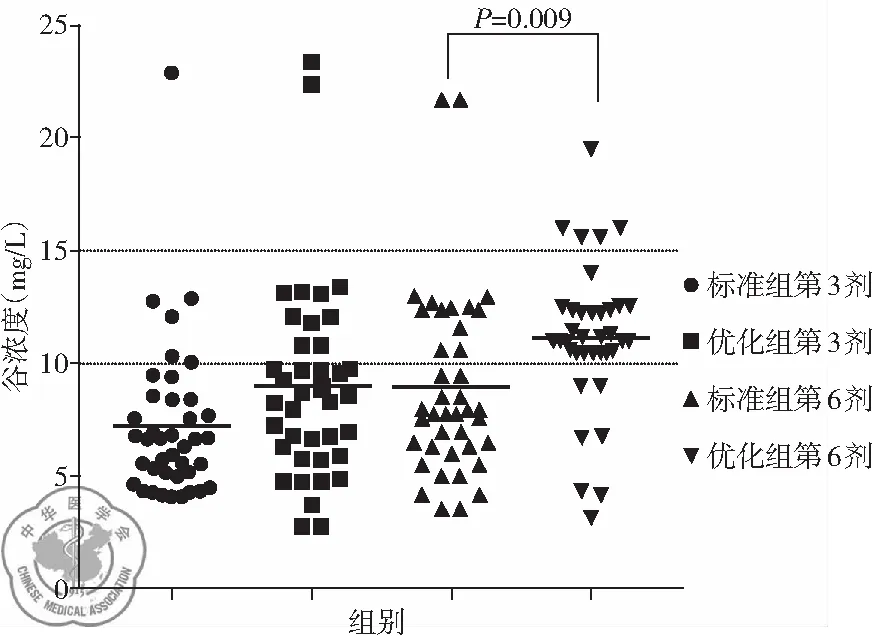
图2 两组患者第3、6剂谷浓度分布情况
优化组AUC0-24/MIC值、AUC0-24/MIC≥345的达标率高于标准组,P<0.05。 两组AUC0-24/MIC≥125达标率无显著差异,见表4。 从分布情况看,标准组AUC0-24/MIC集中在125-250,优化组分布较为散乱,见图3。
四、疗效及不良反应比较
两组患者炎症指标较前均有所改善,优化组患者WBC、CRP下降更快,P<0.05。体温变化情况无显著差异,P>0.05,见表5。
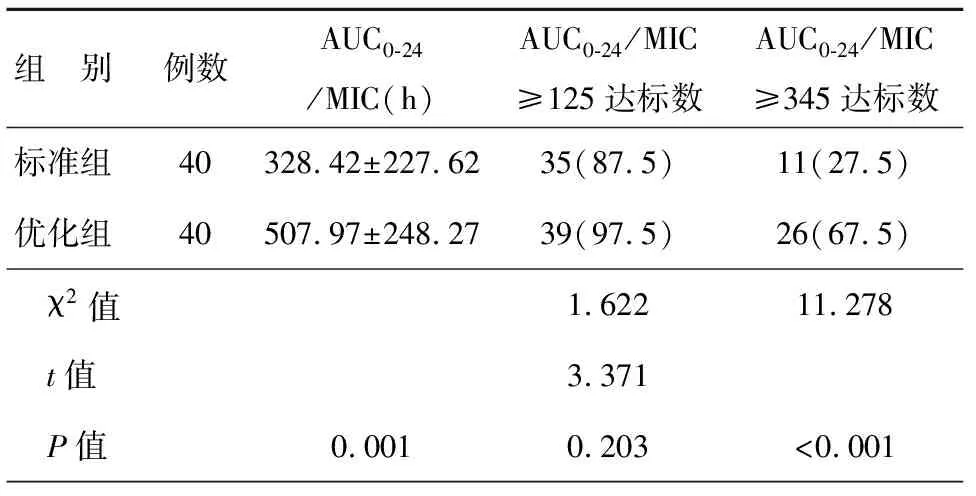
表4 两组患者 AUC0-24/MIC及两组AUC0-24/MIC≥125,AUC0-24/MIC≥345达标率的比较[n(%)]
注:AUC:血药浓度曲线下面积;MIC:最小抑菌浓度
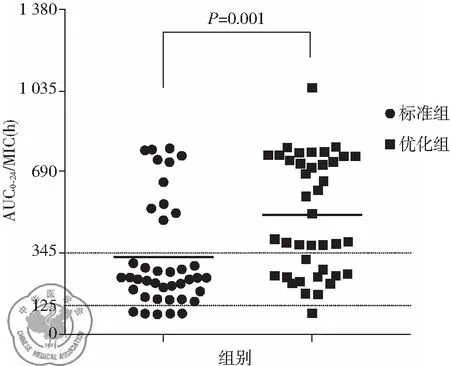
图3 两组患者AUC0-24/MIC分布情况

表5 两组患者T、WBC、CRP在第1、4天的变化
注:P=0.042, 白细胞标准组vs. 优化组;P=0.044 CRP标准组vs. 优化组
标准组与优化组,治愈10%vs. 22.5%,显效20%vs. 37.5%,改善35%vs. 25%,无效35%vs. 15%,优化组疗效更优(85%vs. 65%),P<0.05;两组患者不良反应发生率无显著差异,P>0.05,肝功能2.5%vs. 2.5%,肾功能0vs. 0,血小板减少2.5%vs. 0。优化组患者菌清除率显著高于标准组(80%vs. 55%),P<0.05。
五、谷浓度影响因素
与第3剂谷浓度关系(C3)最为密切的是负荷剂量(kg,mg/kg)和肌酐清除率(CLcr3,ml/min);与第6剂谷浓度(C6)关系最为密切的是维持剂量(kg6,mg/kg)和当日肌酐清除率(CLcr6)。拟合方程式:LogC3=0.405+0.068kg3-0.001 CLcr3(VIF 1.023,R2=61.8%,P<0.001);LogC6=0.92+0.042kg6-0.004 CLcr6(VIF 1,R2=73.5%,P<0.001)。
讨论
G+菌感染,特别是耐药G+菌感染,如MRSA,VRE,VRSE等,直接威胁患者生命[9-10]。替考拉宁较万古霉素、利奈唑胺更优的安全性、相同的疗效,逐渐成为重症G+菌感染患者的最优选择[11-14]。其最优给药剂量和方式仍在不断探索,是目前研究的热点,但通过重症感染人群药代动力学特征进行指导给药目前鲜有报道。
在药代动力学的指导下,尝试将血药浓度分层给予不同剂量的调节后,优化组较标准组患者第6剂谷浓度(mg/L)增加(11.16±3.16vs. 8.96±4.10,P=0.009);达标率提高(82.5%vs. 27.5%,P<0.0001);AUC0-24/MIC≥345达标率也显著上升(67.5%vs. 27.5%,P<0.001)。优化组患者炎症指标下降更快(两组第1、4天白细胞比较,P=0.042,两组第1、4天CRP比较,P=0.044);细菌清除率更高(80%vs. 55%,P=0.017);结局指标更优(总治疗有效率85%vs. 65%,0.013);治疗时间更短(8±3 dvs. 9±4 d,P=0.012)。总之,优化组患者疗效更佳,且并未增加不良反应发生率(2.5%vs. 5%,P=1)和病死率(5%vs. 7.5%,P=1)。上述结果均提示药代动力学参数的综合分析指导用药具有显著优势。
本组研究中,标准组第3剂谷浓度(7.25±3.48)mg/L和第6剂谷浓度(8.96±4.10)mg/L较10 mg/L的目标值相差甚远。AUC0-24/MIC(328.42±227.62)h相对于345的目标值也不足。AUC0-24/MIC≥345的达标率(27.5%)也很低,而AUC0-24/MIC≥125的达标率尚可(87.5%),提示400 mg的负荷剂量和维持剂量对于重症患者远不足,仅适用于一般感染。优化组虽然提高了第6剂谷浓度及AUC0-24/MIC值,但治疗总有效率仍未达90%,而标准组第6剂谷浓度和AUC0-24/MIC≥345的达标率则更低,考虑与目标谷浓度、AUC0-24/MIC不足有关。国外文献报道建议MRSA耐甲氧西林金黄色葡萄球菌感染患者目标谷浓度(>15~30 mg/L),AUC0-24≥750-800(MIC≤1 mg/L)才能取得较好的疗效,AUC0-24/MIC≥900才能达到较高的细菌清除率[15-18]。因此,建议提高剂量、目标谷浓度及AUC0-24/MIC值以进一步到达满意疗效。
重症患者药代动力学参数变异率大,考虑与治疗中分布容积(Vd)和清除率(CL)发生改变,影响了药物在病灶的浓度有关。本试验也证实重症患者血药浓度、AUC0-24/MIC值的分布较为散乱,跨度也较大,有必要进行TDM监测[19-22]。在此基础上,本文探寻了谷浓度与影响因素的关系,主要是剂量/kg(给药剂量/公斤体重)和CLcr(内生肌酐清除率,采用Cockcroft公式),并拟合出方程式,即假设一位肌酐清除率100 ml/min,体重60 kg的患者,要达到目标谷浓度,根据LogC3=0.405+0.068kg3-0.001 CLcr3计算得出需要至少600 mg的负荷剂量,如治疗过程中体重和肌酐清除率基本不变,根据LogC6=0.92+0.042kg6-0.004 CLcr6计算得出至少也需要600 mg的维持剂量,该拟合方程为个体化治疗提供了一定的参考价值。目前国内相关研究还很少,且大多通过不同的负荷剂量和维持剂量进行不同的组合。例如将患者分成600 mg负荷剂量+600 mg维持剂量与600 mg负荷剂量+400 mg维持剂量两组,根据不同的疗效来判定最优给药剂量和方式,而台湾及日本等有医院已研发出相关软件(输入患者个体数据,如身高,体重,血肌酐,白蛋白水平等)可得出个体化给药剂量。国外研究较为深入,已有不同人群、不同病种患者血药浓度、AUC0-24/MIC分布情况,并可根据这些分布情况结合不同的方法如贝叶斯定理,蒙特卡洛模拟法等数学方法共同制定出患者优化给药剂量。同时还研究了血清白蛋白和游离替考拉宁浓度对不同时段谷浓度的影响及其相关性,为精准化治疗提供了可能,值得我们深入探索[23-32]。
通过HPLC方法学验证结果证实本方法准确,可靠,能实时监测患者血药浓度,并利于及时发现超过安全范围(≥60 mg/L)的患者,避免不良反应的发生。本文中两组患者第3剂谷浓度无明显差异,考虑与两组患者体重,血肌酐无明显差异,故负荷剂量差异不大。两组患者的体温在治疗前后对比差异不大考虑与患者合并症多,个体对体温的调节能力不同有关。本次试验病例数仍较少,时间相对较短,有望纳入更多的患者进一步研究。
综上所述,对于重症G+菌感染的重症患者,推荐进行TDM监测,在药代动力学指导下给药,并提高剂量、目标谷浓度及AUC/MIC值,可纳入更多的患者进一步证实和优化拟合方程式,为临床用药提供一定的参考,以期进一步达到低耗、高效、优质、安全的精准化治疗,使更多的重症患者受益。
