一测多评法测定茵栀黄颗粒中4个黄酮类成分的含量
2019-02-25李艳芳黄传亮范建伟刘武占关永霞
李艳芳,黄传亮,范建伟,刘武占*,关永霞*
(1. 鲁南厚普制药有限公司,山东 临沂 276006;2. 中药制药共性技术国家重点实验室,山东 临沂 276006;3. 鲁南制药集团股份有限公司,山东 临沂 276006)
茵栀黄颗粒是由茵陈、栀子、黄芩、金银花4味中药提取物制成的常用中成药制剂,源于《伤寒论》中“茵陈蒿汤”[1],具清热解毒、利湿退黄之功效,用于肝胆湿热所致的黄疸,症见面目悉黄,胸胁胀痛,恶心呕吐,小便黄赤,急、慢性肝炎见上述证候者[2];临床上对新生儿生理性和病理性黄疸有较好的疗效[3-5]。2015年版中国药典以黄芩苷作为茵栀黄颗粒中黄芩提取物的检测指标,而黄芩提取物作为处方的主要组成(约占60.25 %),仅控制黄芩苷单一成分的含量难以保证黄芩提取物及茵栀黄颗粒的质量。多成分同步质量控制是目前国际上广泛认可的质量评价模式[6],但由于所需对照品物质大多难以获得,极大地限制了该模式的实际应用。王智民等[7]提出了“一测多评”的中药多指标质量评价模式,本课题组前期曾用该方法测定栀子中环烯醚萜苷类成分的含量[8]。基于此,本实验选择特征性强、供应充足的黄芩苷作为内参物,采用高效液相色谱法(HPLC)测定其与野黄芩苷、汉黄芩苷、黄芩素和汉黄芩素间的相对校正因子,建立茵栀黄颗粒“一测多评”含量测定方法,为茵栀黄颗粒的质量控制提供参考。
1 仪器与试药
1.1 仪器
Agilent 1100液相色谱系统(OpenLAB CDS化学工作站,美国Agilent公司),Shimadzu LC-20A高效液相色谱系统(包括LC solution工作站,日本Shimadzu公司);色谱柱Diamonsi C18(4.6 mm×250 mm,5 µm),Kromasil C18(4.6 mm×250 mm,5 µm),Platisil C18(4.6 mm×250 mm,5 µm);AG285型电子分析天平(瑞士Mettler Toledo公司);KQ250 DB数控超声波清洗器(昆山超声仪器公司,160 W,40 kHz)。
1.2 试药
对照品野黄芩苷(批号110842-200403),黄芩苷(批号110715-200514),汉黄芩苷(批号112002-201702),黄芩素(批号111595-200905)购自中国食品药品检定研究院,均为含量测定用;对照品汉黄芩素(批号MUST-14110311,成都曼斯特,质量分数≥98 %);茵栀黄颗粒(规格:3 g/袋,鲁南厚普,批号为00917229,00917230,00917231,00917232,00917233,00917234);乙腈为色谱纯,水为超纯水,其余试剂均为分析纯。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液制备 精密称取野黄芩苷、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素对照品适量,分别置50 ml量瓶中,以甲醇溶解并定容置刻度,摇匀,即得各对照品储备液。依次精密吸取各储备液适量于同一量瓶中,以甲醇定容至刻度,摇匀,即得浓度分别为27.98,95.28,35.46,70.92,9.6 mg/L的混合对照品溶液。上述混合对照品溶液于4 ℃冷藏,备用。
2.1.2 供试品溶液制备 取茵栀黄颗粒1 g,精密称定,置具塞锥形瓶中,精密加入50 %甲醇20 ml,称定重量,超声30 min,取出,放冷,用50 %甲醇补足失重,摇匀,滤过,即得。
2.1.3 阴性溶液制备 取按茵栀黄颗粒制备方法制得的缺黄芩提取物的阴性样品,按2.1.2项方法操作,即得。
2.2 液相色谱条件
采用Agilent 1100 高效液相色谱仪,OpenLAB CDS化学工作站。色谱柱:Diamonsi C18(4.6 mm×250 mm,5 µm);流动相:乙腈(A)-0.1 %磷酸溶液(B),梯度洗脱(0 ~1 5 min,5 %~6 % A;15~23 min,6 %~10 % A;23~42 min,10 %~20 % A;42~60 min,20 %~25 %A;60~90 min,25 %~60 % A);流速:1.0 ml/min;检测波长:274 nm;柱温:30 ℃;进样量:5 µl。
2.3 测定法
分别精密吸取混合对照品溶液和供试品溶液各 5 μl,注入液相色谱仪,测定。
2.4 方法学验证
2.4.1 专属性试验 分别吸取对照品溶液、供试品溶液和阴性溶液各5 μl,按上述色谱条件进样测定,结果见图 1。由图1 可见,各待测色谱峰均达到基线分离,阴性对照色谱中,在与野黄芩苷、黄芩苷、汉黄芩苷、黄芩素和汉黄芩素相对应的保留时间处无干扰。

图1 对照品(A)、茵栀黄颗粒(B)和缺黄芩提取物阴性样品(C)的HPLC图谱
2.4.2 线性关系考察、检测限、定量限 分别精密吸取2.1.1项下对照品溶液2,4,6,8,10 µl,注入液相色谱仪,按2.2项下色谱条件测定。以峰面积Y为纵坐标,进样量(X,μg)为横坐标,绘制标准曲线,得回归方程:野黄芩苷Y=4×106X-8532,r=0.9993,线性范围0.056~0.280 μg,定量限1.680 ng,检测限0.560 ng;黄芩苷Y=7×106X-1449,r=0.9995,线性范围0.191~0.953 μg,定量限1.906 ng,检测限0.572 ng;汉黄芩苷Y=9×106X+6063,r=0.9995,线性范围0.071~0.355 μg,定量限0.709 ng,检测限0.213 ng;黄芩素Y=1×107X-10 625,r=0.9991,线性范围0.142~0.709 μg,定量限1.418 ng,检测限0.425 ng;汉黄芩素Y=1×107X-15124,r=0.9996,线性范围0.019~0.096 μg,定量限0.576 ng,检测限0.192 ng。
2.4.3 精密度试验 取2.1.1项下对照品溶液,按2.2项色谱条件连续进样6次,记录野黄芩苷、黄芩苷、汉黄芩苷、黄芩素和汉黄芩素的峰面积,计算RSD值。结果各成分峰面积的RSD(n=6)分别为0.59 %,0.22 %,0.74 %,0.99 %,0.65 %,表明仪器精密度良好。
2.4.4 重复性试验 取同一批茵栀黄颗粒(批号00917229)6份,按2.1.2项下方法制备供试品溶液,按2.2项色谱条件进样测定。结果野黄芩苷、汉黄芩苷、黄芩素和汉黄芩素平均含量分别为0.526,0.738,1.509,0.175 mg/g,RSD分别为1.11 %,0.35 %,1.02 %,0.83 %。表明方法重复性良好。
2.4.5 稳定性试验 取同一批茵栀黄颗粒(批号00917229),按2.1.2项方法制备供试品溶液,分别于制备后0,4,8,12,16,24 h进样测定,测得野黄芩苷、汉黄芩苷、黄芩素和汉黄芩素峰面积的RSD分别为0.91 %,0.74 %,1.06 %,1.04 %,表明供试品溶液在24 h内稳定。
2.4.6 加样回收率试验 精密称取已知含量的茵栀黄颗粒(批号00917229)0.5 g,平行6份,分别精密加入混合对照品溶液10.0 ml,按2.1.2项方法制备供试品溶液,测定,计算加样回收率及RSD。结果野黄芩苷、汉黄芩苷、黄芩素和汉黄芩素的平均加样回收率为98.59 %,97.91 %,99.03 %,100.90 %,RSD分别为2.76 %,1.97 %,1.45 %,2.14 %。表明本方法具有良好的回收率。
2.4.7 耐用性试验 取茵栀黄颗粒(批号00917229)适量,按2.1.2项方法制备供试品溶液,考察柱温变化(25、30、35 ℃)及不同的色谱柱(Diamonsi C18、Kromasil C18、Platisil C18和Zorbax SB-C18)对测定结果的影响。结果显示上述变化对测定结果无明显影响,表明耐用性佳。
2.5 相对校正因子的确定
2.5.1 待测组分相对校正因子的计算 参照文献[9],根据多点校正法计算相对较正因子, 即以多个质量浓度点计算所得的相对校正因子的平均值作为含量计算用相对校正因子(fs/i)。按相对校正因子计算公式式中As为内参物对照品s峰面积,Cs为内参物对照品s浓度,Ai为某待测成分对照品i峰面积,Ci为某待测成分对照品i浓度。取2.1.1项下对照品溶液,分别进样2,4,6,8,10 µl,测定野黄芩苷、黄芩苷、汉黄芩苷、黄芩素和汉黄芩素的峰面积。以黄芩苷为内参物,分别计算黄芩苷(s)对野黄芩苷(a)、汉黄芩苷(b)、黄芩素(c)和汉黄芩素(d)的相对校正因子,见表1。

表1 茵栀黄颗粒中4个黄酮类成分的相对校正因子(n=2)
2.5.2 不同色谱柱对相对校正因子的影响 采用Agilent 1100高效液相色谱系统,分别考察了Diamonsi C18、Kromasil C18、Platisil C18和Zorbax SB-C18色谱柱对茵栀黄颗粒中黄酮类成分相对校正因子的影响,结果见表2。由表2可见,重现性良好(RSD<3 %)。

表2 不同色谱柱测得相对校正因子(n=2)
2.5.3 不同仪器对相对校正因子的影响 采用Diamonsi C18(4.6 mm×250 mm,5 μm)色谱柱,分别考察了Agilent 1100和LC-20A 2种不同的高效液相色谱系统对茵栀黄颗粒中黄酮类成分相对校正因子的影响,结果见表3。由表3可见,重现性良好(RSD<3 %)。

表3 不同仪器测得相对校正因子(n=2)
2.5.4 不同柱温对相对校正因子的影响 采用Agilent 1100高效液相色谱系统和Diamonsil C18(4.6 mm×250 mm,5 µm)色谱柱,分别考察了不同柱温(25,30,35 ℃)对茵栀黄颗粒中黄酮类成分相对校正因子的影响,结果见表4。由表4可见,重现性良好(RSD<3 %)。

表4 不同柱温测得相对校正因子(n=2)
2.6 待测组分色谱峰的定位
在仅使用黄芩苷1个对照品的情况下,为实现对茵栀黄颗粒中其他几个黄酮类成分的准确指认,分别考察采用2种高效液相系统及4种规格色谱柱黄芩苷对野黄芩苷等成分的相对保留时间和保留时间差,结果相对保留时间波动较小,其RSD为1.07 %~2.40 %,保留时间差的RSD为1.91 %~3.96 %,因此本实验采用相对保留时间作为色谱峰的定位依据。根据实验结果最终确定的茵栀黄颗粒中黄芩苷对野黄芩苷等各色谱峰相对保留时间分别为rs/a=1.289,rs/b=0.852,rs/c=0.789,rs/d=0.717。
2.7 QAMS与外标法测定结果的比较
实验采用QAMS和外标法对6批茵栀黄颗粒的含量进行了测定,结果见表5。由表5可见,2种方法测得的含量无显著性差异,相对偏差均小于2 %,表明本实验建立的QAMS法可用于茵栀黄颗粒的多成分质量评价研究。
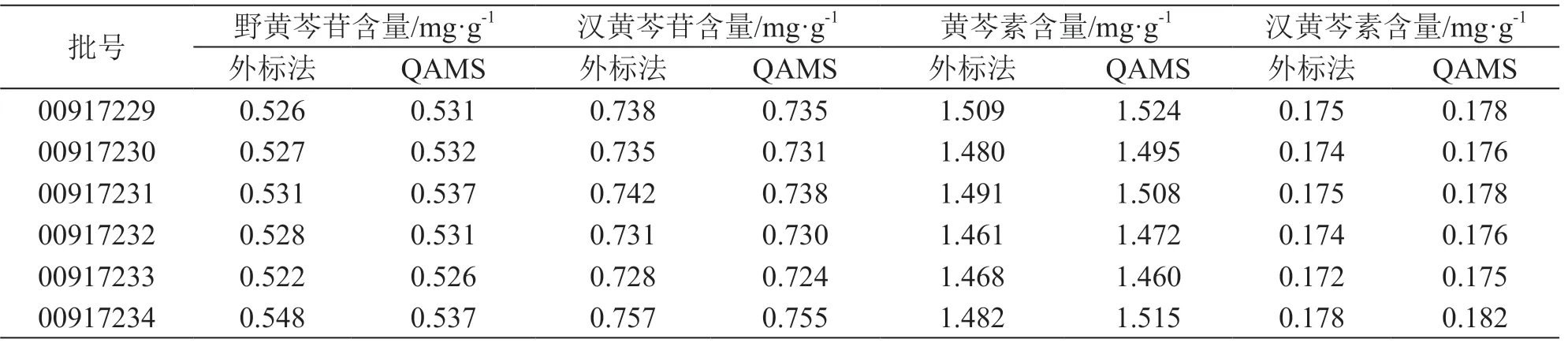
表5 外标法和QAMS测定4个黄酮类成分的含量比较(n=2)
3 讨论
因黄芩苷性质稳定、价廉易得,故本实验选取黄芩苷作为内参物进行一测多评。2015年版中国药典规定茵栀黄颗粒每袋(3 g)含黄芩苷180~220 mg[2],即60.0~73.3 mg/g,本课题组研究发现野黄芩苷等4个成分的含量与黄芩苷含量差异较大,在同一条件下同时检测黄芩苷与野黄芩苷等4个成分的含量,会产生较大的误差。因此本次实验建立以黄芩苷为内参物,同时测定茵栀黄颗粒中野黄芩苷、汉黄芩苷、黄芩素和汉黄芩素含量的一测多评法,未同时测定黄芩苷。
在一测多评法中,如何将待测组分色谱峰进行准确定位,是该法能否顺利或成功应用的关键。本实验通过考察2种高效液相系统及4种规格色谱柱对相对保留时间、保留时间差的影响,结果发现二者重现性均较好(RSD<5 %),最终选择了波动较小的相对保留时间作为色谱峰的定位依据。
经查阅文献黄酮类成分检测波长为2 8 0 nm[10]、278 nm[11]、275 nm[12]、274 nm[6,13]等,本实验采用DAD检测器对样品全波长扫描,发现在274 nm处,野黄芩苷峰前面的干扰峰降至最低,对其含量测定无影响;其他3个成分亦均有较大吸收,且分离度均大于1.5,因此选取274 nm作为吸收波长。另外在试验过程中,流动相比例的变化和流速的变化对野黄芩苷的重现性有影响,因此在耐用性试验中,未考察流动相比例和流速的变化。
采用一测多评法测得茵栀黄颗粒中4个黄酮类成分含量与常规的外标法测得的含量间无显著差异,说明在对照品缺乏的情况下,一测多评法作为多指标含量测定方法的一种补充,可用于茵栀黄颗粒的质量控制与评价。
