PDOX联合细胞减灭术加腹腔热灌注化疗治疗VX-2胃癌并幽门梗阻的实验研究
2018-12-17郭豫吉王春荣
郭豫吉 王春荣 金 颖
胃癌属于临床上最为常见的恶性肿瘤疾病之一,由于该病在发病早期具有较强的隐匿性,患者一经确诊便已是中晚期,丧失了手术根治的时机,甚至合并幽门梗阻,增加了临床治疗难度,不利于患者预后[1]。且有研究报道显示,幽门管属于消化道中狭窄程度最大的部位,部分消化道肿瘤患者早期便可能形成幽门梗阻,而胃癌中晚期患者发生幽门梗阻的概率可达20%[2]。此外,随着近年来相关研究的不断深入,越来越多的学者发现幽门梗阻会促进胃癌的扩散转移,且扩散转移风险与梗阻时间存在正相关关系[3]。由此,寻找一种有效的手段治疗胃癌并幽门梗阻显得尤为重要。鉴于此,本文通过研究PDOX联合细胞减灭术加腹腔热灌注化疗治疗VX-2胃癌并幽门梗阻的效果并予以分析,旨在为临床有效控制胃癌的进展以及缓解幽门梗阻提供参考依据,现报道如下。
资料与方法
一、一般资料
选取40只健康大鼠作为研究对象,将其以随机数字表法均分为研究组和对照组。其中研究组大鼠体质量为184 ~ 227 g,平均体质量为(199.2 ± 10.5)g;鼠龄3 ~ 6个月,平均(4.3 ± 1.2)个月;性别公者12例,母者8例。对照组大鼠体质量为186 ~ 230 g,平均体质量为(198.7 ± 10.3)g;鼠龄3 ~ 7个月,平均(4.4 ± 1.4)个月。性别公者13例,母者7例。两组大鼠的以上资料比较,差异均无统计学意义(P> 0.05),组间存在可比性。所有大鼠均购自河南省实验动物中心,生产许可证号:SCXK(豫)2010-0002。
二、研究方法
1. VX-2胃癌并幽门梗阻鼠模型建立
首先将所有大鼠麻醉,均取仰卧位,将其四肢固定于手术台上。以硫化钠溶液对腹部进行涂擦,予以脱毛处理,并采用活力碘进行常规消毒、铺巾。随后选择大鼠上腹部正中剑突下2 cm作长度为3 cm的切口,依次切开皮肤、皮下组织,完成开腹操作。然后提起胃,暴露幽门管和胃下部,采用1 mL注射器通过胃浆膜层斜穿入幽门管上方2 cm邻近大弯侧处的黏膜下,注入0.1 mL的VX-2肿瘤细胞悬液。术中重点关注无菌操作,避免因感染引发的造模失败。VX-2胃癌并幽门梗阻鼠模型建立完成后采用丝线缝合,并逐层关腹。
2. 干预方式
所有大鼠均予以细胞减灭术加腹腔热灌注化疗治疗,具体方式如下:首先予以静脉注射浓度为2%的戊巴比妥钠针3.5 mL,待麻醉成功后予以消毒、铺巾处理,切口部位取腹正中,将全腹腔暴露,观察肿瘤情况,并切除肉眼可见的肿瘤组织。对于切除难度较大者则予以无水乙醇注射灭瘤。待细胞歼灭术完成后予以腹腔热灌注化疗,首先取250 mL温度略高于正常体温的生理盐水对腹腔进行反复两次的冲洗,随后将相同温度的含有多西紫杉醇10 mg以及卡铂50 mg 的生理盐水250 mL灌入腹腔内,恒温灌注30 min。随后吸出化疗药物,探查止血后关腹。术后3 d,每天重复上述治疗。研究组则在细胞减灭术加腹腔热灌注化疗的基础上,于术后第16 d开始采用PDOX治疗,间隔4 d治疗1次,治疗剂量为10 mg/kg(2.5 mL/kg)。药物经耳缘静脉推注,给药前预防性予以2.5 mg/0.5 mL的地塞米松针避免过敏。给药后追加葡萄糖溶液2 mL,降低化疗药物可能对给药部位局部血管造成的损害。
三、观察指标
分别比较两组各区域腹膜癌指数评分,腹水量、荷瘤质量以及生存期,脏器受累情况等。将大鼠腹腔分为4个不同的区域,分别为Ⅰ区(膈下以及肝膈面)、Ⅱ区(肝、胃、脾、肝脾韧带、大网膜以及上述脏器邻近的腹壁)、Ⅲ区(小肠、结肠以及邻近腹壁)、Ⅳ区(泌尿生殖系统、盆腔、直肠以及系膜),每个区域根据以下标准进行评分:①无肿瘤转移为0分;②肿瘤直径 < 0.2 cm为1分;③肿瘤直径0.2 ~ 2.0 cm为2分;④肿瘤直径 > 2 cm为3分。受累脏器主要包括肺、心脏、肝、脾、肾、盆腔、膀胱以及肠壁等。
四、统计方法
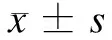
结 果
一、两组大鼠各区域腹膜癌指数情况对比
研究组大鼠各区域腹膜癌指数明显低于对照组,差异均有统计学意义(P< 0.05),见表1。
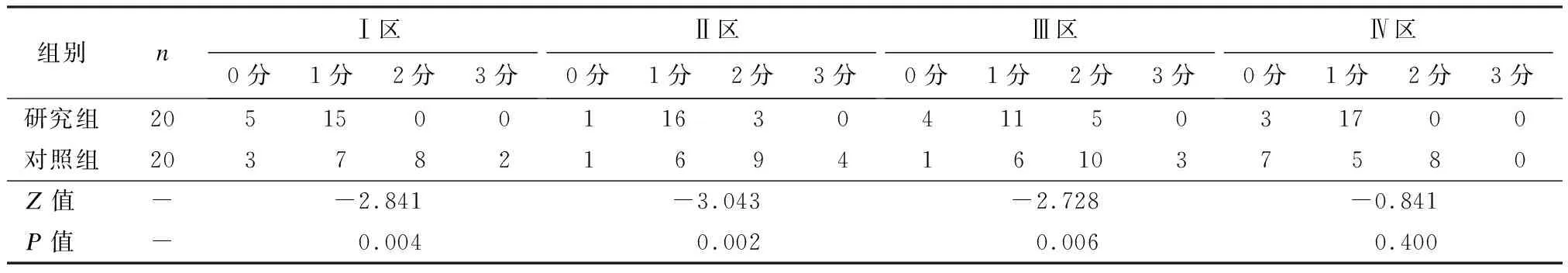
表1 两组大鼠各区域腹膜癌指数情况对比 (n)
二、两组腹水量、荷瘤质量以及生存期对比
研究组腹水量与荷瘤质量明显低于对照组,而生存期明显高于对照组,差异均有统计学意义(P< 0.05),见表2。
三、两组脏器受累情况对比
研究组肺受累、盆腔受累以及肠壁受累占比均明显低于对照组,差异有统计学意义(P< 0.05),见表3。

表2 两组腹水量、荷瘤质量以及生存期对比

表3 两组大鼠脏器受累情况对比 [n(%)]
注:*采用连续校正χ2值,#采用Fisher精确检验
讨 论
幽门梗阻是进展期胃癌患者最为常见的并发症,其主要与胃壁浸润挛缩、胃窦部肿瘤增大以及癌溃疡出血水肿等密切相关[4-6]。胃癌并幽门梗阻患者普遍存在长期禁食、呕吐,且伴有一定程度的脱水、酸中毒以及水电解质紊乱等,会促进病情逐渐恶化,甚至增加胃癌扩散转移的风险[7-9]。随着近年来临床医学对胃癌以及幽门梗阻的认识逐渐深入,相关治疗手段也日益成熟,目前临床上主要采用手术治疗为主。由于胃癌极易发展成为腹膜转移癌,因此临床上主要采用细胞减灭术联合腹腔热灌注化疗治疗[10-12]。该治疗术式综合了手术、区域化疗、热疗以及大容量液体灌洗作用,术中可清除游离癌细胞以及微癌灶[13-14]。为了进一步提高细胞减灭术联合腹腔热灌注化疗的治疗效果,临床上开发了一种阿霉素前体药PDOX。然而,目前临床上关于PDOX对胃癌并幽门梗阻的作用效果相关研究并不多见。
本文结果发现,研究组各区域腹膜癌指数明显低于对照组,这与张珏等[15]人的研究报道相符,提示了PDOX联合细胞减灭术加腹腔热灌注化疗治疗VX-2胃癌并幽门梗阻的效果明显。其中主要原因在于PDOX主要是通过发挥组织蛋白酶B于肿瘤进展不为特异性高表达的特点,从而促使PDOX直达肿瘤靶点,随后于局部释放大量具有抗癌活性的阿霉素分子,进一步发挥抗癌作用,达到靶向杀伤肿瘤细胞的目的。另有研究报道表明,PDOX本身并不具有细胞毒性,进入机体后,于无或低活性组织蛋白酶B组织中,其特异修饰基团无法被酶解,因此无法释放游离DOX,不具有细胞杀伤能力,有效防止了毒副反应的发生。而在进入肿瘤组织后,由于存在高活性组织蛋白酶B表达,因此可特异酶解Phe-Lys肽段,促使PABC-DOX的生成,并经由自发脱酰基水解,大量释放游离DOX,进一步发挥靶向杀伤肿瘤细胞的目的。且在肿瘤侵袭的前锋部位,组织蛋白酶B表达最显著,活性最高,可释放较多的游离DOX,进一步对肿瘤侵袭、转移产生抑制作用[16]。此外,研究组腹水量与荷瘤质量均明显低于对照组,而生存期明显高于对照组,这提示了PDOX联合细胞减灭术加腹腔热灌注化疗治疗VX-2胃癌并幽门梗阻,可显著减少腹水量、荷瘤质量,同时延长大鼠的生存期。分析原因,笔者认为PDOX在不含有组织蛋白酶B的人血浆中可维持数个小时结构不改变,但在含有丰富的组织蛋白酶B环境下,其在十几分钟内便会迅速酶解[17-18]。这同时也提示了PDOX在血液循环中可稳定存在,且不会被水解或破坏,而在组织蛋白酶B丰富的肿瘤组织中可迅速释放。因此,其具有明显的靶向抗肿瘤活性,且不会对患者造成严重的毒副反应,为患者生存期的延长创造了有利条件。另外,研究组大鼠肺受累、盆腔受累以及肠壁受累占比均明显低于对照组,这表明了PDOX联合细胞减灭术加腹腔热灌注化疗治疗VX-2胃癌并幽门梗阻可显著降低大鼠脏器受累风险。究其原因,笔者认为PDOX于正常组织以及外周血中无活性,而在恶性肿瘤侵袭转移过程中,由于癌细胞会分泌大量的组织蛋白酶B,从而会促使PDOX释放出游离阿霉素分子,对周围癌细胞产生灭杀作用,从而降低了患者脏器受累风险。然而,本研究尚且存在样本量较少的缺陷,从而可能导致研究结果发生一定程度的偏倚。因此,在今后的研究中我们应增大样本量,以获取更为准确、可靠的数据。
综上所述,PDOX联合细胞减灭术加腹腔热灌注化疗治疗VX-2胃癌并幽门梗阻具有显著的效果,可有效延长大鼠生存期,且有利于降低器官受累情况,具有较高的临床推广应用价值,值得临床重点关注。
