多孔TiO2/SiO2负载磺化酞菁铜的制备及其催化肾上腺素氧化的性能
2018-11-07谭苏芸牟静文李明田
谭苏芸, 牟静文, 聂 鑫, 李明田*
(1.四川理工学院材料科学与工程学院,四川自贡643000;2.绿色催化四川省高校重点实验室,四川自贡 643000)
金属酞菁具有18π电子的平面大环结构,小分子化合物能够与酞菁环内的金属原子发生轴向配位作用产生分子间的电子传递,表现出优异的催化性能,底物可以是烃类、酚类、胺类、杂环化合物等有机物[1],目前已广泛用于还原反应、氧化反应、分解反应、聚合反应、羰基化反应等领域[2 - 3]。但是作为固相催化剂,金属酞菁存在于溶液中易形成二聚体而降低催化能力,以及由于无法回收而造成二次污染,因此,负载型金属酞菁的制备成为近年来研究的热点[4]。将金属酞菁负载于合适的载体上,一方面可以提高金属酞菁在溶液中的分散性能,提高催化效率,另一方面负载型金属酞菁能够很好地实现回收,减少催化剂的流失[5 - 7]。前期研究工作表明,金属酞菁能够很好地催化儿茶酚胺类物质的氧化,而且负载型金属酞菁具有比游离金属酞菁更优的催化性能[4,8]。
纳米TiO2具有化学性质稳定、抗光腐蚀性好、无毒、易合成等优点,被广泛应用于日用化工、医学、催化、纺织、吸波和环保等领域[9]。但TiO2的机械强度和热稳定性较差,在制备与应用过程中极易发生团聚,所以需要对TiO2进行改性[10 - 11]。SiO2纳米粒子孔径均匀,比表面积大,在水中分散性好,且具有良好的生物相容性,将TiO2和SiO2复合,可有效提高其亲水性,所以TiO2/SiO2材料不仅具有比表面积大、孔容大和孔径大的特性,而且还具有良好的机械性能和热稳定性,可用于催化剂及其载体[12 - 13]。本文选用具有水溶性的磺化酞菁铜(CuTsPc),通过将其负载到多孔TiO2/SiO2载体上制备仿生催化剂,并用来研究催化肾上腺素(AD)氧化的性能。
1 实验部分
1.1 仪器与试剂
NICOLET6700傅立叶红外光谱仪(美国,Thermo Scientific公司);DXR激光显微拉曼光谱仪(美国,Thermo Scientific公司);VEGA 3SBU型扫描电子显微镜(捷克,TESCAN公司);JEM-2010透射电子显微镜(日本,电子公司);DX-2700X-射线衍射仪(丹东浩元仪器有限公司);Lambda 35紫外-可见分光光度计(美国,珀金埃尔默公司);TL0614陶瓷纤维马弗炉(北京中科奥博科技有限公司)。
钛酸丁酯、正硅酸乙酯、十六烷基三甲基溴化铵(CTAB)、Na2HPO4和NaH2PO4等均为分析纯;无水乙醇、丙酮等有机溶剂均为分析纯,使用时没有进一步纯化;氨水、浓HCl为化学纯;盐酸肾上腺素溶液(1.0 mg/mL,吉林市华牧动物保健品有限公司);实验用水为去离子水。
CuTsPc参照文献方法[13]合成。
1.2 CuTsPc-TiO2/SiO2的制备
称取1.2 g CTAB,溶于18 mL去离子水和16 mL氨水(25.0%)的混合溶液中,在搅拌条件下,缓慢滴加正硅酸乙酯6 mL,滴加完毕后,继续向混合液中滴加9 mL钛酸丁酯的HCl溶液(5 mol/L),在50 ℃下搅拌反应4 h后,过滤,滤饼用乙醇洗涤后抽滤、干燥,固体置于马弗炉中在550 ℃煅烧6 h,除去模板剂CTAB,即得多孔TiO2/SiO2。将1 g TiO2/SiO2置于水和乙醇(1∶1,V/V)的混合溶剂中,分散均匀后加入0.1 g CuTsPc,静置24 h,抽滤、真空干燥,研磨,得到CuTsPc-TiO2/SiO2复合材料。
1.3 CuTsPc-TiO2/SiO2的表征
采用KBr压片,对TiO2/SiO2和CuTsPc-TiO2/SiO2进行红外光谱测试,范围为450~4 000 cm-1;对TiO2/SiO2和CuTsPc-TiO2/SiO2进行X-射线衍射XRD测试,角度为5°~80°,步进角度0.02°/s,采样时间0.5 s,管电压和电流为40 kV和30 mA;对TiO2/SiO2和CuTsPc-TiO2/SiO2进行拉曼光谱测试,范围为200~2 300 cm-1;用扫描电子显微镜和透射电子显微镜对样品进行形貌观察和分析。
1.4 催化实验
称取一定量CuTsPc-TiO2/SiO2,将其分散于不同pH值的0.1 mol/L的Na2HPO4-NaH2PO4缓冲溶液(PBS)中,在一定温度下恒温10 min,加入适量的AD溶液,混合均匀后恒温反应一定时间。过滤除去CuTsPc-TiO2/SiO2,滤液以相应的PBS作参比,用紫外-可见光谱仪记录相应AD的吸收光谱,扫描范围为200~800 nm。
为了评价CuTsPc-TiO2/SiO2的催化活性,引入公式:
η=At/Amax
(1)
其中,At代表反应tmin后356 nm处的吸光度,Amax为同一组内数值最大的吸光度值。通过公式(1)可评估不同的条件下CuTsPc-TiO2/SiO2催化剂的相对催化活性。同一条件下的实验至少平行重复3次,取平均值,实验误差小于5%。
2 结果与讨论
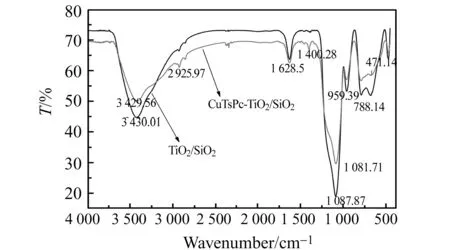
图1 TiO2/SiO2和CuTsPc-TiO2/SiO2红外(IR)光谱图Fig.1 IR spectra of TiO2/SiO2and CuTsPc-TiO2/SiO2
2.1 CuTsPc-TiO2/SiO2的表征
2.1.1红外光谱在450~4 000 cm-1的范围内测得的TiO2/SiO2和CuTsPc-TiO2/SiO2的红外光谱如图1所示。图1中TiO2/SiO2的红外光谱,3 430.01 cm-1和1 628.5 cm-1为表面-OH和样品表面吸附水的振动峰;471.14cm-1和680 cm-1附近的吸收峰分别是Ti-O-Ti的弯曲和收缩振动吸收峰;788.14 cm-1和1 087.87 cm-1是Si-O-Si的伸缩振动峰和不对称伸缩振动峰[14]。理论上TiO2和SiO2的相互作用可分为物理吸附(弱的范德华力)和化学键结合(Ti-O-Si键的形成),红外光谱中930~970 cm-1的吸收峰是Ti-O-Si键的振动吸收,是TiO2/SiO2复合氧化物特征吸收频率[15 - 16],因此在TiO2/SiO2红外光谱中出现了959.39 cm-1吸收峰,表明制成了TiO2/SiO2复合粒子。与TiO2/SiO2相比,CuTsPc-TiO2/SiO2的红外光谱与其基本相似,没有CuTsPc的特征峰的原因,一方面是部分峰重合,另一方面是CuTsPc进入孔洞中。
2.1.2XRD分析图2为TiO2/SiO2和CuTsPc-TiO2/SiO2的XRD测试结果。由TiO2/SiO2的XRD图可知,2θ为24.86°、30.88°、37.84°、48.04°、53.96°、55.16°、62.72°处是锐钛矿TiO2的衍射峰,这与文献报道[17]一致,没有出现SiO2的特征衍射峰,可能SiO2是无定形态[18]。CuTsPc-TiO2/SiO2与TiO2/SiO2相比,两个图谱几乎相同,没有出现CuTsPc的特征衍射峰,其原因是CuTsPc在TiO2/SiO2中处于分散状态,没有结晶态的缘故。
2.1.3拉曼光谱采用拉曼光谱仪在200~2 300 cm-1范围内测试TiO2/SiO2和CuTsPc-TiO2/SiO2的拉曼光谱,测试结果如图3所示。TiO2/SiO2的拉曼光谱图中出现了398 cm-1、521 cm-1和643 cm-13个TiO2的特征峰,这与文献报道[19]类似。对比CuTsPc-TiO2/SiO2和TiO2/SiO2的拉曼光谱图,可以看出CuTsPc-TiO2/SiO2的主要峰中包括TiO2/SiO2的主要峰,其中出现的1 000~1 600 cm-1之间的峰为酞菁中苯环的特征峰[20],表明CuTsPc负载到了TiO2/SiO2上。
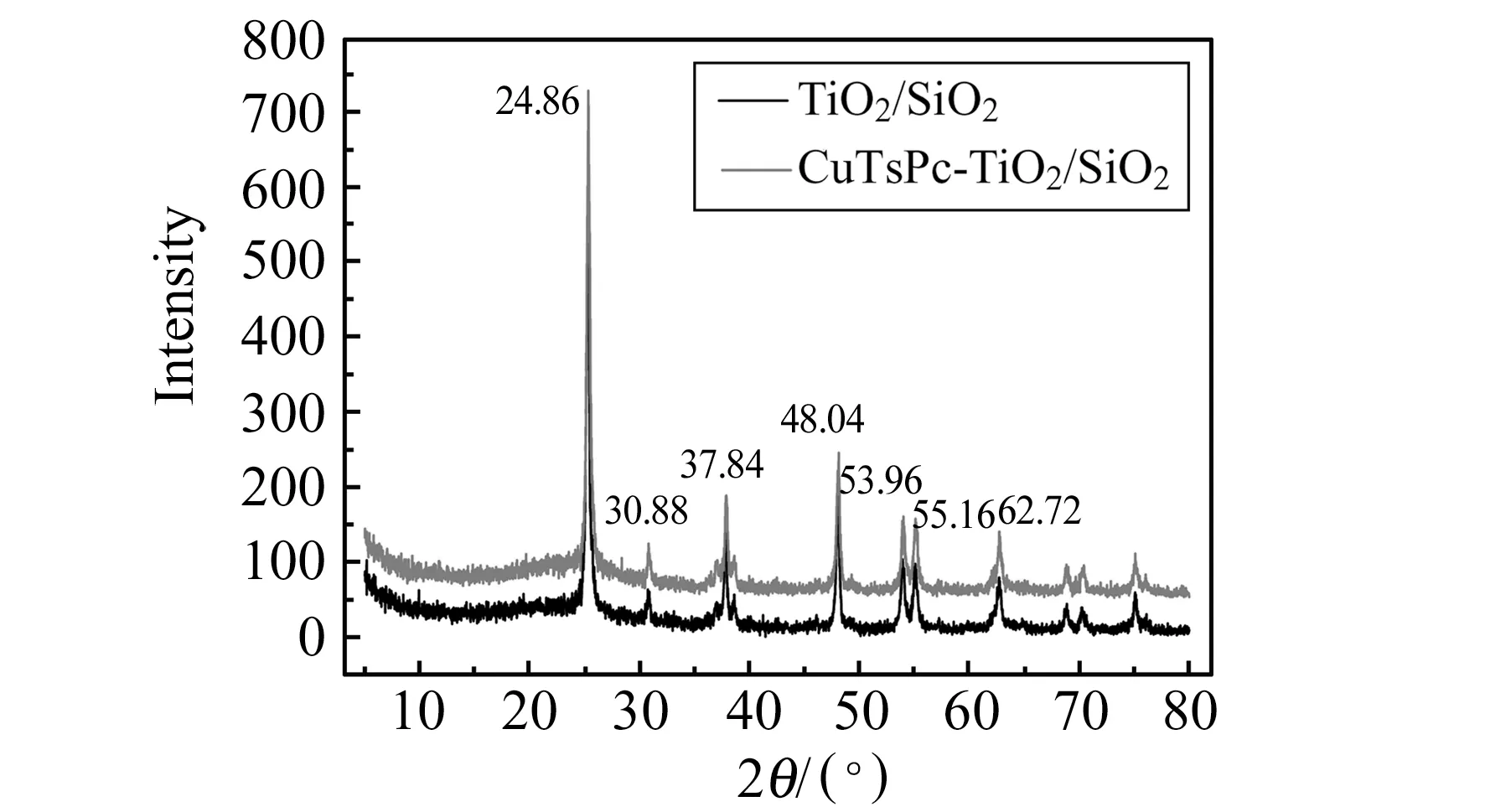
图2 TiO2/SiO2与CuTsPc-TiO2/SiO2的XRD图Fig.2 XRD patterns of TiO2/SiO2and CuTsPc-TiO2/SiO2
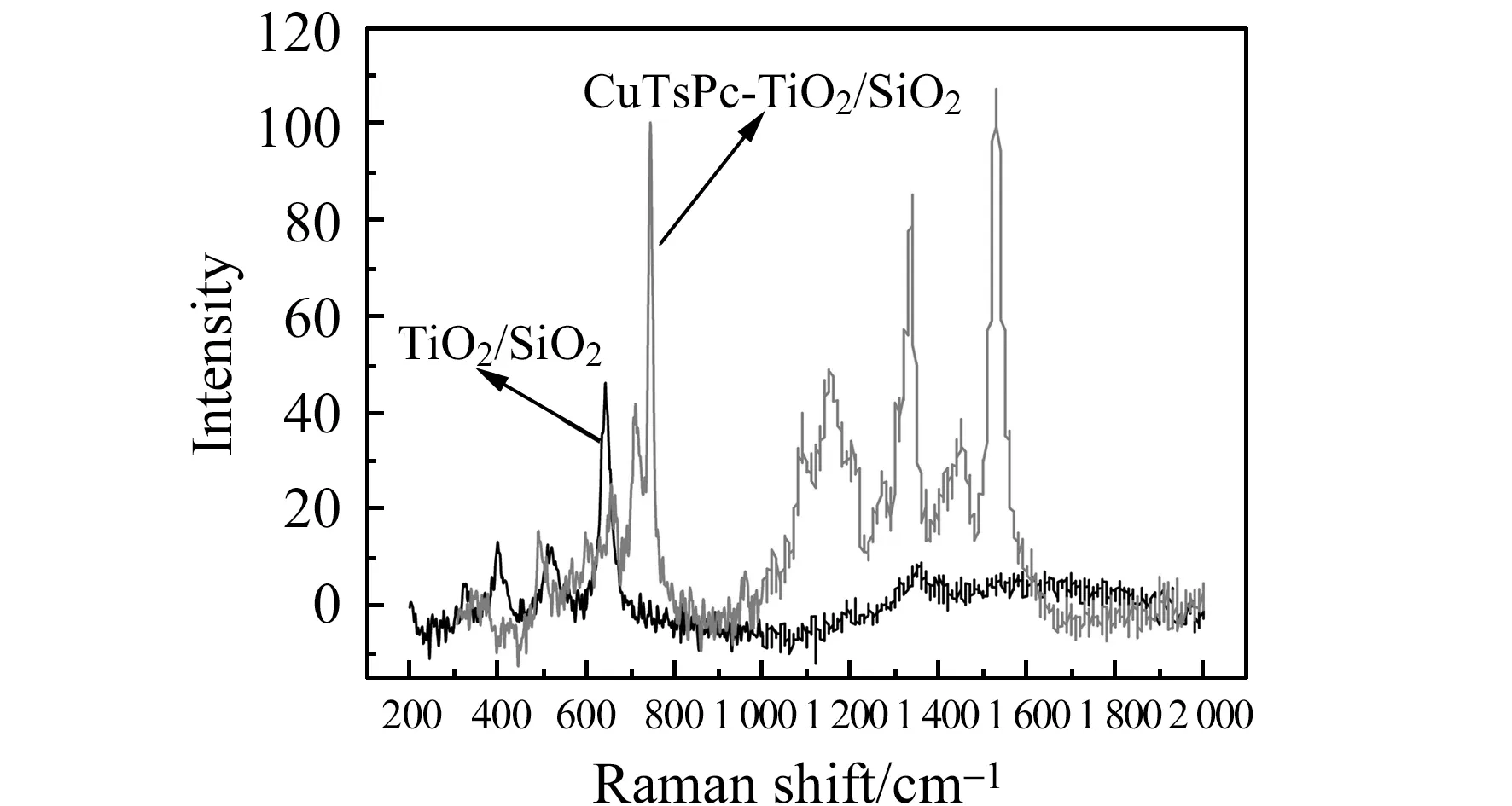
图3 TiO2/SiO2和CuTsPc-TiO2/SiO2的拉曼光谱图Fig.3 Raman spectra of TiO2/SiO2and CuTsPc-TiO2/SiO2
2.1.4形貌分析用扫描电子显微镜(SEM)和透射电子显微镜(TEM)对CuTsPc-TiO2/SiO2的形貌进行扫描,结果如图4所示。由图4a可以看出,CuTsPc-TiO2/SiO2是形状不规则的颗粒,呈松散的团聚状态;在图4b中,大的深色部分是CuTsPc,浅色部分为TiO2/SiO2颗粒,TiO2/SiO2呈现无序交联的多孔结构,CuTsPc不均匀的分散在TiO2/SiO2上。

图4 CuTsPc-TiO2/SiO2的扫描电镜(SEM)(a)和透射电镜(TEM)(b)图Fig.4 SEM(a)and TEM(b) images of CuTsPc-TiO2/SiO2
综合以上结果,说明成功地制备了多孔TiO2/SiO2负载的磺化酞菁铜CuTsPc-TiO2/SiO2复合材料。
2.2 CuTsPc-TiO2/SiO2催化AD的紫外-可见吸收光谱
AD属于儿茶酚胺类物质,含有儿茶酚和胺基,具有重要的生理作用[2]。AD具有邻苯二酚的骨架,其α位有一个-CH(-OH)基团,在催化剂作用下容易被氧化生成相应的氧化产物,图5为不同时间下AD在0.1 mol/L PBS(pH=8.0)中被CuTsPc-TiO2/SiO2催化氧化的吸收光谱图。由图5可知,在0.1 mol/L PBS中AD的特征吸收峰出现在279 nm[2]。在CuTsPc-TiO2/SiO2的催化下,AD的吸收光谱发生明显的变化:随着催化氧化反应的不断进行,在279 nm处的吸收峰强度不断增加,同时在356 nm处出现了一个新的吸收峰且强度随着时间的增加而增强,这是醌式肾上腺素的特征峰[21],表明CuTsPc-TiO2/SiO2能够有效地催化AD氧化。实验结果还证明,AD浓度在2.5×10-4mol/L和1.0×10-3mol/L时,未被氧化时,279 nm处的吸收峰强度分别为0.134和0.811,而氧化产物在356 nm处吸收峰的强度分别为0.721和0.775,强度与浓度的线性关系不好,因此选择最合适的浓度5.0×10-4mol/L,其相应强度为0.343和0.361。
2.3 反应时间对CuTsPc-TiO2/SiO2催化AD氧化的催化活性影响
采用公式(1)计算,得到反应时间对CuTsPc-TiO2/SiO2催化AD氧化的催化效率影响的示意图,其结果如图6所示。可以看出:在开始的60 min内,η值迅速增加,在40 min时已经达到了最大催化效率的60%,高于游离金属酞菁的催化效率[7],而后η值虽然仍在增加但增加幅度较小,80 min时才达到最大催化效率的90%。在测试时间范围内,虽没有到达完全催化氧化的程度,但从最后20 min内的吸收光谱可以观察到AD氧化几乎已经结束,若再延长催化时间,其相对催化效率可能会出现下降现象[2]。
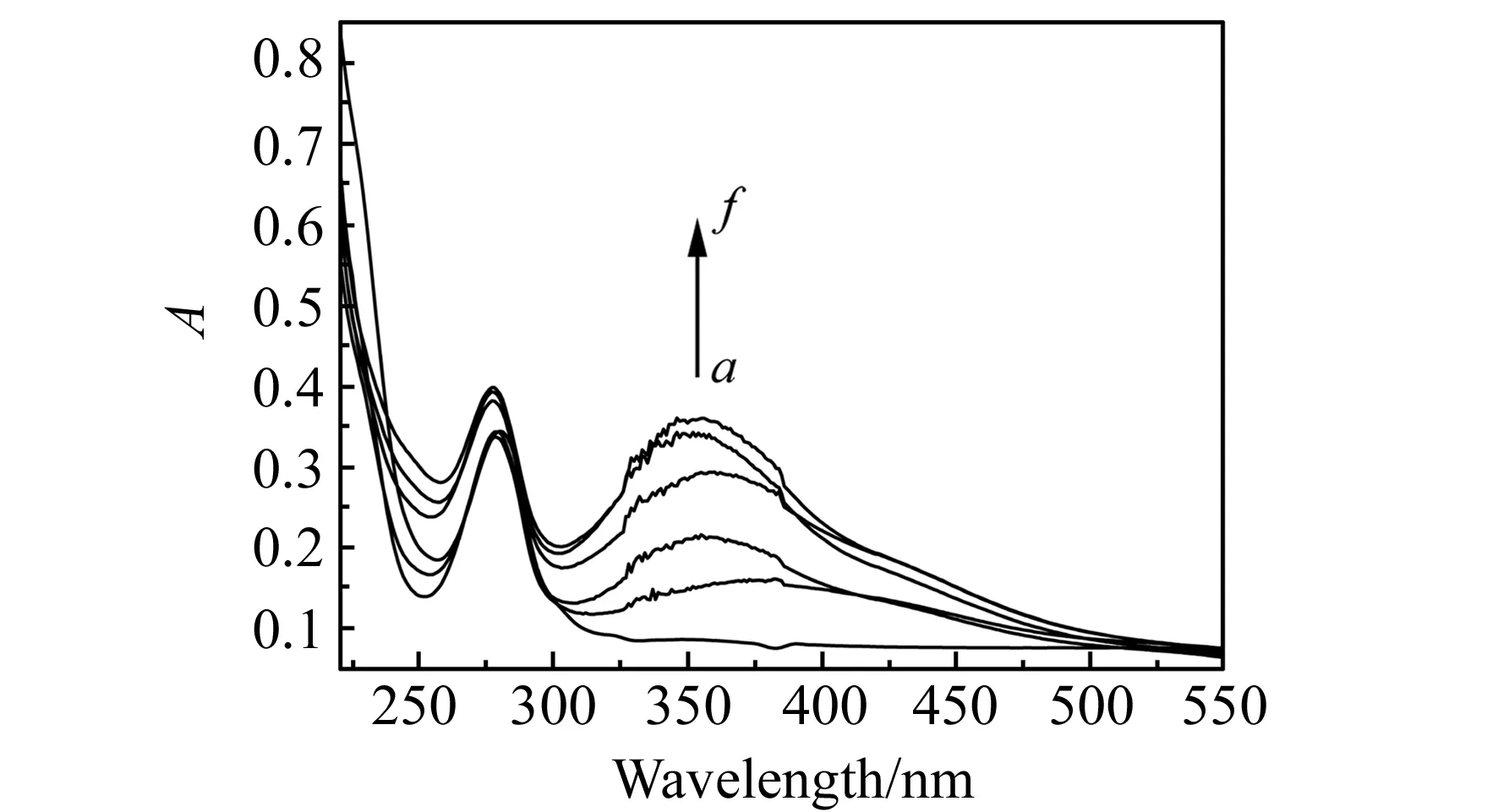
图5 在不同时间下CuTsPc-TiO2/SiO2催化AD氧化的紫外-可见(UV-Vis)吸收光谱Fig.5 UV-Vis spectra of AD using CuTsPc-TiO2/SiO2 as catalyst pH=8.0,T=45 ℃,[AD]=5.0×10-4 mol/L,[CuTsPc-TiO2/SiO2]=0.74 mg/mL.a-f:0,20,40,60,80,100 min.

图6 CuTsPc-TiO2/SiO2催化AD氧化的催化效率与时间的关系Fig.6 Effect of incubation time on the catalytic efficiency of CuTsPc-TiO2/SiO2 to AD oxidationpH=8.0,T=45 ℃,[AD]=5.0×10-4 mol/L,[CuTsPc-TiO2/SiO2]=0.74 mg/mL.
2.4 pH值对CuTsPc-TiO2/SiO2催化AD氧化的催化活性影响

图7 pH值对CuTsPc-TiO2/SiO2催化AD氧化效率的影响Fig.7 Effect of pH on the catalytic efficiency of AD oxidation(a:CuTsPc-TiO2/SiO2,b:none)T=45 ℃,[AD]=5.0×10-4 mol/L,[CuTsPc-TiO2/SiO2]=0.74 mg/mL,time=100 min.
采用公式(1)计算,得到溶液pH值对CuTsPc-TiO2/SiO2催化AD氧化的催化效率的影响,见图7。从图7可以看出,有催化剂时在pH值从3.0~8.0的范围内,η值是逐渐地增加,而在pH=8.5处稍有下降,然后在pH=9.0时又突然增大,其现象不同于游离金属酞菁催化AD氧化的现象,其可能的原因是由于pH值过大AD发生自动氧化增加了其氧化的程度[2]。未添加催化剂的条件下,当pH≤8.5时,未见催化反应发生,当pH≥9.0时,有明显的氧化反应发生,pH=10.0时,已达到最高催化效率的83.2%,说明在高pH值环境下AD能够自动地被空气中的O2氧化。前期的催化机理表明:酸性环境不利于催化底物AD和O2与Cu(Ⅱ)的配位而形成AD离子进一步发生氧化反应,但pH值过大时,AD又能够自动被氧化,因此研究AD催化氧化的pH值范围应该小于9.0。
2.5 温度对CuTsPc-TiO2/SiO2催化AD氧化的催化活性影响
从40 ℃到70 ℃的测试温度范围内,η值是先增加后减小的,在55 ℃达到最佳,与游离金属酞菁的催化[2]和Y型分子筛负载FePc催化AD氧化[22]的现象相似,其中MPc(M=Mn(Ⅱ),Fe(Ⅱ),Ni(Ⅱ),Cu(Ⅱ))和FePc/Y的最佳催化温度分别为55 ℃和50 ℃。这可以理解为:温度越高越有助于催化底物AD和O2与中心离子的配位与解离,配位作用有助于提高催化效率,而在没有完成电子转移之前,配体的离去则减小催化反应的速率,在测试的温度范围内,这两种作用共同作用的结果是η值先增加后减小,说明先是配位作用后是离子的解离作用占主要地位。
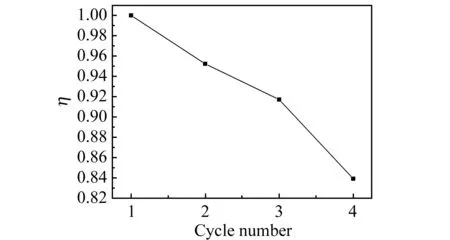
图8 CuTsPc-TiO2/SiO2的重复利用性能Fig.8 Reusability of CuTsPc-TiO2/SiO2 for AD oxidationpH=8.0,T=55 ℃,[AD]=5.0×10-4 mol/L,[CuTsPc-TiO2/SiO2]=0.74 mg/mL,time=100 min.
2.6 CuTsPc-TiO2/SiO2用量对AD氧化的催化活性影响
45 ℃时,在pH=8.0的PBS中,CuTsPc-TiO2/SiO2催化AD氧化的催化效率随着催化剂用量的增加先增大后减小。当CuTsPc-TiO2/SiO2的用量在0.74 mg/mL时,η就达到52.7%,且增加到2.82 mg/mL时,η才达到91.3%,而且在3.36 mg/mL时达到最大,其后在3.62 mg/mL时又降低。造成这种现象的可能原因是此催化剂结构较大,大分子之间相互屏蔽,造成空间位阻,不利于反应活性中心、AD和O2之间相互碰撞。综合考虑,在其他组催化实验中催化剂的用量均为0.74 mg/mL。
2.7 催化剂稳定性的研究
在最佳催化条件下,考察了CuTsPc-TiO2/SiO2的稳定性。反应结束后,离心分离回收催化剂,并用去离子水和乙醇洗涤2~3次,再在100 ℃焙烧除去催化剂表面的副产物,然后用于下一次反应,结果示于图8。从图中可以看出,催化剂使用后其催化性能有所降低,但降低并不明显,使用4次后仍然保持80%以上的催化剂活性。
3 结论
成功制备了多孔TiO2/SiO2粒子,再用浸渍法,将磺化酞菁铜负载到多孔TiO2/SiO2粒子制备了复合粒子CuTsPc-TiO2/SiO2。肾上腺素在PBS中能够被CuTsPc-TiO2/SiO2有效地催化氧化,采用紫外-可见吸收光谱法评价了催化效率,合适的催化条件是:pH=8.0,T=55 ℃,催化剂用量为0.74 mg/mL。
