基于主客体识别作用构筑的聚合物前药胶束及其药物控释性能研究
2018-07-12刘彩萍
刘彩萍, 白 阳
(陕西科技大学 化学与化工学院 陕西省轻化工助剂重点实验室, 陕西 西安 710021)
0 引言
近年来,基于金属配合、π-π堆积、主客体识别、氢键等非共价作用力构筑的超分子聚合物(SPs)因其构筑驱动力动态可逆和多重刺激响应性的特点备受关注,广泛应用于构筑刺激响应性聚合物、药物控释载体和生物成像领域[1-4].目前,基于主客体识别的非共价作用在环境刺激条件下表现出丰富的包合和解包合特性,而且主客体识别诱导的自组装过程只需在合适条件下进行“模块化”组分配比和简单的后处理即可自发形成,不需进行催化或化学反应,方法简单,产物易得,并具有丰富的环境刺激响应性[5,6].在众多主体大环分子中,β-环糊精具有溶解性好、低毒廉价、来源丰富的特点,不仅能在生物利用率方面增强细胞膜吸收,并能促进其在细胞膜中的渗透[7-10],具有十分优异的性能表现.基于环糊精-客体分子的主客体包合作用构筑的超分子聚合物也因其具有多种刺激响应性优点,可用于包载抗癌药物,实现药物控制释放[11-15].例如,Peng L等[16,17]多次制备的基于β-环糊精与二茂铁主客体识别作用的超分子聚合物可在水中自组装形成胶束,用以包载疏水性的药物分子,实现氧化还原控制的药物释放. Zhang H等[18]以环糊精和偶氮苯的主客体包合作用制备了可“呼吸”空心纳米球,并实现药物在温度刺激响应下的控制释放.
目前,化学治疗是国内外治疗癌症最主要和最有效的方法,但多数抗癌药物水溶性差、吸收困难,并具有一定的毒副作用[19-26].由于肿瘤细胞与人体正常细胞内微环境的差异[27-31],如肿瘤细胞内酸性的内涵体/溶酶体环境(pH 5.0~5.5),因此制备对肿瘤细胞的内部环境具有刺激响应性的聚合物药物运送载体,并利用肿瘤组织的高通透性和滞留效应(EPR效应),有望实现药物在肿瘤细胞内的富集和靶向释放,提高有效利用率,降低由药物本身的毒性而产生的毒副作用.
本论文首先通过对β-环糊精进行改性制备环糊精-阿霉素的前药分子,阿霉素与环糊精之间以pH响应性动态化学键-酰腙键相连,然后利用环糊精和偶氮苯的主客体包合作用构筑超分子聚合物并在纯水中自组装形成以疏水性抗癌药阿霉素为核,亲水性聚甲基丙烯酸N,N-二甲氨基乙酯为壳的前药胶束.最后对所构筑聚合物-前药胶束的体外药物控释行为进行了研究,超分子聚合物的构筑及药物控释行为如图1所示.

图1 CD-DOX/Azo-PDMA超分子聚合物-前药纳米胶束的制备及酸性环境诱导的体外药物释放行为
1 实验部分
1.1 原料与仪器
(1)主要原料:β-环糊精(β-CD),天津市科密欧化学试剂有限公司,分析纯;溴乙酸乙酯、水合肼(NH2NH2·H2O)、甲基丙烯酸-N,N-二甲氨基乙酯(DMA),上海麦克林生化科技有限公司;盐酸阿霉素(DOX·HCl),萨恩化学技术(上海)有限公司;4-(苯基偶氮基)苯酚(Azo-OH)、1,1,4,7,7-五甲基二亚乙基三胺(PMDETA),北京百灵威科技有限公司;氢化钠(NaH),质量分数为60%,保存于煤油中,北京百灵威科技有限公司;2-溴异丁酰溴(BIBB),阿拉丁试剂.以上试剂均为直接使用.溴化亚铜(CuBr)使用前在乙酸中搅拌过夜,乙醇中洗涤三次除去残留乙醇,25 ℃下真空干燥两天,天津市天力化学试剂有限公司;三乙胺(TEA)使用前用4A级分子筛除水,广州市金华大化学试剂有限公司.
(2)主要仪器:傅立叶红外光谱(FTIR)在VECTOR-22型红外光谱仪上测定,测试试样为KBr涂片,分辨率4 cm-1,每个样品扫描32次;1H NMR及2D1H NMR NOESY采用Bruker AV-400 核磁共振仪(Bruker BioSpin,Switerland)测定,CDCl3,DMSO-d6或D2O为溶剂,以四甲基硅烷为内标;分子量和分子量分布在美国waytt公司凝胶渗透色谱/多角度激光光散射联用仪(SEC/MALLS)上测定,色谱柱型号为:MZ 103 Å(300×6.8 mm),THF为流动相,进样量0.2 mL,溶剂流出速度为0.5 mL/min,测定温度为40 ℃,聚合物溶液的dn/dc值通过Optilab rEX型示差折光仪测定,使用Waters 515型泵.
1.2 实验步骤
1.2.1酯化环糊精β-cyclodextrin-ester(β-CD-ester)的制备

1.2.2酰肼化环糊精β-CD-hydrazide的制备
向10mL圆底烧瓶中加入β-CD-ester(1 g,0.81 mmol),NH2NH2·H2O(3 mL)和2 mL DMF,室温下磁力搅拌24 h.反应完成后,使用冰丙酮沉淀,抽滤并真空干燥,得到白色固体β-CD-hydrazide.FTIR(KBr):1 662 cm-1(ν,C=O).1H NMR(DMSO-d6,TMS,δ):1.74~2.0(2H,-NH2),3.20~3.90(2,3,4,5,6H inβ-CD),4.39~4.61(6H,6-OH),4.78~4.92(7H,1H inβ-CD),5.69~5.87(14H,2,3-OH),7.93~8.01(1H,-NHNH2).
1.2.3β-环糊精-阿霉素前药分子(β-CD-hydrazone- DOX)的制备
参考文献[32]的方法,向圆底烧瓶中加入β-CD-hydrazide(62.1 mg,0.05 mmol),DOX·HCl (43.5 mg,0.075 mmol),25 mg无水Na2SO4和2.5 mL DMF,搅拌5 min.随后加入一滴冰乙酸并通氮气10 min,于避光状态下室温搅拌40 h.反应完成后,抽滤除去无水Na2SO4,滤液在冰丙酮中沉淀,抽滤,将粗产物用无水乙醇洗三次,真空干燥,得红色固体β-CD-hydrazone-DOX,产率22.2%.FTIR(KBr):1 659 cm-1(ν,C=O).1H NMR(DMSO-d6,TMS,δ):1.01~1.31(3H,-CH3),3.99(3H,-OCH3),7.61~8.00(3H,Ar).
1.2.4引发剂2-溴-2-异丁酯偶氮苯(Azo-Br)的制备
参考文献[33]的方法,将4-(苯基偶氮基)苯酚(1.5 g,7.6 mmol)和三乙胺(1.53 g,15.2 mmol)溶于50 mL CH2Cl2,在冰浴条件下将2-溴异丁酰溴溶液(3.5 g 溶于20 mL CH2Cl2,15.2 mmol)逐滴加入反应瓶中,室温下搅拌24 h.反应完成后,抽滤除去不溶性盐,将滤液用每次不少于50 mL的去离子水萃洗3次,并用无水Na2SO4干燥,浓缩得粗产物.将粗产物在乙醇中重结晶3次,得到橙黄色晶体产物,产率47.02%.1H NMR(CDCl3,TMS,δ):2.079(6H,-CH3),7.38~8.05(9H,Ar).MS,Found m/z:369.02[M+Na]+.
1.2.5偶氮苯封端的聚甲基丙烯酸-N,N-二甲氨基乙酯(Azo-PDMA)的制备
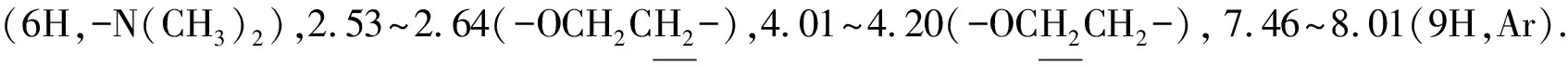
1.2.6CD-DOX/Azo-PDMA超分子聚合物胶束溶液的制备与表征
将β-CD-hydrazone-DOX(2 mg)和Azo-PDMA(6 mg)溶于2 mL的DMF,搅拌30 min后加入40μL TEA作为缚酸剂,继续搅拌30 min后缓慢滴加2 mL的去离子水,搅拌过夜.使用截留分子量为1 000的透析袋透析上述混合溶液,得CD-DOX/Azo-PDMA超分子聚合物胶束溶液7.5 mL,向胶束溶液中加入0.5 mL去离子水,定容至1 mg/mL.超分子聚合物的制备如图2(c)所示.
超分子聚合物胶束溶液超声20 min,磁力搅拌30 min后,使用Nano Brook 90Plus Zeta型多角度激光粒度仪(DLS)测定Dz值,测试温度25 ℃,散射光由垂直极化的He-Ne激光器发射,测试角度90°.将7μL胶束溶液滴于铜网上,5 min后除去附着液体,使用Hitachi-760型透射电子显微镜测试,加速电压75 KV.
1.2.7DOX体外控制释放实验
(1)DOX溶液标准曲线的建立
用pH为7.4的磷酸盐缓冲液配浓度2.5×10-5mmol/mL的盐酸阿霉素溶液,稀释此溶液,得到浓度为0.1 mmol/mL、0.25 mmol/mL、0.5 mmol/mL、0.75 mmol/mL、1.0 mmol/mL、2.5 mmol/mL、5.0 mmol/mL、7.5 mmol/mL和10×10-6mmol/mL的一系列标准溶液,并测568 nm处荧光强度,得到荧光标准曲线.
(2)体外控释实验
两个广口瓶中分别加入pH为5.0和7.4的磷酸盐缓冲液40 mL,取CD-DOX/Azo-PDMA超分子聚合物胶束溶液2 mL移入截留分子量1 000的透析袋,将透析袋浸没在缓冲液中,于37 ℃下恒温振荡.特定的时间点在广口瓶中取出3 mL缓冲液,并再加入相同体积的缓冲液.pH为5.0和7.4的实验分别平行进行三次.将取出的溶液测荧光,根据DOX的荧光标准曲线,得到DOX的浓度,并计算累计释放率,累计释放率的计算公式如式(1)所示:

(1)

(a)β-CD-hydrazone-DOX的合成路线
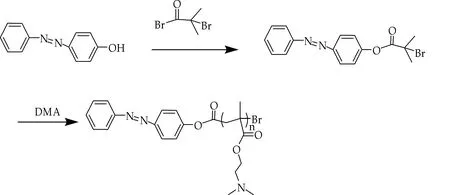
(b)Azo-PDMA的合成路线
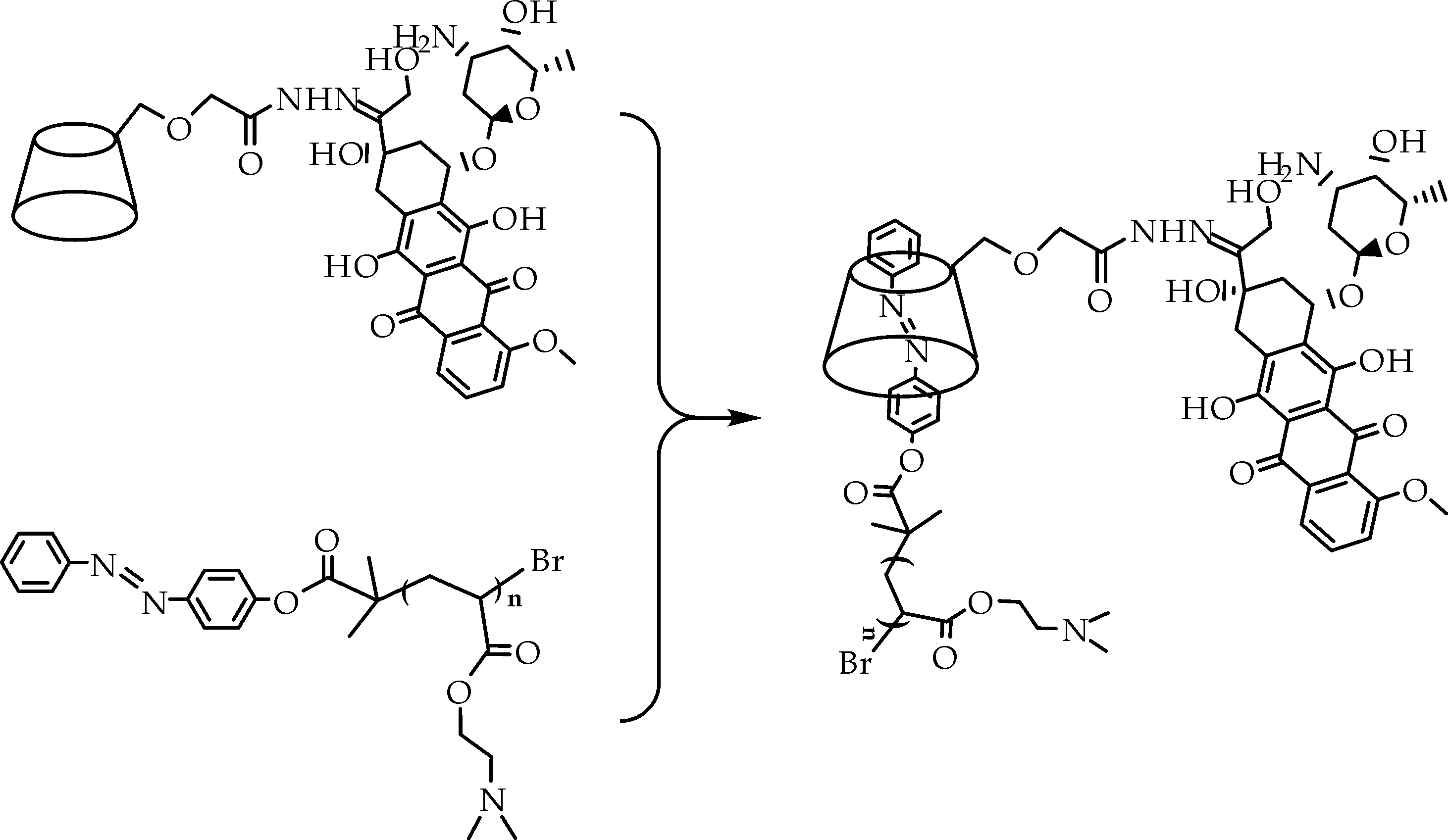
(c)CD-DOX/Azo-PDMA超分子聚合物的制备图2 β-CD-hydrazone-DOX,Azo-PDMA的合成路线和CD-DOX/Azo-PDMA超分子聚合物的制备
2 结果与讨论
2.1 β-CD-hydrazone-DOX的合成及表征
β-CD-hydrazone-DOX的合成路线如图2(a)所示.首先通过β-环糊精的酯化反应制备其衍生物β-CD-ester,由于β-环糊精6位羟基较活泼,当其与过量氢化钠反应后脱去H2生成醇钠,并进一步与溴乙酸乙酯反应制得β-CD-ester.β-CD-ester的FT-IR如图3中a曲线所示,1 745 cm-1处出现酯基的特征吸收峰;结合1H NMR谱图4(a),δ=1.215、4.145和4.127处出现溴乙酸乙酯特征氢a,b,c的吸收峰,证明成功合成了β-CD-ester.通过对溴乙酸乙酯氢a的吸收峰和β-环糊精2,3位的羟基氢的吸收峰进行积分计算,峰面积比约为1∶3,因此溴乙酸乙酯对β-环糊精的平均取代度为1.5.接下来通过氨解反应制备酰肼化β-环糊精衍生物β-CD-hydrazide,其FT-IR如图3中b曲线所示,1 662 cm-1处出现酰肼键的特征吸收峰,且1 745 cm-1处酯基特征吸收峰消失,此外,在其1H NMR谱图4(b)出现仲胺和伯胺氢的特征吸收峰,同时溴乙酸乙酯a和c氢的特征峰消失,以上测试结果证明酯基氨解完全,生成了酰肼键.最后通过β-CD-hydrazide与DOX羰基在冰醋酸催化下的席夫碱反应制得目标产物β-CD-hydrazone-DOX,粗产物使用无水乙醇反复溶洗除掉未反应的DOX.如图4(c)所示,1H NMR谱图上出现DOX的特征吸收峰,表明β-CD-hydrazide与DOX发生了反应.DOX的氢e与β-环糊精2,3位的羟基氢吸收峰面积积分比为1∶3.1,平均取代度为1.6,与溴乙酸乙酯对β-环糊精的平均取代度相一致.以上结果表明最终成功制备了 DOX以酰腙共价键连接在环糊精上的前药分子β-CD-hydrazone-DOX.

图3 β-CD-ester,β-CD-hydrazide和β-CD-hydrazone-DOX的FT-IR图

(a)β-CD-ester (b)β-CD-hydrazide (c)β-CD-hydrazone-DOX图4 β-CD-ester,β-CD-hydrazide和β-CD-hydrazone-DOX 的1H NMR图
2.2 偶氮苯端基聚合物Azo-PDMA的合成及表征
聚合物Azo-PDMA以Azo-Br作为引发剂,通过ATRP聚合反应得到,合成路线如图2(b)所示.引发剂由Azo-OH与过量BIBB进行酯化反应制备,反应以三乙胺为缚酸剂,粗产物在无水乙醇重结晶制得.Azo-Br的1H NMR如图5(a)所示,偶氮苯对应氢原子a,b,c,d与BIBB的异丁基特征氢e均可被观察到,峰面积比接近2∶2∶3∶2∶6.此外,质谱测试的分子量为369.02[M+Na]+(如图6所示),与理论分子量相符.表明成功合成了引发剂Azo-Br.ATRP聚合以CuBr为催化剂,60 ℃条件下聚合3 h.其中引发剂Azo-Br,单体DMA,配体PMDETA和催化剂CuBr的摩尔比为1∶20∶1∶1.1H NMR如图5(b)所示,可清楚地观察到Azo和PDMA的特征吸收峰,通过积分计计算Azo-Br特征氢c的吸收峰和PDMA链上特征氢e的吸收峰的面积比得出PDMA的平均聚合度DPNMR=37,由此计算出Azo-PDMA的数均分子量(Mn,NMR)为37×157+346=6 155,此外,SEC/MALLS测试Azo-PDMA的分子量为5 800,两者保持一致,同时,分子量分布为1.12,测试淋洗曲线呈单窄峰分布,如图7所示,以上结果均表明成功制得了窄分子量分布的聚合物Azo-PDMA.

(a)Azo-Br (b)Azo-PDMA图5 Azo-Br和Azo-PDMA的1H NMR图
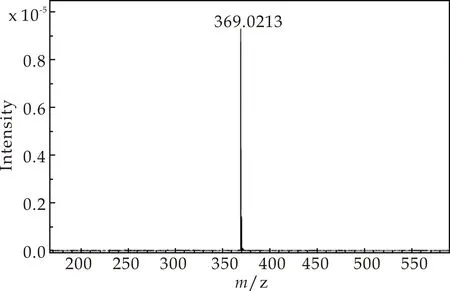
图6 Azo-Br的质谱图

图7 Azo-PDMA的SEC/MALL淋洗曲线
2.3 CD-DOX/Azo-PDMA超分子聚合物的构筑及其自组装性能
CD-DOX/Azo-PDMA 超分子聚合物通过混合溶剂溶解并透析的方法制得.β-CD的疏水空腔对偶氮苯具有强包结络合作用,在水溶液中,偶氮苯能够进入β-环糊精的空腔,2D1H NMR NOESY如图8所示,β-环糊精的3,5-H质子与偶氮苯的a,c氢质子之间出现了交叉峰,说明CD-DOX/Azo-PDMA超分子聚合物是由环糊精与偶氮苯的主客体相互作用形成的.所构筑的超分子聚合物为两亲性聚合物,其中药物分子DOX具有疏水性,聚合物链PDMA具有亲水性,因此超分子聚合物在水中可形成以DOX为核,PDMA为壳层并具有一定尺度的胶束自组装体.动态光散射(DLS)如图9(b)所示,平均粒径82 nm,TEM如图9(a)所示,可清楚观察到球形纳米粒,粒径分布在100 nm,两者测试结果基本保持一致.这表示通过主客体识别作用已构筑出形态尺寸稳定的纳米胶束.
2.4 DOX的体外药物控释行为
将盐酸阿霉素标准溶液在λex=484 nm,λem=556 nm的条件下测试荧光,以吸光度对阿霉素的浓度进行线性回归,得到标准曲线方程.
药物分子DOX通过共价酰腙键与β-环糊精相连接,酰腙键具有pH敏感的特性,在酸性条件下,酰腙键发生水解.体外pH=5.0的药控实验中,53 h后,DOX的累计释放率达到了76%,然而,在9 h内,累计释放率就已达到60%左右,相较pH=7.4的药控实验,50 h时,DOX的累计释放率仅为31%(图10),充分说明酰腙键对酸性环境极为敏感,DOX的快速释放是由酰腙键的水解引起的.肿瘤细胞内酸性的内涵体/溶酶体环境pH为5.0~5.5,而正常细胞和人体血液的pH为7.4,因此,有望实现药物在肿瘤细胞的靶向释放,从而降低药物的毒副作用.

图8 CD-DOX/Azo-PDMA超分子聚合物的2D 1H NMR NOESY谱图

(a)TEM图

(b)DLS图图9 CD-DOX/Azo-PDMA超分子聚合物的TEM和DLS图

图10 CD-DOX /Azo-PDMA超分子聚合物在pH 5.0和pH 7.4磷酸盐缓冲液中DOX的累计释放率
3 结论
本文通过主客体识别作用构筑了基于环糊精前药分子和偶氮苯封端聚合物的聚合物前药胶束.测试结果表明聚合物前药胶束为具有合适尺度的纳米组装体.纳米胶束通过化学键合的方式负载药物分子,提高了药物的稳定包载,而由于胶束中存在对pH敏感的酰腙键,因此超分子聚合物胶束在较低pH下可实现酰腙键的断裂,从而有效还原释放出药物分子DOX.此类pH敏感型超分子聚合物-前药纳米胶束的制备在肿瘤的靶向治疗方面有着潜在的应用价值.
