药品质量投诉调查实例及对策分析
2018-06-21周华琴
周华琴
(上海上药新亚药业有限公司,上海201203)
0 引言
作为药品生产企业的QA人员,在日常工作中会收到各种涉及本公司产品信息、质量投诉、咨询等方面的反馈,通常将这些反馈归纳为3种情况:
(1)药品的不良反应,如皮疹、腹泻等,需按《药品不良反应报告和监测管理办法》进行处理,并按需上报;
(2)不合理用药,如药品因配伍禁忌产生的沉淀浑浊,溶液放置时间过长导致的颜色异常等;
(3)由质量缺陷引起的投诉,如包装破损、瓶内异物、颜色发黄等。
对于收到的药品质量投诉及不良反应信息,均应记录在册;分析调查由产品质量缺陷引起的投诉,采取必要的纠正与预防措施,避免同一质量问题反复发生。
抗生素粉针剂作为处方药,在药品的生产和流通环节可能会出现各种问题,最终影响医护人员和患者的使用,因此,对于由质量缺陷引起的用户质量投诉,应通过对药品生产各工序和药品检验环节进行分析调查,查找出引发质量问题的原因,采取必要的纠正与预防措施,确保产品质量和用药安全。
本文以某抗生素粉针剂产品的质量投诉为例,梳理和分析导致出现质量缺陷的原因,并探讨相应的对策。
1 药品质量投诉调查及对策流程
1.1 样品的确认
根据用户提供的相应照片或实样,对收到的投诉产品进行包装形式、外观的确认,可与同品种、同批次产品的留样进行比对,以确认其是否为我公司生产的产品,并对产品包装的完整性进行确认。
1.2 原因分析
各部门相互配合,对被投诉产品的生产、检验相关环节进行调查分析及确认,查找引起质量缺陷的原因,必要时对原因进行模拟验证。
1.2.1 生产方面
对被投诉产品的生产过程进行追溯。追溯被投诉产品的批生产记录、岗位记录,复核生产时所使用的原辅料、生产设备性能、生产工艺过程参数控制、生产环境以及人员的操作等环节是否有异常情况发生;追溯相关设备的检修、运行情况;追溯空气净化、水处理等公用系统的运行情况。必要时,对相关的其他批次的生产过程进行追溯。
1.2.2 检验方面
对被投诉产品的批检验记录进行复核,并复核检验时所用的原辅料、包装材料以及成品检验过程是否有异常情况发生。
如需对被投诉产品内在质量进行进一步确认的,可对被投诉样品或留样产品进行检验。
1.2.3 储存方面
对被投诉产品的储存过程进行复核,检查其是否有异常情况发生,调取温湿度监控记录等。
1.2.4 运输方面
对于有特殊储存条件的被投诉产品(对温湿度、光照比较敏感的产品),可追溯其运输过程的贮藏记录等。
1.3 对策的制定、实施及效果确认
对于由质量问题引起的投诉,制定相关纠正与预防措施,并对纠正与预防措施的实施效果进行跟踪确认。
2 投诉调查实例分析
在某用户反馈的一批抗生素粉针剂产品中,发现有一瓶瓶内有异物,经沟通收到投诉样品后,立即展开调查,并进行产品确认、原因分析、对策制定以及对策的实施和效果确认,以保证我公司产品的质量。
2.1 产品确认
将投诉样品与我公司同一批号、同一规格的留样产品进行比对,发现包装形式和外观完全一致,确认为我公司产品,且产品包装完整性良好。
对投诉样品中的药粉进行成分分析,发现成分与标签一致,异物取出后不溶于水,为6mm左右的白色塑料材质异物,初步分析该异物可能是在生产环节中带入。
2.2 原因分析
结合该产品的生产工艺,确认白色异物的成分和带入原因。
抗生素粉针剂产品的生产工艺如图1所示。由于胶塞与抗生素模制瓶都是与药品直接接触的包装材料,且产品分装岗位是高污染风险岗位,因此在产品中带入上述塑料材质异物的环节和岗位可能是玻璃瓶的清洗灭菌、胶塞的清洗灭菌和分装岗位。
2.2.1 抗生素瓶的清洗灭菌
抗生素瓶拆除内层塑料包装袋后推入洗瓶机前端的过渡输送带,经轨道进入超声波洗瓶机;瓶体经超声波预洗后,再用注射用水、洁净压缩空气依次进行“三水三气”的喷淋、清洗、吹干;完成清洗的抗生素瓶再经隧道灭菌烘箱进行灭菌干燥并冷却;最后在RABS保护下出瓶,传入分装机分装岗位。
在日常生产中,洗瓶岗位未出现过设备维修及其他异常情况,洗瓶机运行情况良好,人员和环境亦无类似异物带入,此工序可能带入异物的环节为玻璃瓶内本身带入和拆除塑料包装袋时带入。若是上述两种情况带入异物,且经洗瓶工序未能冲洗去除,经过隧道烘箱高温灭菌干燥后应呈现黄色或黑色的烤焦残留物,与投诉的白色异物不符。因此,可以排除该异物在玻璃瓶清洗灭菌岗位带入的可能性。
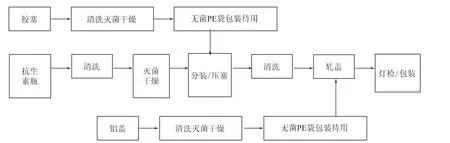
图1 抗生素粉针剂产品的生产工艺流程图
2.2.2 胶塞的清洗灭菌
胶塞拆除内层塑料包装袋后,经真空吸料送入全自动胶塞清洗机内清洗,分别经过纯化水清洗和注射用水清洗后,再经纯蒸汽灭菌与真空干燥。干燥冷却后,在胶塞清洗机出料,在RABS内装入无菌PE袋中,随后进行塑封备用。
在日常生产中,胶塞清洗灭菌工序未出现设备维修及其他异常情况,胶塞清洗机运行情况良好,人员和环境亦无类似异物带入,此工序可能带入异物的环节为胶塞本身带入和拆除塑料包装袋时带入。在胶塞拆包时,需要用剪刀剪开包装胶塞的塑料袋,可能会产生微小的塑料屑,如果塑料屑粘在胶塞上或塞芯内,则在清洗和湿热灭菌过程中可能无法被去除。因此,胶塞清洗灭菌岗位存在带入白色塑料异物的可能性。
2.2.3 分装岗位
在分装岗位中,原料粉经过螺杆分装机完成定容量加粉及压塞的过程。螺杆分装机原理:电机带动主动轮,通过同步带带动抗生素瓶间歇输送,并间接带动下粉连轴器,驱动螺杆旋转,将原料粉定容量加至瓶内,再通过振荡盘与轨道将胶塞定向输送,并在轨道末端释放胶塞,送入压塞机构,完成胶塞的压入。整个过程在RABS中完成。
现分析分装岗位的人、机、料、环四个方面带入异物的可能性。
2.2.3.1 人员
我公司生产的抗生素粉针剂通过螺杆分装机进行分装,原料桶在RABS中开启,通过蝶阀与分装机对接,原料粉经送粉管加入粉斗,通过搅拌后由螺杆和小嘴巴加入抗生素瓶中,压塞后的产品通过传送带进入轧盖间。整个过程的操作人员均不接触原料桶内部,对分装机的必要干预也是通过RABS上的隔离手套进行,且RABS在生产过程中始终处于A级层流的保护下。同时,在分装岗位的操作人员都是经过培训和有资质的人员。综合分析认为,该异物不可能由分装间的人员操作时带入。
2.2.3.2 物料
原料是从合格供应商处采购,原料粉使用药用铝瓶包装,入厂检验均符合法定标准及我公司内控标准。原料粉分装前,车间质量员对每个铝瓶的原料进行可见异物检查,待检查合格后方可进行分装。若异物来自原料药,原料粉是送入加料箱并通过搅拌后由小嘴巴处加入抗生素瓶中,而小嘴巴孔和螺杆都是配套的。以投诉中的异物体积而言,是不可能经过小嘴巴孔加入到抗生素瓶中的。
胶塞经清洗灭菌后,用无菌双层PE袋密封待用,使用前的胶塞在RABS缓冲区拆包,拆包过程中可能会带入塑料材质的异物。但是若由该工序带入塑料异物,应该为暗透明色,这与投诉的白色异物不符。
2.2.3.3 设备、环境
通过查阅分装岗位当天的空调系统及设备发现其运行状况良好,并无异常情况出现,且环境及各设备中均无此类白色塑料材质物品,故该异物不可能由设备、环境中带入。
2.3 模拟验证
图2为被投诉样品(塑料屑)。为进一步确认白色异物是否为塑料袋屑和是否由胶塞清洗灭菌岗位带入,我们进行了模拟实验,将塑料袋屑放置于胶塞内芯中,然后按日常胶塞清洗灭菌程序进行操作,经清洗、灭菌、干燥与冷却后,将放有塑料屑的胶塞取出,发现其塞芯内的塑料屑与被投诉产品中的异物外观上基本相似,如图3所示。因此,认为被投诉产品中的异物是胶塞清洗前的拆包过程中带入的塑料包装屑。

图2 被投诉样品(塑料屑)

图3 验证实验中的塑料屑
3 对策制定与实施
通过上述原因分析可知,此类白色塑料材质异物可能是由于胶塞拆包时,开口处剪的不光滑,导致塑料屑掉进胶塞内。针对此类情况,我们立即进行了试验,确定合适的拆包剪裁方式,确保剪口处光滑。
经过试验,当纵向剪裁的时候,由于胶塞外包装塑料袋的长度较长,无法一刀完成剪裁过程,导致剪口处不光滑;而横向剪裁则能一刀完成剪裁过程,确保剪口处的光滑。因此,立即对相关操作人员进行培训,统一胶塞拆包的剪裁方式,并加强抽查力度。
同时,对分装间灭菌待用的胶塞和轧盖间灭菌待用的铝盖PE袋拆除方式进行了规定。
4 结语
本文以某抗生素粉针剂产品的质量投诉为例,通过调查分析产品的生产工艺流程,确认引起质量投诉的原因,制定相应的对策,并跟踪确认对策的实施效果,同时需要关注同批次产品的质量和使用情况。
若引起质量缺陷的原因并非偶然,且经评估确实影响产品质量或使用的,因予以召回,确保临床用药的安全。
