FOLFIRINOX方案在Ⅳ期胰腺癌治疗中与吉西他滨联合卡培他滨方案的对比研究
2018-02-24陈泽勉苏国钿赵楚英
陈泽勉 苏国钿 赵楚英
【摘要】 目的:探讨FOLFIRINOX方案治疗Ⅳ期胰腺癌与吉西他滨联合卡培他滨方案的效果差异。
方法:选取本院病理学确诊的Ⅳ期胰腺癌患者68例,收集时间2016年5月-2018年5月,其中34例患者接受FOLFIRINOX方案治疗(A组)、34例患者接受吉西他滨联合卡培他滨方案治疗(B组),对比两组患者的临床疗效、预后及毒副反应。结果:A组患者PR 68.75%、SD 25.00%、PD 6.25%,B组患者PR 41.18%、SD 44.12%、PD 14.71%,两组比较差有统计学意义(P<0.05);A组患者白细胞减少、恶心呕吐发生程度显著高于B组患者,两组比较差异均有统计学意义(P<0.05);A组患者6、12个月生存率与B组比较差异均无统计学意义(P>0.05);A组患者的PFS时间9.0个月长于B组患者的7.0个月(P<0.05),A组患者的OS时间10.0个月长于B组患者的8.0个月(P<0.05)。结论:FOLFIRINOX方案治疗Ⅳ期胰腺癌的效果优于吉西他滨联合卡培他滨方案,但是毒副反应发生率相对较高,为一般状况良好Ⅳ期胰腺癌患者的较好选择。
【关键词】 FOLFIRINOX方案; 胰腺癌; 吉西他滨; 卡培他滨
胰腺癌属于临床严重的消化系统恶性肿瘤之一,预后较差,2年生存率不到20%,5年生存率低于6%,近年来本病发病率和死亡率逐年升高,目前手术切除是效果较好的治疗手段,但是仅有15%左右患者在确诊时有手术机会,大部分患者就诊时已属于晚期,只能选择化学治疗方案抑制肿瘤进展[1]。研究显示FOLFIRINOX方案最初用于转移性胰腺癌系统化疗中,其同吉西他滨加卡培他滨经典化疗方案比较可以显著改善转移性胰腺癌中位生存期,但是由于受到样本量限制对该方案的安全性和有效性均未能得出一致性结论,因此该方案在应用中受到了一定的限制[2]。为了观察FOLFIRINOX方案应用在Ⅳ期胰腺癌患者中的治疗效果及安全性,本院将其同吉西他滨联合卡培他滨方案做了对比,现汇报如下。
1 资料与方法
1.1 一般资料 选取本院病理学确诊的Ⅳ期胰腺癌患者68例,收集时间2016年5月-2018年5月,其中34例患者接受FOLFIRINOX方案治疗(A组),34例患者接受吉西他滨联合卡培他滨方案治疗(B组)。纳入标准:(1)病理组织学确诊胰腺癌;(2)上腹部、胸部增强CT等检查临床分期确定为Ⅳ期患者,具有影像学可测量的实体病灶;(3)ECOG评分:0~1分,KPS评分≥70分;(4)年龄18~79岁;(5)肝、肾、骨髓功能正常[白细胞数>4000/dL,血小板数>
10万/dL,丙氨酸转氨酶(ALT)<两倍正常值,总胆红素<1.5 mg/dL,血肌酐(Cr)<1.5倍正常值];(6)患者知情同意。排除标准:(1)伴有严重感染、肝肾功能疾病;(2)既往具有放化疗治疗史;(3)对化疗药物具有严重的不耐受性,中途退出研究。
1.2 方法 A组给予FOLFIRINOX方案:奥沙利铂(湖北一半天制药有限公司生产,药品批准文号:国药准字H20143170,规格:50 mg)85 mg/m2体表面积,伊立替康(上海创诺制药有限公司生产,药品批准文号:国药准字H20153067,规格:5 mL︰0.1 g)180 mg/m2体表面积,亚叶酸钙(开封康诺药业有限公司生产,药品批准文号:国药准字H41021710,规格:25 mg)400 mg/m2;氟尿嘧啶(上海通用药业股份有限公司生产,药品批准文号:国药准字H31021277,规格:4 g︰0.1 g)400 mg/m2,静脉推注,此后以2 400 mg/m2持续输注46 h,每两周一次,上述治疗直到疾病进展或出现严重不良反应。B组采取吉西他滨(哈尔滨誉衡药业股份有限公司生产,药品批准文号:国药准字H20040958,规格:0.2 g)+卡培他滨(上海罗氏制药有限公司生产,药品批准文号:国药准字H20073024,规格:0.5 g×12片)联合化疗,吉西他滨1000 mg/m2 d1、d8、d15,卡培他滨2500 mg/(m2·d)分两次服用,连服14 d,28 d为1个周期,上述治疗直到疾病进展或出现严重不良反应。
1.3 观察指标与疗效判断标准 依据RECIST实体瘤疗效评价标准,化疗结束后的患者根据病灶变化分为:完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD)。CR:可见病灶完全消失,维持一个月以上;PR:肿瘤最大直径及最大垂直直径的乘积缩小达到50%以上;SD:肿瘤最大直径及最大垂直直径的乘积缩小<50%,增大<25%;PD:患者出现一个多个病灶的肿瘤最大直径及最大垂直直径的乘积>25%。缓解患者为CR+PR,有效患者为CR+PR+SD。觀察两组患者的无进展生存时间(PFS)、总生存时间(OS)。毒副反应参照WHO毒副反应5级分级标准:0度:无毒副作用;Ⅰ度:轻度反应;Ⅱ度:中度毒副反应;Ⅲ度:毒副反应重度;Ⅳ度:有严重的并发症。
1.4 统计学处理 统计软件采用SPSS 16.0进行分析,计量资料采用(x±s)表示,比较采用t检验,计数资料采用率(%)表示,组间比较采用字2检验,生存分析采用Kaplan-meier法,以P<0.05为差异有统计学意义。
2 结果
2.1 两组基线资料比较 A组中男21例,女13例;年龄46~78岁,平均(59.4±10.5)岁;肿瘤部位:胰头部17例,胰腺体尾部17例;发生肝转移26例,淋巴结转移18例;中途退出研究2例。B组中男19例,女15例;年龄43~79岁,平均(61.0±12.4)岁;肿瘤部位:胰头部20例,胰腺体尾部14例;发生肝转移28例,淋巴结转移20例;中途无患者退出。两组患者的年龄、性别、肿瘤部位、肝转移、淋巴结转移情况比较,差异均无统计学意义(P>0.05)。
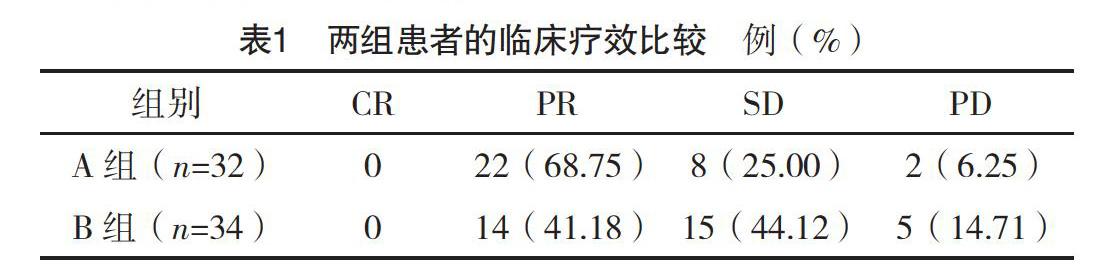
2.2 两组患者的临床疗效比较 A组患者临床疗效优于B组,两组比较差异有统计学意义(Z=-2.231,P=0.026<0.05),见表1。
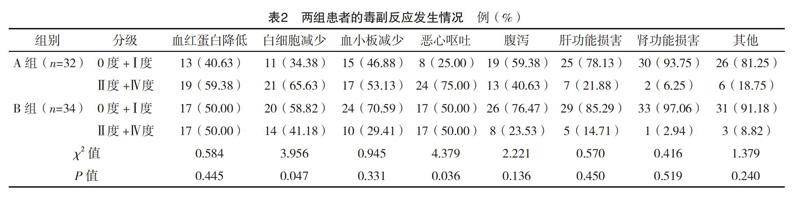
2.3 两组患者的毒副反应发生情况比较 A组患者白细胞减少、恶心呕吐发生程度显著高于B组患者,两组比较差异均有统计学意义(P<0.05)。两组患者血红蛋白降低、血小板减少、肝肾功能损害、腹泻及其他类型的毒副反应发生率比较,差异均无统计学意义(P>0.05),见表2。
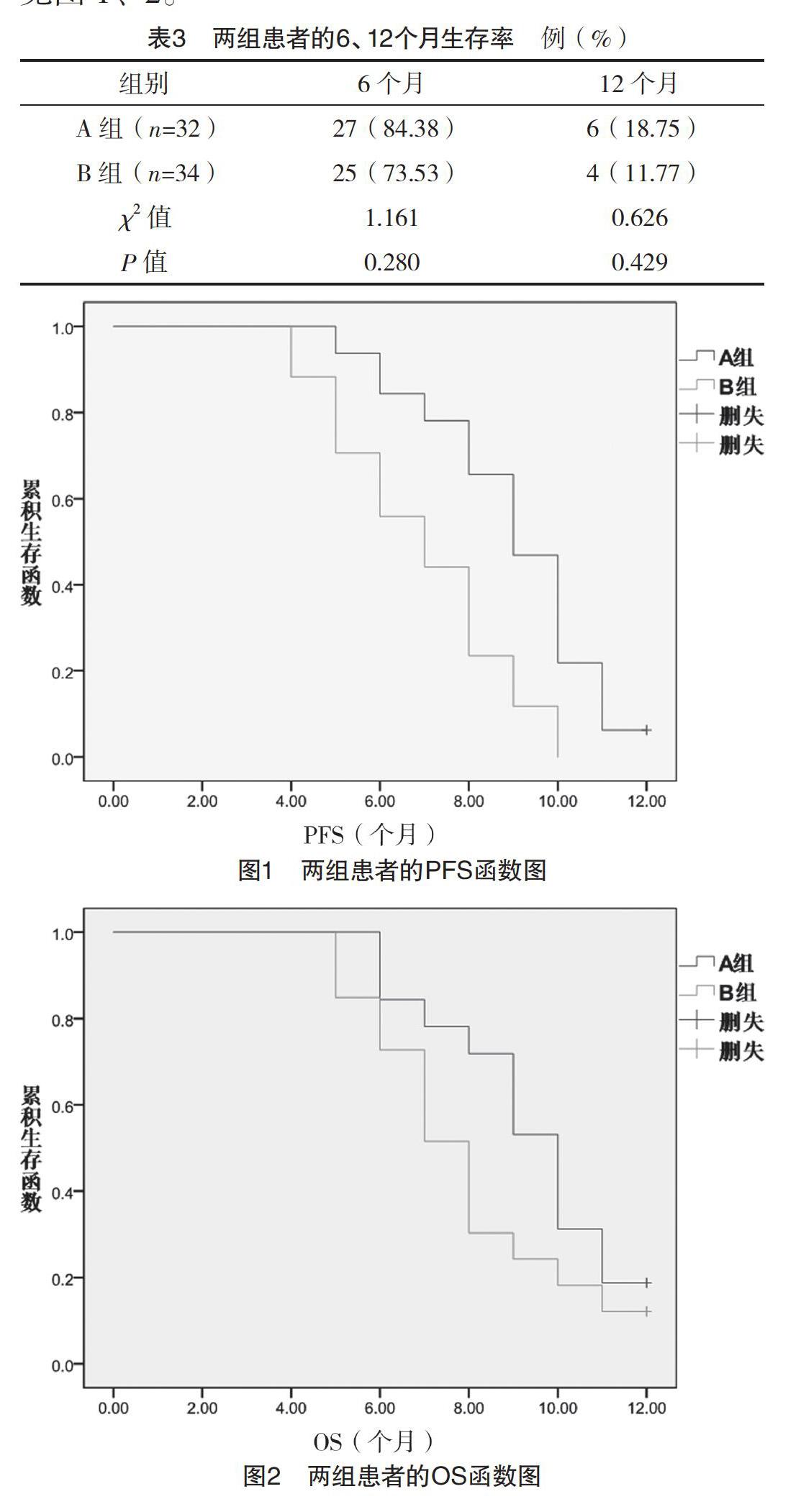
2.4 两组患者的预后情况比较 A组患者6、12个月生存率与B组比较,差异均无统计学意义(P>0.05),见表3。A组患者的PFS时间9.0个月长于B组患者的7.0个月(P<0.05),A组患者的OS时间10.0个月长于B组患者的8.0个月(P<0.05),见图1、2。
3 讨论
胰腺癌属于临床恶性程度较高的恶性肿瘤,具有病程短、进展快、死亡率高的特点,發病率占到所有恶性肿瘤1%~2%,由于其恶性程度高,病情进展快,死亡率呈现升高趋势,已经成为常见恶性肿瘤死亡原因之一,有研究称胰腺癌在初次确诊后一年死亡率高达80%,三年死亡率在95%,严重威胁患者生命安全[3-4]。目前胰腺癌主要采取手术切除方法,但是由于起病隐匿早期难以发现,多数患者就诊时已处于晚期,无法切除,根治性手术切除率仅不到20%,但容易出现肝转移和局部复发,因此采取内科治疗特别是化疗成为重要的治疗方法[5-6]。吉西他滨一直是进展期胰腺癌一线化疗的金标准药物,但是疗效远不能让人满意,随着新药的研发,近年来吉西他滨联合卡培他滨治疗的联合用药方案在临床广泛应用,卡培他滨属于口服的5-FU,可以选择性在肿瘤组织内提高浓度5-FU,提升疗效降低毒性,而且具有很好的耐受性,两者联合用药其剂量限制性毒性不存在交叉,吉西他滨剂量限制小毒性为骨髓毒性,卡培他滨则是胃肠道毒性与手足综合征,两种药物的联合用药既可以提升临床疗效,同时又不会加重不良反应程度,但是其在提升患者生存期方面仍然具有一定的局限性[7]。在过去的数十年胰腺癌患者长期存活率一直没有明显提升,患者中位生存期仅为2~3个月,而不断涌现的新化疗方案也为患者带来了一线希望,FOLFIRINOX方案的出现在部分研究中显示可以将晚期胰腺癌患者中位生存时间提高到11.1个月,还有个别病例伴有肝转移的患者经过此方案化疗后实现R0切除的报道。但是不可否认FOLFIRINOX方案副作用较大,患者耐受性较差,因此是否需要对方案进行调整以及如何控制毒副反应均是需要解决的问题[8-9]。
转移性胰腺癌胰腺治疗方案选择主要考虑患者身体状况,NCCN指南中将胰腺癌体能状态良好定义为ECOG评分在0~1分、疼痛控制良好、胆道支架通畅和营养摄入良好4个方面,因此在治疗中可以从上述四个方面入手增强患者耐受能力,有助于更好地接受FOLFIRINOX方案治疗[10-11]。此外在治疗期间因密切关注患者不良反应发生情况,及时处理毒副反应确保方案能够正常顺利开展。FOLFIRINOX方案中奥沙利铂属于新的铂类抗癌药,其中铂原子与1,2二氨环己烷(DACH)及一个草酸基结合,在体内和体外研究中奥沙利铂可以和5-氟尿嘧啶联合应用发挥协同细胞毒作用,已有研究表明,奥沙利铂通过产生水化衍生物作用于DNA,形成链内和链间交联,从而抑制DNA的合成,产生细胞毒作用和抗肿瘤活性[12-13]。伊立替康则是喜树碱的半合成衍生物,喜树碱可特异性地与拓扑异构酶Ⅰ结合,后者诱导可逆性单链断裂,从而使DNA双链结构解旋,伊立替康及其活性代谢物SN-38可与拓扑异构酶Ⅰ-DNA复合物结合,从而阻止断裂单链的再连接[14-15]。亚叶酸钙属于四氢叶酸的甲酰衍生物,主要用于高剂量甲氨蝶呤等叶酸拮抗剂的解救,同二氢叶酸还原酶结合,阻断二氢叶酸转变为四氢叶酸,从而抑制DNA的合成[16-17]。5-氟尿嘧啶是尿嘧啶的同类物,尿嘧啶是核糖核酸的一个组分,在细胞内转化为有效的氟尿嘧啶脱氧核苷酸后,通过阻断脱氧核糖尿苷酸受细胞内胸苷酸合成酶转化为胸苷酸,从而干扰DNA的合成[18-20]。
本研究显示,A组患者PR 68.75%、SD 25.00%、PD 6.25%,B组患者PR 41.18%、SD 44.12%、PD 14.71%,两组比较差异有统计学意义(P<0.05),说明FOLFIRINOX方案治疗Ⅳ期胰腺癌优于吉西他滨联合卡培他滨方案。在化疗副作用方面研究显示,A组患者白细胞减少、恶心呕吐发生程度显著高于B组患者,两组比较差异均有统计学意义(P<0.05),说明FOLFIRINOX方案治疗Ⅳ期胰腺癌可以增加白细胞减少和恶心呕吐不良反应发生率。A组患者6、12个月生存率与B组比较差异均无统计学意义(P>0.05),说明FOLFIRINOX方案对患者生存率影响不大。但在患者生存时间和无进展生存时间方面比较,A组患者的PFS时间9.0个月长于B组患者的7.0个月(P<0.05),A组患者的OS时间10.0个月长于B组患者的8.0个月(P<0.05),说明FOLFIRINOX方案在延长患者生存时间和无进展生存时间方面优于吉西他滨联合卡培他滨方案。本研究优势在于证实了FOLFIRINOX方案应用在胰腺癌晚期治疗中的效果,虽然副作用方面FOLFIRINOX更大,但是临床通过合理选择治疗患者,在一般状况较好的Ⅳ期患者中用效果更为显著;但是本研究受到时间、病例数等限制未能开展大样本量、随机对照研究,还有待以后深入分析。
综上所述,FOLFIRINOX方案治疗Ⅳ期胰腺癌的效果优于吉西他滨联合卡培他滨方案,但毒副反应发生率较高,临床上一般状况较好的Ⅳ期胰腺癌病例,FOLFIRINOX方案可列为其化疗方案的较好选择。
参考文献
[1]胡丹旦,戴梦华.胰腺癌新辅助治疗和转化治疗的研究进展[J].中华外科杂志,2017,55(1):69-72.
[2] Sudo K,Ishihara T,Hirata N,et al.Randomized controlled study of gemcitabine plus S-1 combination chemotherapy versus gemcitabine for unresectable pancreatic cancer[J].Cancer Chemother Pharmacol,2014,73(1):389-396.
[3] Agrawal A,Purandare N,Shah S,et al.Response assessment in metronomic chemotherapy: RECIST or PERCIST[J].IJNM,2014,29(1):74-80.
[4] Ke Q H,Zhou S Q,Yang J Y,et al.S-1 plus gemcitabine chemotherapy followed by concurrent radiotherapy and maintenance therapy with S-1 for unresectable pancreatic cancer[J].World J Gastroenterol,2014,20(1):13987-13992.
[5]李小明,胡愛虹,张帆.吉西他滨联合替吉奥治疗晚期转移性胰腺癌的临床疗效和安全性评价[J].中国临床药理学杂志,2015,31(1):261-263.
[6]慕春红,吕邦策,马平安.FOLFIRINOX为基础的新辅助化疗后局部进展期胰腺癌的手术疗效分析[J].中国普通外科杂志,2017,26(3):281-288.
[7]白雪莉,苏日嘎,马涛,等.改良FOLFIRINOX方案治疗进展期胰腺癌单中心经验[J].中华外科杂志,2016,54(4):270-275.
[8] Ky V,Hav M,Berrevoet F,et al.Cisplatin-modified de gramont in second-line therapy for pancreatic adenocarcinoma[J].Pancreas,2013,42(7):1138-1142.
[9] Blazer M,Wu C,Goldberg R M,et al.Neoadjuvant Modi-fied (m) FOLFIRINOX for Locally Advanced Unresectable (LAPC) and Borderline Resectable (BRPC) Adenocarcinoma of the Pancreas[J].Ann Surg Oncol,2015,22(4):1153-1159.
[10] Papadatos-Pastos D,Thillai K,Rabbie R,et al.
FOLFIRINOX-a new paradigm in the treatment of pancreatic cancer[J].Expert Rev Anticancer Ther,2014,14(10):1115-1125.
[11] Teague A,Lim K H,Wanggillam A.Advanced pancreatic adenocarcinoma: a review of current treatment strategies and developing therapies[J].Therapeutic Advances in Medical Oncology,2015,7(2):68-84.
[12]2Nd M R,Kwon D,Chalikonda S,et al.Treatment of 200 locally advanced (stage Ⅲ) pancreatic adenocarcinoma patients with irreversible electroporation: safety and efficacy[J].Annals of Surgery,2015,262(3):486.
[13] Yue Z,Lu Z,Ischenko I,et al.Antisense inhibition of microRNA-21 and microRNA-221 in tumor-initiating stem-like cells modulates tumorigenesis, metastasis, and chemotherapy resistance in pancreatic cancer[J].Targeted Oncology,2015,10(4):535-548.
[14] Ghorani E,Wong H H,Hewitt C,et al.Safety and Efficacy of Modified FOLFIRINOX for Advanced Pancreatic Adenocarcinoma:A UK Single-Centre Experience[J].Oncology,2015,89(5):281.
[15] Rombouts S J,Mungroop T H,Heilmann M N,et al.
FOLFIRINOX in Locally Advanced and Metastatic Pancreatic Cancer: A Single Centre Cohort Study[J].Journal of Cancer,2016,7(13):1861-1866.
[16]程月鹃,孟长婷,邵亚娟,等.吉西他滨联合替吉奥治疗晚期胰腺癌的疗效分析[J].中国医学科学院学报,2017,39(4):562-567.
[17]王威巍,李靖,张宇,等.吉西他滨为基础的化疗方案治疗进展期胰腺癌的临床疗效分析[J].北京医学,2017,39(4):360-363.
[18]尹显飞.吉西他滨联合替吉奥一线治疗晚期胰腺癌疗效及安全性评价[J].中国全科医学,2017,20(S2):81-82.
[19]卓萌,崔玖洁,王理伟.胰腺癌化疗方案的选择及疗效评价[J].临床肝胆病杂志,2017,33(1):53-56.
[20]王天朋,刘枭荣,陈飞,等.RRMl、hENT1的表达与胰腺癌吉西他滨化疗疗效相关性研究进展[J].肝胆胰外科杂志,2018,30(1):84-86.
(收稿日期:2018-08-18) (本文编辑:周亚杰)
