利用碱酶耦合法预处理竹粉制备羧甲基纤维素钠
2017-12-18,,,,,
,,,,,
(浙江树人大学生物与环境工程学院,浙江杭州 310015)

唐霞,叶杭钰,陈嘉诚,刘家辉,蔡王芝,陈蔚青*
(浙江树人大学生物与环境工程学院,浙江杭州 310015)
以竹粉为原料,经碱-纤维素酶耦合法预处理,提取纤维素,制备羧甲基纤维素钠。碱液-纤维素酶耦合处理的工艺为:竹粉4 g,5% NaOH 40 mL,碱解温度为50 ℃,时间1 h,减压过滤后加入400 U/mL酶液30 mL,酶的最适pH为5.5,酶解温度为49 ℃,时间30 min。经该工艺处理,竹粉中的α-纤维素含量达84.1%,以此为原料制备的CMC 2%浓度水溶液粘度值达162 mPa·s,取代度为0.95,红外光谱检测显示产物具有羧甲基特征峰,扫描电镜检测显示产物具有盐的特征。本研究在原料预处理上采用生物-化学耦合方法,对环境污染少,成本相对较低,促进了绿色经济的发展,也为制备羧甲基纤维素钠提供了新的途径。
羧甲基纤维素钠,竹粉,纤维素,碱-酶耦合,制备
羧甲基纤维素钠(Sodium carboxymethyl cellulose,CMC)是天然纤维素经改性后的衍生物,为离子型、直链、水溶性的羧甲基纤维素醚的钠盐,是种类繁多、应用领域宽广、生产量大、研究价值高的一种纤维素衍生产品。由于其具有优异的性能和广泛的用途,CMC被誉为“工业味精”[1-3]。CMC目前已广泛应用于造纸工业、油田开采、食品工业、医药工业、日用化工、陶瓷制造、纺织工业等各经济领域[4-9]。在食品加工业中,主要作为增稠剂、成膜剂、稳定剂、固化剂及增量剂等[10-13]。
制备羧甲基纤维素钠主要以精制棉短绒、木材浆粕等为原料,其原料成本较高,来源较少,而市场上对CMC的需求量越来越大,所以开发其他资源丰富、来源广泛、廉价的纤维素原料,便成为当下的一种趋势[14]。竹制品加工副产物(如竹屑、竹刨花等)是一种具有较高研究价值和和应用前景的原材料,其纤维素含量达45%~52%[15]。竹子中的纤维素和半纤维素、木质素组成木质纤维素,其中半纤维素与木质素共价结合形成木质素-碳水化合物结构,再将纤维素包裹,三者结合牢固,难以完全分离,此外,还含有果胶、蛋白质、灰分等成分[15-16]。
目前,分离木质纤维素中纤维素的基本方法有酸水解与碱处理等方式的化学法[6]、汽爆法[17]、热-机械耦合开纤法[18]等物理方法,以及酶催化水解、微生物发酵等生物处理法[19]。采用单一化学或物理法,虽然效率较高,但随之产生设备腐蚀、环境污染、纤维素降解或者高能耗、高成本等问题,不利于可持续发展。以复合型纤维素酶催化反应为主的生物处理法条件温和、节能环保,但存在预处理周期长、效率低等问题。本研究先将样品经化学法初步处理,再通过酶法,将木质纤维素中的包裹纤维素的木质素和半纤维素等物质有效分离去除,最后用提纯后的预处理产物制备羧甲基纤维素钠。
1 材料与方法
1.1 材料与仪器
竹粉 安吉某竹制品加工厂,碎屑状,经水洗、烘干、粉碎,60目过筛备用,经检测其α-纤维素含量为65.8%(干重);绿色木霉产纤维素酶(酶活≥400 U/mg) 上海瑞永生物科技有限公司;市售食品级CMC(纯度≥99%) 杭州三和食品科技有限公司;其他试剂均为分析纯。
NDJ-5S数字粘度计 上海精晖仪器设备有限公司;恒温水浴振荡器 上海智城分析仪器制造有限公司;FW100型高速万能粉碎机 天津市泰斯特仪器有限公司;Bruker T27型红外光谱仪 德国BRUKER光谱仪器公司;TM-1000扫描电子显微镜 日本日立公司;紫外可见分光光度计 上海仪电分析仪器有限公司;DC-2006低温恒温槽 宁波天恒仪器厂;DGX-9143B-1电热恒温鼓风干燥箱 上海福玛实验设备有限公司;BS-6WL电子天平 赛多利斯科学仪器(北京)有限公司。
1.2 实验方法
1.2.1 纤维素酶最适作用条件的确定
1.2.1.1 纤维素酶对CMC的水解 取4支比色管各加入6 mL 1% CMC溶液,1号比色管加2 mL蒸馏水,其他三支比色管各加入2 mL 以缓冲液配制在一定的pH下的400 U/mL纤维素酶溶液。在一定温度下恒温水浴30 min。取出,向各管分别加入2 mL DNS试剂,沸水浴8 min,迅速冷却至室温,用蒸馏水定容至10 mL,以1号比色管试液作为对照,在530 nm波长条件下测量2~4号比色管试液的吸光度[20]。
1.2.1.2 纤维素酶酶促反应最适温度的确定 取7组比色管,每组4支,编为1~4号,向各组比色管加入6 mL 1% CMC溶液,再向1号比色管加入2 mL蒸馏水,其他三支比色管各加入2 mL 以无菌水配制的400 U/mL纤维素酶溶液,调节各组pH为5.5,分别在37、41、45、49、53、57、61 ℃下恒温水浴30 min。取出,向各管分别加入2 mL DNS试剂,沸水浴8 min,迅速冷却至室温,用蒸馏水定容至10 mL,以1号比色管试液作为对照,在530 nm波长条件下测量2~4号比色管试液的吸光度。
1.2.1.3 纤维素酶酶促反应最适pH的确定 取5组比色管,每组2支,编为1~2号,向各组比色管加入6 mL 1% CMC溶液,再向1号比色管加入2 mL蒸馏水,另一支比色管加入2 mL 以HAc-NaAc缓冲液配制在一定的pH下的400 U/mL纤维素酶溶液。各组HAc-NaAc缓冲液pH分别为4、4.5、5、5.5、6。在49 ℃下恒温水浴30 min。取出,向各管分别加入2 mL DNS试剂,沸水浴8 min,迅速冷却至室温,用蒸馏水定容至10 mL,以1号比色管试液作为对照,在530 nm波长条件下测量2号比色管试液的吸光度。以NaH2PO4-Na2HPO4缓冲液配成pH为5.8、6.3、6.8、7.3、7.8的400 U/mL纤维素酶溶液,重复上述步骤。以Tris-HCl缓冲液配成pH为7.2、7.6、8、8.4、8.8的400 U/mL纤维素酶溶液,重复上述步骤。
以上实验均重复三次。
1.2.2 竹粉预处理 水煮法/弱酸法/碱液法:称取4 g竹粉3份,分别加入40 mL 蒸馏水/0.1 mol/L盐酸溶液/5% NaOH溶液,置于恒温水浴振荡器中,50 ℃反应1 h后迅速冷却,减压过滤,用400 mL蒸馏水分次洗涤试样,将滤渣放入135 ℃电热恒温鼓风干燥箱中烘干3 h 。将烘干后的产物放入密封袋避光储存。
酶解法:称取4 g竹粉,加入40 mL 400 U/mL纤维素酶溶液,pH5.5,置于恒温水浴振荡器中,49 ℃反应30 min后迅速冷却,减压过滤,用400 mL蒸馏水分次洗涤试样,取滤渣于135 ℃电热恒温鼓风干燥箱中烘干3 h。将烘干后的产物放入密封袋避光储存[21]。
弱酸-酶解耦合法/水煮-酶解耦合法/碱液-酶解耦合法:称取4 g竹粉3份,分别加入40 mL 0.1 mol/L盐酸溶液/蒸馏水/5% NaOH溶液,置于恒温水浴振荡器中,50 ℃反应1 h后迅速冷却,减压过滤,用400 mL蒸馏水分次洗涤试样,取滤渣,加入30 mL 400 U/mL纤维素酶溶液,调节pH为5.5,置于恒温水浴振荡器中,49 ℃反应30 min后减压过滤,取滤渣于135 ℃电热恒温鼓风干燥箱中烘干3 h,将烘干后的产物放入密封袋避光储存[22]。
以上实验均重复三次。
1.2.3 羧甲基纤维素钠的制备 取40 mL 95%乙醇和4.4 mL 35% NaOH溶液,充分搅拌混合,加入2 g预处理产物,于30 ℃、130 r/min恒温水浴振荡器中反应6 h。在搅拌状态下,加入75%氯乙酸乙醇溶液5.84 mL。55 ℃醚化反应90 min后取出,放入恒温水浴锅中70 ℃保温10 min,再置于50 ℃、180 r/min恒温水浴振荡器中30 min后取出,用31%冰醋酸调pH至中性,减压过滤,75%乙醇洗涤2次,105 ℃电热恒温鼓风干燥箱烘干5 h。将烘干后的产物放入密封袋避光储存[23-24]。
1.2.4α-纤维素含量测定 取30 mL 17.5%氢氧化钠加入瓷杯中,称取2.00 g竹粉等待测样品放入瓷杯中,搅拌均匀,盖上盖子;放置30 min,每隔10 min搅拌一次,每次搅拌约1 min,30 min后,加入30 mL蒸馏水,搅拌,减压过滤,再将滤渣多次洗涤。加30 mL体积分数为10%的冰乙酸溶液浸泡5 min,减压过滤,并用热蒸馏水洗涤至中性;将洗净的滤渣置135 ℃电热恒温鼓风干燥箱中3 h。将烘干后的产物放入密封袋避光储存[15]。
1.2.5 CMC产物粘度和pH测定 称取2 g CMC产物,加入98 mL蒸馏水,用磁力搅拌机搅拌2.5 h,减压过滤,取滤渣,烘干,得到杂质质量M1,根据纯度比例,按所需2 g 纯CMC称取M2CMC产物,加入98 mL蒸馏水,用磁力搅拌机搅拌2.5 h,在25 ℃下,测粘度[15]和pH。
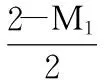
式中:W为CMC产物中纯CMC的含量(%);M1为CMC产物中未溶杂质的质量(g);M2为CMC产物的质量(g)。
1.2.6 CMC产物取代度和产率测定 利用灰碱法测定取代度[15]。产率计算方法为:
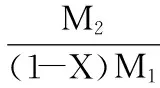
式中:W为CMC产物产率(%);M1为竹粉质量(g);X为竹粉的水分含量(%);M2为预处理产物质量(g);M3为制备CMC时投入的预处理产物质量(g);M4为CMC产物质量(g)。
1.2.7 CMC产物的鉴定 利用红外光谱中羧甲基纤维素钠的特征峰来确定[25]。

表1 碱-酶耦合处理所得CMC产物指标检测Table 1 Evaluation index of CMC product obtained by the alkali-cellulase coupling method
红外光谱检测:将溴化钾和待测样品混合,碾磨,烘干。5 min后,取出,制压片,放入红外光谱仪检测。
1.2.8 扫描电子显微镜检测 所测样品喷金粉进行导电处理,使用TM-1000扫描电子显微镜进行检测[26]。
1.3 数据处理
采用Excel软件计算并绘图,采用IBM SPSS Statistics 21软件进行方差分析,红外光谱图采用Origin Pro 2017软件绘图。
2 结果与分析
2.1 纤维素酶的最适作用条件
由图1可见,当温度低于49 ℃时,纤维素酶活性随温度的升高而增加;当温度高于49 ℃时,纤维素酶活性随温度的降低而减小;当以HAc-NaAc溶液作缓冲液,pH为5.5时,纤维素酶活性最大,且pH为5时,纤维素酶仍保持较大活性。绿色木霉来源的纤维素酶最适作用温度为49 ℃,pH为5.5。
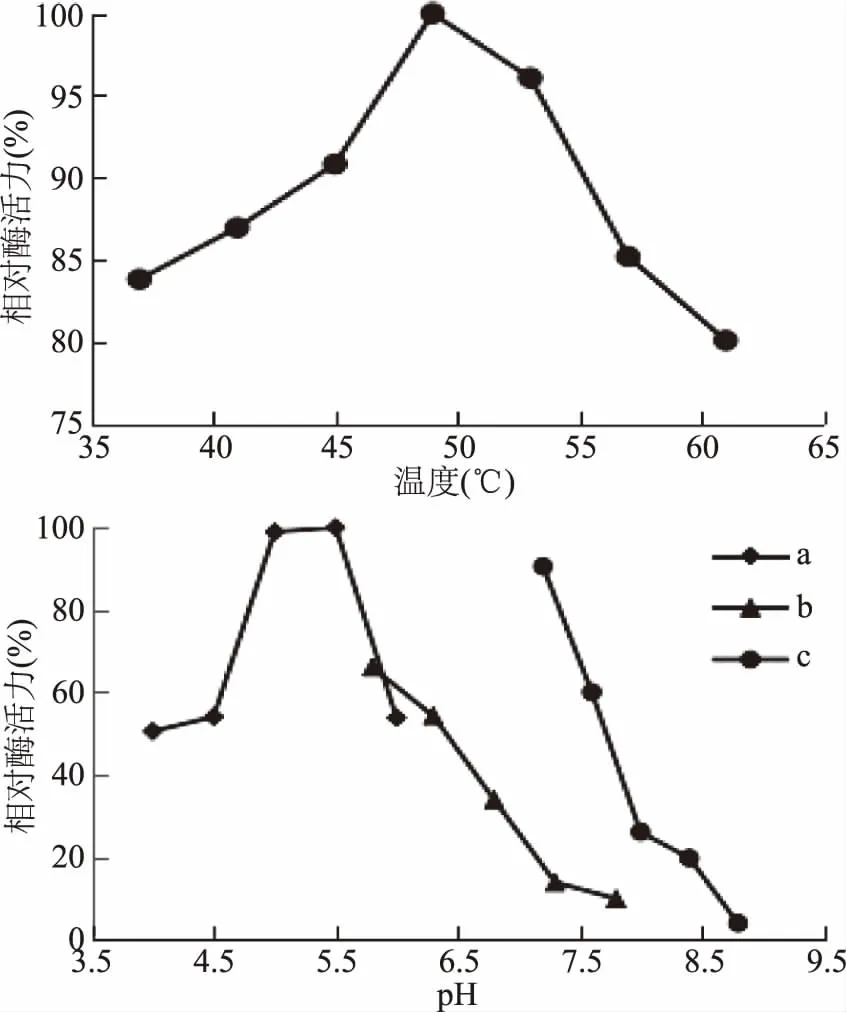
图1 温度、pH对纤维素酶活的影响Fig.1 Effect of temperature and pH on cellulase activity注:a:HAc-NaAc缓冲液;b:NaH2PO4-Na2HPO4缓冲液;c:Tris-HCl缓冲液。
2.2 竹粉预处理后α-纤维素含量的比较
以α-纤维素含量作为评判标准,由图2可知,各种预处理方法获得产物的α-纤维素含量均≥70%,水煮法、酶解法、弱酸法、碱液法、弱酸-酶解耦合法、水煮-酶解耦合法、碱液-酶解耦合法所得α-纤维素含量分别为73.6%±0.3%、74.2%±1.8%、73.8%±0.1%、78.7%±1.1%、74.7%±0.9%、75.6%±0.6%、84.1%±3.2%。其中碱液-酶解耦合处理法所得到产物的α-纤维素含量与碱液法所得α-纤维素含量差异不显著(p>0.05),与其他方法所得α-纤维素含量差异显著(p<0.05),并且,碱液-酶解耦合处理法所得到产物的α-纤维素含量高于碱液法所得α-纤维素含量。
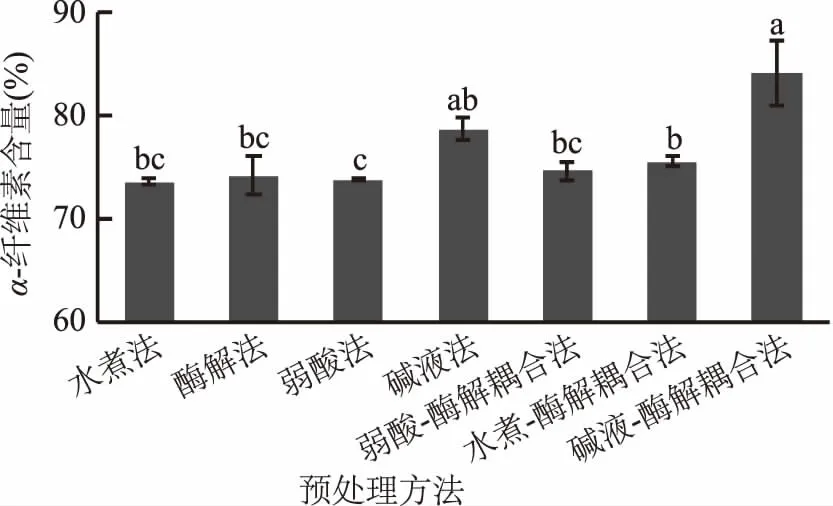
图2 竹粉经不同预处理方法后得到的α-纤维素含量的比较Fig.2 Comparision of α-cellulose content of bamboo powder after different pretreatment methods注:不同字母表示差异显著(p<0.05)。
2.3 CMC质量评价
经碱液-纤维素酶耦合法处理后的竹粉为原料所制备的CMC产物取代度相对较高,为0.95,产率仅有66.19%,仍有较大的优化空间;其2%水溶液在25 ℃下的粘度达到162 mPa·s,pH为7.2。
2.4 红外光谱(FTIR)分析
竹粉碱-酶耦合法预处理前后样品、CMC产物及标准品市售食品级CMC的红外光图谱如图3所示。CMC产物是经碱液-酶解耦合法预处理后的竹粉所制得的。据文献[27]报道,羧甲基纤维素钠分别在1423 cm-1和1620 cm-1处具有特征峰。所制备的CMC产物中能找到羧甲基特征峰的归属,符合此特征。可以得出,所制备产物符合CMC产品特性。
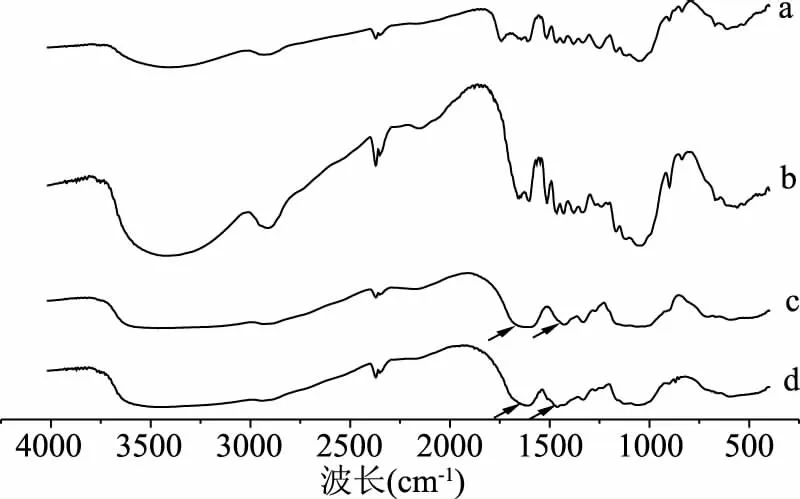
图3 预处理前后竹粉、CMC产物、市售食品级CMC的红外光谱图Fig.3 FT-IR spectra of bamboo powder before and after pretreatment,CMC product,food grade CMC in market注:a:竹粉;b:预处理后竹粉;c:产物CMC;d:市售食品级CMC。
2.5 扫描电镜(SEM)分析
竹粉预处理前后样品和产物CMC的电镜扫描如图4所示。产物CMC是经碱液-酶解耦合法预处理后的竹粉所制得的。从图4可以看出,竹粉的纤维成束,表面光滑,结构致密。经酶解法或碱解法预处理后,纤维素分成小束,其结构松散,而碱解-酶解耦合法得到的纤维素结构更加松散,有利于下一步的处理。CMC的表面被破坏,结构变得更加松散,并显示出盐的特征[28]。

图4 竹粉预处理前后及CMC产物的电镜扫描图Fig.4 Scanning electron micrographs of bamboo powder before and after pretreatment and CMC product注:a:竹粉(1000×),b:碱解后的竹粉(500×),c:酶解后的竹粉(1000×),d:碱解-酶解处理后的竹粉(1000×),e:产物CMC(1200×)。
3 结论
以竹制品副产物的竹粉为原料,经过与5% NaOH反应,再酶解后,得到了结构较松散的α-纤维素,以α-纤维素为原料制备了羧甲基纤维素钠。经过实验,纤维素酶的最适温度为49 ℃,pH为5.5。碱液-酶解耦合法所得预处理产物α-纤维素含量显著高于除碱液法的其他方法所得α-纤维素含量(p<0.05),且含量最高。经碱-纤维素酶耦合处理法预处理后所制得的CMC产物,取代度为0.95,产率为66.19%,其2%的水溶液在 25 ℃ 下的粘度可达到 162 mPa·s,技术指标符合中低粘度CMC的产品要求。本研究在原料预处理上采用生物-化学耦合方法,对环境污染少,成本相对较低,促进了绿色经济的发展,也为制备羧甲基纤维素钠提供新的途径。在后续研究中,可以继续优化CMC制备条件,提高产品粘度,使其适应工业化生产;此外,可以研究在预处理的废液中回收半纤维素和木质素的技术方法,以进一步提高资源的利用率。
[1]张光华,朱军峰,徐晓凤. 纤维素醚的特点、制备及在工业中的应用[J]. 纤维素科学与技术,2006(4):60-65.
[2]刘 鎏,张美云,申前锋. 羧甲基纤维素的合成及其在造纸中的应用[J]. 西南造纸,2005,34(4):50-52.
[3]Cheng L H,Karim A A,Seow C C. Characterisation of composite films made of konjac glucomannan(KGM),carboxymethyl cellulose(CMC)and lipid[J]. Food Chemistry,2008,107(1):411-418.
[4]李建,刘亚楠,刘宁,等. 羧甲基纤维素的制备研究及应用现状[J]. 食品工业科技,2014,35(8):379-382.
[5]Ibrahim A A,Adel A M,El-Wahab Z H A,et al. Utilization of carboxymethyl cellulose based on bean hulls as chelating agent. Synthesis,characterization and biological activity[J]. Carbohydrate Polymers,2011,83(1):94-115.
[6]Yan H,Zhang W X,Kan X W,et al. Sorption of methylene blue by carboxymethyl cellulose and reuse process in a secondary sorption[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects,2011,380(1-3):143-151.
[7]王卉,孙宏元,何节玉,等. 羧甲基纤维素钠纳米抗菌复合膜的制备及其性能研究[J]. 食品工业科技,2016,37(5):277-280.
[8]王丽,庞方亮,王爱勤. 羧甲基纤维素钠/蒙脱土纳米复合材料的制备及结构表征[J]. 硅酸盐学报,2010,38(9):1820-1825.
[9]李俊巧,张杨,王慧霞,等. 羧甲基纤维素在防油纸表面施胶中的应用[J]. 纸和造纸,2015,34(3):4-6.
[10]谢丽源,甘炳成. 羧甲基纤维素钠在食品工业中的应用研究[J]. 农产品加工学刊,2007(88):55-67.
[11]刘俊亮,邬娟,张洪斌. 羧甲基纤维素钠稳定酸性乳饮料的研究进展[J]. 中国乳品工业,2012,40(1):38-41.
[12]孙瑶,王瑞,腾飞,等. 海藻酸钠-羧甲基纤维素-山梨酸钾复合抗菌膜的制备[J]. 食品工业科技,2013,43(9):90-93.
[13]汪磊,李飞,张欢子,等. 羧甲基纤维素钠对莜麦馒头品质影响[J]. 粮食与油脂,2013,26(1):49-51.
[14]杨开良. 我国竹产业发展现状与对策[J]. 经济林研究,2012,30(2):140-143.
[15]邵自强. 纤维素醚[M]. 北京:化学工业出版社,2007.
[16]王春红,王瑞,于飞. 竹原纤维的化学脱胶工艺[J]. 纺织学报,2007,28(4):26-29.
[17]谢涛,余秉琦.竹纤维素分离级分的结构特性[J].纺织学报,2011,32(6):22-27.
[18]张袁松,谢吉祥,李晓龙,等. 基于闪爆-碱煮联合工艺的天然竹纤维提取[J]. 纺织学报,2012,33(10):56-61.
[19]张磊,俞建勇,刘丽芳,等. 木聚糖酶和漆酶对竹原纤维精细化处理效果[J]. 东华大学学报(自然科学版),2009,35(3):309-313.
[20]于跃,张剑,何德志. 纤维素酶活力测定条件研究及其在洗涤剂中的应用[J]. 日用化学工业,2015(8):457-461.
[21]何珣,缪冶炼,陈介余,等. 纤维素酶用量和底物浓度对玉米秸秆酶解的影响[J]. 食品科技,2010,35(2):47-51.
[22]JunYu,Jibin Zhang,Jin He,et al.Combinations of mild physical or chemical pretreatment with biological pretreatment for enzymatic hydrolysis of rice hull[J]. Bioresource Technology,2009,100(2):903-908.
[23]Singh R K. Optimization of Reaction Conditions for Preparing Carboxymethyl Cellulose from Corn Cobic Agricultural Waste[J]. Waste & Biomass Valorization,2013,4(1):129-137.
[24]Pushpamalar V,Langford S J,Ahmad M,et al. Optimization of reaction conditions for preparing carboxymethyl cellulose from sago waste[J]. Carbohydrate Polymers,2006,64(2):312-318.
[25]Mansouri S,Khiari R,Bettaieb F,et al. Synthesis and Characterization of Carboxymethyl Cellulose from Tunisian Vine Stem:Study of Water Absorption and Retention Capacities[J]. Journal of Polymers & the Environment,2015,23(2):190-198.
[26]Palme A,Idström A,Nordstierna L,et al. Chemical and ultrastructural changes in cotton cellulose induced by laundering and textile use[J]. Cellulose,2014,21(6):4681-4691.
[27]Adinugraha M P,Marseno D W,Haryadi. Synthesis and characterization of sodium carboxymethylcellulose from cavendish banana pseudo stem(Musa cavendishii LAMBERT)[J]. Carbohydrate Polymers,2005,62:164-169.
[28]余小龙,刘健,甘礼惠,等. 竹屑制备高取代度羧甲基纤维素钠的优化及其表征[J]. 现代化工,2015,35(8):109-114.
Preparationofsodiumcarboxymethylcellulosebypretreatmentofbamboopowderwithalkalienzymecouplingmethod
TANGXia,YEHang-yu,CHENJia-cheng,LIUJia-hui,CAIWang-zhi,CHENWei-qing*
(College of Biological and Environmental Engineering,Zhejiang Shuren University,Hangzhou 310015,China)
The bamboo powder was pretreated to increase the product’s cellulose content,then the sodium carboxymethyl cellulose(CMC)was prepared by the pretreated material. The process of alkali-cellulase coupling method were as follows:bamboo powder 4 g,5% NaOH 40 mL,alkali hydrolysis at 50 ℃ for 1 h. After vacuum filtration,adjusted pH5.5,adding 400 U/mL cellulase solution 30 mL,then the enzymatic reaction kept at 49 ℃ for 30 min. After the process,the contentα-cellulose of the treated bamboo powder was 84.1%,and the viscosity of the 2% CMC solution made from this material attained 162 mPa·s,the degree of substitutin(DS)was 0.95.The infrared spectroscopy showed that the product had characteristic peak of carboxymethyl group,scanning electron microscopy showed that the product had salt characteristics. There is less environmental pollution and relatively low cost by adopting the bio-chemical coupling method in the pretreatment of raw materials,and it would promote the development of green economy and provide a new way for the preparation of CMC.
sodium carboxymethyl cellulose;bamboo powder;cellulose;alkali-cellulase method;preparation
2017-07-20
唐霞(1995-),女,本科,主要从事植物资源利用方面的研究,E-mail:18268823075@163.com。
*通讯作者:陈蔚青(1967-),女,硕士,教授,主要从事生物催化与转化技术方面的研究,E-mail:cwq135790@sina.com。
浙江省公益性技术应用研究计划项目(2015C32036);浙江省大学生科技创新项目(2017R421022)。
TS202.3
A
1002-0306(2017)23-0100-05
10.13386/j.issn1002-0306.2017.23.020
