35组同成分不同厂家药品说明书情况分析
2017-08-31韩永鹏张文涛徐佳张琪
韩永鹏,张文涛,徐佳,张琪
北京市中西医结合医院药剂科,北京 100039
35组同成分不同厂家药品说明书情况分析
韩永鹏,张文涛,徐佳,张琪
北京市中西医结合医院药剂科,北京 100039
目的 通过比较分析35组同成分不同厂家药品说明书的差异,以更好服务临床,提高用药安全性。方法 收集该院所有同成分、同剂型、不同厂家西药药品说明书比较共35组,对其说明书内容进行比较分析。结果35组药品说明书的适应证、用法用量、注意事项、不良反应等各项存在一定差异。结论同成分不同厂家药品的一致性存在一定不足,监管部门、药学人员、医护人员、药品研发企业应当加强合作,重视药品说明书差异性的分析总结,确保临床用药安全。
说明书;一致性;风险
药品说明书详细包含了药品的安全性、有效性等信息,是医护人员、患者所接触的第一手用药资料并直接指导临床用药。同成分的药品其说明书理论上应当是基本一致的。但有研究发现国产药品与进口药品相比,存在不同程度的不良反应报告数据不全,安全性警示不足和临床试验数据缺失等现象[1-2],同成分不同厂家的国产药品的药品说明书也存在一定差异[3]。此外,由于我国医药工业以仿制药为主,相关法律相对缺失,导致了我国普遍出现多厂家生产同一通用名药品的现象,且有多项研究表明不同厂家同一通用名药品的一致性较差[4]。故为了更好的安全、合理用药以服务临床工作,对该院35组同成分不同厂家的药品说明书各事项进行比较分析。
1 资料与方法
1.1 一般资料
收集该院现有同成分不同厂家说明书70张,成分相同者分为一组,共35组。
1.2 研究方法
按照《药品说明书和标签管理规定》等相关规定对同成分不同厂家药品说明书进行比较分析。
2 结果
经过分析后发现,总共有10组药品的警示语存在差异,主要表现为药物重要禁忌是否进行警示。例如厄贝沙坦片(赛诺菲)警示语要求一旦发生妊娠应当即刻停止使用以避免对胚胎造成伤害,而厄贝沙坦片(扬子江)则无此警示。分析发现共有9组药品适应证的描述存在一定差异,其中有7组为进口药品/国产药品的适应证差异,例如格列美脲适应证为不适用于1型糖尿病(例如有酮症酸中毒病史的糖尿病患者的治疗)、糖尿病酮症酸中毒或糖尿病前驱昏迷或昏迷的治疗,格列美脲(万邦生化)则无此描述。分析发现共有12组药品存在用法用量方面的差异,主要表现为部分进口药品较国产药品的用法用量项上更加详细以及部分药品对于特殊用药人群用药未加详述。格列美脲推荐最大剂量为6 mg,认为其日用量在6 mg后疗效达到最大,增加剂量无法增强疗效[7](见表1),而格列美脲的推荐最大剂量为8 mg,两者存在较大的差异。分析发现共有8组药品不良反应描述不一致,主要表现国产药品对于不良反应描述相对简略,而进口药品对于不良反应的描述则较为详细,例如的氯雷他定(先灵葆雅)不良反应项下面共11条,且内容较为详细,而氯雷他定(扬子江)不良反应项共8条信息,且内容较为简单。分析发现共有11组药物禁忌项描述存在差异。例如卡维地洛片(齐鲁制药)禁忌为手术前48 h以内禁用,而卡维地洛片(宁波天衡)禁忌为糖尿病酮症酸中毒、代谢性酸中毒,两种同成分不同厂家药品对于禁忌的描述完全不一致,而根据国家食药监局公布的卡维地洛片说明书中禁忌包含糖尿病酮症酸中毒,可见卡维地洛片(齐鲁制药)禁忌项标注不全。另外部分国产药品的禁忌项较为简略,而进口药品的禁忌项明显更加详细。分析发现12组药品注意事项存在差异。此项描述较为凌乱,例如盐酸二甲双胍片(施贵宝)对于注意事项的描述较为详细,而盐酸二甲双胍缓释胶囊(河北爱尔海泰)则相对简单,苯磺酸氨氯地平滴丸(北京九龙)注意事项内有对β受体阻滞剂突然停药出现的危险不能给予保护,而苯磺酸氨氯地平片(辉瑞)未见此描述,洛芬待因片(国药集团)注意事项为4项,洛芬待因缓释片(西南药业)注意事项为11条,存在较大差异。分析发现孕妇及哺乳期妇女用药,儿童用药,老年用药等特殊人群用药分别有6组、4组、7组不一致。例如厄贝沙坦片(赛诺菲)妊娠和哺乳期停止使用本品,禁止用于妊娠4~9月,厄贝沙坦片(扬子江)为妊娠和哺乳期妇女禁用,可能与厄贝沙坦片(赛诺菲)临床研究数据更加翔实有关,氢溴酸西酞普兰片(丹麦灵北)对于老年人的极量为20 mg,氢溴酸西酞普兰胶囊(四川科伦)的极量为40 mg,存在较大差异。分析发现共4组药品存在差异,主要表现为进口药品对于药物过量的研究数据更加翔实。例如进口国产厄贝沙坦片对于药物过量的处理方式一致,但厄贝沙坦(赛诺菲)记载成年人剂量达900 mg/d,连续8周给药没有显示毒性,较国产药研究数据更加明确。进口国产帕罗西汀的药物过量处理方式均为对症处理,但帕罗西汀(中美天津史克)用药过量的症状记载较为详细,而国产则无此项数据。分析发现共12组药品的临床试验存在较大差异,全部表现为进口药品临床试验数据翔实,国产药品的临床试验数据存在较大不足。将对各组说明书进行比较分析,发现大多数说明书均存在一定差异,见表1。
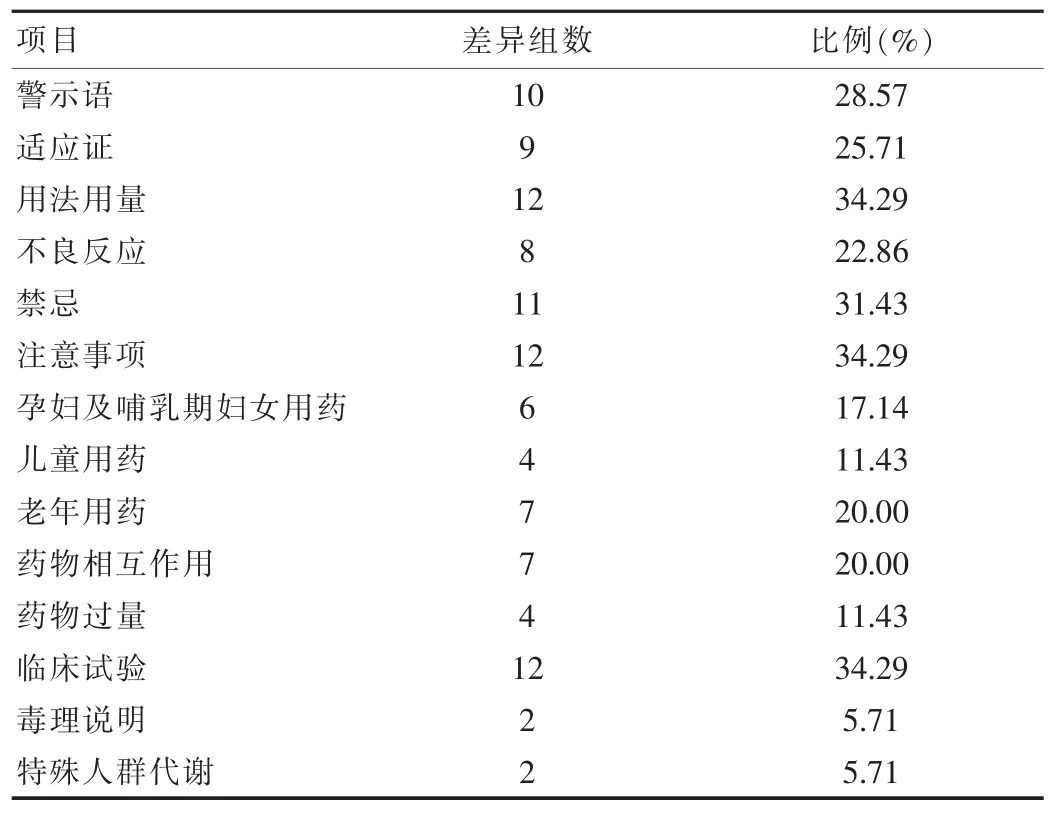
表1 35组同成分不同厂家药品说明书各项目的内容比较
3 讨论
3.1 警示语差异
“警示语”是对药品严重不良反应及其潜在的安全性问题的警告。2007年食药局要求在所有含兴奋剂的药品说明书或标签上注明“运动员慎用”字样进行警示,取得了良好的效果[5]。根据相关法律法规,药企应当及时修正药品的安全性、有效性信息,可见部分厂家未及时更新药品警示语不仅对于自身的经营存在一定风险,对于用药安全更是一种潜在威胁,相关企业应当及时更新警示语以利于临床用药安全。
3.2 适应证
适应证是指明确用于预防、治疗、诊断、缓解或者辅助治疗某种疾病(状态)或者症状。国产药品说明书适应症项内容描述不够严谨、应用限制和预期临床受益不确定性描述普遍缺失、内容不够具体的状况[6]。可见相比较而言进口药品说明书对于适应证的描述更加详细,部分国产药品说明书适应证项目描述不够具体,存在一定的临床的用药安全隐患。
3.3 用法用量
说明书用法用量项包括用法和用量两部分。用法用量项是设计给药方案的主要参考标准,主要通过上市前的临床试验获得,以获益/风险比为基本原则,完善的用法用量信息有助于确保临床安全用药。
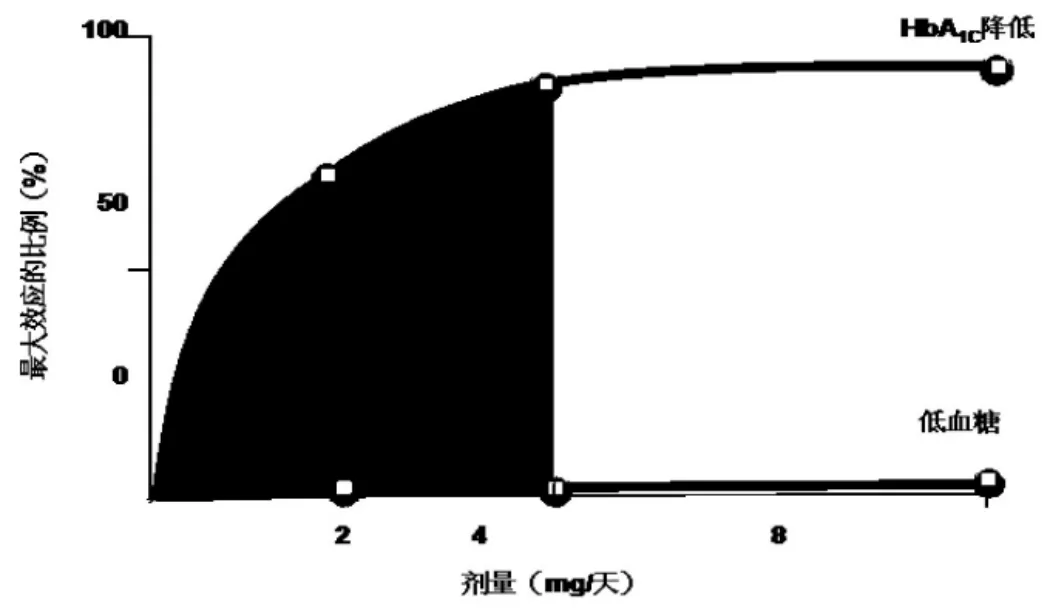
表1 格列美脲(赛诺菲)量效关系图
3.4 不良反应
不良反应是药物在正常用法、用量的情况下,发生与治疗目的无关的有害反应。医师及药师对于不同厂家同成分的说明书不良反应存在差异可能认识不足,容易影响临床用药安全。故说明书有必要及时更新不良反应事项,规避用药风险。
3.5 禁忌
禁忌指药物不适宜应用于某些疾病、情况或特定的人群(儿童、老年人、孕妇及哺乳期妇女、肝肾功能不全者)。或应用后会引起不良后果,在具体给药上应予禁止或顾忌。对禁止的指征应绝对禁止使用。这些禁忌的差异可能对于临床安全用药构成严重威胁,生产厂家有必要根据药监局的相关标准进行说明书更新,以确保临床用药安全。
3.6 注意事项
药品说明书的[注意事项]是用药的重要参考,完善的注意事项有利于安全用药。这些注意事项的差异不利于临床的安全有效用药,有必要及时统一。
3.7 特殊人群用药
孕妇及哺乳期妇女用药,儿童用药,老年等特殊人群,生理心理特点不同于正常人群,这类人群用药安全显得尤其重要。由于孕妇、哺乳期妇女、儿童、老人因其生理的特殊性不能接受药品实验数据的论证,如何获取特殊人群的用药信息一直是药物研究的难点,不同厂家科研实力差异较大,导致对于特殊人群用药信息的研究存在差异。
3.8 药物过量
药物过量应当详细列出过量应用该药品可能发生的毒性反应、剂量及处理方法。可见部分国产药品对于药物过量的数据不够详细,不利于临床安全用药。3.9临床试验
临床试验是指任何在人体(患者或健康志愿者)进行药物的系统性研究。良好的临床研究是药品的安全性及有效性的研究基础,进口药品多为原研药品,进行了大量的临床试验,故而具有较好的研究基础,而国产药品仿制药较多,根据我国临床试验的相关法律法规完成了临床试验,其研究基础较原研药存在一定差异。
4 结论
根据相关规定,医院药品可“一品双规”,因此总结分析相同通用名不同厂家药品说明书的差异性具有很实用的临床意义。该研究发现进口药品说明书的规范化和详细程度较国产药品说明书有明显的差异,原因可能是不同厂家在研发能力、生产工艺、质量管控等各方面存在差异,从而导致了药品质量及药品说明书在同一问题观点上的差异。因此为促进临床的安全用药及有效用药,药品监管部门应当加强对药品说明书的规范和管理,保证说明书各项目的完整性、内容的准确性及同成分不同厂家药品说明书的相对一致性。生产企业也应当应使用规范的药品标准术语,主动更新说明书,确保安全有效用药。药学人员需掌握药品的说明书信息,并重点关注同成分不同厂家药品说明书各事项可能存在的差异,规避用药风险,有必要及时归纳总结药物说明书信息,更好的促进药物的合理使用。
[1]叶芳敏,吴明东,刘丽仙,等.国产和进口奥氮平片使用说明书的比较和分析[J].海峡药学,2013(6):264-265.
[2]曾明艺,刘滔滔,黄丽荣.国产与进口心血管系统药物说明书中特殊人群用药的异同比较[J].中国药业,2009(4):11-12.
[3]陈华彪.30组同成分不同厂家或规格注射剂药品说明书调查分析[J].中国药房,2015(10):1437-1440.
[4]冯毅,朱波.关于我国仿制药质量一致性评价的研究及建议[J].中国新药杂志,2016(1):19-26.
[5]洪兰,朱俊怡.国内外药品说明书和标签管理中有关警示语的比较研究[J].中国药房,2014(33):3161-3164.
[6]萧惠来.FDA对处方药说明书[适应症]的要求[J].药物评价研究,2014(5):396-400.
[7]Riddle MC.Combined therapy with insulin plus oral agents:is there any advantage An argument in favor[J].Diabetes Care,2008,31(2):S125-S130.
Analysis of Situations of 35 Groups of Congruent Dispensatories of Different Factories
HAN Yong-peng,ZHANG Wen-tao,XU Jia,ZHANG Jia
Department of Pharmacy,Beijing Traditional Chinese and Western Medicine Hospital,Beijing,100039 China
Objective To compare and analyze the differences of 35 groups of congruent dispensatories of different factories in order to better serve the clinic and improve the medication safety.Methods All the same component,same dose and different factories of western dispensatories in our hospital were collected and 35 groups were compared and the contents of dispensatories were compared and analyzed.Results There were a certain differences in the indications,dosage,notes and adverse reactions among the 35 groups.Conclusion There is a certain deficiency of consistency of the congruent dispensatories of different factories,and the supervision department,pharmaceutical personnel,medical staff and drug research and development enterprises should enhance the cooperation,and pay attention to the analysis and summarization of differences of dispensatories and ensure the clinical medication safety.
Dispensatories;Consistency;Risk
R954
A
1672-5654(2017)07(b)-0095-03
2017-04-13)
10.16659/j.cnki.1672-5654.2017.20.095
韩永鹏(1982-),男,山东烟台人,本科,主管药师,研究方向:临床药学。
