肝上皮样血管内皮瘤的超声造影和增强CT表现
2017-07-01徐亚丹
徐亚丹
王文平1,2WANG Wenping
王 希1WANG Xi
张小龙1ZHANG Xiaolong
汪瀚韬1,2WANG Hantao
国 敏2,3GUO Min
肝上皮样血管内皮瘤的超声造影和增强CT表现
徐亚丹1,2XU Yadan
王文平1,2WANG Wenping
王 希1WANG Xi
张小龙1ZHANG Xiaolong
汪瀚韬1,2WANG Hantao
国 敏2,3GUO Min
1.Department of Ultrasound, Zhongshan
Hospital, Fudan University, Shanghai
200032, China; 2.Shanghai Institute of
Medical Imaging, Shanghai 200032, China
Address Correspondence to:WANG Wenping
E-mail: puguang61@126.com
中国医学影像学杂志
2017年 第25卷 第6期:452-456
Chinese Journal of Medical Imaging 2017 Volume 25 (6): 452-456
目的分析肝上皮样血管内皮瘤(HEHE)的超声造影(CEUS)表现与增强CT表现特点。资料与方法回顾性分析16例经病理证实为HEHE患者的CEUS和增强CT表现,其中5例行增强CT检查,8例行CEUS检查,3例同时行两种检查。结果11例HEHE在CEUS上共选取14个病灶;在增强方式上,5个病灶表现为环状增强,9个病灶表现为整体增强;在增强时相上,与肝实质相比,动脉期11个病灶同步增强,3个病灶快速增强;达峰时,2个病灶呈高增强,9个病灶呈等增强,3个病灶呈低增强;全部病灶在门静脉期及延迟期减退呈低回声。8例HEHE在增强CT上共发现29个病灶;动脉期9个病灶(31.0%)表现为轻度不均匀强化,4个病灶(13.8%)未见明显强化,16个病灶(55.2%)表现为轻度边缘强化;所有病灶在延迟期持续轻度强化。结论HEHE在CEUS和增强CT的表现各自具有特征性,两种检查方法对于HEHE均具有较高的诊断价值。
血管内皮瘤,上皮样;肝肿瘤;超声检查,多普勒,彩色;造影剂;体层摄影术,X线计算机;图像增强
肝上皮样血管内皮瘤(hepatic epithelioid hemangioendothelioma,HEHE)是一种罕见的间叶来源肿瘤,发病率低于1/100万,恶性程度介于肝血管瘤和肝血管肉瘤之间[1-3],术前诊断主要依靠影像学检查方法,但是目前其影像学表现尤其是超声造影(CEUS)表现报道极少,大多数为病例报道,且样本量较少。为提高对HEHE影像学表现的认识及术前诊断率,指导临床进一步治疗,本文分析16例HEHE的CEUS和增强CT表现。
1 资料与方法
1.1 研究对象 2006年1月-2016年7月在复旦大学附属中山医院经手术或穿刺病理证实为HEHE的患者共16例,2例患者病灶单发,14例患者病灶多发;其中男7例,女9例;年龄27~68岁,平均(46.5±12.5)岁;病灶最大径为13~140 mm,平均(49.3±36.3)mm。1例患者HBsAg阳性,全部患者甲胎蛋白正常,1例患者CA199升高,3例患者肝功能异常。患者术前或穿刺前于我院行CEUS或增强CT检查,其中5例患者行增强CT检查,8例患者行CEUS检查,3例患者同时行增强CT和CEUS检查。
1.2 仪器与方法 采用Philips iU22型、Toshiba Aplio 500型、Logiq E9型彩色多普勒超声诊断仪,探头频率1.5~5.5 MHz,造影剂使用SonoVue。二维常规超声在选定病灶后进入造影模式,经肘静脉团注SonoVue 2.4 ml,随后快速注入5 ml 0.9%氯化钠溶液,观察所选取病灶的造影表现,包括病灶的增强起始时间、达峰时间、消退时间、增强方式及动脉期(0~40 s)、门静脉期(41~120 s)、延迟期(>120 s)的表现等。持续造影观察5~10 min,造影过程中用超声仪全程同步录像并保存。如需重复造影,2次间隔时间>15 min。最后,将造影资料全程回放,由2名高年资超声医师进行分析并作出判断。
采用16层CT(Sensation 16,Siemens Medical Solutions,Forchheim,Germany),动态增强扫描时采用高压注射器经肘静脉注射非离子型碘对比剂(浓度为300 mgI/ml),对比剂总量90 ml,注射速度3 ml/s,延迟25~35 s行动脉期扫描,75~85 s行门静脉期扫描,每次扫描时嘱患者屏气,层厚5~7 mm,螺距1.0。在每个时期,与肝脏正常组织相比较,将病灶的密度分为高密度、等密度、低密度3种情况,所有影像资料由1名高年资主治医师评估后作出诊断,再由1名高年资副主任医师进行审核。
2 结果
2.1 常规超声表现 11例HEHE患者共发现35个病灶,在灰阶图像上的特征表现见表1。2例患者病灶之间互相融合(图1),4例患者病灶周围伴暗环(图2)。在彩色多普勒血流显像(CDFI)上,4例患者测及病灶周边彩色血流信号,3例患者测及病灶周边及内部彩色血流信号(图2),阻力指数平均为0.63±0.02。

表1 HEHE的常规超声特征表现[例数(%)]

图1 男,30岁,HEHE低回声病灶互相融合且沿肝包膜下生长(箭)
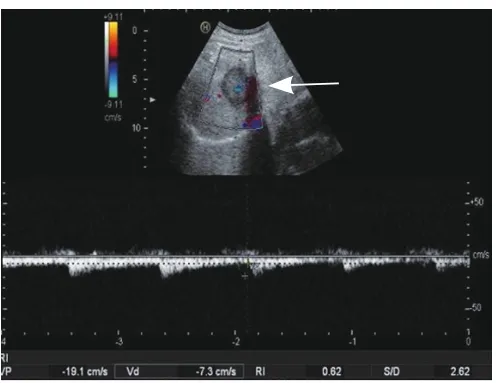
图2 男,74岁,HEHE等回声病灶周围伴暗环,CDFI测及周边及内部血流信号,阻力指数为0.62(箭)
2.2 CEUS表现 在CEUS上共选取14个病灶观察,其中3例患者观察2个病灶,其余8例患者均观察1个病灶,14个病灶在CEUS上的特征表现见表2。在增强方式上,5个病灶表现为环状增强,病灶中央部分始终未见明显增强;其余9个病灶表现为整体增强,其中4个病灶表现为整体不均匀增强,5个病灶表现为整体均匀增强。3个病灶内部出现“血管征”(图3)。在增强时相上,动脉期11个病灶表现为与肝实质同步开始增强,3个病灶表现为稍快于肝实质增强。达峰时,2个病灶强度高于周围肝实质,3个病灶强度低于周围肝实质,9个病灶强度等于周围肝实质。全部病灶在门静脉期及延迟期快速减退表现为低回声改变。1例HEHE患者在CEUS上的特征表现见图4。
2.3 平扫CT表现 8例患者的29个病灶平扫时均呈低密度,其中20个病灶沿包膜下分布(指病灶边缘与肝包膜的最近距离<30 mm),15个病灶紧贴肝包膜下生长。1例患者出现钙化,4例患者病灶之间互相融合,4例患者出现“包膜收缩征”,即沿肝周分布的病灶局部肝包膜向内凹陷(图5)。
2.4 增强CT表现 增强CT共发现29个病灶,其中4个病灶(13.8%)未见明显强化,9个病灶(31.0%)表现为轻度不均匀强化,16个病灶(55.2%)表现为轻度边缘强化。所有增强病灶在动脉期均表现为低增强,在门静脉期所有病灶持续强化,程度不一(图6)。2例患者病灶在门静脉期出现“靶征”(图7),即低密度病灶内部出现更低密度影;2例患者内部出现“血管征”(图 8)。

表2 HEHE的CEUS特征表现

图3 女,52岁,CEUS动脉期HEHE病灶内部出现“血管征”(箭)

图4 女,30岁,HEHE。病灶在二维上呈低回声,边界欠清(箭,A);CEUS上19 s,病灶与周围肝实质同步开始增强(箭,B);26 s达峰,病灶强度基本等于周围肝实质(箭,C);而在35 s,病灶快速减退呈稍低回声(箭,D);在门静脉期及延迟期,病灶表现为低回声(箭,E)

图5 女,36岁,HEHE病灶局部出现“包膜收缩征” (箭)

图6 女,49岁,HEHE病灶在增强CT动脉期表现为边缘轻度强化(箭,A);在门静脉期及延迟期表现为持续性强化(箭,B)

图7 男,54岁,门静脉期HEHE低密度病灶内部出现更低密度影即“靶征”部(箭)

图8 女,48岁,门静脉期可清楚显示病灶之间互相融合,病灶内出现“血管征”(箭)
3 讨论
原发于肝脏的HEHE由Ishak等[1]于1984年首次报道,由于其发病率极低,术前影像及术后病理均诊断困难[4]。随着近年影像学及病理学的发展,HEHE作为一种罕见的低中度恶性肿瘤逐渐受到关注。HEHE与原发性肝癌和转移性肝癌等其他肝脏恶性肿瘤的发展过程、临床治疗方法和预后存在明显的差异,术前对HEHE与其他肝脏恶性疾病进行鉴别诊断具有重要的临床意义。
3.1 HEHE的病因及病理学基础 HEHE好发于中青年女性[4],发病机制尚不明确,临床表现多为腹痛、腹部不适等非特异性表现[5],偶有患者出现Budd-Chiari综合征的表现[6],部分患者初诊时已出现其他部位转移[7],转移率为27%~45%,最多见于肺,约占81%[1]。本组5例患者发现时已发生肺部转移,与以往报道相符。HEHE由上皮样细胞和树突状细胞组成,部分细胞腔内可含红细胞,类似印戒样细胞,形成特征性的胞质内血管[8]。随着病情进展,中央以纤维硬化区为主,周边为肿瘤细胞活跃区,肿瘤细胞进一步增殖可以侵犯、闭塞肝窦、门静脉以及肝静脉分支,造成自身缺血变性和坏死[7]。
3.2 HEHE的影像学表现
3.2.1 超声表现 影像学表现以多结节型为主,单结节型少见[9-10],本组表现与以往报道一致。二维超声多表现为肝内多发、不规则形、低回声团块,回声均匀或不均匀,周边可伴暗环,病灶之间可以相互融合。以往报道CDFI上可无彩色血流信号,也可测及周边或内部彩色血流信号;可测及动脉血流,也可测及静脉血流[11-12]。本组11例患者中,7例在病灶周边或内部测及彩色血流信号,1例测及静脉血流,6例测及动脉血流,阻力指数平均为0.63,整体低于肝细胞肝癌[13]。既往研究报道HEHE的CEUS以环状增强多见[14],而本组患者以整体增强多见,推测可能与肿瘤的纤维化程度相关;纤维化程度轻时,病灶以整体增强为主;肿瘤内部纤维化程度较重时,病灶以外周环状增强为主,中央纤维硬化区不增强。在增强时相上,本组HEHE患者主要表现为动脉期病灶与肝实质同步增强(11/14),门静脉期及延迟期均呈低回声改变(14/14),与一般典型的肝细胞肝癌的“快进快出”不完全一致;病灶增强达峰时,增强强度与肝实质相同或低于周围肝实质(12/14),增强强度普遍不高,与典型的肝细胞肝癌表现不同。
3.2.2 CT表现 本组HEHE患者CT平扫时病灶大部分为散在、多发、低密度结节,密度均匀或不均匀,与既往报道相似。本组HEHE多沿肝包膜下生长[15],局部邻近肝包膜可出现“包膜收缩征”,此征象不同于肝脏其他恶性肿瘤向外膨胀生长,推测此征象可能与肿瘤内含有纤维间质较多相关,病灶较大时可互相融合。文献报道20%的患者可出现钙化[2],本组仅1例患者(12.8%)出现钙化,可能与病例数较少有关。CT增强扫描后多数病灶为轻度增强(25/29),4个病灶未见明显强化,与本组患者CEUS呈低增强或等增强基本一致,可能与HEHE呈低中度恶性潜能而血供不足有关。既往研究报道HEHE在增强CT上多表现为边缘轻度强化[7,15],门静脉期及延迟期边缘持续强化,亦有报道显示病灶无明显强化[16],本组患者大多数表现与既往报道一致。部分患者表现为病灶不均匀强化,可能与病灶纤维化程度不一相关;门静脉期部分病灶可见“靶征”,与中央的纤维硬化区不增强而周边肿瘤细胞增强有关[17]。HEHE的“血管征”是肿瘤侵犯血管的早期表现,随着病情发展,管腔逐渐狭窄甚至闭塞[18]。
3.3 HEHE的鉴别诊断
3.3.1 原发性肝癌 原发性肝癌灰阶超声多表现为肝内低回声团块,边界欠清,周围亦可伴暗环,CDFI示阻力指数大多高于HEHE;CEUS典型表现为“快进快出”,即动脉期快于周边正常肝实质早期增强,动脉晚期或门静脉期快速减退呈低回声改变,且病灶达峰时强度往往高于周围正常肝实质。原发性肝癌平扫CT多表现为肝内低密度结节,较少出现病灶沿肝包膜下生长,若病灶临近肝包膜大多数包膜向外膨胀性生长,而与HEHE的“包膜收缩征”不同。原发性肝癌增强CT与CEUS表现一致,呈“快进快出”,且强度高于周围正常肝实质。另外,大多数原发性肝癌患者HBsAg阳性,且甲胎蛋白明显升高。
3.3.2 肝血管瘤 肝血管瘤在超声上多表现为肝内高回声团块,边界清,典型者出现“浮雕征”;当血管瘤呈低回声表现时,周边往往伴有高回声环,病灶较大时内部可呈网状。肝血管瘤CT平扫显示病灶边界清楚,对周围组织无压迫。肝血管瘤CEUS和增强CT均表现为周边结节状向心性增强,门静脉期和延迟期不减退,几乎不出现“靶征”。另外,血管瘤无肝包膜下生长趋势,亦无“包膜收缩征”,较少出现病灶之间相互融合。
3.3.3 肝血管肉瘤 肝血管肉瘤恶性程度极高,多见于老年男性,常伴有明显的恶病质。肿瘤恶性程度高,发展较快,肿块常常发生变性、出血和坏死,回声/密度大多混杂不均匀。CEUS和增强CT大多表现为不均匀增强,增强强度往往高于周围正常肝实质,典型增强表现为周边和中心区明显强化,门静脉期及延迟期持续填充式强化,但多数不能完全填充[19]。
3.3.4 转移性肝癌 转移性肝癌与HEHE的超声及CT均表现为肝内多发病灶;二维超声亦以低回声多见,周围可出现“暗环”,但一般血流阻力指数高于HEHE,且无沿肝包膜下生长的特点;注射造影剂后,在CEUS和增强CT上多呈“快进快出”的表现;达峰时增强强度一般高于周围正常肝实质,此增强特征与HEHE不同;肿块较大时易发生坏死增强不均匀。若HEHE表现为不典型的“快进快出”,则与转移性肝癌鉴别困难。另外,转移性肝癌常有原发灶,临床上肿瘤标志物阳性者多见。
本研究结果显示,HEHE的CEUS特征性表现为:动脉期与肝实质同步增强,达峰时病灶强度与周围正常肝实质相等甚至低于周围正常肝实质,门静脉期及延迟期病灶快速减退呈低回声改变,部分患者可出现“血管征”。在增强CT上,HEHE的增强程度大多数较轻或几乎不增强,以边缘增强为主,门静脉期及延迟期持续轻度强化,部分患者在门静脉期可出现“靶征”及“血管征”。出现以上典型增强表现时,如果病灶多发且多沿肝脏包膜下生长,伴“包膜收缩征”,发展后期病灶之间互相融合,临床上患者肿瘤标志物正常,伴其他部位转移但身体状况尚可,应高度怀疑是HEHE。尽管HEHE的CEUS表现与增强CT表现并不完全一致,但两者均有特征性表现,联合应用有助于HEHE的诊断。
[1]Ishak KG, Sesterhenn IA, Goodman ZD, et al. Epithelioid hemangioendothelioma of the liver: a clinicopathologic and follow-up study of 32 cases. Hum Pathol, 1984, 15(9): 839-852.
[2] Makhlouf HR, Ishak KG, Goodman ZD. Epithelioid hemangioendothelioma of the liver: a clinicopathologic study of 137 cases.Cancer, 1999, 85(3): 562-582.
[3] Weiss SW, Enzinger FM. Epithelioid hemangioendothelioma: a vascular tumor often mistaken for a carcinoma. Cancer, 1982,50(5): 970-981.
[4]Mehrabi A, Kashfi A, Fonouni H, et al. Primary malignant hepatic epithelioid hemangioendothelioma: a comprehensive review of the literature with emphasis on the surgical therapy.Cancer, 2006, 107(9): 2108-2121.
[5]周易, 林江, 曾蒙苏, 等. 五例肝脏上皮样血管内皮瘤的影像表现与病理对照分析. 中华放射学杂志, 2008, 42(4):432-434.
[6]Walsh MM, Hytiroglou P, Thung SN, et al. Epithelioid hemangioendothelioma of the liver mimicking Budd-Chiari syndrome. Arch Pathol Lab Med, 1998, 122(9): 846-848.
[7]赵桂玖, 王庆兵, 曾蒙苏, 等. 肝上皮样血管内皮瘤的CT和MRI表现. 中国临床医学影像杂志, 2015, 26(8): 577-580.
[8]Dong K, Wang XX, Feng JL, et al. Pathological characteristics of liver biopsies in eight patients with hepatic epithelioid hemangioendothelioma. Int J Clin Exp Pathol, 2015, 8(9):11015-11023.
[9]刘权, 彭卫军, 王坚. 肝上皮样血管内皮瘤影像学表现及征象分析. 肿瘤影像学, 2014, 23(1): 8-13.
[10] Schweitzer N, Soudah B, Gebel M, et al. Gray scale and contrast-enhanced ultrasound imaging of malignant liver tumors of vascular origin. United European Gastroenterol J,2015, 3(1): 63-71.
[11] Wang LR, Zhou JM, Zhao YM, et al. Clinical experience with primary hepatic epithelioid hemangioendothelioma: retrospective study of 33 patients. World J Surg, 2012, 36(11): 2677-2683.
[12] 张小龙, 曹佳颖, 王文平. 肝上皮样血管内皮瘤超声造影表现(附2例报告). 肿瘤影像学, 2015, 24(4): 317-318.
[13] 谭洁贞. 超声对肝细胞肝癌和肝胆管细胞癌的鉴别诊断.临床超声医学杂志, 2012, 14(5): 356-357.
[14] Dong Y, Wang WP, Cantisani V, et al. Contrast-enhanced ultrasound of histologically proven hepatic epithelioid hemangioendothelioma. World J Gastroenterol, 2016, 22(19): 4741-4749.
[15] Gan LU, Chang R, Jin H, et al. Typical CT and MRI signs of hepatic epithelioid hemangioendothelioma. Oncol Lett, 2016,11(3): 1699-1706.
[16] 朱岩, 李海, 张春节, 等. 肝上皮样血管内皮瘤2例临床病理分析. 临床与实验病理学杂志, 2011, 27(6): 655-657.
[17] 李巧媚, 周华邦, 胡和平. 肝脏上皮样血管内皮瘤17例临床和病理特征分析. 中华消化杂志, 2014, 34(8): 527-530.
[18] 赵越, 龙世亮, 田执南, 等. 肝上皮样血管内皮瘤的CT与MRI特征及病理基础. CT理论与应用研究, 2015, 24(4):563-569.
[19] 张伟, 王兰荣, 薛鹏, 等. 原发性肝血管肉瘤的CT和MRI表现. 临床放射学杂志, 2014, 33(5): 734-738.
(本文编辑 饶亚岚)
Contrast-enhanced Ultrasound and Dynamic Contrast-enhanced CT Features of Hepatic Epithelioid Hemangioendothelioma
PurposeTo analyze and compare the imaging characteristics of contrastenhanced ultrasound (CEUS) and dynamic contrast-enhanced CT for hepatic epithelioid hemangioendothelioma (HEHE) diagnosis.Materials and MethodsThe imaging characteristics of CEUS and dynamic contrast-enhanced CT performed on 16 patients with pathological-con fi rmed HEHE were retrospectively analyzed. Dynamic contrast-enhanced CT was performed on 5 patients, real-time CEUS was performed on 8 patients, and both examinations were performed on 3 patients.ResultsOn CEUS, 14 lesions were selected from 11 HEHE cases. In the case of enhancement mode, 5 lesions displayed ringenhancement, and 9 lesions displayed global enhancement; in the case of arterial phase,11 lesions were synchronously enhanced, and 3 lesions were rapidly enhanced compared with liver parenchyma; in the case of peak time, hyper-enhancement, iso-enhancement and hypo-enhancement were observed in 2 lesions, 9 lesions and 3 lesions, respectively;all 14 lesions manifested hypoechoic mass in portal phase and delayed phase. On dynamic contrast-enhanced CT, 29 lesions were found in 8 HEHE cases. In the case of arterial phase,9 lesions (31.0%) showed slight inhomogeneous enhancement, 4 lesions (13.8%) showed no obvious enhancement and 16 (55.2%) lesions showed slight edge enhancement; all 29 lesions presented continuous hypo-enhancement in delayed phase.ConclusionBoth CEUS and dynamic contrast-enhanced CT have respective characteristic manifestations,and are of high value for the diagnosis of HEHE.
Hemangioendothelioma, epithelioid; Liver neoplasms; Ultrasonography,Doppler, color; Contrast media; Tomography, X-ray computed; Image enhancement
1. 复旦大学附属中山医院超声科 上海200032
王文平
国家自然科学基金项目(81371577);国家自然科学基金项目(81571676)。
2016-10-23
10.3969/j.issn.1005-5185.2017.06.013
2016-12-06
2.上海市影像医学研究所 上海 200032
3. 复旦大学附属中山医院放射科 上海200032
R445.1;R445.3;R735.7
