HPLC法测定复方阿胶膏中4种氨基酸的含量
2017-04-21张洁白娟朱倩云李成网
张洁 白娟 朱倩云 李成网
[摘要]目的建立复方阿胶膏中4种的含量测定方法。方法采用HPLC法,Shimpack ODS C18柱(4.6mm×250mm,5um),以乙腈-0.1mol/L乙酸钠溶液(用冰乙酸调节pH值至6.5,7:93)为流动相A,以乙腈-水(4:1)为流动相B,进行梯度洗脱。结果L-羟脯氨酸、甘氨酸、丙氨酸、L-脯氨酸分别在12.46~124.6ug/mL、23.62~236.2ug/mL、8.47~84.7ug/mL、19.14~191.4ug/mL范围内浓度与峰面积呈良好的线性关系(r=0.9999,n=6),平均加样回收率分别为97.91%、97.77%、97.67%、97.65%,RSD分别为1.70%、1.18%、1.31%、1.29%(n=9)。结论本法准确可靠,可用于复方阿胶膏的质量控制。
[关键词]高效液相色谱;复方阿胶膏;-羟脯氨酸;甘氨酸;丙氨酸;L-脯氨酸
复方阿胶膏为安徽中医药大学第二附属医院院内制剂,由阿胶、黄芪、枸杞子、核桃仁等八味中药组成,以养血益气为主,滋补肝肾、健胃消食、温肺润肠为辅。主用于气血两虚证所致的诸多疾病。其中阿胶为君药,阿胶中的主要有效成分为蛋白质、多肽和氨基酸。该方原采用凯氏定氮法测总氮含量为质量标准,但由于该制剂为复方制剂,干扰较大,该方法测得的结果误差较大,不够准确。因此在参考文献的基础上,于2015年10月~2016年1月期间,采用HPLC法以甘氨酸、丙氨酸、L-羟脯氨酸和L-脯氨酸四种阿胶中含量较高的氨基酸为定量指标,对复方阿胶膏进行质量标准研究。
1.仪器与试药
LC-20ATvp岛津液相色谱仪(日本岛津公司);SPD-20Avp检测器(日本岛津公司);梅特勒AG285电子分析天平(瑞士);梅特勒xp56型百万分之一电子天平(瑞士);JK-300型超声波清洗器(合肥金尼克机械制造有限公司)。复方阿胶膏(安徽中医药大学第二附属医院,批号:20150306、20150313、20150320),缺阿胶阴性制剂为自制。L一羟脯氨酸对照品(批号110766-200518)、甘氨酸对照品(批号110805-200306)、丙氨酸对照品(批号110780-200506)、L-脯氨酸对照品复(批号111626-200906)均购自中国食品药品检定研究院。甲醇、乙腈均为色谱纯,水为超纯水,其他试剂均为分析纯。
2.方法与结果
2.1色谱条件嘲
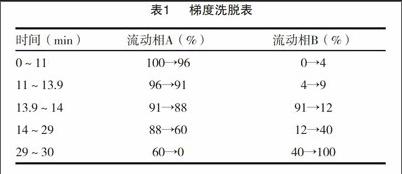
色谱柱:Shimpack ODS C18柱(4.6mm×250mm,5um);检测波长:254nm;流动相:以乙腈-0.1mol/L乙酸鈉溶液(用冰乙酸调节pH值至6.5,7:93)为流动相A,以乙腈-水(4:1)为流动相B,按表1中的规定进行梯度洗脱;流速:1.0mL/min;进样量:10uL;柱温:43℃。
2.2对照品溶液的制备
精密称取甘氨酸、丙氨酸、L-羟脯氨酸、L-脯氨酸对照品适量,加0.1mol/L的HCl溶液制成每lmL含甘氨酸110ug、丙氨酸40ug、L-羟脯氨酸50ug、L-脯氨酸90ug的混合对照品溶液,即得。
2.3供试品溶液的制备
取样品1g,精密称定,置25mL量瓶中,加0.1mol/L盐酸溶液20mL超声使溶解,加0.1mol/L盐酸溶液至刻度,摇匀。精密量取5mL,加盐酸5mL,150℃水解1h,放冷,移至蒸发皿中,用水10mL分次洗涤容器,洗液并入蒸发皿中,蒸干,残渣加0.1mol/L盐酸溶液溶解,转移至25mL量瓶中,加0.1mol/L盐酸溶液至刻度,摇匀,即得。
2.4阴性供试品溶液的制备
取缺阿胶的阴性制剂1g,同法制成阴性供试品溶液。
2.5柱前衍生化
精密量取上述溶液各5mL,分别置25mL量瓶中,分别加0.1mol/L异硫氰酸苯酯(PITC)的乙腈溶液2.5mL和lmol/L三乙胺的乙腈溶液2.5mL,摇匀,室温放置1h后,加50%乙腈至刻度,摇匀。取10mL,加正己烷10mL振摇萃取,放置10min,分取下层液,滤过,取续滤液,即得。
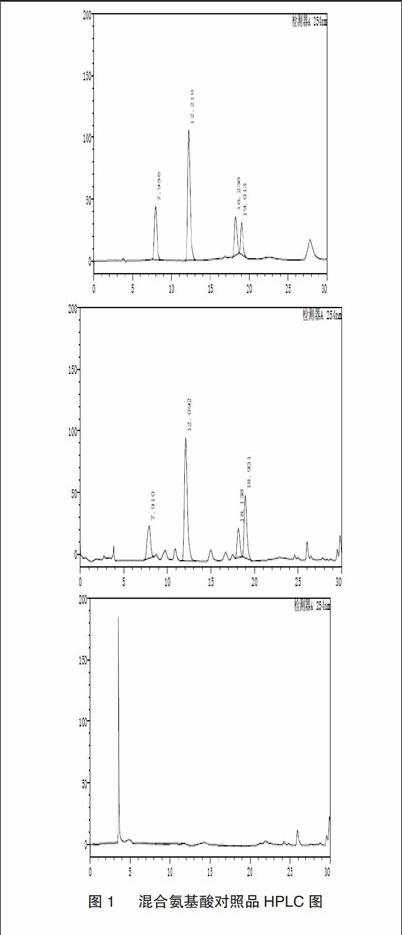
2.6系统适应性试验
分别精密吸取衍生化后的混合氨基酸对照品溶液、供试品溶液及阴性供试品溶液各10uL,注入液相色谱仪,按2.1项下色谱条件进行测定,记录色谱图,结果理论塔板数按甘氨酸计N=8725,分离度R=2.7,拖尾因子t=1.03。阴性供试品溶液无干扰。色谱图见图1。
2.7线性考察
精密称取甘氨酸对照品5.906mg、丙氨酸对照品2.118mg、L-羟脯氨酸对照品3.115mg、L-脯氨酸对照品4.784mg,置25mL量瓶中,加0.1mol/L盐酸溶液溶解并稀释至刻度,摇匀,即得含甘氨酸236.2ug/mL、丙氨酸84.7ug/mL、L-羟脯氨酸124.6ug/mL、L-脯氨酸191.4ug/mL的混合对照品溶液,分别精密吸取1.0、2.0、4.0、6.0、8.0mL置10mL量瓶中,加0.1mol/L盐酸溶液稀释至刻度,摇匀,即得。分别精密吸取上述混合对照品溶液各10uL,依次注入液相色谱仪中,依法测定,记录峰面积积分值,以对照品浓度为横坐标,峰面积积分值为纵坐标,计算线性回归方程分别为:甘氨酸A=20963C-39112(R=0.9999,n=6);丙氨酸A=15000C-31897(R=0.9999,n=6);L-羟脯氨酸A=12997C-14346(R=0.9999,n=6);L-脯氨酸A=12997C-14346(R=0.9999,n=6)。结果:甘氨酸在23.62~236.2ug/mL范围内;丙氨酸在8.47~84.7ug/mL范围内;L-羟脯氨酸在12.46~124.6ug/mL范围内;L-脯氨酸在19.14~191.4ug/mL范围内,浓度与峰面积呈良好的线性关系。
2.8精密度试验
取供试品溶液,衍生化处理后,精密吸取同一供试品溶液10uL,连续进样6次,依法测定,记录4种氨基酸的峰面积,计算。结果:L-羟脯氨酸、甘氨酸、丙氨酸、L-脯氨酸的RSD分别为0.46%、0.46%、0.43%、1.03%,说明仪器精密度良好。
2.9稳定性试验
取供试品溶液,衍生化处理后,置室温下放置,分别于配制后0、2、4、6、8、lOh,精密吸取10uL依法测定,记录峰面积,计算。结果:L-羟脯氨酸、甘氨酸、丙氨酸、L-脯氨酸的RSD分别为0.52%、0.69%、0.43%、0.96%,说明供试品溶液中的4种氨基酸在室温下10h内稳定。
2.10重现性试验
取同一批样品,平行6份,分别依法制备供试品溶液,衍生化处理,分别精密吸取10uL依法测定,计算含量。结果:L-羟脯氨酸平均含量为6.74mg,g,RSD=1.34%、甘氨酸平均含量为14.37mg/g,RSD=0.80%、丙氨酸平均含量为5.22Mg/g,RSD=1.55%、L-脯氨酸平均含量为11.23mg/g,RSD=1.12%。说明本方法重现性良好。
2.11日间精密度试验
取同一批样品共6份,分别由不同操作人员在不同时间依法制备供试品溶液,衍生化处理,依法测定,计算含量,结果:L-羟脯氨酸日间平均含量为6.76mg/g,日间RSD=1.18%、甘氨酸日间平均含量为14.30mg/g,日间RSD=0.89%、丙氨酸日间平均含量为5.14mg,g,日间RSD=1.06%、L-脯氨酸日间平均含量为11.25mg/g,日间RSD=0.40%。说明本方法日间精密度良好。
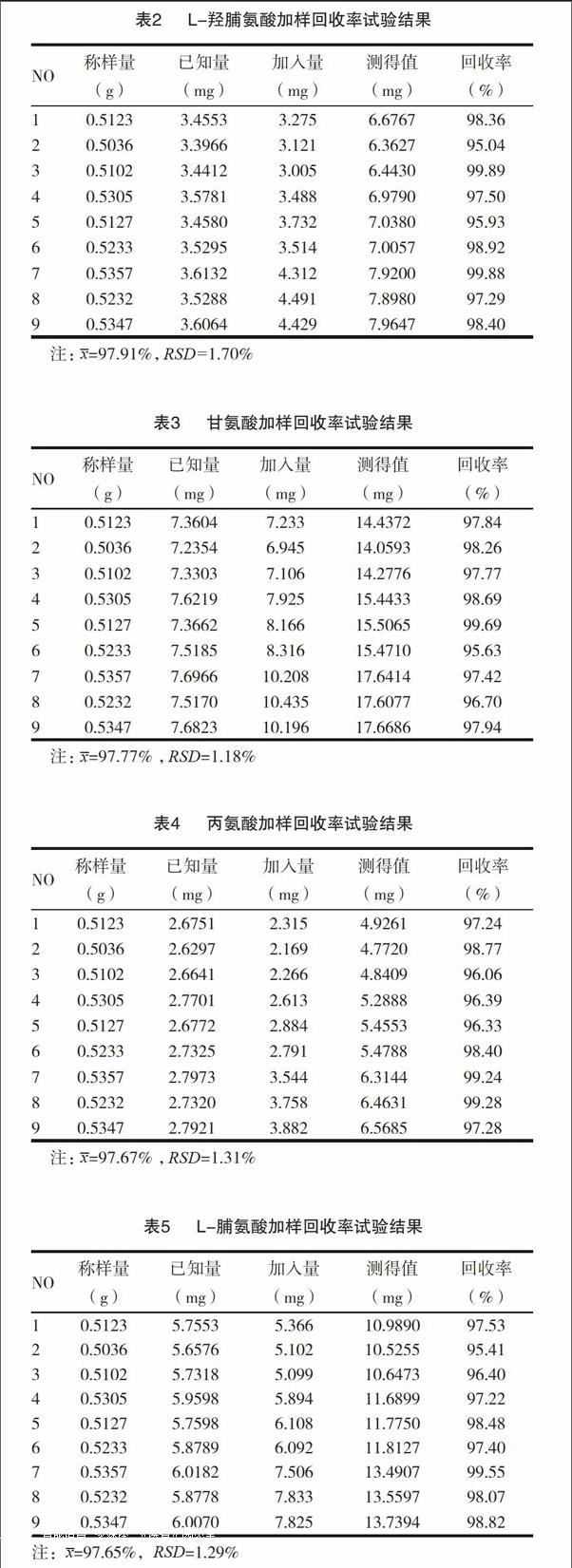
2.12加样回收率试验
取重现性样品约0.5g,平行9份精密称定,分别置25mL量瓶中,精密加入混合对照品适量,依法制备、测定、计算回收率,见表2~5。
试验结果表明:加样回收率良好,供试品溶液的制备过程不影响各氨基酸的含量。
2.13樣品测定
取中试样品,依法测定各氨基酸含量,计算。结果:L-羟脯氨酸的含量分别为6.78、6.70、6.62mg/g;甘氨酸的含量分别为14.78、14.49、14.37mg/g;丙氨酸的含量分别为4.75、4.83、4.92mg,g;L-脯氨酸的含量分别为11.19、11.12、11.30mg/g。
3.讨论
2015年版中国药典规定阿胶药材按干燥品计算,含L-羟脯氨酸不得少于8.0%,甘氨酸不得少于18.0%,丙氨酸不得少于7.0%,L-脯氨酸不得少于10.0%。故制剂中各氨基酸的最低理论含量分别为L-羟脯氨酸8.0mg/g、甘氨酸18.0mg/g、丙氨酸7.0mg/g、L-脯氨酸10.0mg/g。根据3批中试样品的测定结果,考虑到制剂过程中的损失,将本制剂中各氨基酸的含量限度暂定为:本品每1g中含L-羟脯氨酸不得少于5.0mg/g,甘氨酸不得少于10.0mg/g,丙氨酸不得少于3.0mg/g,L-脯氨酸不得少于8.0mg/g。
供试品溶液制备过程中需在150℃水解1h,本文采用的是顶空进样瓶密封后置烘箱中加热水解,也有文献报道采用安剖瓶密封后水解。此外,笔者还考察了柱前衍生化后正己烷的萃取次数对测定影响,发现萃取1次,2次,3次对结果没有影响。另有文献报道,柱前衍生化法可同时测定阿胶中17种氨基酸的含量,本文也进行了相关实验,但发现除了甘氨酸、丙氨酸、L-羟脯氨酸和L-脯氨酸以外,其他氨基酸含量均较低,且相互分离度和峰型也不佳。考虑到不同产地和批次的药材差异,以及文献报道均为阿胶单昧药材的含量测定,而本文讨论的是复方制剂的含量测定,处方中其他药味的化学成分,水解后都会对氨基酸的测定造成干扰,故未收载其他氨基酸的含量测定。
本文使用的流动相参考了2015版中国药典一部阿胶项下的流动相,但按照药典规定的梯度洗脱步骤,丙氨酸和L-脯氨酸的分离度达不到R>1.5的要求,经不断调整发现,流动相的比例,酸度和柱温都对氨基酸的峰型、保留时间和分离度均有显著影响。尤其是柱温,低于40℃或者高于45℃,都会减小丙氨酸和L-羟脯氨酸的分离度,只有在43℃时,分离度达到最大。因此在实验中应严格控制柱温和环境温度,以保证分析效果最佳。
本方法可为含阿胶的复方制剂建立质量控制标准提供参考。但由于实验条件有限,还有很多工作有待进一步完善,未来还计划使用氨基酸专用色谱柱、蒸发光散射检测器、氨基酸分析仪等,对复方阿胶膏中的多种氨基酸进行分析及定量。
