相变溶剂捕集CO2技术的研究进展
2017-03-14安山龙汪黎东于松华伍思宇
安山龙 ,汪黎东,于松华,伍思宇
(华北电力大学 环境科学与工程学院,河北 保定 071003)
相变溶剂捕集CO2技术的研究进展
安山龙 ,汪黎东,于松华,伍思宇
(华北电力大学 环境科学与工程学院,河北 保定 071003)
化学溶剂吸收法是目前应用最广泛的燃烧后CO2捕集技术。介绍了化学溶剂吸收法的基本原理,综述了化学溶剂吸收法的研究现状,比较分析了几种常用CO2吸收剂的优缺点。重点阐述了两类新型相变吸收剂(液-液相变溶剂和液-固相变溶剂)的研究进展。指出:新型相变溶剂是理想的CO2吸收剂,用其捕集CO2可有效降低吸收剂的再生能耗;相变溶剂吸收CO2的传质反应动力学以及不同类型相变溶剂的挥发和降解特性应作为今后该领域的研究重点。
二氧化碳;化学吸收;相变溶剂
近年来,全球气候变暖问题一直是国际社会关注和争论的焦点[1]。一般认为,导致全球变暖的主要因素是CO2等温室气体的过量排放[2],控制化石燃料的CO2排放是应对全球变暖的重要举措。国际能源署2015年报告称,按现有减排路线,到2100年全球平均升温将达2.6 ℃,2200年后将达3.5 ℃。2015年12月12日,《联合国气候变化框架公约》近200个缔约方一致通过《巴黎协定》,各方将加强对气候变化威胁的全球应对,把全球平均气温较工业化前水平的升高值控制在2.0 ℃之内,进而为控制在1.5 ℃之内而努力。全球将尽快实现温室气体排放达标,本世纪下半叶实现温室气体净零排放。因此,CO2减排形势严峻。
CO2减排是一项系统工程。减排途径包括节能、发展低碳能源(如核能和可再生能源)、CO2捕集与封存(CCS)等,其中CCS是应对气候变化问题最具发展前景的解决方案之一[3]。目前国内外CO2捕集主要有3条技术路线:燃烧前捕集、燃烧后捕集和富氧燃烧[4]。其中,燃烧后捕集技术因对现有电厂烟气特点具有良好的适应性、无需进行大规模改造而被认为是近期可行性最高的CO2减排方法[5]。燃烧后捕集技术主要包括化学溶剂吸收法、膜分离法、物理吸附法、低温蒸馏法等,其中化学溶剂吸收法目前应用最多且发展最为成熟[6]。
本文介绍了化学溶剂吸收法的基本原理,综述了化学溶剂吸收法的研究现状,比较分析了几种常用CO2吸收剂的优缺点。重点阐述了两类新型相变吸收剂(液-液相变溶剂和液-固相变溶剂)的研究进展。
1 化学溶剂吸收法
1.1 基本原理
化学溶剂吸收法的基本原理是:碱性吸收剂有选择性地与混合烟气中的CO2发生化学反应,生成不稳定的盐类,如碳酸盐、碳酸氢盐、氨基甲酸盐等,该盐可在一定条件下逆向解吸出CO2,从而实现CO2的脱除和再生过程。
醇胺溶液是目前应用最多的CO2化学吸收剂[7],典型代表为链烷醇胺吸收剂,按氮原子上活泼氢原子的个数可分为伯胺(2个氢原子)、仲胺(1个氢原子)和叔胺(氢原子数为0)3类。链烷醇胺吸收CO2的过程可用穿梭机理描述[8]。伯胺和仲胺与CO2反应形成两性离子[9],然后两性离子再与胺反应生成氨基甲酸根(见式(1)和式(2),R1、R2为烷基):
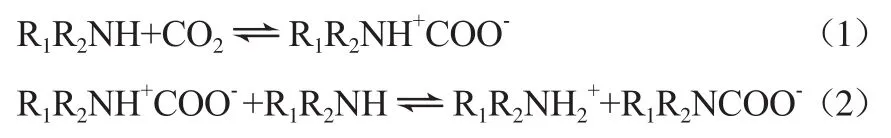
总反应如下:
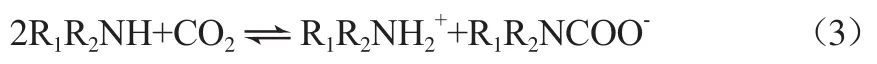
叔胺氮原子中没有多余的H原子,因而在与CO2反应时不会形成氨基甲酸根,它在吸收过程中扮演CO2水解时的催化剂,被吸收的CO2形成碳酸氢根离子[10]。反应式如下(R1、R2、R3为烷基):
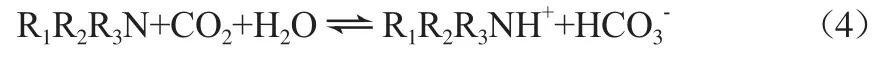
由式(4)可见,每摩尔伯胺和仲胺的最大吸收能力为0.5 mol CO2,而每摩尔叔胺的最大吸收能力为1 mol CO2。因此,伯胺和仲胺作为CO2吸收剂时反应速率较快,但CO2吸收容量较小;叔胺作为CO2吸收剂时反应速率相对较慢,但CO2吸收容量较大。
混合胺吸收剂是将不同类型的伯胺、仲胺和叔胺按照一定比例进行混合后所得的溶液,其吸收CO2反应机理与上文所述伯胺、仲胺、叔胺相一致,与单一有机胺溶液不同之处在于:混合胺吸收剂中不同类型反应会同时进行或先后进行。混合胺吸收剂综合利用了伯胺、仲胺的高吸收速率和叔胺的高吸收容量。碳酸钾溶液吸收CO2时,总反应如下:

主要包括如下两个反应[11]:
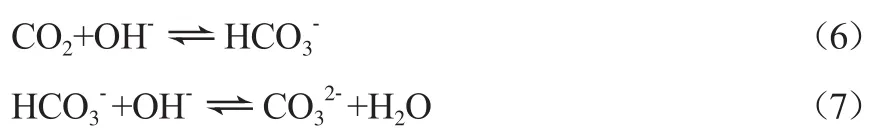
氨基酸盐溶液吸收CO2的反应机理也可用两性离子理论解释,反应过程如下所示[12]:

式中:B为反应体系中任意一种碱,包括游离的RNH2+,OH-,H2O。此外,CO2还可以与溶液中的H2O和OH-反应生成HCO3-,反应如下:
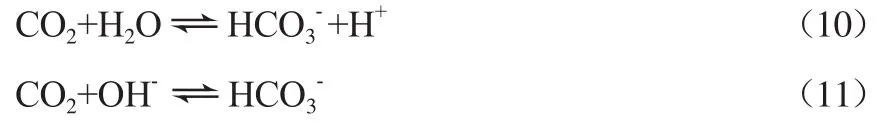
1.2 研究现状
为提高捕集效率,化学溶剂吸收法研究的重点主要集中在吸收剂的筛选、反应器的选择、反应机理的研究和操作条件的确定等方面,而吸收剂是化学溶剂吸收法脱除CO2的核心,所以对吸收剂的筛选和改良一直是各国研究者努力的方向[13]。当前化学溶剂吸收法常用的吸收剂包括:醇胺溶液、氨水、碳酸钾溶液、氨基酸盐溶液和离子液体[14]。
利用醇胺溶液作为吸收剂捕集CO2是非常成熟的工艺[15]。由于传统的单一有机胺溶液吸收CO2存在各自的缺陷,当前研究的方向主要为混合胺溶剂[16-17]。主要思路是根据不同类型醇胺溶液吸收CO2的特点,合理选择不同醇胺进行混合,改变溶液的整体性质,从而改善CO2吸收过程,提高吸收效率。但该吸收剂具有腐蚀性,且抗氧化降解和热降解能力差、挥发性强、再生能耗高。
氨水具有吸收容量大、再生能耗低、不易降解等优点[18],且可实现多种酸性气体(如SO2,NOx,HCl,CO2,HF)的联合脱除[19]。但氨水吸收剂易挥发的问题限制了其进一步发展,当前针对氨水吸收剂研究的热点是向其中添加活化剂和氨挥发抑制剂[20]。
碳酸钾溶液具有成本低、再生能耗小、稳定性高等优点,但以碳酸钾溶液作为CO2吸收剂存在一个明显缺点,即吸收反应速率慢。因此,在碳酸钾溶液中加入高效活化剂(如无水哌嗪、单乙醇胺、氨基酸等)是解决上述问题的主要方法[21-22]。
氨基酸盐溶液吸收CO2具有与醇胺溶液相当的吸收性能和吸收容量,且氨基酸盐类还具有低挥发性和抗氧化降解能力强等优点[23]。在众多的氨基酸盐中,对肌氨酸盐、甘氨酸盐、脯氨酸盐、丙氨酸盐的研究较多。由于氨基酸盐能够形成较稳定的氨基甲酸盐,故相对于醇胺溶液其再生能耗相对比较高[24]。
离子液体是近年来发展起来的新型CO2吸收剂[25],其蒸气压非常低,挥发性小,再生能耗低,且在反应过程中不会产生有害气体。但离子液体合成过程复杂,价格高昂[26],这些缺点限制了离子液体捕集CO2技术的进一步发展。
现有的CO2捕集技术主要是利用醇胺类及其组合溶液,但由于再生过程能耗较大,约占整个捕集过程能耗的60%[27],因而在经济性方面难以承受。开发新的低成本、低能耗的CO2吸收剂是目前学术界研究的热点。相变溶剂由于在吸收过程中出现吸收剂-吸收产物的分相现象[28],可大幅降低再生过程的能耗,故被认为是理想的CO2吸收剂[29]。
2 新型相变溶剂
根据反应产物的形态可将相变溶剂分为两类,一类是液-固相变溶剂,即反应产物在吸收CO2后以固态形式析出,经分离后热解再生,吸收剂得以重复利用。这种再生产物几乎不包含物理水,从而避免了解吸过程中因水分离而需的大量汽化潜热,再生过程能耗得以大幅降低。另一类是液-液相变溶剂,即反应产物在吸收CO2后仍以液相形式存在,但因CO2负载量不同,贫液和富液分为上下两层,经分离后可将下层的富液送入解吸塔,上层的贫液则返回吸收塔重新使用。与传统的化学吸收法相比,由于进入解吸塔的富液量大幅减小,再生能耗显著降低。
2.1 液-液相变溶剂
为了寻找潜在的相变溶剂,Xu等[30]利用半间歇式反应器对12种不同浓度的单胺和混合胺进行CO2吸收实验,分别测定计算了各溶剂最大CO2负载量和反应速率,并利用滴定法确定了相变溶剂分层后上下两相的CO2负载量。实验结果显示,3 mol/L 1,4-丁二胺(BDA,伯胺)和3 mol/L 1,6-己二胺(HAD,伯胺)在CO2负载量和反应速率方面均优于其他溶剂,且2 mol/L N,N-二甲基丁胺(DMBA,叔胺)和4 mol/L二乙氨基乙醇(DEEA,叔胺)混合溶液吸收CO2后具有良好的液-液相变性能。在此基础上,他们还系统研究了BDA和DEEA组成的高效两相吸收剂[31],并确定最佳配比为2 mol/L BDA+4 mol/L DEEA,其在吸收CO2后出现分相现象,下层CO2的量可达总吸收量的97.4%,且其循环负载量高于其他浓度配比和5 mol/L单乙醇胺(MEA,常用吸收剂)。2 mol/L BDA+4 mol/L DEEA混合溶液发生液-液分相的机制是由于伯胺BDA与CO2有很快的反应速率,CO2通入到混合溶液后首先与BDA反应,且DEEA在BDA与CO2的反应产物中的溶解度很低,同时DEEA的密度较小,于是DEEA从混合溶液中分离出来并转移至上层,BDA则停留在下层;当BDA与CO2反应达到平衡后,叔胺DEEA才开始与CO2反应,其反应产物可与BDA和CO2的反应产物互溶,故DEEA与CO2的反应产物转移至下层。之后的溶解度实验证实了2 mol/L BDA+4 mol/L DEEA的液-液分相机制[32]。
Ciftja等[33]系统研究了DEEA和N-甲基-1,3-丙二胺(MAPA,仲胺)混合溶液吸收CO2的特性,并发现5 mol/L DEEA+2 mol/L MAPA混合溶液在吸收一定量CO2后会出现明显的液-液分层现象。分别对分层后的上下两相进行核磁共振分析,结果显示下层溶液主要包括CO2和MAPA,而上层溶液主要是DEEA且几乎没有CO2。在此基础上,Pinto[34]提出了5 mol/L DEEA+2 mol/L MAPA混合溶液吸收CO2的液-液分层过程:MAPA与CO2迅速反应,CO2通入到混合溶液后首先与MAPA溶液反应并存于溶液底部,当MAPA全部负载CO2后,DEEA开始吸收CO2并向下层转移。这与Xu等[32]得到的2 mol/L BDA+4 mol/L DEEA的相变机理基本一致。并且,随着更多的CO2通入到混合溶液体系中,更多的DEEA会转移至下层,下层溶液的体积也会逐渐增大。此外,DEEA-MAPA相变溶剂吸收CO2体系结合了仲胺的高吸收速率和叔胺的高吸收容量,MAPA具有与CO2反应的高反应速率,而DEEA具有吸收CO2的高吸收容量。
亲脂性胺具有低临界温度的特点,随着温度的升高,胺在水中的溶解度会逐渐降低。通过加热可使胺溶液发生液-液或液-固分离。Zhang等[35]对亲脂性胺类进行了一系列研究,提出含有吸收剂和活化剂的亲脂性胺的热致两相溶剂体系可以解决溶剂再生过程的高能耗问题。Zhang等[36]在25~90℃下研究了伯胺、仲胺和叔胺等30多种亲脂性胺的相变温度、CO2负载量、反应动力学和再生性能。通过实验筛选出的两种混合吸收剂N,N-二甲基环己胺(DMCA,叔胺)+A1(一种仲烷基胺)和A1+B1(一种位阻烷基胺)在CO2负载、溶剂再生性能和化学稳定性方面表现出优于传统链烷醇胺的特性,而解吸温度可降至80 ℃左右,从而大幅降低能耗。在两种混合吸收剂DMCA+A1和A1+B1吸收CO2的过程中,A1作为吸收活化剂加速吸收过程,而DMCA和B1常作为再生促进剂促进再生过程。筛选实验表明伯胺和仲胺在反应过程中常作为吸收活化剂而叔胺常作为再生促进剂。在此基础上,Zhang等[37]对DMCA+A1相变溶剂进行了更深入研究,并开发出α-DMCA(A1与DMCA的摩尔比为1)试剂,具有高CO2负载量(3.34 mol/L,30 ℃)和高再生率(98%,80 ℃)。为进一步降低解吸能耗,Zhang等[38]采用搅拌、超声、溶剂萃取等方法来强化解吸过程。实验结果表明,利用惰性疏水性溶剂萃取可将解吸温度降至40~50 ℃,通过多级萃取再生系统可将90%以上的CO2解吸出来。此外,他们还对热致两相溶剂的气液平衡、起泡、挥发性和降解进行了全面研究,并提出了一系列相应问题的解决方法。
Raynal等[39-40]开发了DMXTM相变溶剂,该吸收剂吸收CO2后变成两相,CO2集中于其中一相。分相后的CO2贫液被送至吸收塔循环吸收,而CO2富液被送至再生塔再生。相对于再生能耗为3.7 GJ/t(以CO2计,下同)的MEA溶剂,针对DMXTM相变溶剂开发的DMXTM工艺的再生能耗只有2.3 GJ/t,在一定条件下再生能耗甚至可降至2.1 GJ/t,具有很大的发展潜力。
2.2 液-固相变溶剂
基于液-固相变的吸收剂也取得了一定进展。Ma’mun等[41]对5 mol/L的肌氨酸钾盐吸收CO2的特性进行了一系列研究,利用自建的实验装置分别测定了CO2在溶液中的平衡溶解度、气-液-固平衡温度、蒸气压和反应热。实验结果显示,当溶液CO2负载量大于0.52 mol/mol(以肌氨酸钾盐计)时,溶液中开始观察到沉淀和结晶,利用聚焦光束反射测定仪对沉淀颗粒的粒径进行现场监测,发现晶体粒径随CO2负载量的增加而增大。此外,当肌氨酸钾盐溶液中开始形成沉淀时,CO2吸收反应速率会出现加快的现象。在此基础上,他们总结出肌氨酸钾盐溶液体系吸收CO2的3点优势:1)相比于常规MEA吸收剂,肌氨酸钾盐溶液体系的挥发性更小;2)肌氨酸钾盐溶液与MEA相比具有更高的吸收速率和更高的循环负载量,其净循环能力比MEA高34%;3)当溶液中产生沉淀时,CO2与溶液之间具有更强的驱动力,故可保持较高的吸收速率。
高浓度碳酸钾溶液吸收法也是一种广受关注的固-液相变吸收技术,其主要原理是以易溶的高浓度碳酸钾溶液为吸收剂,吸收CO2后生成溶解度较小的碳酸氢钾并沉淀析出,其中碳酸氢钾结晶送入解析塔再生后再次制成碳酸钾吸收液。Zhang等[42]对碳酸钾/碳酸氢钾(PCB)相变体系进行了一系列研究,考察了解吸温度、PCB浓度和CO2负载量对解吸过程的影响。实验结果表明,提高解吸温度、PCB浓度或碳酸钾转化率可显著降低解吸过程所需热量,质量分数为50%的PCB溶液在160 ℃、碳酸钾转化率为80%的工艺(PCB50-80)条件下,解吸过程所需的总热量可降至2 172 kJ/kg,而5 mol/ L MEA在108 ℃条件下解吸过程所需总热量为4 300 kJ/kg;100 ℃条件下,解吸过程所需总热量为6 200 kJ/kg。Ye等[43]利用结晶反应器探讨了搅拌速率、结晶温度、平均停留时间和相对过饱和度等因素对碳酸氢钾结晶生长速率的影响。结果表明,晶体的生长速率依赖于晶体的尺寸,随晶体粒径的增大而加快,且当晶体临界尺寸达到约600 μm时开始趋于平稳。此外,增大搅拌速率可加快晶核形成,但会减慢晶体的生长,最终导致晶体粒径减小。在此基础上,建立了用于描述晶体生长速率和预测晶体平均粒径的模型。
Sanchez-Fernandez等[44-45]提出了牛磺酸钾和α-丙氨酸钾吸收烟气中CO2的工艺(DECAB工艺和DECAB Plus工艺)。该工艺吸收CO2后可产生氨基酸和碳酸氢盐沉淀。研究发现,牛磺酸钾溶液吸收CO2过程中固相的形成对吸收过程和解吸过程均有益:在CO2吸收过程中,固相反应产物的形成可促进反应平衡向生成反应产物的方向移动,从而加强吸收过程;在解吸过程中,液-固分离可在汽提塔内形成低pH环境,从而加强解吸过程。DECAB工艺和DECAB Plus工艺的主要优势包括:1)低能耗,DECAB Plus工艺过程能耗仅为传统MEA溶剂的65%,约为2.40 GJ/t;2)环境影响小,分离过程使用的吸收剂为氨基酸盐溶液,基本无大气污染物排放;牛磺酸钾溶液不易降解,故吸收过程中产生的降解产物少;氨基酸盐的毒性远低于常规链烷醇胺吸收剂;3)相比于MEA,牛磺酸盐对设备的腐蚀性更小。
表1列出了5 mol/L MEA及上文提到的几种相变吸收工艺的再生能耗数据。表中数据表明,相比5 mol/L MEA吸收剂,几种相变溶剂吸收工艺吸收CO2的再生能耗均降低40%左右。因此,相变溶剂类吸收剂具有巨大的节能潜力。

表1 几种吸收剂/工艺的再生能耗比较
3 结语
化学溶剂吸收法是目前最为成熟的CO2燃烧后捕集技术,常用的吸收剂有醇胺溶液、氨水、碳酸钾溶液、氨基酸盐溶液和离子液体,其中醇胺溶液类吸收剂应用最为广泛。但再生能耗高是化学溶剂吸收法捕集CO2技术面临的最大挑战。新型相变溶剂是理想的CO2吸收剂,用其捕集CO2可有效降低吸收剂的再生能耗。总体而言,现有研究对相变溶剂的开发及胺类的配比优化提供了有益参考,并分析了相变溶剂的生成产物及其在两相中的分配规律。然而,目前对于利用相变溶剂吸收CO2的传质反应动力学研究较少,尤其缺乏CO2在相变溶剂中的传质机理及过程分析。此外,不同类型相变溶剂的挥发和降解特性尚研究不足。以上两点应作为今后相变溶剂领域研究的重点。
[1] 姜大膀,富元海. 2 ℃全球变暖背景下中国未来气候变化预估[J]. 大气科学,2012,36(2):234 - 246.
[2] Specht E,Redemann T,Lorenz N. Simplified mathematical model for calculating global warming through anthropogenic CO2[J]. Int J Therm Sci,2016,102:1 - 8.
[3] Tan Yuting,Nookuea W,Li Hailong,et al. Property impacts on Carbon Capture and Storage(CCS)processes:A review[J]. Energy Convers Manage,2016,118:204 - 222.
[4] Mondal M K,Balsora H K,Varshney P. Progress and trends in CO2capture/separation technologies:A review[J]. Energy,2012,46(1):431 - 441.
[5] Rabensteiner M,Kinger G,Koller M,et al. Pilot plant study of aqueous solution of piperazine activated 2-amino-2-methyl-1-propanol for post combustion carbon dioxide capture[J]. Int J Greenh Gas Con,2016,51:106 - 117.
[6] Liang Zhiwu,Rongwong W,Liu Helei,et al. Recent progress and new developments in post-combustion carbon-capture technology with amine based solvents[J]. Int J Greenh Gas Con,2015,40:26 - 54.
[7] 陈健,罗伟亮,李晗. 有机胺吸收二氧化碳的热力学和动力学研究进展[J]. 化工学报,2014,65(1):12 - 21.
[8] Puxty G,Rowland R. Modeling CO2mass transfer in amine mixtures:PZ-AMP and PZ-MDEA[J]. Environ Sci Technol,2011,45(6):2398 - 2405.
[9] Hartono A,Svendsen H F. Kinetics reaction of primary and secondary amine group in aqueous solution of diethylenetriamine(DETA)with carbon dioxide[J]. Energy Procedia,2009,1(1):853 - 859.
[10] 李伟斌,董立户,陈健. 仲胺和叔胺水溶液吸收CO2的动力学[J]. 过程工程学报,2011,11(3):422 -428.
[11] Cullinane J T. Thermodynamics and kinetics of aqueous piperazine with potassium carbonate for carbon dioxide absorption[D]. Austin:The University of Texas at Austin,2005.
[12] 周旭萍,方梦祥,项群扬,等. 氨基酸盐吸收二氧化碳过程的传质特性[J]. 浙江大学学报:工学版,2016,50(2):312 - 319.
[13] Wang Meihong,Joel A S,Ramshaw C,et al. Process intensification for post-combustion CO2capture with chemical absorption:A critical review[J]. Appl Energy,2015,158:275 - 291.
[14] 方梦祥,周旭萍,王涛,等. CO2化学吸收剂[J]. 化学进展,2015,27(12):1808 - 1814.
[15] Rochelle G T. Amine scrubbing for CO2capture[J]. Science,2009,325(5948):1652 - 1654.
[16] Arshad M W,von Solms N,Thomsen K,et al. Heat of absorption of CO2in aqueous solutions of DEEA,MAPA and their mixture[J]. Energy Procedia,2013,37:1532 - 1542.
[17] Luo Xiao,Liu Sen,Gao Hongxia,et al. An improved fast screening method for single and blendedamine-based solvents for post-combustion CO2capture[J]. Sep Purif Technol,2016,169:279 - 288.
[18] Yu Jingwen,Wang Shujuan. Modeling analysis of energy requirement in aqueous ammonia based CO2capture process[J]. Int J Greenh Gas Con,2015,43:33 - 45.
[19] 曾庆. 氨法吸收二氧化碳的实验研究[D]. 北京:清华大学,2011.
[20] Yu Jingwen,Wang Shujuan,Yu Hai. Experimental studies and rate-based simulations of CO2absorption with aqueous ammonia and piperazine blended solutions[J]. Int J Greenh Gas Con,2016,50:135 - 146.
[21] 申淑锋. 基于碳酸钾溶液吸收CO2的研究进展[J]. 河北科技大学学报,2013,34(2):142 - 146.
[22] Yoon Yeoil,Nam Sungchan,Jung Sunkwan,et al. K2CO3/hindered cyclic amine blend(SEFY-1)as a solvent for CO2capture from various industries[J]. Energy Procedia,2011,4:267 - 272.
[23] Wei Chiao-Chien,Puxty G,Feron P. Amino acid salts for CO2capture at fl ue gas temperatures[J]. Chem Eng Sci,2014,107:218 - 226.
[24] Knuutila H,Aronu U E,Kvamsdal H M,et al. Post combustion CO2capture with an amino acid salt[J]. Energy Procedia,2011,4:1550 - 1557.
[25] 孙雅钗,朱佳媚,钟昌祥,等. 硅胶固载季鏻离子液体CO2的吸附[J]. 化工环保,2015,35(4):414 -419.
[26] 樊丽华,聂阳,梁英华. 离子液体吸收CO2的研究进展[J]. 化工环保,2010,30(2):136 - 140.
[27] Kim Huiyong,Lee Kwang Soon. Design guidance for an energy-thrift absorption process for carbon capture:Analysis of thermal energy consumption for a conventional process configuration[J]. Int J Greenh Gas Con,2016,47:291 - 302.
[28] Pinto D D D,Knuutila H,Fytianos G,et al. CO2post combustion capture with a phase change solvent:Pilot plant campaign[J]. Int J Greenh Gas Con,2014,31:153 - 164.
[29] 张政,刘彪,覃显业,等. 相变溶剂吸收CO2研究进展[J]. 材料导报,2014,28(21):94 - 99.
[30] Xu Zhicheng,Wang Shujuan,Zhao Bo,et al. Study on potential biphasic solvents:Absorption capacity,CO2loading and reaction rate[J]. Energy Procedia,2013,37:494 - 498.
[31] 徐志成,王淑娟,陈昌和. BDA/DEEA两相吸收剂吸收CO2的研究[J]. 工程热物理学报,2013,34(5):993 - 997.
[32] Xu Zhicheng,Wang Shujuan,Chen Changhe. CO2absorption by biphasic solvents:Mixtures of 1,4-butanediamine and 2-(diethylamino)-ethanol[J]. Int J Greenh Gas Con,2013,16:107 - 115.
[33] Ciftja A F,Hartono A,Svendsen H F. Experimental study on phase change solvents in CO2capture by NMR spectroscopy[J]. Chem Eng Sci,2013,102:378 - 86.
[34] Pinto D D D,Zaidy S A H,Svendsen H F,et al. Evaluation of a phase change solvent for CO2capture:Absorption and desorption tests[J]. Int J Greenh Gas Con,2014,28:318 - 327.
[35] Zhang Jiafei,Qiao Yu,Wang Wanzhong,et al. Development of an energy-ef fi cient CO2capture process using thermomorphic biphasic solvents[J]. Energy Procedia,2013,37:1254 - 1261.
[36] Zhang Jiafei,Qiao Yu,Agar D W. Improvement of lipophilic-amine-based thermomorphic biphasic solvent for energy-ef fi cient carbon capture[J]. Energy Procedia,2012,23:92 - 101.
[37] Zhang Jiafei,Agar D W,Zhang Xiaohui,et al. CO2absorption in biphasic solvents with enhanced low temperature solvent regeneration[J]. Energy Procedia,2011,4:67 - 74.
[38] Zhang Jiafei,Qiao Yu,Agar D W. Intensi fi cation of low temperature thermomorphic biphasic amine solvent regeneration for CO2capture[J]. Chem Eng Res Des,2012,90(6):743 - 749.
[39] Raynal L,Alix P,Bouillon P A,et al. The DMX™process:An original solution for lowering the cost of post-combustion carbon capture[J]. Energy Procedia,2011,4:779 - 786.
[40] Aleixo M,Prigent M,Gibert A,et al. Physical and chemical properties of DMXTMsolvents[J]. Energy Procedia,2011,4:148 - 155.
[41] Ma’mun S,Kim I. Selection and characterization of phase-change solvent for carbon dioxide capture:Precipitating system[J]. Energy Procedia,2013,37:331 - 339.
[42] Zhang Shihan,Ye Xinhuai,Lu Yongqi. Development of a potassium carbonate-based absorption process with crystallization-enabled high-pressure stripping for CO2capture:Vapor-liquid equilibrium behavior and CO2stripping performance of carbonate/bicarbonate aqueous systems[J]. Energy Procedia,2014,63:665 -675.
[43] Ye Qing,Wang Xinlei,Lu Yongqi. Kinetic behavior of potassium bicarbonate crystallization in a carbonatebased CO2absorption process[J]. Chem Eng Res Des,2015,93:136 - 147.
[44] Sanchez-Fernandez E,de Miguel Mercader F,Misiak K,et al. New process concepts for CO2capture based on precipitating amino acids[J]. Energy Procedia,2013,37:1160 - 1171.
[45] Sanchez-Fernandez E,Heffernan K,van der Ham L,et al. Precipitating amino acid solvents for CO2capture:Opportunities to reduce costs in post combustion capture[J]. Energy Procedia,2014,63:727 - 738.
(编辑 魏京华)
Research progresses in CO2capture technology using phase change solvents
An Shanlong,Wang Lidong,Yu Songhua,Wu Siyu
(School of Environmental Science and Engineering,North China Electric Power University,Baoding Hebei 071003,China)
Chemical solvent absorption method is the most used technology for post-combustion capture of CO2. The mechanism and research status of chemical solvent absorption method are introduced. Several kinds of common CO2absorbents are compared by their advantages and disadvantages. The research progresses on two new phase change absorbents(liquid-liquid phase change solvent and liquid-solid phase change solvent)are explained. It is pointed out that:The new phase change solvents are ideal CO2absorbents,which can effectively reduce the energy consumption of absorbent regeneration after CO2capture;The future research should be focused on the mass transfer reaction kinetics for CO2absorbed by phase change solvent and the volatilization and degradation characteristics of different phase change solvents.
carbon dioxide;chemical absorption;phase change solvent
X701
A
1006-1878(2017)01-0031-07
10.3969/j.issn.1006-1878.2017.01.006
2016 - 07 - 01;
2016 - 11 - 18。
安山龙(1991—),男,河北省新乐市人,硕士生,电话 18331126652,电邮 anshanlong136@163.com。
中央高校基本科研业务费项目(2016ZZD08)。
