低温水热法制备竹生物炭及其对有机物的吸附性能
2017-01-09单胜道杨瑞芹盖希坤毛建卫黄宁宁钭焱萍MeasArun
李 音,单胜道,杨瑞芹,盖希坤,毛建卫,黄宁宁,钭焱萍,Meas Arun
低温水热法制备竹生物炭及其对有机物的吸附性能
李 音1,2,单胜道1,杨瑞芹1,盖希坤1,毛建卫1,黄宁宁1,钭焱萍1,Meas Arun1
(1. 浙江省农产品化学与生物加工技术重点实验室,浙江科技学院生物与化学工程学院,杭州 310023; 2. 浙江大学生物质化工教育部重点实验室,杭州 310027)
竹是一类常见的生物质资源,竹加工中产生的废弃物是制生物炭的理想原料。该研究采用水热炭化法,在较低的水热温度下制备竹生物炭,并通过NaOH浸泡和N2氛围下高温煅烧2种方法,对竹生物炭进行进一步改性,所得产品用于去除水溶液中2-萘酚和刚果红。结果显示:仅采用水热炭化得到的竹生物炭产品得率大于54%,表面官能团丰富,均能吸附水溶液中的2-萘酚和刚果红,其中160 ℃3 h下制备的样品对2-萘酚吸附效果最好,200 ℃7 h下制备的样品对刚果红吸附效果最好;改性处理会降低终产品得率并影响表面官能团,NaOH浸泡改性处理能增加竹生物炭对2-萘酚和刚果红的吸附容量,N2氛围下高温煅烧改性则不能提高竹生物炭对这2种物质的吸附效果。研究结果可为废弃生物质制炭及生物炭在水污染物吸附分离中的应用提供参考。
生物质;吸附;炭化;竹;水热法;2-萘酚;刚果红
0 引 言
竹是一类常见的生物质资源,在中国分布广泛。竹适应性强、生长快、成材早、产量高,一般栽种成活2~3 a后便可砍伐利用,是优良的可再生资源,被广泛应用于建筑、造纸、纺织、手工业、食品、能源等各种行业[1-3]。目前竹的利用以竹纤维为主,竹纤维加工过程中往往产生大量废弃物和剩余物,不经处理直接丢弃不仅造成资源浪费,还会造成环境污染[4]。竹废料主要含纤维素、半纤维素和木质素[3,5],是制生物炭的理想原料。
生物炭是指生物质在高温、缺氧条件下形成的稳定的富含碳的固体。生物炭可作为能源直接使用,也可作为功能性材料使用,如生物炭作为土壤改良剂可改善土壤肥力、促进作物生长,并抑制温室气体的释放,另外,生物炭作为吸附剂可吸附土壤或水体中的污染物,起到环境修复的作用[6-8]。因此,将废弃生物质转化成生物炭是一种有效固碳和生物质资源化的方法。由于生物炭具有较大的比表面积,丰富的表面官能团,近年来,其作为吸附剂被越来越多地用于水处理领域[9-13]。生物炭可由热解炭化或水热炭化两种方法制得[9,14]。其中热解炭化是指将生物质在惰性气氛下加热到较高温度并停留一定时间使其炭化的方法[14];水热炭化则指以水为反应介质,密闭体系中,在一定温度下(130~350 ℃),水自身产生压力或惰性气体加压下,生物质发生一系列复杂反应从而炭化转化成生物炭的过程[14-17]。与传统的热解炭化相比,水热炭化的特点在于:首先,由于水热炭化在水溶液中进行,不仅可直接处理高含水率的原料,还有助于生物炭表面含氧、含氮官能团的保留;另外,水热炭化设备操作简便,通常在较温和的反应条件下进行,且水热过程中发生的脱水脱羧反应能释放出一部分能量,能耗较低[14,18]。竹的热解炭化已有较多的研究与应用[19-21],制得的产品可作为生物质燃料,也可作为吸附剂使用。竹热解炭表面官能团保留较少,在用作吸附剂时,可使用化学试剂处理增加表面氧、氮官能团,以增加吸附活性与选择性[3]。水热炭化法由于其特点,有望克服热解炭化法难以保留生物质表面官能团的缺点,成为制备竹生物炭吸附剂的理想方法。竹在190 ℃下草酸溶液中的水热炭化已有报道[22],然而该文献未对竹水热炭的吸附性能进行研究与优化。
本研究拟以竹废弃物为原料,采用水热炭化法制备竹生物炭,以2-萘酚和刚果红作为芳香有机化合物和染料分子的模型物,探索竹生物炭对水溶液中这两种污染模型物的吸附去除作用;目的在于探索以水热炭化法制备表面官能团丰富、对有机污染物吸附效果良好的竹生物炭吸附剂的可行性,并优化竹水热炭吸附剂的制备条件。
1 材料与方法
1.1 试验材料
竹废弃物购自浙江省安吉县某企业。2-萘酚与刚果红均为分析纯,分别购自江苏永华精细化学品有限公司与精细化工研究所,去离子水由Milipore Direct-Q 3纯水系统制得。
1.2 竹生物炭的制备与改性
称取约5.0 g竹粉置于带聚四氟乙烯内衬的水热合成反应釜中,加入50 mL去离子水,密闭水热釜,于一定温度下碳化数小时。达到设定时间后,取出放入冷水中冷却至室温,开釜导出混合物,过滤分离,固相产物即为生物炭样品。每一样品均平行制备2份,其中一份以50 mL去离子水水洗后过滤分离,重复水洗3次后于烘箱中105 ℃下烘干至恒重,转移至干燥器中冷却至室温,用于后续吸附;另一份不经水洗,于相同条件下干燥后,用于后续生物炭的改性。
以吸附效果较优的竹生物炭为原料,采用NaOH溶液浸泡和N2氛围高温煅烧两种方法对水热炭化制得的竹生物炭进行改性。NaOH溶液浸泡改性的处理过程为:称取一定量的竹生物炭浸泡于1 mol/L的NaOH溶液中,一定时间后,过滤,固体产物用去离子水洗涤至洗涤液呈中性,于烘箱中105 ℃下烘干至恒重,转移至干燥器中冷却至室温,备用。N2高温煅烧改性的处理过程为:称取一定量的竹生物炭置于石英舟内,放入高温管式炉中,于一定温度下在N2气氛中煅烧4 h,冷却至室温后放入干燥器中干燥,备用。
所制得的竹生物炭样品以制备条件和改性条件命名,得率以样品干质量与原料干质量的比值计算。具体样品名称和制备工艺如表1所示。

表1 竹生物炭样品的制备工艺
1.3 竹生物炭的表征
灰分采用灼烧法测定,灼烧条件为空气中550 ℃下灼烧3 h。采用Bruker Vertex V70红外光谱仪对竹生物炭的表面官能团进行了表征。竹生物炭的BET比表面积采用氮气吸附-脱附法测定,在Quantachrome Autosorb iQ气体吸附分析仪上进行,样品预处理条件为100 ℃下真空脱气3 h。竹生物炭中的C、H、O、N、S元素含量采用Vario MICRO cube元素分析仪分析。以S-3700N(Hitachi)扫描电镜观察竹生物炭的形貌特征。
1.4 竹生物炭对2-萘酚和刚果红的吸附
称取约0.1000 g的竹生物炭样品若干份,分别置于150 mL具塞锥形瓶中,分别加入50 mL的具有一定浓度梯度的吸附质溶液(2-萘酚、刚果红)于以上锥形瓶中,置于25 ℃、转速为170 r/min的恒温振荡器中振荡9 h以确保吸附达到平衡。吸附后溶液中吸附质的浓度由紫外可见分光光度计(元析UV-5500PC)测定,萘酚的检测波长为274 nm,刚果红为499 nm。以式(1)计算平衡吸附量
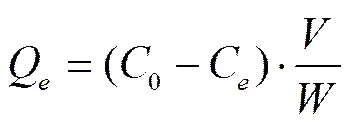
式中Q为平衡吸附量,mg/g;0为初始浓度,mg/mL;C为平衡浓度,mg/mL;为溶液体积,mL;为竹生物炭质量,g。
以平衡浓度C为横坐标,平衡吸附量Q为纵坐标作图,可得两种吸附质在不同生物炭样品表面的吸附等温线。吸附等温线用Langmuir和Freundlich方程进行拟合。
Langmuir方程
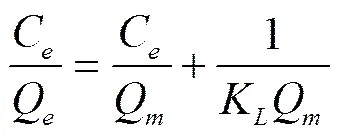
Freundlich方程
(3)
以上二式中,Q为单分子层最大吸附量,mg/g;K为Langmuir常数;K为与吸附剂的饱和吸附量有关的Freundlich常数;是与吸附剂表面非均匀性以及吸附作用强弱有关的经验常数。
2 结果与讨论
2.1 竹生物炭得率
竹生物炭的得率如图1所示。未经改性的竹生物炭得率在54.12%~71.53%之间,160 ℃下水热炭化的样品得率随着炭化时间的延长而下降,200 ℃下制得的各生物炭则得率相当,炭化时间对生物炭得率没有显著影响,在相同的炭化时间下,200 ℃下制得的样品得率略低于160 ℃下制得的样品。其中,160 ℃、3 h条件下制得的竹生物炭得率最高,为71.53%。生物质的水热炭化一般认为经历了水解、脱水、脱羧、芳香化、缩聚等过程[16-17],其中水解是起始反应,且反应温度较低(100~170 ℃)[23],而脱水、芳香化、缩聚等炭化过程则需要有更高的反应温度(160~280 ℃)[24],因此推测,较低的温度下炭化并不完全,较高的反应温度和较长的水热炭化时间均有利于炭化过程的进行从而引起质量的损失和产率的下降。
生物炭经2种方法改性后得率进一步下降,其中N2煅烧处理后的样品(得率12.99%~16.21%)质量损失较大,远大于经NaOH浸泡处理后的样品(得率36.93%~62.61%)。这可能是因为经N2氛围高温煅烧的生物炭样品发生进一步热解,H、O组分大量损失导致最终样品的得率较低[14];NaOH浸泡处理则在常温下进行,且NaOH只与原料生物炭样品的表面进行接触、发生反应,改性只在表面进行,因此生物炭质量损失较小。不同的N2煅烧温度和不同的NaOH浸泡时间对生物炭样品的得率影响不大。
2.2 竹生物炭的表面改性
竹生物炭样品160-3和200-7以及改性后样品的FTIR谱图如图2所示。由图2可见,仅水热炭化得到的竹生物炭样品表面的官能团与原料相比1700 cm-1附近羧酸的C=O吸收峰消失,这可能是由于水热炭化过程中的脱羧反应[16-17],其他官能团并未发生明显变化,竹生物炭保有丰富的含氧官能团如-OH(3 200~3 600 cm-1)、C=O(1 650~1 735 cm-1)、C-O(1 000~1 250 cm-1)等。经NaOH浸泡改性的竹生物炭样品与改性前相比表面官能团未发生明显改变,1 650 cm-1左右的峰出现了裂分,这可能是由NaOH与竹生物炭表面的酸性官能团反应生成盐所造成的[25-26],由此推测NaOH浸泡会在一定程度上改变生物炭表面的酸碱性。经N2氛围下高温煅烧改性后,竹生物炭表面各含氧官能团的吸收峰均大幅减弱,几乎完全消失,仅剩1 650 cm-1左右的C=O还有少量残留。
表2列出了部分生物炭样品的灰分、比表面积与元素组成。从表中可以看出,仅水热炭化制备的竹生物炭比表面积较小,两种改性方式均能有效增加竹生物炭的比表面积。其中N2氛围下高温煅烧改性能将改性后竹生物炭的比表面积提高到52.39 m2/g,结合红外光谱图来看,N2氛围下高温煅烧能使原本炭化程度较低的竹生物炭样品发生进一步炭化,损失有机组分、产生孔道, NaOH则能与生物炭表面的某些官能团发生反应,溶解部分有机质,生成新的孔道,提高终产物的比表面积。此外,从元素分析的结果来看,NaOH浸泡改性后,C元素的比例并未增加,C/H比反而稍有下降,O元素的含量则略有上升,这说明NaOH浸泡不能进一步增加竹生物炭的炭化程度,但有助于含氧官能团的保留。与此相反的是,N2氛围下高温煅烧后O元素含量大幅下降,C元素比例显著升高,C/H比大大提升,这也佐证了此前的推论,即N2氛围高温煅烧后的生物炭样品进一步热解炭化,H、O组分大量损失,芳香性增加,炭化程度进一步提高。竹废弃物的灰分测定值为1.33%,样品200-7的灰分与原料相比有所降低,两种改性方式则均使最终产物的灰分增加。水热炭化过程中,水不仅作为反应物参与炭化反应,还能作为溶剂溶解生物炭表面的无机矿物,这可能是水热炭化产物灰分较低的原因[27]。NaOH浸泡能增加竹生物炭表面的无机矿物,N2氛围下高温煅烧则能使灰分在煅烧过程中积累,因此,改性后的竹生物炭灰分增加[28]。总体来看,竹生物炭样品的灰分较低,将竹生物炭用于水溶液中污染物的吸附分离将不会造成二次污染[10]。
a. N2煅烧改性前后的竹生物炭
a. Bamboo biochars with and without modification by calcination in N2
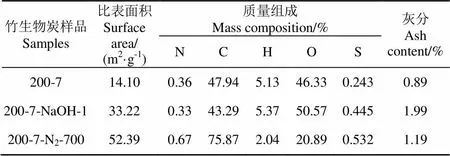
表2 部分竹生物炭样品的灰分、比表面积与元素组成
从扫描电镜(SEM)照片(如图3所示)来看,水热炭化前后,生物炭的整体结构发生了明显收缩,但纤维状结构的形貌没有发生明显变化。NaOH浸泡改性后的竹生物炭表面与改性前相比变得略为粗糙,显示出该样品可能出现了一些新的孔结构。N2氛围下高温煅烧后的生物炭与文献报道的竹热解炭具有类似的结构[29],与改性前相比形貌发生了较大变化,褶皱增多,结构进一步收缩,表面更显粗糙,显示出该样品的孔道结构与煅烧前相比可能出现了改变,在其他生物质的热解炭化中也有类似的结果报道[30-31]。
100X 300X
a. 竹粉原料
a. Bamboo
100X 300X
b. 200-7
100X 300X
c. 200-7-NaOH-1
2.3 竹生物炭对2-萘酚和刚果红的吸附性能
25 ℃下,不同水热工艺条件下制得的竹生物炭对水溶液中2-萘酚和刚果红(初始质量浓度0.5 mg/mL)的饱和吸附量如图4所示。
从图4中可以看出,直接水热炭化制得的竹生物炭样品对2-萘酚的吸附量在22.9~50.3 mg/mL之间,对刚果红的吸附量在44.1~63.7 mg/mL之间,统计学检验显示竹生物炭对2-萘酚和刚果红的吸附量差异非常显著(<0.01)。总体而言,水热炭化温度和水热炭化时间对吸附均有影响,2-萘酚在160 ℃下制备的竹生物炭表面吸附量较高,刚果红则在200 ℃下制备的竹生物炭表面吸附量较高,但温度对样品吸附量的影响并不显著。在相同的炭化温度下,炭化时间越长,制得的生物炭样品越不利于2-萘酚的吸附,样品160-3的2-萘酚吸附量最高。在较低的炭化温度和较短的炭化时间下,生物质炭化不完全,所得生物炭既含有炭化组分也含有非炭化组分[32],非炭化组分即有机物含量高时,分配作用是主要的吸附机制,而随着炭化温度的升高和炭化时间的延长,生物炭的孔隙度和表面积增大,有机成分减少,对有机物的吸附以表面吸附作用为主[7,33],由此可见,以分配作用为主的吸附机制更适合于2-萘酚的吸附。与2-萘酚的吸附情况不同,相同炭化温度下,刚果红的吸附效果与炭化时间的长短没有表现出明显的线性关系,样品200-7的刚果红吸附量最大,因此推测,表面吸附作用的增加有利于刚果红在生物炭表面的吸附。此外,刚果红是一种分子量较大的阴离子染料,除了吸附和分配作用以外,孔隙的大小和生物炭表面官能团的分布也会对其吸附产生影响[2],样品200-7对刚果红较大的吸附量可能是以上因素共同作用的结果。
选择了对2-萘酚和刚果红吸附效果较好的样品160-3和200-7进行了进一步改性处理,并同样评价了它们对于水溶液中2-萘酚和刚果红的吸附效果。NaOH浸泡改性前后和N2煅烧改性前后的竹生物炭样品在25 ℃下对2-萘酚、刚果红的吸附等温线如图5、图6所示。
从图5可以看出,2-萘酚在NaOH浸泡改性前后各竹生物炭样品表面的等温吸附曲线基本呈线性,显示吸附作用以分配为主,刚果红的等温吸附曲线呈非线性,表明刚果红在竹生物炭样品表面的吸附并不以分配作用为主。另外,改性后的竹生物炭样品单位质量对于2-萘酚和刚果红的吸附能力均有所增加,其中样品200-7-NaOH-1对2-萘酚和刚果红均表现出最佳的吸附效果。与改性前的竹生物炭样品200-7相比,在2-萘酚和刚果红的平衡质量浓度均为0.3 mg/mL时,改性后生物炭样品200-7-NaOH-1对2-萘酚的吸附量由30.2mg/g提高到62.3mg/g,对刚果红的吸附量则由49.2mg/g提高到69.1mg/g,该样品的得率为37.94 %,将改性前后的样品质量损失考虑在内,改性前后样品对刚果红的吸附总量没有明显改变,对2-萘酚的吸附总量有了较大提高。这可能是因为NaOH浸泡在一定程度上改变了生物炭表面的酸碱性,并溶解了部分生物炭表面组分而使样品产生了一些新的孔道,从而提高了生物炭对2-萘酚的吸附效果,而刚果红分子体积较大,难以进入细小的孔道中,因此在改性后生物炭表面吸附量的增加不如2-萘酚显著。此外,NaOH浸泡时间与改性样品的吸附效果并未表现出线性关系,如200 ℃、7 h下制备的竹生物炭经NaOH浸泡改性后的各样品对2-萘酚的吸附表现为:样品200-7-NaOH-1在各平衡浓度下吸附量均最大,样品200-7-NaOH-3在较低的平衡浓度下(<0.3 mg/mL)吸附量小于样品200-7-NaOH-2,在较高的平衡浓度下(>0.3 mg/mL)吸附量大于样品200-7-NaOH-2,而这些样品对刚果红的吸附表现为:e(200-7-NaOH-1)>e(200-7-NaOH-2)>e(200-7-NaOH-3),由此可见,长时间的NaOH浸泡并不能持续增加生物炭对2-萘酚和刚果红的吸附容量,根据吸附质选择适宜的NaOH浸泡改性时间将有助于获得较好的吸附效果。
a. 2-萘酚
a. 2-naphthol
N2煅烧改性的结果与NaOH浸泡改性完全不同,从图6a可以看出,N2氛围下的高温煅烧改性并不能显著提高竹生物炭样品对于水溶液中2-萘酚的吸附量,相反的,样品160-3经高温煅烧后吸附量反而有所下降。由样品160-3在N2氛围下高温煅烧改性前后的红外光谱图可知,竹生物炭样品经高温煅烧后,表面官能团几乎损失殆尽,此时样品对2-萘酚的吸附主要以表面吸附作用为主,吸附等温线呈非线性,这并不利于2-萘酚与生物炭之间的相互作用以及吸附量的提高,这和我们此前推测的分配机制更有利于2-萘酚在竹生物炭表面吸附的推论相一致。与2-萘酚吸附不同的是,这些样品对刚果红的吸附量与改性前相比有了较大幅度的提升(图6b),其中,样品160-3-N2-800的刚果红吸附量最大,当平衡质量浓度为0.3 mg/mL时,吸附量由改性前的34.2 mg/g提高到76.0 mg/g,这可能是因为改性后的生物炭样品表面官能团稀少,从而使得这些样品与刚果红的相互作用以表面吸附为主,利于刚果红的吸附,这也与此前推测的吸附机制更利于刚果红吸附的推断吻合,同时,改性后竹生物炭比表面积的增加也有利于刚果红表面吸附的发生。然而,N2氛围下的高温煅烧将造成生物炭有机组分的大量损失,从而导致收率较低,因此,虽然此方法能提高最终产品单位质量对于刚果红的吸附,但并不能从整体上提高吸附效果。
a. 2-萘酚
a. 2-naphthol
为更好地对2-萘酚和刚果红在竹生物炭表面的吸附特性进行探讨,采用两种常用的等温吸附模型Langmuir方程和Freundlich方程对2-萘酚和刚果红在不同生物炭样品表面吸附的等温线进行了拟合。拟合参数如表3所示。
从表3中可以看出,对于2-萘酚在各竹生物炭样品表面的吸附,Langmuir模型拟合的相关系数略高于Freundlich模型拟合,对于刚果红的吸附,两模型拟合的相关系数则基本相当,且Langmuir模型拟合的相关系数除样品200-3-NaOH-1外均大于0.98,Langmuir模型是以吸附剂表面均匀、单分子层吸附、吸附质之间无相互作用为基本假设的理想模型,由此推测,2-萘酚和刚果红在竹生物炭样品上的吸附更接近于单分子层吸附。Freundlich方程参数1/可反映体系吸附作用力的强弱,1/值小于1显示优惠型吸附,大于1显示非优惠型吸附,本研究制备的样品中除160-3对刚果红吸附和200-3-NaOH-3对2-萘酚吸附外的1/值均小于1,可见2-萘酚和刚果红在大多数样品上的吸附均为优惠型吸附。另外,N2高温煅烧改性后的竹生物炭样品对于刚果红的吸附均显示出较其他样品高的Langmuir模型拟合相关系数,由此可见,此类样品对刚果红的吸附更符合理想表面的单分子层吸附,这也佐证了此类样品对刚果红的吸附机制以表面吸附为主的推论。
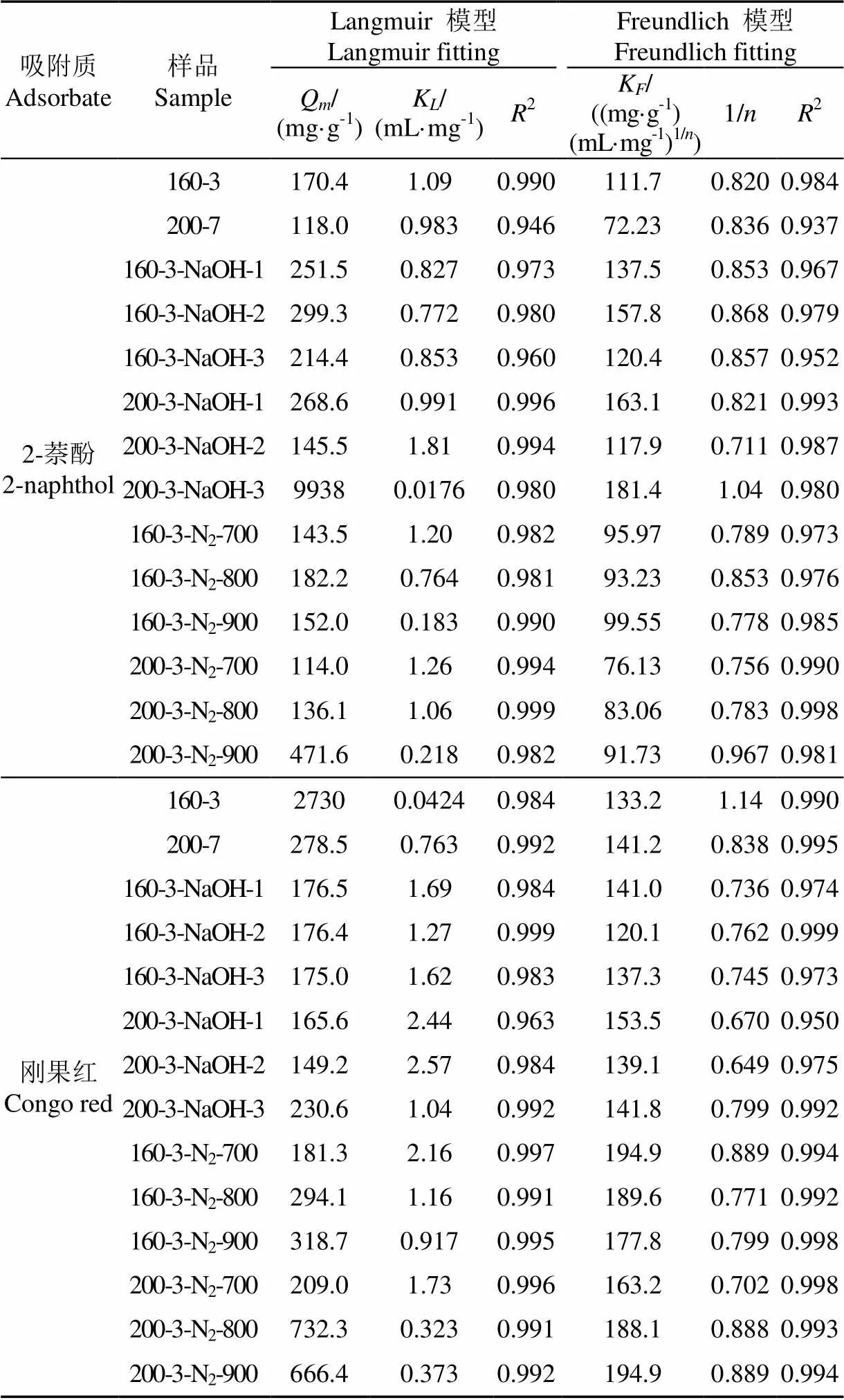
表3 25 ℃下2-萘酚、刚果红在竹生物炭上吸附等温线的模型拟合参数
3 结 论
1)水热炭化法制备的竹生物炭产率高(54.12%~71.53%)、表面官能团丰富,有望作为吸附剂用于水中有机污染物的吸附去除。
2)竹生物炭对2-萘酚和刚果红的吸附量差异显著,水热炭化温度和时间对竹生物炭的吸附效果均有影响。
3)NaOH浸泡改性是提高单位竹水热炭对2-萘酚和刚果红吸附效果的有效方式。其中吸附效果最佳的样品与改性前相比,在平衡质量浓度均为0.3 mg/mL时,对2-萘酚的吸附量由30.2mg/g提高到62.3mg/g,对刚果红的吸附量由49.2mg/g提高到69.1mg/g。
4)N2氛围下高温煅烧改性大幅降低了竹生物炭得率,并使官能团损失严重,无法从总体上提高竹水热炭对2种吸附质的吸附效果。
[1] 徐伟. 天然竹纤维的提取及其结构和化学性能的研究[D]. 苏州:苏州大学, 2006.
Xu Wei. Enxtraction of Natural Bamboo Fiber and the Research on its Structure and Chemical Properties[D]. Suzhou: Soochow University, 2006.(in Chinese with English abstract)
[2] 陆志科. 竹叶生物活性成分提取分离及其抗菌活性研究[D]. 长沙:中南林学院博士论文,2004.
Lu Zhike. Extraction&Isolation of Bio-activated Constituents in Bamboo Leaves and its Antifungi Activities[D]. Changsha: Central-South Forestry University, 2004.(in Chinese with English abstract)
[3] 辜夕容,邓雪梅,刘颖旎,等. 竹废弃物的资源化利用研究进展[J]. 农业工程学报,2016,32(1):236-242.
Gu Xirong, Deng Xuemei, Liu Yingni, et al. Review on comprehensive utilization of bamboo residues[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2016, 32(1): 236-242. (in Chinese with English abstract)
[4] Shen S, Nges I A, Yun J, et al. Pre-treatments for enhanced biochemical methane potential of bamboo waste[J]. Chem Eng J, 2014(240): 253-259.
[5] 蒋建新,杨中开,朱莉伟,等. 竹纤维结构及其性能研究[J]. 北京林业大学学报,2008,30(1):128-132.
Jiang Jianxin, Yang Zhongkai, Zhu Liwei, et al. Structure and property of bamboo fiber[J]. Journal of Beijing Forestry University, 2008, 30(1): 128-132. (in Chinese with English abstract)
[6] 李力,刘娅,陆宇超,等. 生物炭的环境效应及其应用的研究进展[J]. 环境化学,2011,30(8):1411-1421.
Li Li, Liu Ya, Lu Yuchao, et al. Review on environmental effects and applications of biochar[J]. Environmental Chemistry, 2011, 30(8): 1411-1421. (in Chinese with English abstract)
[7] 王萌萌,周启星. 生物炭的土壤环境效应及其机制研究[J]. 环境化学,2013,32(5):768-780.
Wang Mengmeng, Zhou Qixing. Environmental effects and their mechanisms of biochar applied to soils[J]. Environmental Chemistry, 2013, 32(5): 768-780. (in Chinese with English abstract)
[8] 王宁,侯艳伟,彭静静,等. 生物炭吸附有机污染物的研究进展[J]. 环境化学,2012,31(3):287-295.
Wang Ning, Hou Yanwei, Peng Jingjing, et al. Research progess on sorption of organic contaminants to biochar[J]. Environmental Chemistry, 2012, 31(3): 287-295. (in Chinese with English abstract)
[9] Liu Z, Zhang F S, Wu J, etal. Characterrization and application of chars produced from pinewood pyrolysis and hydrothermal treatment[J]. Fuel, 2010, 89: 510-514.
[10] Parshetti G K, Chowdhury S, Balasubramanian R, etal. Hydrothermal conversion of urban food waste to chars for removal of textile dyes from contaminated waters[J]. Bioresource Technol, 2014, 161: 310-319.
[11] Elaigwu S E, Rocher V, Kyriakou G, etal. Removal of Pb2+and Cd2+from aqueous solution using chars from pyrolysis and microwave-assisted hydrothermal carbonization ofshell [J]. J Ind Eng Chem, 2014, 20: 3467-3473.
[12] Mohan D, Sarswat A, Ok Y S, et al. Organic and inorganic contaminants removal from water with biochar, a renewable, low cost and sustainable adsorbent: A critical review[J]. Bioresource Technol, 2014, 160: 191-202.
[13] 王章鸿,郭海艳,沈飞,等. 蚯蚓粪便制备生物炭及其对罗丹明B吸附的研究[J]. 环境科学学报,2015,35(10):3170-3177.
Wang Zhanghong, Guo Haiyan, Shen Fei, et al. Production of biochar by vermicompost carbonization and its adsorption to Rhodamine-B[J]. Acta Scientiae Circumstantiae, 2015, 35(10): 3170-3177. (in Chinese with English abstract)
[14] 吴倩芳,张付申. 水热炭化废弃生物质的研究进展[J]. 环境污染与防治,2012,34(7):70-75.
Wu Qianfang, Zhang Fushen. Progress on hydrothermal carbonization of waste biomass[J]. Environmental Pollution and Control, 2012, 34(7): 70-75. (in Chinese with English abstract)
[15] 黄维,范同祥. 水热碳化法的研究进展[J]. 材料导报,2014,28(23):131-135.
Huang Wei, Fan Tongxiang. Research progress of hydrothermal carbonnization method[J]. Materials Review, 2014, 28(23): 131-135. (in Chinese with English abstract)
[16] Fakkaew K, Koottatep T, Polprasert C, etal. Effects of hydrolysis and carbonization reactions on hydrochar production[J]. Bioresource Technol, 2015, 192: 328-334.
[17] Funke A, Ziegler F. Hydrothermal carbonization of biomass: A summary and discussion of chemical mechanisms for process engineering[J]. Biofuel Bioprod Bior, 2010, 4(2): 160-177.
[18] 李保强,刘钧,李瑞阳,等. 生物质炭的制备及其在能源与环境领域中的应用[J]. 生物质化学工程,2012,46(1):34-38.
Li Baoqiang, Liu Jun, Li Ruiyang, et al. Biochars preparation and its applications in energy and environment field[J]. Biomass Chemical Engineering, 2012, 46(1): 34-38. (in Chinese with English abstract)
[19] Kajita M, Kimura T, Norinaga K, et al. Catalytic and noncatalytic mechanisms in steam gasification of char from the pyrolysis of biomass[J]. Energ Fuel, 2010, 24(1): 108-116.
[20] Mui E L K, Cheung W H, Valix M, et al. Dye adsorption on to char from bamboo[J]. J Hazard Mater, 2010, 177(1/2/3): 1001-1005.
[21] Jiang Z, Liu Z, Fei B, et al. The pyrolysis characteristics of moso bamboo[J]. J Anal Appl Pyrol, 2012, 94: 48-52.
[22] Li X, Li M-F, Bian J, et at. Hydrothermal carbonization of bamboo in an oxalic acid solution: Effects of acid concentration and retention time on the characteristics of products[J]. RSC Adv, 2015(5): 77147-77153.
[23] Abelleira J, Perez-Elvira S I, Sanchez-Oneto J, et al. Advanced Thermal Hydrolysis of secondary sewage sludge: A novel process combining thermal hydrolysis and hydrogen peroxide addition[J]. Resour Conserv Recy, 2012, 59: 52-57.
[24] Falco C, Baccile N, Titirici M M. Morphological and structural differences between glucose, cellulose and lignocellulosic biomass derived hydrothermal carbon[J]. Green Chem, 2011, 13(11): 3273-3281.
[25] 回瑞华,关崇新,侯冬岩.羧酸及其盐红外光谱特性的研究[J]. 鞍山师范学院学报,2001,3(1):95-98.
Hui Ruihua, Guan Chongxin, Hou Dongyan. Study on IR characteristics of carboxylic acid and their salts[J]. Journal of Anshan Teachers College, 2001, 3(1): 95-98. (in Chinese with English abstract)
[26] 罗曼,关平,刘文汇. 利用红外光谱鉴别饱和脂肪酸及其盐[J]. 光谱学与光谱分析,2007,27(2):250-253.
Luo Man, Guan Ping, Liu Wenhui. The identification of several saturated fatty acids and their salts by means of infrared spectrometry[J]. Spectroscopy and Spectral Analysis, 2007, 27(2): 250-253. (in Chinese with English abstract)
[27] Tekin K, Karagöz S, Bektaş S. A review of hydrothermal biomass processing[J]. Renew Sust Energ Rev, 2014(40): 673-687.
[28] 安增莉,侯艳伟,蔡超,等. 水稻秸秆生物炭对Pb(Ⅱ)的吸附特性[J]. 环境化学,2011,30(11):1851-1857.
An Zengli, Hou Yanwei, Cai Chao, et al. Lead (Ⅱ) adsorption characteristics on different biochars derived from rice straw[J]. Environmental Chemistry, 2011, 30(11): 1851-1857. (in Chinese with English abstract)
[29] 李允超,王贤华,杨海平,等. 竹炭表面结构与其对糠醛的吸附性能[J]. 农业工程学报,2012,28(12):257-263.
Li Yunchao, Wang Xianhua, Yang Haiping, et al. Surface structure of bamboo charcoal and its adsorption property on furfural[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2012, 28(12): 257-263. (in Chinese with English abstract)
[30] 郎印海,刘伟,王慧. 生物炭对水中五氯酚的吸附性能研究[J]. 中国环境科学,2014,34(8):2017-2023.
Lang Yinhai, Liu Wei, Wang Hui. Adsorption efficiencies of pentachlorophenol from aqueous solution onto biochars[J]. China Environmental Science, 2014, 34(8): 2017-2023. (in Chinese with English abstract)
[31] 黄华,王雅雄,唐景春,等. 不同烧制温度下玉米秸秆生物炭的性质及对萘的吸附性能[J]. 环境科学,2014,35(5):1884-1890.
Huang Hua, Wang Yaxiong, Tang Jingchun, et al. Properties of maize stalk biochar produced under different pyrolysis temperatures and its sorption capability to naphthalene[J]. Environmental Science, 2014, 35(5): 1884-1890. (in Chinese with English abstract)
[32] Chen Z M, Chen B L, Chiou C T. Fast and slow rates of naphthalenesorption to biochars produced at different temperatures[J]. Environ Sci Technol, 2012, 46(20): 11104-11111.
[33] 张明,徐立恒,吕黎. 浒苔生物炭对水中萘的吸附作用[J]. 科技导报,2015,33(14):78-81.
Zhang Ming, Xu Liheng, Lu Li. Sorption of naphthalene in water by biochar derived from[J]. Science&Technology Review, 2015, 33(14): 78-81. (in Chinese with English abstract)
Preparation of bamboo biochars by low-temperature hydrothermal method and its adsorption of organics
Li Yin1,2, Shan Shengdao1, Yang Ruiqin1, Gai Xikun1, Mao Jianwei1, Huang Ningning1,Tou Yanping1,Meas Arun1
(1.,310023; 2.310027)
Biochar is a kind of carbon-rich solid material obtained from biomass resources, which can be used as source of energy, catalyst, adsorbent and soil conditioner.Bamboo is a kind of widely used biomass resource containing high fraction of lignocellulose, and bamboo waste from industrial processing is a kind of good raw material for producing biochars. Hydrothermal carbonization approach was applied at low temperatures to produce bamboo biochars, and the selected biochar samples were further modified by being immersed in the sodium hydroxide (NaOH) solution or calcined in nitrogen atmosphere. The effects of the preparation conditions on the physico-chemical properties of the bamboo biochars were investigated, and the adsorption properties of the biochars for 2-naphthol and Congo red from their aqueous solutions were evaluated. The results showed that the yields of the bamboo biochars from hydrothermal carbonization without modification were between 54.12% and 71.53%, and the functional groups containing oxygen such as -OH (3 200-3 600 cm-1), C=O (1 650-1 735 cm-1) and C-O (1 000-1 250 cm-1) were found to be rich on the surfaces of these biochars; the oxygen content of the bamboo biochar produced at 200 ℃ and 7 h was as high as 46.33%, and the surface area of the same carbon sample was measured to be 14.10 m2/g. The bamboo biochars modified by being immersed in the NaOH solution still showed rich oxygen-containing groups on their surfaces, high yields were also achieved with these samples,much larger surface area (33.22 m2/g) was obtained for the biochar sample produced at 200 ℃ and 7 h and modified by soaking in NaOH solution for 1 h, and the oxygen content of this carbon sample was 50.57%, which was higher than that of the sample before modification treatment. On the other hand, few functional groups were found on the surfaces of the bamboo biochars modified by calcination in nitrogen atmosphere, the yields of these biochar samples were much lower (between 12.99% and 16.21%), even higher surface area (52.39 m2/g) was observed for the biochar sample produced at 200 ℃ and 7 h and modified by calcining in nitrogen atmosphere at 700 ℃, the carbon content of this carbon sample was 75.87%, and the oxygen content of this sample decreased to 20.89%. All of the bamboo biochar samples without modification treatment could adsorb 2-naphthol and congo red from aqueous solutions, of which the sample produced at 160 ℃ and 3 h showed the largest adsorption capacity for 2-naphthol (50.3 mg/mLat 25 ℃, initial concentration of 0.5 mg/mL), and the sample produced at 200 ℃ and 7 h showed the largest adsorption capacity for Congo red (63.7 mg/mLat 25 ℃, initial concentration of 0.5 mg/mL), and these 2 kinds of bamboo biochar samples were chosen as the most promising adsorbents for the adsorptive removal of 2-naphthol and Congo red. Surface adsorption was inferred to be the predominant mechanism for the adsorption of Congo red on the surfaces of the bamboo biochars, while a complex mechanism involving partition was suggested for the adsorption of 2-naphthol on the biochars. The NaOH immersion method was favorable for obtaining biochars with higher adsorption capacities for both 2-naphthol and Congo red, and the bamboo biochar sample produced at 200 ℃and 7 h and modified by soaking in NaOH solution for 1 h displayed the largest adsorption capacities for both 2-naphthol (62.3 mg/mL at 25 ℃, equilibrium concentration of 0.3 mg/mL) and Congo red (69.1 mg/mL at 25 ℃, equilibrium concentration of 0.3 mg/mL). However, calcination in nitrogen didn’t show positive effects on the adsorption properties of the bamboo biochars especially for the adsorption of 2-naphthol. The results obtained show that bamboo biochars produced through hydrothermal carbonization can be applied as low cost adsorbents for adsorptive removal of 2-naphthol and Congo red from wastewater.
biomass; absorption; carbonization; bamboo; hydrothermal method; 2-naphthol; congo red
10.11975/j.issn.1002-6819.2016.24.032
S19
A
1002-6819(2016)-24-0240-08
2016-03-16
2016-10-26
浙江省公益性技术应用研究计划项目(No. 2015C33006);国家国际科技合作专项项目(No. 2014DFE90040);生物质化工教育部重点实验室(浙江大学)开放基金资助项目(No. 2015BCE003)。
李音,女,浙江杭州人,讲师,博士,从事生物质资源化利用研究。杭州 浙江科技学院,310023。Email:cherryli1986@126.com
