估算肾小球滤过率与急性ST段抬高型心肌梗死患者心肌无复流的相关性研究
2016-12-21李凤丽任法新董梅
李凤丽,任法新,董梅
冠心病研究
估算肾小球滤过率与急性ST段抬高型心肌梗死患者心肌无复流的相关性研究
李凤丽*,任法新,董梅
目的:探讨估算肾小球滤过率(eGFR)与急性ST段抬高型心肌梗死(STEMI)患者心肌无复流(MNR)的相关性。
方法:收集2013-01至2015-06期间烟台毓璜顶医院因STEMI接受急诊经皮冠状动脉介入治疗(PCI) 的患者461例,其中男373例,女88例,平均年龄(61.46±12.29)岁。PCI成功开通心外膜血管后仍有部分患者存在心肌灌注不足的表现,即心肌无复流(MNR)。MNR 定义为心肌梗死溶栓治疗临床试验(TIMI)血流分级<3级或TIMI 3级且心肌呈色分级(MBG)≤2。 461例患者中98例发生MNR(无复流组),363例成功复流(复流组)。根据MDRD(Modification of Diet in Renal Disease)公式计算eGFR。比较两组球囊扩张时间、病变长度变化。
结果:461例患者中共计98例(21.26%)患者发生MNR。410例(88.94%)患者PCI 术后冠状动脉血流达TIMI 3级(复流组363例,无复流组47例);334例(72.45%)患者 MBG3 级(复流组334 例,无复流组0例),两组比较差异均有统计学意义(P<0.001)。与复流组相比,无复流组发病至球囊扩张时间较长(P<0.001),syntax评分较增加(P<0.001),病变长度较延长(P=0.017),差异均有统计学意义。多因素Logistic回归分析表明收缩压[比值比(OR):0.984,95%可信区间(CI):0.970~0.984,P=0.023]、左心室射血分数(OR:0.957, 95% CI:0.913~0.987, P=0.031)、eGFR(OR:0.964,95% CI:0.950~0.964, P<0.001)、发病至球囊扩张时间(OR:1.004,95% CI:1.002~1.004, P=0.001)是MNR发生的独立危险因素。受试者工作特征 (ROC) 曲线显示eGFR[曲线下面积:0.801,95% CI:0.743~0.859, P<0.001; 理想阈值74.78 ml/(min·1.73m2), 敏感性为73.7%,特异性为77.3%]可以较好的预测MNR发生。
结论:eGFR降低与STEMI患者行急诊PCI术后MNR的发生密切相关。
肾小球滤过率;心肌梗死;无复流
Objective: To explore the relationship between estimated glomerular filtration rate (eGFR) and myocardial no-refow (MNR) in patients with ST-segment elevation myocardial infarction (STEMI) after primary percutaneous coronary intervention (PCI).
Methods: A total of 461 eligible STEMI patients treated by primary PCI in our hospital from 2013-01 to 2015-06 were enrolled including 373 male and 88 female with the mean age of (61.46±12.29) years. MNR was defned as TIMI<grade 3 or TIMI grade 3 with myocardial blush grades (MBG)≤2. The patients were divided into 2 groups: MNR group, n=98 (21.26%) and Re-fow group, n=363. eGFR was calculated by MDRD (modifcation of diet in renal disease) equation. The balloon dilatation time and lesion length were compared between 2 groups.
Results: There were 410 (88.94%) patients reached post PCI TIMI grade 3 including 363 in Re-fow group and 47in MNR group; 334 (72.45%) patients with MBG grade 3 including 334 in Re-fow group, 0 in MNR group, all P<0.001. Compared with Re-fow group, MNR group had prolonged time form onset to balloon dilatation, P<0.001, increased syntax score, P<0.001 and extend length of lesion, P=0.017. Multi Logistic regression analysis showed that systolic blood pressure (OR=0.984, 95% CI 0.970-0.84, P=0.023), left ventricular ejection fraction (OR=0.957, 95% CI 0.913-0.987, P=0.031), eGFR (OR=0.964, 95% CI 0.950-0.964, P<0.001), the time from onset to balloon dilatation (OR=1.004, 95% CI 1.002-1.004, P=0.001) were the independent risk factors for MNR occurrence. The area of ROCeGFR=0.801, (95% CI 0.743-0.859, P<0.001) and the optimal threshold=74.78 ml/(min•1.73m2) with the sensitivity of 73.7% and specifcity of 77.3% may better predict the incidence of MNR.
Conclusion: Decreased eGFR was closely related to MNR occurrence in STEMI patients after primary PCI.
(Chinese Circulation Journal, 2016,31:1064.)
急诊经皮冠状动脉介入治疗(PCI) 再灌注治疗使急性ST段抬高型心肌梗死(STEMI)患者的死亡率显著下降。但是,心外膜冠状动脉阻塞血管的开通并不意味着心肌组织水平的有效灌注。PCI成功开通心外膜血管后仍有部分患者存在心肌灌注不足的表现,即心肌无复流(MNR)。MNR的发生与心肌梗死面积延展、心力衰竭、恶性心律失常发生密切相关,增加急性心肌梗死(AMI)患者PCI后短期和长期死亡率,是AMI患者临床预后的独立预测因子之一[1]。目前,MNR的发生机制尚不清楚。研究表明,内皮细胞损伤、炎症反应、氧化应激、白细胞和血小板阻塞微血管、微栓塞等可能是MNR发生的主要机制[2]。
估算肾小球滤过率(eGFR)是评估肾功能的可靠指标。研究证实,eGFR越低,心血管疾病发病率越高[3],eGFR下降是STEMI患者PCI后短期和长期预后的独立危险因子[4]。参与动脉粥样硬化的因素如内皮细胞功能障碍、血管炎症反应和氧化应激损伤可能影响肾功能,导致eGFR下降。基础和临床试验均已证实慢性肾脏疾病患者存在明显的炎症反应和氧化应激状态[5]。eGFR与STEMI患者PCI术后MNR发生的关系尚不清楚。本研究通过收集行急诊PCI的STEMI患者,探讨eGFR与STEMI患者PCI后MNR发生之间的关系,为早期识别MNR高危患者提供有效的预测因子。
1 资料与方法
对象:收集2013-01至2015-06期间烟台毓璜顶医院因STEMI 接受急诊PCI 的490例患者的临床资料。纳入标准:持续性胸痛>30 min,对硝酸甘油反应差;12导联标准心电图示两个或两个以上相邻导联 ST 段抬高≥0.2 mV或新发完全性左束支传导阻滞;心肌损伤标志物肌酸激酶 MB 同工酶(CKMB)或肌钙蛋白I(TnI)≥正常值上限2倍;发病12 h内行急诊PCI。排除标准:既往急、慢性冠状动脉性疾病或心力衰竭病史;发病至球囊扩张时间>12 h;未成功PCI;溶栓治疗;急、慢性感染或炎症性疾病;恶性肿瘤疾病病史。490例患者中29例(17例因发病至球囊扩张时间>12 h,8例未成功PCI,3例术前应用溶栓药物,1例自通)被排除。本研究最终纳入461例STEMI患者。
急诊PCI:所有STEMI患者均于入院后即刻口服阿司匹林300 mg、硫酸氢氯吡格雷(波立维)300 mg后转入心导管室。采用桡动脉作穿刺点使用5F或6F 动脉鞘管(Cordis公司,美国)进行选择性冠状动脉造影,经标准体位,多角度投射,确定梗塞相关动脉。据血栓负荷情况决定是否应用抽吸导管(Diver CE,Invatec)抽吸血栓。依据梗塞相关动脉冠状动脉造影狭窄程度决定是否通过球囊扩张开通狭窄血管,球囊预扩张后置入支架或直接置入支架。PCI术中静脉给予普通肝素3000~10000 IU,必要时给予血小板糖蛋白Ⅱ b/ Ⅲ a 受体抑制剂。
冠状动脉血流评估及分组:应用 QCA 系统评价冠心病患者的冠状动脉造影结果。采用心肌梗死溶栓治疗临床试验(TIMI)血流分级[6]、校正的TIMI计帧数(cTFC)[7]和心肌呈色分级(MBG)[8]评估冠状动脉血流情况。分别由2名心脏造影专家对造影结果进行评估,结果不一致时,由2名专家协商解决。急诊PCI后MNR定义为TIMI<3或TIMI 3且心肌呈色分级(MBG)≤2。461例患者中98例发生MNR(无复流组),363例成功复流(复流组)。
eGFR:入院即刻经肱静脉采集血样本测定血肌酐水平。根据MDRD(Modification of Diet in Renal Disease)公式计算eGFR。MDRD:eGFR[ml/(min·1.73m2) ] =186×血肌酐-1.154×年龄-0.203,女性患者×0.742。
统计学方法:采用SPSS17.0软件包对数据资料进行统计分析。计量资料以均数±标准差表示,计数资料以实际数目和百分数(%)表示。计量资料两组间比较采用t检验,计数资料两组间比较采用Fisher exact检验。多因素Logistic回归分析eGFR与MNR的发生是否独立相关。P<0.05为差异有统计学意义。
2 结果
2.1 两组一般临床资料比较(表1)
与复流组相比,无复流组女性患者增多(P=0.005),合并高龄(P=0.002)、糖尿病(P=0.014)的发生率增加,收缩压(P<0.001)和舒张压(P=0.012)下降,入院时killp分级>2级(P<0.001)和左心室射血分数(P<0.001)代表的心功能减低,肌酸激酶MB同工酶(P<0.001)和尿酸(P=0.028)水平升高,eGFR(P<0.001)和甘油三酯(P=0.043)水平下降。其余指标两组间比较差异无统计学意义 (P>0.05)。
表1 两组患者一般临床资料比较

表1 两组患者一般临床资料比较
注:1 mmHg=0.133 kPa
项目 复流组(n=363)无复流组(n=98) P值年龄 (岁) 61.21±12.00 65.59±12.34 0.002女性[例 (%)] 59 (16.25) 29 (29.59) 0.005体重指数 ( kg/m2) 24.70±2.20 25.10±2.30 0.097心率 (次/min) 74.86±16.29 76.80±19.74 0.319吸烟[例 (%)] 174 (47.93) 45 (45.92) 0.734高血压[例 (%)] 185 (50.96) 49 (50.00) 0.910糖尿病[例 (%)] 124 (34.16) 47 (47.96) 0.014收缩压 (mmHg) 131.45±24.93 120.42±22.97<0.001舒张压 (mmHg) 78.88±16.77 74.18±15.13 0.012入院时killp分级>2级[例 (%)] 12 (3.30) 22 (22.40) <0.001左心室射血分数 (%) 46.00±8.00 38.00±10.00<0.001血红蛋白 (g/dl) 147.01±16.45 144.05±16.06 0.114血小板 (×109/L) 205.46±54.55 200.11±62.55 0.405白细胞 (×109/L) 10.16±3.23 10.91±3.76 0.051肌酸激酶MB同工酶峰值 (ng/ml) 231.1±82.3 262.4±80.7 <0.001尿酸 (µmol/L) 336±89.35 358.57±91.89 0.028估算肾小球滤过率[ml/ (min·1.73 m2)] 101.48±29.96 69.46 ±23.73 <0.001血糖 (mmol/L) 7.11±3.19 7.40±2.41 0.412胆固醇 (mmol/L) 5.07±1.05 4.92±1.02 0.213甘油三酯 (mmol/L) 1.64±1.22 1.38±0.65 0.043高密度脂蛋白胆固醇 (mmol/L) 1.19±0.27 1.20±0.24 0.603低密度脂蛋白胆固醇 (mmol/L) 3.24±0.89 3.25±1.02 0.942
2.2 两组患者PCI资料比较(表2)
共计98(21.26%)例STEMI患者发生MNR。410例(88.94%)患者PCI 术后冠状动脉血流达TIMI 3级(复流组363例,无复流组47例),两组比较差异有统计学意义(P<0.001)。334例(72.45%)患者MBG3 级(复流组334 例,无复流组0例),两组比较差异有统计学意义(P<0.001)。与复流组相比,无复流组发病至球囊扩张时间较长(P<0.001),syntax评分较增加(P<0.001),病变长度较延长(P=0.017),差异均有统计学意义。
表2 两组患者经皮冠状动脉介入治疗资料比较()
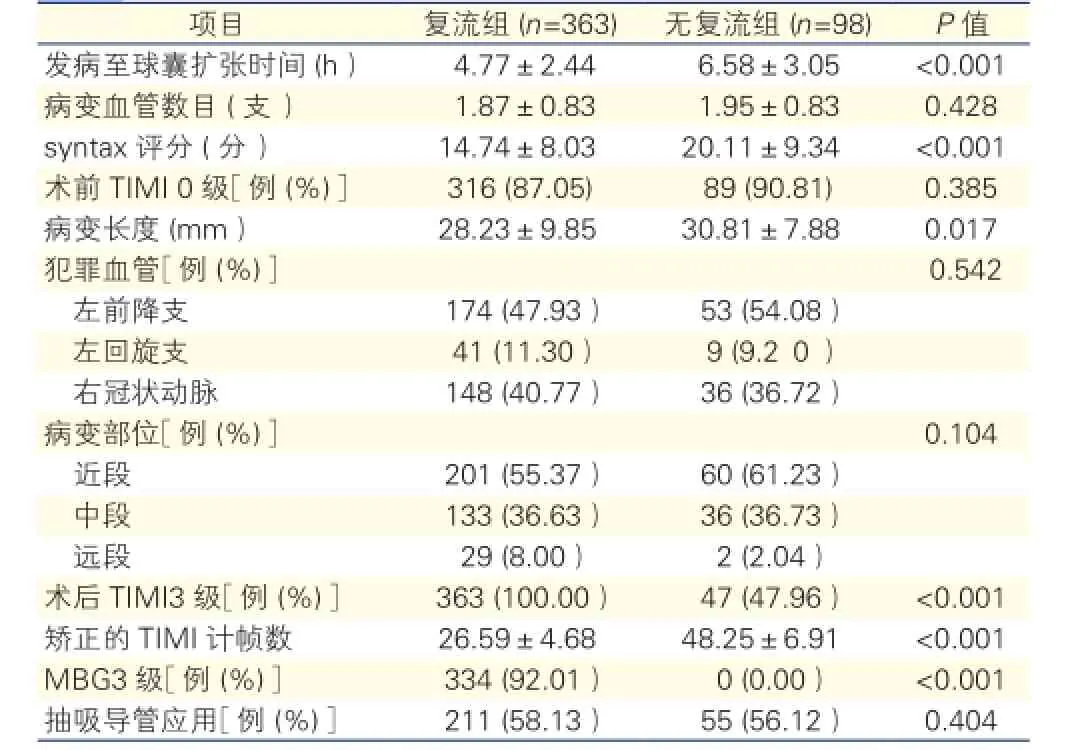
表2 两组患者经皮冠状动脉介入治疗资料比较()
注:TIMI:心肌梗死溶栓治疗临床试验;MBG:心肌呈色分级
项目 复流组 (n=363) 无复流组 (n=98) P值发病至球囊扩张时间 (h) 4.77±2.44 6.58±3.05 <0.001病变血管数目 (支) 1.87±0.83 1.95±0.83 0.428 syntax评分 (分) 14.74±8.03 20.11±9.34 <0.001术前TIMI 0级[例 (%)] 316 (87.05) 89 (90.81) 0.385病变长度 (mm) 28.23±9.85 30.81±7.88 0.017犯罪血管[例 (%)] 0.542左前降支 174 (47.93) 53 (54.08)左回旋支 41 (11.30) 9 (9.2 0)右冠状动脉 148 (40.77) 36 (36.72)病变部位[例 (%)]0.104近段 201 (55.37) 60 (61.23)中段 133 (36.63) 36 (36.73)远段 29 (8.00) 2 (2.04)术后TIMI3级[例 (%)] 363 (100.00) 47 (47.96) <0.001矫正的TIMI计帧数 26.59±4.68 48.25±6.91 <0.001 MBG3级[例 (%)] 334 (92.01) 0 (0.00) <0.001抽吸导管应用[例 (%)] 211 (58.13) 55 (56.12) 0.404
2.3 MNR的独立预测因素(表3)
对影响事件发生的变量包括年龄、糖尿病、吸烟、收缩压、左心室射血分数、白细胞、血糖、eGFR、发病至球囊扩张时间、syntax评分、病变长度进行回归分析。单因素分析结果提示年龄、收缩压、左心室射血分数、eGFR、发病到球囊扩张时间是MNR发生的危险因素(P<0.05)。多因素Logistic回归分析表明收缩压[比值比(OR)=0.984,95% 可信区间(CI):0.970~0.984,P=0.023]、左心室射血分数(OR:0.957,95% CI:0.913~0.987,P=0.031)、eGFR(OR:0.964,95% CI:0.950~0.964,P<0.001)、发病至球囊扩张时间(OR:1.004,95% CI:1.002~1.004,P=0.001)是MNR发生的独立危险因素。
2.4 ROC曲线结果(图1)
显示eG F R[曲线下面积:0.801,95% CI:0.743~0.859,P<0.001; 理 想 阈 值 74.78m l/(min·1.73 m2)]对MNR发生具有较好的预测价值,敏感性为 73.7%,特异性为 77.3%。
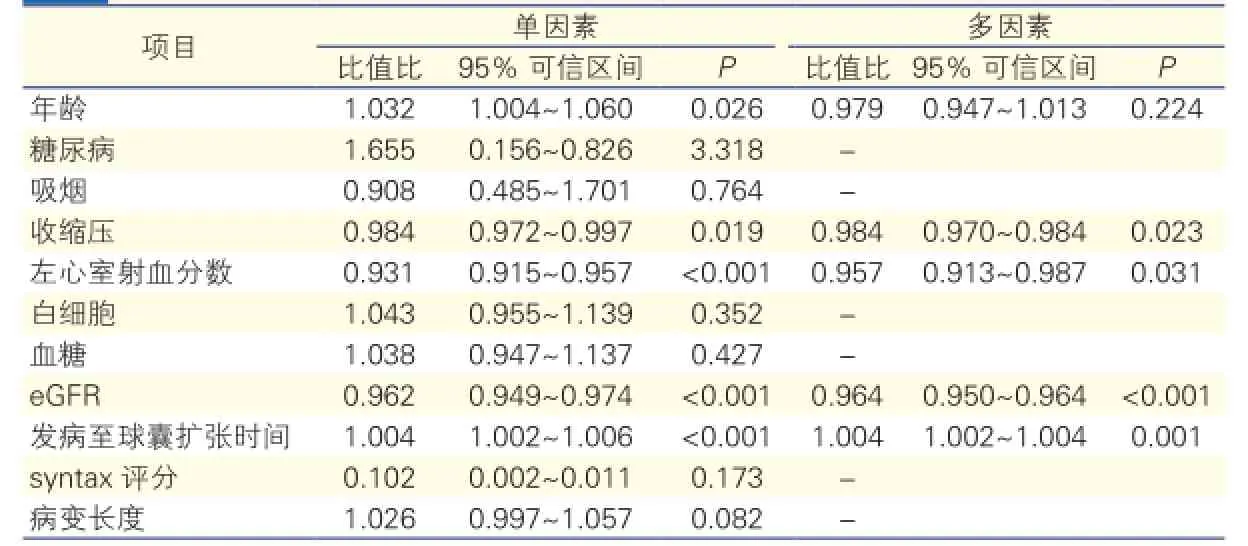
表3 心肌无复流的独立预测因素
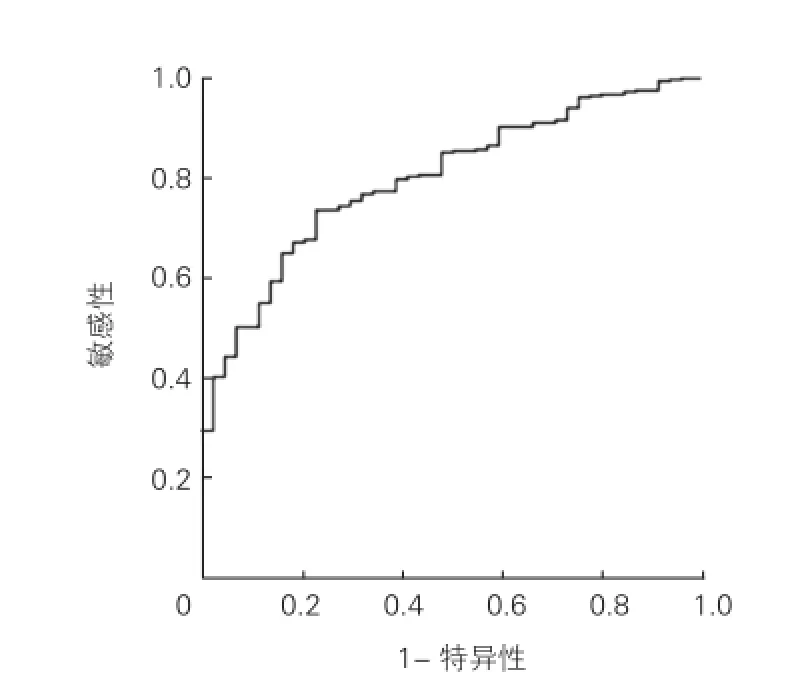
图1 受试者工作特征曲线结果
3 讨论
本研究结果发现入院时eGFR下降是STEMI患者PCI术后MNR发生的独立危险因子,有利于识别MNR高危患者,为MNR的防治提供了新的靶点。
肾功能不全作为心血管疾病的等危症,是一个新的心血管疾病独立危险因素。慢性肾脏疾病2期患者即出现动脉硬化度增加的表现[9],3期(慢性肾脏病分期)患者左心室收缩和舒张功能减低,左心房容积增加[10]。eGFR轻度降低与左心室肥厚亦高度相关[11]。Marenzi等[12]研究表明肾功能不全是PCI术后造影剂肾病的独立危险因素。Shlipak等[13]纳入130 000余例AMI患者研究发现入院1个月内中度肾功能不全患者死亡率较肾功能正常者显著升高(44%vs13%),提示慢性肾脏病与AMI患者预后密切相关,其他学者研究也证实了上述研究结果[14]。此外,有研究显示eGFR降低的AMI患者对缺血再灌注损伤的敏感性增加[15],是AMI患者PCI术后心肌缺血再灌注损伤的独立危险因子[16]。由此可见,eGFR降低代表的肾功能不全是心血管疾病的重要影响因素。
本研究发现eGFR下降与STEMI患者PCI术后MNR发生密切相关,与近期其他学者研究结果相似。Sobkowicz等[17]应用矫正的TIMI计帧数(cTFC)评估终末期肾病患者冠状动脉血流量,发现左前降支、左回旋支和右冠状动脉cTFC分别为34.7±16、41.5±25和30.9±18,较正常冠状动脉明显升高,提示终末期肾病患者冠状动脉血流量降低。Kurtul等[18]纳入673例行急诊PCI的STEMI患者,依据入院时eGFR分为正常肾功能组[eGFR>90 ml/(min·1.73m2)]、轻度肾功能不全组[eGFR 60~89 ml/(min·1.73m2)]和中度肾功能不全组[eGFR 30~59 ml/(min·1.73m2)],探讨入院时eGFR与MNR的相关性,发现轻-中度肾功能不全是MNR独立危险因子(OR=0.942,P<0.001)。参与动脉粥样硬化的因素如内皮细胞功能障碍、氧化应激反应和血管炎性损伤可能影响肾功能,导致eGFR下降。Ferrer-Hita等[19]研究报道肾功能不全患者多伴有高龄、糖尿病等合并症。高龄和糖尿病是肾功能不全发生和不断进展的重要危险因素。本研究中无复流组年龄较复流组显著升高,糖尿病患者较复流组显著增多,考虑为无复流组eGFR降低可能与该组患者年龄增加,合并糖尿病患者较多有关。此外,本研究发现收缩压降低是STEMI患者MNR的独立危险因素,与Zhou等[20]研究结果一致。因此该研究结果需要除外AMI后心脏泵血功能减低,收缩压下降引起的肾脏灌注减少导致的eGFR下降。
eGFR下降促进STEMI患者PCI术后MNR发生的具体机制尚不清楚,可能包含多种因素。eGFR下降患者肾脏清除促炎细胞因子功能下降,醛固酮水平升高,常存在持续炎症-氧化状态[21]。C反应蛋白水平是炎症反应的有效标志物。研究已表明肾功能不全早期C反应蛋白水平即较肾功能正常时明显升高[22],慢性肾功能衰竭患者C反应蛋白水平更是明显升高[23]。慢性肾功能损伤是一个多因素参与的复杂病理过程,其中氧化应激在肾功能损伤不断进展中具有关键地位。Kuczmarsk等研究表明肾大部切除鼠心肌缺血再灌注后心肌组织中氧化应激标志物(H2O2)水平显著升高。Gür等[2]研究证实氧化应激与STEMI患者发生MNR现象有关。由此可以推测,eGFR下降可能加重MNR患者的炎症氧化应激损伤,是MNR发生的重要因素之一。另外,与eGFR下降相关的内皮细胞损伤[24],血小板活性增强和血液高凝等病理生理学状态以及慢性肾脏疾病合并急性冠状动脉综合征患者药物治疗(如抗血小板药物、他汀类药物、血管紧张素转换酶抑制剂/血管紧张素Ⅱ受体拮抗剂等)不足[25]等因素也可能在MNR发生中具有一定作用。
MNR的发生是一个不断发展变化的复杂病理过程,受多种因素影响。该研究表明入院时eGFR下降是MNR发生的独立危险因素,为早期识别MNR高危患者的有效标志物,在围手术期对eGFR下降患者采取肾脏保护措施可能是降低MNR的有效方法,为MNR的防治提供了一个新的靶点。
[1] Muller O, Trana C, Eeckhout E. Myocardial no-reflow treatment. Curr Vasc Pharmacol, 2013, 11: 278-285.
[2] Gür M, Türkoğlu C, Tas kın A, et al. Paraoxonase-1 activity and oxidative stress in patients with anterior ST elevation myocardial infarction undergoing primary percutaneous coronary intervention with and without no-reflow. Atherosclerosis, 2014, 234: 415-420.
[3] Irie F, Iso H, Sairenchi T, et al. The relationships of proteinuria, serum creatinine, glomerular filtration rate with cardiovascular disease mortality in Japanese general population. Kidney Int, 2006, 69: 1264-1271.
[4] Akkaya E, Ayhan E, Uyarel H, et al. The impact of chronic kidney disease on in-hospital clinical outcomes in patients undergoing primary percutaneous angioplasty for ST-segment elevation myocardial infarction. Turk Kardiyol Dern Ars, 2011, 39: 276-282.
[5] Cottone S, Lorito MC, Riccobene R, et al. Oxidative stress, inflammation and cardiovascular disease in chronic renal failure. J Nephrol, 2008, 21: 175-179.
[6] Gibson CM, Murphy SA, Rizzo MJ, et al. Relationship between TIMI frame count and clinical outcomes after thrombolytic administration. Thrombolysis In Myocardial Infarction (TIMI) Study Group. Circulation, 1999, 99: 1945-1950.
[7] Wang MC, Tsai WC, Chen JY, et al. Step wise increase in arterial stiffness corresponding with the stages of chronic kidney disease. Am J Kidney Dis, 2005, 45: 494-501.
[8] van't Hof AW, Liem A, Suryapranata H, et al. Angiographic assessment of myocardial reperfusion in patientstreated with primary angioplasty for acute myocardial infarction: myocardial blush grade. Zwolle Myocardial Infarction Study Group. Circulation, 1998, 97: 2302-2306.
[9] Gibson CM, Murphy SA, Morrow DA, et al. Angiographic perfusion score: an angiographic variable that integrates both epicardial and tissue level perfusion before and after facilitated percutaneous coronary intervention in acute myocardial infarction. Am Heart J, 2004, 148: 336-340.
[10] Edwards NC, Ferro CJ, Townend JN, et al. Aortic distensibility and arterial-ventricular coupling in early chronic kidney disease: a pattern resembling heart failure with preserved ejection fraction. Heart, 2008, 94: 1038-1043.
[11] Shi HT, Wang XJ, Li J, et al. Association of left ventricular hypertrophy with a faster rate of renal function decline in elderly patients with nonend-stage renal disease. J Am Heart Assoc, 2015, Nov 9;4(11). pii: e002213. doi: 10. 1161/JAHA. 115. 002213.
[12] Marenzi G, Lauri G, Assanelli E, et al. Contrast-induced nephropathy in patients undergoing primary angioplasty for acute myocardial infarction. J Am Coll Cardiol, 2004, 44: 1780-1785.
[13] Shlipak MG, HeideMNReich PA, Noguchi H, et al. Association of renal insufficiency with treatment and outcomes after myocardial infarction in elderly patients. Ann Intern Med, 2002, 137: 555-562.
[14] Chan MY, Becker RC, Sim LL, et al. Reperfusion strategy and mortality in ST-elevation myocardial infarction among patients with and without impaired renal function. Ann Acad Med Singapore, 2010 , 39: 179-184.
[15] Song Y, Yu Q, Zhang J, et al. Increased myocardial ischemiareperfusion injury in renal failure involves cardiac adiponectin signal deficiency. Am J Physiol Endocrinol Metab, 2014, 306: 1055-1064.
[16] Shacham Y, Leshem-Rubinow E, Gal-Oz A, et al. Relation of time to coronary reperfusion and the development of acute kidney injury after ST-segment elevation myocardial infarction, 2014 , 114: 1131-1315.
[17] Sobkowicz B, Tomaszuk-Kazberuk A, Kralisz P, et al. Coronary blood flow in patients with end-stage renal disease assessed by thrombolysis in myocardial infarction frame count method. Nephrol Dial Transplant, 2010, 25: 926-930.
[18] Kurtul A, Murat SN, Yarlioglues M, et al. Mild to moderate renal impairment is associated with no-reflow phenomenon after primary percutaneous coronary intervention in acute myocardial infarction. Angiology, 2015, Aug;66(7): 644-651. doi: 10. 1177/0003319714546738.
[19] Ferrer-Hita JJ, Dominguez-Rodriguez A, Garcia-Gonzalez MJ, et al. Renal dysfunction is an independent predictor of in-hospital mortality in patients with ST-segment elevation myocardial infarction treated with primary angioplasty. Int J Cardiol, 2007, 118: 243-245.
[20] Zhou H, He XY, Zhuang SW, et al. Clinical and procedural predictors of no-reflow in patients with acute myocardial infarction after primary percutaneous coronary intervention. World J Emerg Med, 2014, 5: 96-102.
[21] 赵振燕, 吴永健. 慢性肾功能不全与心血管疾病关系研究. 中国循环杂志, 2009, 24: 477-479.
[22] Suzuki M, Seike F, Miyoshi A, et al. Critical role of systemic inflammation in patients with ST-segment elevation myocardial infarction complicated with renal dysfunction. Int J Cardiol, 2013, 168: 3062-3064.
[23] 刘昱圻, 高磊, 薛桥, 等. 肾功能不全老年急性冠状动脉综合征患者远期预后评. 中国循环杂志, 2012, 27: 342-345.
[24] Batal I, De Serres SA, Mfarrej BG, et al. Glomerular inflammation correlates with endothelial injury and with IL-6 and IL-1β secretion in the peripheral blood. Transplantation, 2014, 97: 1034-1042.
[25] Narala KR, Hassan S, LaLonde TA, et al. Management of coronary atherosclerosis and acute coronary syndromes in patients with chronic kidney disease. Curr Probl Cardiol, 2013 , 38: 165-206.
(编辑:梅平)
Relationship Between Estimated Glomerular Filtration Rate and Myocardial No-reflow in Patients With Acute ST-elevation Myocardial Infarction
LI Feng-li**, REN Fa-xin, DONG Mei.
Department of Cardiology Yuhuangding Hospital, Yantai (264000), Shandong, China
Corresponding Author: DONG Mei, Email: dongmei0212@126.com.
Glomerular fltration rate; Myocardial infarction; No-refow
山东省自然科学基金联合专项(批准编号:ZR2014HL009)
264000 山东省烟台市,烟台毓璜顶医院 心内科
李凤丽 住院医师 硕士 主要从事冠心病临床研究 Email:muzilishiwo@163.com 通讯作者:董梅 Email:dongmei0212@126.com*现在山东省淄博市中心医院重症医学科工作(255000)**Now working in Zibo City Central Hospital of Shandong Province
R541.4
A
1000-3614(2016)11-1064-05
10.3969/j.issn.1000-3614.2016.11.006
( 2015-11-26)
