冠状动脉内注射比伐卢定预防直接经皮冠状动脉介入治疗术中无复流或慢血流的探索性临床研究
2016-12-20梁振洋刘美丽赵雪东李毅王贺阳赵昕陶杰王斌聂绍平韩雅玲
梁振洋 刘美丽 赵雪东 李毅 王贺阳 赵昕 陶杰 王斌 聂绍平 韩雅玲
·临床研究·
冠状动脉内注射比伐卢定预防直接经皮冠状动脉介入治疗术中无复流或慢血流的探索性临床研究
梁振洋 刘美丽 赵雪东 李毅 王贺阳 赵昕 陶杰 王斌 聂绍平 韩雅玲
目的 探讨冠状动脉内注射比伐卢定预防急性ST段抬高心肌梗死(ST-segment elevation myocardial infarction,STEMI)患者直接经皮冠状动脉介入治疗(primary percutaneous coronary intervention,PPCI)术中冠状动脉无复流或慢血流的作用。方法 选取2015年7月至2015年12月沈阳军区总医院心内科及北京安贞医院急诊危重症中心收治的拟行PPCI的STEMI患者84例,以1∶1的比例随机分为对照组(不进行冠状动脉内注射比伐卢定,仅接受标准剂量静脉注射比伐卢定)40例和试验组(经冠状动脉内推注剂量为静脉负荷剂量50%的比伐卢定)44例。比较两组患者PPCI术后靶血管无复流或慢血流(TIMI血流≤Ⅱ级)的发生情况。结果 对照组和试验组患者术中[25例(62.5%)比24例(54.5%),P=0.460]、术后[6例(15.0%)比6例(13.6%),P=0.428]无复流或慢血流(TIMI血流≤Ⅱ级)的发生率比较,差异均无统计学意义,且未发现与术后无复流或慢血流发生相关的危险因素。结论 冠状动脉内应用比伐卢定在预防STEMI患者PPCI术中无复流或慢血流方面的获益并不明显,需要进一步探索合适的剂量,并进行大样本随机对照研究来验证。
比伐卢定; 无复流; 慢血流; 急性ST段抬高心肌梗死; 经皮冠状动脉介入治疗
尽早最大限度地恢复梗死相关动脉(infarct-related artery,IRA)血流并将因缺血而导致的心肌损伤范围降至最小,是急性ST段抬高心肌梗死(ST-segment elevation myocardial infarction,STEMI)患者救治最重要的治疗目标。直接经皮冠状动脉介入治疗(primary percutaneous coronary intervention,PPCI)已成为STEMI患者最有效的治疗方式之一[1]。然而,PPCI虽能有效恢复心外膜冠状动脉血流灌注,但仍有5%~25%的患者由于种种原因导致微循环功能障碍,使得心肌组织水平无法得到有效再灌注,即为“无复流或慢血流”现象,其实质为心肌组织水平的再灌注不良[2-3]。研究证实,无复流或慢血流不仅影响介入治疗术后近期、远期的预后,亦是主要不良心脏事件的独立危险因素,与心肌梗死后恶性心律失常、早期充血性心力衰竭、晚期左心室纤维化重构、因心力衰竭再住院、病死率等相关,预示着不良的临床预后[4]。目前如何有效改善STEMI患者PPCI术中IRA的血流,预防无复流或慢血流现象发生,最大限度地恢复心肌有效再灌注,已成为心血管学界关注的热点问题之一,对提高STEMI患者获益具有重要的临床意义。
发生无复流或慢血流的基本病理原因可能与以下几个方面有关:(1)冠状动脉远端微循环血栓或栓塞;(2)心肌缺血性受损;(3)再灌注性心肌损伤;(4)微循环受损易感性;(5)内皮功能障碍;(6)心肌细胞及基质肿胀;(7)氧化应激反应损伤心肌细胞和微循环等。其中冠状动脉远端血管床内微血栓形成及栓塞是导致无复流或慢血流的重要机制之一,且与介入治疗术中操作密切相关,主要是由于心外膜的冠状动脉内斑块碎屑、坏死脂质、炎性物质、脱落的微血栓随着心动周期栓塞了冠状动脉远端血管床,同时介入过程所引发的血小板活化可能进一步加重了冠状动脉远端微循环栓塞,继而加重心肌微血管床损伤,最终导致心肌组织水平再灌注障碍[5]。因此,在介入治疗围术期如何进一步强化抗凝、抗血小板治疗以期有效减少远端血管床栓塞,是恢复心肌有效再灌注、防治无复流或慢血流发生、发展的有效措施之一。
比伐卢定作为一种新型的抗凝药物,能够在有效改善缺血事件的同时降低出血发生率,在PPCI术中应用已较为广泛。既往曾有病例报道,冠状动脉内推注比伐卢定可以对冠状动脉无复流或慢血流的患者起到较好的治疗作用,能够有效地恢复介入治疗术中冠状动脉内血流[6]。而在全身应用静脉全剂量负荷比伐卢定的情况下,在STEMI患者PPCI术中应用冠状动脉内推注比伐卢定是否能有效预防术中无复流或慢血流的发生,有待进一步证实。本研究拟对该问题进行初步探讨。
1 对象与方法
1.1 研究对象
选取2015年7月至2015年12月沈阳军区总医院心内科及北京安贞医院急诊危重症中心收治的拟行PPCI的STEMI患者,将符合入选标准的84例患者采用随机数列的分配方式,以1∶1的比例随机分为对照组(不进行冠状动脉内注射比伐卢定,仅接受标准剂量静脉注射比伐卢定)40例和试验组(经冠状动脉内推注剂量为静脉负荷剂量50%的比伐卢定)44例。
入选标准:(1)STEMI发病12 h内[或发病12~24 h仍有胸痛/不适和持续ST段抬高或新发生的左束支传导阻滞(left bundle-branch block delay,LBBB)]并拟行PPCI术的患者;(2)性别不限,年龄18~80岁,体重>50 kg;(3)PPCI术前抗血小板药物已按指南规范应用;(4)对本临床研究无异议、同意参加并签署知情同意书。
排除标准:(1)临床表现、冠状动脉CT/冠状动脉造影(coronary angiography,CAG)等检查提示不适合行经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)者;经溶栓治疗72 h内的STEMI、心源性休克、左主干病变患者。(2)在导管室给予静脉注射负荷剂量比伐卢定后5 min,测定活化凝血时间(activated clotting time,ACT)>380 s。(3)PCI术前48 h内应用过替罗非班、肝素/低分子肝素、华法林等抗凝药物或比伐卢定的患者。(4)具有活动性出血或者出血倾向者,包括1个月内视网膜或玻璃体出血、3个月内消化道或泌尿系出血、3个月内脑梗死和6个月内脑出血病史等。(5)具有较大可能导致血管病变及继发性出血的因素(如颅内动脉瘤、活动性溃疡性结肠炎、活动性胃溃疡)。(6)具有1个月内大手术史或深部穿刺史者(包含眼科或脑科手术)。(7)不排除主动脉夹层、亚急性细菌性心内膜炎或心包炎者。(8)与治疗无关的未控制的高血压[血压>180/110 mmHg(1 mmHg=0.133 kPa)]。(9)血红蛋白<100 g/L,血小板计数<100×109个/L。(10)谷草转氨酶(aspartate aminotransferase,AST)、谷丙转氨酶(alanine aminotransferase,ALT)等肝功能指标高于正常值上限的3倍,且排除由心肌梗死所致的肝功能指标升高。(11)重度肾功能不全[估算的肾小球滤过率(estimated glomerular filtration rate,eGFR)<30 ml/(min·1.73 m2)]者。(12)有肝素导致的血小板减少症病史者。(13)曾明确诊断为过敏体质或已知对研究药物(比伐卢定、阿司匹林、氯吡格雷、对比剂等)及器械(冠状动脉支架材料不锈钢)有明确过敏史者。(14)有生育计划或者孕妇、哺乳期的女性患者。(15)其余研究者认为不适合参加本研究的任何情况。
1.2 研究方法
全部患者均于PPCI术前服用负荷剂量阿司匹林(300 mg)+氯吡格雷(300 mg或600 mg)或阿司匹林(300 mg)+替格瑞洛(180 mg)。经桡动脉或股动脉行介入治疗,在导管室中,冠状动脉介入治疗术前均给予比伐卢定0.75 mg/kg静脉推注作为负荷剂量,后立即以1.75 mg/(kg·h)持续输注至手术结束(至少维持30 min)。根据病情判定可在PPCI术后继续滴注比伐卢定达4 h,必要时4 h后可以开始以0.2 mg/(kg·h)的速率额外给予比伐卢定静脉滴注,持续达20 h。首次给药5 min后监测ACT(Hemochron法),若ACT<225 s则追加比伐卢定0.30 mg/kg静脉推注,并于5 min后再次监测ACT,选取ACT≤380 s的患者,采用随机数列的分配方式,以1∶1的比例分为对照组和试验组。所有患者均首先插入指引导丝通过病变,或用小直径球囊导管预扩张,使前向血流恢复至TIMI≥Ⅰ级。对照组不予冠状动脉内注射比伐卢定,进行PPCI常规操作;试验组经指引导管或微导管冠状动脉内一次性推注剂量为静脉负荷剂量50%的比伐卢定(不包括首次ACT<225 s而追加的比伐卢定剂量),此后按照PPCI常规操作,并于术中冠状动脉内推注比伐卢定后以及手术结束时复查ACT(并留存曝光影像一次)。两组患者如血栓负荷较重,由术者决定可行血栓抽吸、冠状动脉内应用替罗非班和(或)硝酸酯类药物等。
1.3 主要终点及相关定义
主要终点:PCI术后靶血管无复流或慢血流(TIMI血流≤Ⅱ级)的发生率。无复流或慢血流的定义[2]:在支架置入术或者球囊扩张术后经CAG证实心肌梗死溶栓治疗临床试验TIMI血流分级≤Ⅱ级(需除外冠状动脉夹层、阻塞、痉挛等因素)。TIMI血流[7]:依据文献报道将TIMI血流0级定义为血管完全闭塞、远端对比剂无通过,即远端血管对比剂无灌注;TIMI血流Ⅰ级为血管部分闭塞,仅有少量对比剂通过血管靶病变处,但是远端血管床充盈不完全,即远端血管对比剂不完全灌注;TIMI血流Ⅱ级为对比剂可使远端血管床显影,但是流经狭窄部位时较正常冠状动脉速度有所减慢,且狭窄远端清除对比剂的速度延缓,即远端血管对比剂缓慢灌注;TIMI血流Ⅲ级为对比剂在管腔内能够正常排空,对比剂能够快速充盈远端的血管床,血流抵达远端的速度与近端一样,即对比剂正常灌注。
1.4 资料收集
患者全部的临床、手术相关资料由课题组负责入选病例的临床医师填写,影像学资料由3位具有丰富手术经验的副高职以上介入医师分别进行判读,来确定术前、术中及术后的冠状动脉TIMI血流。
1.5 统计学处理
所有数据均采用SPSS 21.0统计学软件进行分析及处理。以均数±标准差表示计量资料,以百分数表示计数资料,其中计量资料采用方差分析(ANOVA)或t检验,计数资料采用卡方检验或Fisher确切概率法检验。因变量为二元计数资料采用二元logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者的一般资料比较
两组患者的性别、年龄、体重、近期吸烟史、高血压病、糖尿病、卒中史、慢性肾功能不全、家族史、CYP2C19基因型、肌酸酐、血红蛋白、血小板计数等一般资料比较,差异均无统计学意义(均P>0.05,表1)。
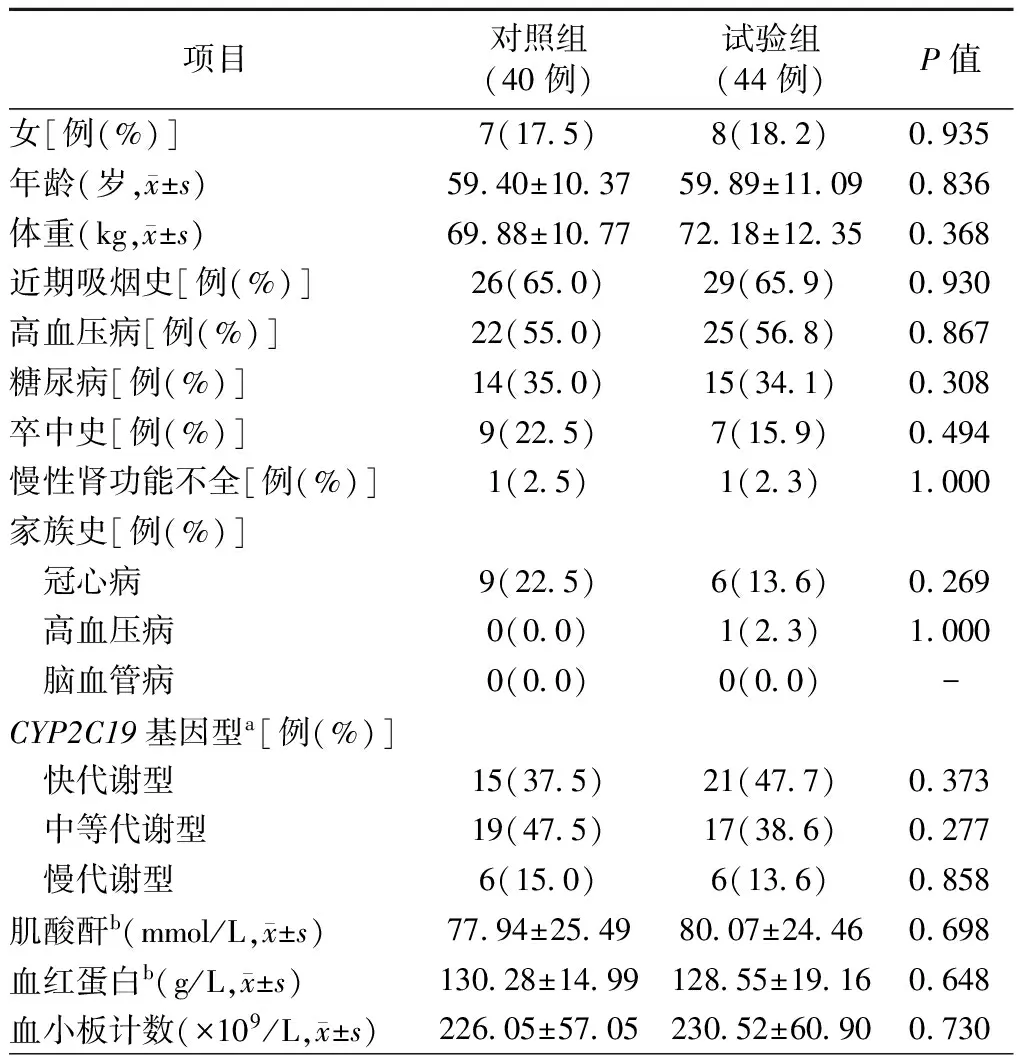
表1 两组患者的一般资料比较
注:a,CYP2C19基因型为基因芯片法测定,于在院期间采血测定;b,检验项目均为术前采血测定
2.2 两组患者的介入治疗相关指标比较
两组患者冠状动脉内比伐卢定推注剂量、冠状动脉内比伐卢定推注后ACT、罪犯血管直径分别比较,差异均有统计学意义(均P<0.05,表2)。两组其他介入治疗相关指标比较,差异均无统计学意义(均P>0.05)。
2.3 两组患者的TIMI血流比较
两组患者术前、术中(指引导丝及球囊导管开通闭塞病变后、冠状动脉内给予比伐卢定后)、术后的各级TIMI血流以及TIMI血流≤Ⅱ级的患者所占比例分别比较,差异均无统计学意义(均P>0.05,表3)。
2.4 术后TIMI血流≤Ⅱ级的多因素分析
应用二元logistic逐步回归法对多个变量进行多因素分析,包括高血压病、年龄、近期吸烟史、症状发作至就诊时间、就诊至球囊扩张时间、比伐卢定静脉负荷剂量、冠状动脉内比伐卢定推注剂量、冠状动脉内比伐卢定推注后ACT、血栓抽吸、冠状动脉内注射替罗非班或硝酸酯类药物等,未发现与术后无复流或慢血流(TIMI血流≤Ⅱ级)发生相关的危险因素(表4)。
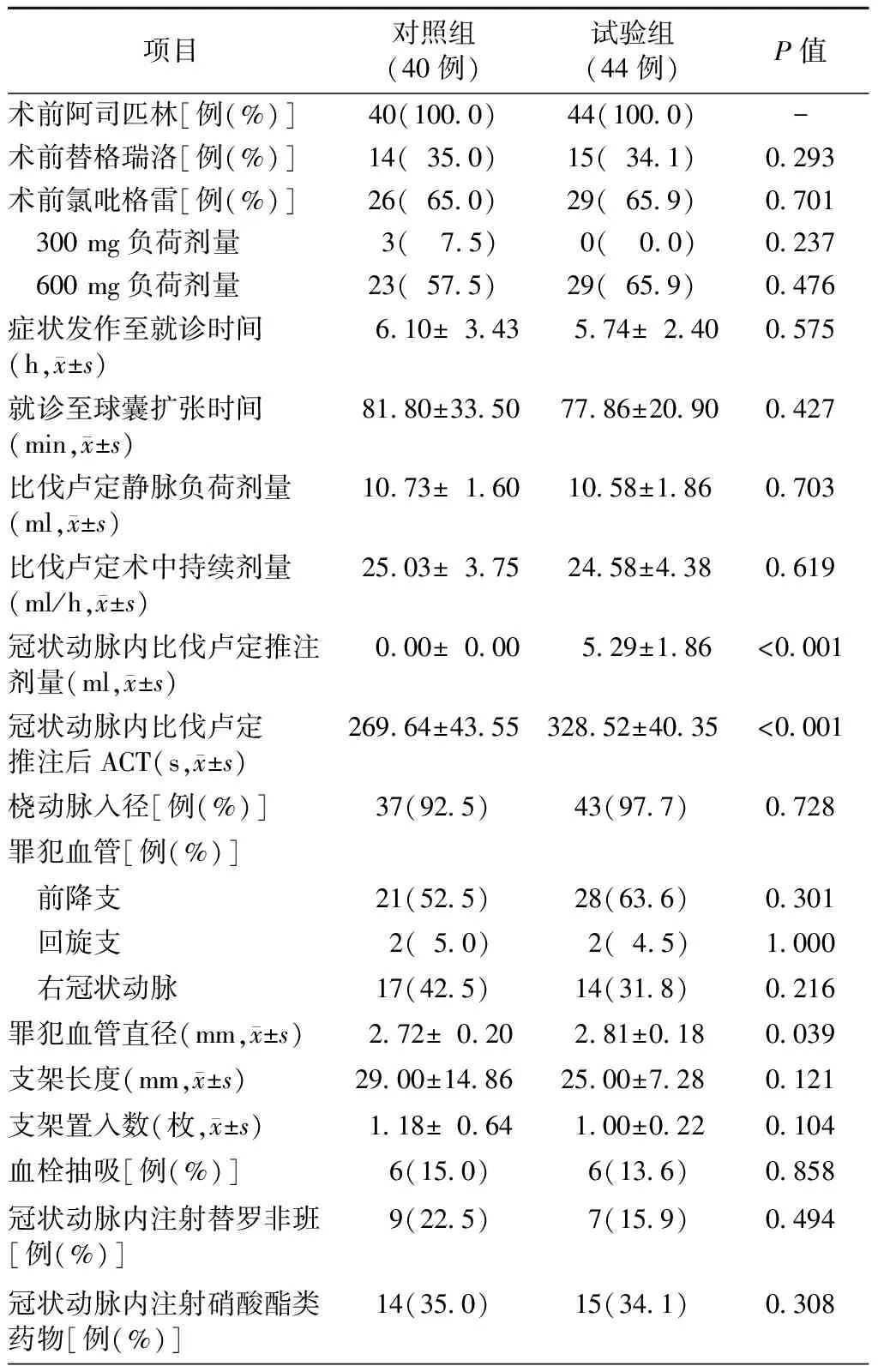
表2 两组患者的介入治疗相关指标比较
注:ACT,活化凝血时间
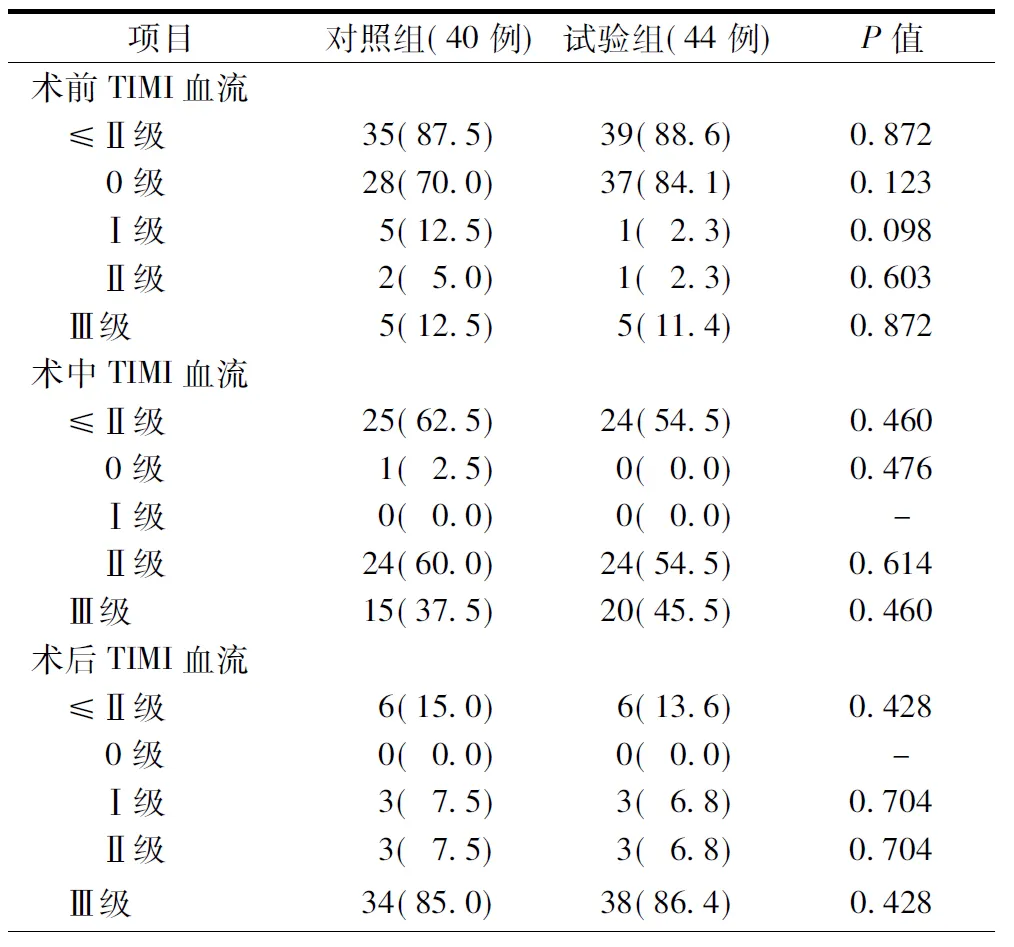
表3 两组患者的TIMI血流比较[例(%)]
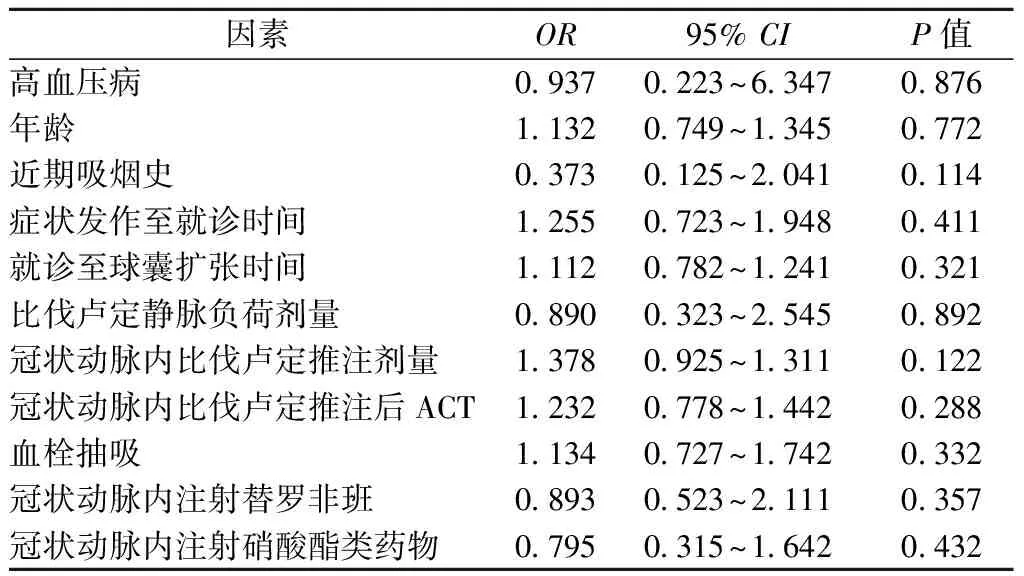
表4 术后TIMI血流≤Ⅱ级的多因素分析
注:ACT,活化凝血时间
3 讨论
STEMI发病的病因主要是由于冠状动脉内不稳定斑块破裂激活血小板并导致大量血小板聚集,进一步引发冠状动脉内血栓形成,最终导致管腔急性闭塞阻断冠状动脉内血液循环[8-10]。PPCI可明显改善STEMI患者的临床预后[11],已被指南推荐为STEMI患者心肌再灌注治疗的首选治疗策略[12]。然而大量的临床研究发现,即便已通过CAG证实IRA恢复血流,仍有5%~25%患者的心肌组织水平尚未得到有效再灌注[13-14],即冠状动脉有效再通并不意味心肌组织水平得到有效再灌注,这一现象被称为“无复流或慢血流”。对于伴有严重血栓负荷拟行冠状动脉内急诊介入术的患者,单纯经皮冠状动脉腔内成形术(percutaneous transluminal coronary angioplasty,PTCA)尚不能有效成功去除腔内血栓,同时球囊扩张或者支架释放过程不可避免地增加了血栓脱落和远端微循环栓塞的概率,进一步增加心肌水平的再灌注障碍,最终引发了心肌组织水平的无复流或慢血流[15]。持续的冠状动脉微循环再灌注障碍会导致心肌组织水平不可逆性受损,相比于正常再灌注人群总体死亡率增高了10倍,难治性无复流或慢血流死亡率进一步升高,约为32%,严重影响STEMI患者临床预后[16-19]。PPCI术后无复流或慢血流的出现,往往预示不良的临床预后,包括心功能下降、心室腔扩大、心室重构明显、死亡率增加。
多个临床及基础研究证实,无复流或慢血流的发病机制是多种因素的相互作用,包括冠状动脉微血管内皮细胞肿胀、白细胞阻塞及渗透、红细胞停滞、血管外心肌细胞水肿坏死、毛细血管和内皮细胞完整性破坏及血小板激活、微栓塞等,最终导致微循环解剖结构损害或功能障碍、微血管血流受阻[14, 20-21]。但无复流或慢血流发病的确切机制尚不清楚。对于无复流的诊治,预防其发生比出现后再进行挽救性治疗更为重要,因为心肌细胞成分及微血管解剖结构一旦损坏,即意味着发生不可逆性解剖型无复流,任何挽救性治疗策略都很难完全逆转这种不可逆性解剖结构的损坏[20]。对于急诊PPCI患者,介入操作过程中远端血栓栓塞是冠状动脉介入治疗中的严重并发症,可直接导致无复流或慢血流现象[22-23]。然而冠状动脉内远端保护装置尚未被指南推荐应用于STEMI患者PPCI术中[12]。血栓抽吸装置可以利用负压将血栓和血管远端的栓子吸出,减少远端血管的栓塞,治疗无复流,然而病变复杂程度及术者操作熟练情况严重影响血栓抽吸成功率。故无复流的防治现状日益转向药物预防,其中包括强化抗凝、抗血小板、扩冠、抗炎等,力求降低血栓栓塞发生率,减少无复流或慢血流事件发生率[24]。
比伐卢定是一种水蛭素衍生物片段,能够直接并特异性抑制凝血酶活性,并不依赖于抗凝血酶,具有较好的可预测的剂量-反应曲线,作用可逆而短暂,出血事件的发生率较低。通常能使ACT明显延长而发挥抗凝作用,预防接触性血栓形成。和传统的肝素抗凝治疗相比,更为安全。比伐卢定这种对凝血酶的直接的、短暂的、可逆性抑制作用使临床工作中更易预测、掌控其抗凝效果。并且比伐卢定的应用不会激活血小板,不会引起免疫介导的血小板减少症。自2000年比伐卢定被FDA批准作为新型抗凝药物应用于临床,多项试验结果显示:比伐卢定与单独应用普通肝素或普通肝素联合血小板糖蛋白Ⅱb/Ⅲa抑制剂相比,抗栓效果相当,但比伐卢定的主要出血事件发生率较低[11-13]。BRIGHT研究[25]显示,比伐卢定与单独应用普通肝素或普通肝素联合血小板糖蛋白Ⅱb/Ⅲa抑制剂相比,可以显著减少急性心肌梗死患者PPCI围术期的出血风险及血小板减少率,进一步减少术后30 d和1年的净不良临床事件发生率;另外PPCI术后常规高剂量延长比伐卢定注射时间可能有助于减少术后急性支架内血栓发生。既往病例报道,冠状动脉内推注比伐卢定可以对冠状动脉无复流或慢血流的患者起到较好的治疗作用,能够有效地恢复介入治疗术中冠状动脉内血流[6]。
但冠状动脉内应用比伐卢定在STEMI患者PPCI术中预防无复流或慢血流的效果如何尚无随机对照临床研究报道。本研究中,冠状动脉内应用比伐卢定与空白对照进行比较,两组患者除靶血管直径的差异有统计学意义外,其余临床、介入治疗相关指标及术前TIMI血流等基线资料均匹配,提示两组数据有可比性。进一步分析主要终点事件:两组患者术前、术中(指引导丝及球囊导管开通闭塞病变后、冠状动脉内给予比伐卢定后)、术后TIMI血流≤Ⅱ级的患者所占比例分别比较,差异均无统计学意义(均P>0.05),提示冠状动脉内注射半量比伐卢定在预防STEMI患者PPCI术中无复流或慢血流方面并不优于对照组。对可能影响梗死相关冠状动脉再灌注的多个变量进行多因素分析,包括高血压病、年龄、近期吸烟史、症状发作至就诊时间、就诊至球囊扩张时间、比伐卢定静脉负荷剂量、冠状动脉内比伐卢定推注剂量、冠状动脉内比伐卢定推注后ACT、血栓抽吸、冠状动脉内注射替罗非班或硝酸酯类药物等因素,未发现与术后无复流或慢血流(TIMI血流≤Ⅱ级)存在明显相关性。但这可能与本项探索性研究的样本量偏小有关,存在选择性偏移有关,如增大样本量可能会发现影响术后无复流或慢血流的相关因素。
本研究存在以下局限性:(1)样本量较小,可能需要更大样本的随机对照研究来进一步判断冠状动脉内应用比伐卢定对预防STEMI患者PPCI无复流或慢血流发生的临床作用。(2)冠状动脉内推注比伐卢定的剂量可能偏小,需要后续研究在确保不增加出血事件的前提下,观察增加冠状动脉内应用比伐卢定剂量的疗效和安全性,以进一步探讨冠状动脉内注射比伐卢定对无复流或慢血流的预防作用。(3)本研究未进行双盲及安慰剂对照,可能对结果判断造成一定的偏倚。
综上所述,冠状动脉内应用比伐卢定在预防STEMI患者PPCI术中无复流或慢血流方面的获益并不明显。需要进一步探索合适的剂量,并进行大样本随机对照研究来验证。
[1] Keeley EC, Boura JA, Grines CL. Primary angioplasty versus intravenous thrombolytic therapy for acute myocardial infarction: A quantitative review of 23 randomised trials. Lancet, 2003, 361(9351):13-20.
[2] Reffelmann T, Kloner RA. The “no-reflow” phenomenon: Basic science and clinical correlates. Heart, 2002, 87(2):162-168.
[3] Jaffe R, Charron T, Puley G, et al. Microvascular obstruction and the no-reflow phenomenon after percutaneous coronary intervention. Circulation, 2008, 117(24):3152-3156.
[4] Brosh D, Assali AR, Mager A, et al. Effect of no-reflow during primary percutaneous coronary intervention for acute myocardial infarction on six-month mortality. Am J Cardiol, 2007, 99(4):442-445.
[5] Heusch G, Kleinbongard P, Bose D, et al. Coronary microembolization: From bedside to bench and back to bedside. Circulation, 2009, 120(18):1822-1836.
[6] Lupi A, Porto I, Rognoni A, et al. Intracoronary bivalirudin: A new way to appease the hostile thrombus? Blood Coagul Fibrinolysis, 2013, 24(7):757-761.
[7] Timi study group. The thrombolysis in myocardial infarction (timi) trial. Phase i findings. N Engl J Med, 1985, 312(14):932-936.
[8] Higuma T, Soeda T, Abe N, et al. A combined optical coherence tomography and intravascular ultrasound study on plaque rupture, plaque erosion, and calcified nodule in patients with st-segment elevation myocardial infarction: Incidence, morphologic characteristics, and outcomes after percutaneous coronary intervention. JACC Cardiovasc Interv, 2015, 8(9):1166-1176.
[9] Matar F, Mroue J. The management of thrombotic lesions in the cardiac catheterization laboratory. J Cardiovasc Transl Res, 2012, 5(1):52-61.
[10] Ino Y, Kubo T, Tanaka A, et al. Difference of culprit lesion morphologies between st-segment elevation myocardial infarction and non-st-segment elevation acute coronary syndrome: An optical coherence tomography study. JACC Cardiovasc Interv, 2011, 4(1):76-82.
[11] Ui S, Chino M, Isshiki T. Rates of primary percutaneous coronary intervention worldwide. Circ J, 2005, 69(1):95-100.
[12] Silber S, Albertsson P, Aviles FF, et al. Guidelines for percutaneous coronary interventions. The task force for percutaneous coronary interventions of the european society of cardiology. Eur Heart J, 2005, 26(8):804-847.
[13] Tanaka A, Kawarabayashi T, Nishibori Y, et al. No-reflow phenomenon and lesion morphology in patients with acute myocardial infarction. Circulation, 2002, 105(18):2148-2152.
[14] Bouleti C, Mewton N, Germain S. The no-reflow phenomenon: State of the art. Arch Cardiovasc Dis, 2015, 108(12):661-674.
[15] Costa RA, Abizaid A, Lotan C, et al. Impact of thrombus burden on outcomes after standard versus mesh-covered stents in acute myocardial infarction (from the mguard for acute st elevation reperfusion trial). Am J Cardiol, 2015, 115(2):161-166.
[16] Hong YJ, Jeong MH, Choi YH, et al. Predictors of no-reflow after percutaneous coronary intervention for culprit lesion with plaque rupture in infarct-related artery in patients with acute myocardial infarction. J Cardiol, 2009, 54(1):36-44.
[17] Chen WR, Tian F, Chen YD, et al. Effects of liraglutide on no-reflow in patients with acute st-segment elevation myocardial infarction. Int J Cardiol, 2016, 208:109-114.
[18] Toprak C, Tabakci MM, Simsek Z, et al. Platelet/lymphocyte ratio was associated with impaired myocardial perfusion and both in-hospital and long-term adverse outcome in patients with st-segment elevation acute myocardial infarction undergoing primary coronary intervention. Postepy Kardiol Interwencyjnej, 2015, 11(4):288-297.
[19] Wozakowska-Kaplon B, Niedziela J, Krzyzak P, et al. Clinical manifestations of slow coronary flow from acute coronary syndrome to serious arrhythmias. Cardiol J, 2009, 16(5):462-468.
[20] Niccoli G, Kharbanda RK, Crea F, et al. No-reflow: Again prevention is better than treatment. Eur Heart J, 2010, 31(20):2449-2455.
[21] Kawano H, Hayashida T, Ohtani H, et al. Histopathological findings of the no-reflow phenomenon following coronary intervention for acute coronary syndrome. Int Heart J, 2005, 46(2):327-332.
[22] Jiecheng P, Ai-Ling W. Clinical significance of no-reflow in different stages of primary angioplasty among patients with acute myocardial infarctions. Perfusion, 2016, 31(4):300-306.
[23] 赵映, 陈韵岱, 田峰, 等. 急性心肌梗死患者急诊PCI术后无复流的危险因素分析. 南方医科大学学报, 2012, 32(2):261-264.
[24] Rezkalla SH, Kloner RA. No-reflow phenomenon. Circulation, 2002, 105(5):656-662.
[25] Han Y, Guo J, Zheng Y, et al. Bivalirudin vs heparin with or without tirofiban during primary percutaneous coronary intervention in acute myocardial infarction: the BRIGHT randomized clinical trial. JAMA, 2015, 313(13):1336-1346.
Pilot study on intra-coronary bivalirudin injection in preventing no/slow (re) flow during primary percutaneous coronary intervention in patients with acute ST-segment elevation myocardial infarction
LIANGZhen-yang,LIUMei-li,ZHAOXue-dong,LIYi,WANGHe-yang,ZHAOXin,TAOJie,WANGBin,NIEShao-ping,HANYa-ling.DepartmentofCardiology,GeneralHospitalofShenyangMilitaryRegion,Shenyang110016,China
Correspondingauthor:HANYa-ling,Email:hanyaling@263.net
Objective To explore the clinical effects of bivalirudin by intracoronary injection in preventing no-reflow or slow-reflow phenomenon during primary percutaneous coronary intervention (PCI) in patients with acute ST segment elevation myocardial infarction. Methods This was a prospective, randomized controlled pilot trial. A total of 84 patients with acute ST segment elevation myocardial infarction were enrolled into this study, and the patients were randomly divided to control group and Bivalirudin intracoronary injection group (Biv.ic group)at the ratio of 1∶1 (40 cases in control group and 44 cases in Biv.ic group). All patients were given intravenous maintaining does-bivalirudin by body weight. After restoring coronary blood flow (TIMI≥Ⅰ) via guide wire or micro catheter, half of the intravenous loading dose of bivalirudin was pushed intracoronary via guide wire or micro catheter in the Biv.ic group. Intracoronary bivalirudin was not given to the control group then following the normal operation. The primary endpoint was defined as no reflow or slow flow (TIMI≤Ⅱ) at the end of PPCI. Results (1) There were similar clinical baseline characters between the two groups except for the total dose of intracoronary bivalirudin [(0.00±0.00) mlvs. (5.29±1.86) ml,P<0.001] and ACT [(269.64±43.55) svs. (328.52±40.35) s,P<0.001] because introcoronary bivalirudin was not given to the control group. Target vessel diameters between the Biv. ic group and the control group [(2.81±0.18) mmvs. (2.72±0.20) mm,P=0.039] was significantly different. (2) No statistical difference was observed on no flow or slow flow (TIMI≤Ⅱ) [15%(6/40)vs. 13.6%(6/44),P=0.428] between the two groups at the end of PPCI. (3) No independent risk factors for no re-flow and slow blood flow (TIMI≤Ⅱ) were found during this pilot study. Conclusions (1) Compared with control group, there were not significantly statistical differences on no-reflow or slow flow for intracoronary bivalirudin group; (2) Large scale randomized clinical trials are needed to further verify the effect of intracoronary administration of different dose bivalirudin on the protection of no-reflow during primary percutaneous coronary intervention.
Bivalirudin; No-reflow; Slow-reflow; Acute ST-segment elevation myocardial infarction; Percutaneous coronary intervention
10.3969/j.issn.1004-8812.2016.11.009
辽宁省自然科学基金指导计划项目(201602779)
110016 辽宁沈阳,沈阳军区总医院心内科 全军心血管病研究所(梁振洋、刘美丽、李毅、王贺阳、赵昕、陶杰、王斌、韩雅玲);北京,首都医科大学附属北京安贞医院急诊危重症中心(赵雪东、聂绍平)
韩雅玲,Email:hanyaling@263.net
R542.22
2016-08-23)
