Elecsys HBsAg COI灰区标本再分析探讨
2016-12-06姚家奎印晓静钱小丽成红霞
姚家奎,印晓静,钱小丽,成红霞
(江苏省苏北人民医院医学检验科,江苏扬州 225001)
·经验交流·
Elecsys HBsAg COI灰区标本再分析探讨
姚家奎,印晓静,钱小丽,成红霞△
(江苏省苏北人民医院医学检验科,江苏扬州 225001)
目的 探讨电化学发光免疫分析(ECLIA)法乙型肝炎病毒(HBV)表面抗原(HBsAg)cut off指数(COI)灰区标本再次进行确证分析的临床价值。方法 被检血清标本均来自2014年1月至2015年3月该院就诊的门诊和住院患者,应用Elecsys HBsAg确证试验对213例ECLIA法检出HBsAg COI灰区标本进行再分析并对受检标本HBV血清标志物两对半(以下简称乙肝两对半)模式进行回顾性分析。结果 213份标本中ECLIA法检测HBsAg COI结果为0.80~0.99 31例,经Elecsys HBsAg确证试验阳性2例[6.45%(2/31)];HBsAg COI结果为1.0~1.99弱反应性标本93例,经Elecsys HBsAg确证试验阳性92例[98.92%(92/93)];HBsAg COI结果为2.0~6.99 89例,经Elecsys HBsAg确证试验均为阳性,阳性率为100.00%(89/89);213例ECLIA法检出HBsAg COI灰区标本经Elecsys HBsAg确证试验阳性183例,检出6种乙肝两对半模式,其中HBsAg、HBV e抗体(HBeAb)、HBV核心抗体(HBcAb)阳性模式155例,占大多数[72.77%(155/213)];经Elecsys HBsAg确证试验阴性30份标本中检出7种乙肝两对半模式,其中HBeAb、HBcAb阳性模式16例,检出率为7.51%(16/213)。结论 ECLIA法乙肝两对半定量检测HBsAg临界或较低水平的弱反应性标本、乙型肝炎感染模式不常见的标本时需经Elecsys HBsAg确证试验再分析以防止假阴性或假阳性结果的出现。
肝炎病毒, 乙型; 肝炎表面抗原,乙型; 电化学; 免疫测定; 乙型肝炎病毒表面抗原定量试验; 乙型肝炎病毒表面抗原确证试验
乙型肝炎病毒(HBV)血清标志物(以下简称乙肝两对半)定量检测是用来评估人体自身免疫系统对抗HBV能力的简单、可靠的方法,其能帮助医生监测和评估患者抗病毒治疗的应答情况,早期预测治疗是否有效[1]。然而在具体操作过程中由于一些HBV低浓度携带者的低抗原量及检测方法学所限等原因造成了HBV表面抗原(HBsAg)的漏检和假阳性,不得不引起临床和检验医生的关注。近年来随着检验技术的不断发展,根据临床需要及各自检测方法优势来选择经济、适用、结果可靠的检验方法,制定标准规范操作程序已成为必然。由于电化学发光免疫分析(ECLIA)法为定量检测、操作简单,亦可对乙肝两对半模式进行确证试验,且在乙型肝炎患者病情的动态观察和药物疗效考核方面具有重要意义,已在临床逐步推广应用[2-3]。本研究探讨了ECLIA法在乙肝两对半定量试验中HBsAg cut off指数(COI)灰区标本的主要模式及再次进行确证分析的临床价值。
1 材料与方法
1.1 标本来源 所有被检血清标本均来自2014年1月至2015年3月本院就诊的门诊和住院患者。
1.2 仪器及信息系统 德国Roche cobas 6000全自动生化分析仪、Roche RSA样品前处理系统、北京智方LIS系统及cabas IT3000 solution软件系统。
1.3 试剂 Roche cobas 6000全自动生化分析仪(ECLIA法)配套乙肝两对半定量试剂、定标液1、定标液2、HBsAg确证试剂及HBsAgⅡ质控品等均由德国罗氏诊断公司生产,所有试剂均在有效期内使用。
1.4 方法 采集被检者空腹静脉血3 mL,经Roche RSA样品前处理系统签收、离心、去除试管盖后采用Roche cobas 6000全自动生化析仪分别对相应样本进行检测分析并对HBsAg临界及弱反应性标本进行Elecsys HBsAg确证试验再分析。为确保受检血清标本与确认试剂、质控试剂反应过程条件一致,确证试验检测前将Roche cobas 6000封闭3个检测池,只保留1个检测池。
1.5 检测结果判定 乙肝两对半定量检测采用ECLIA法由Elecsys软件自动通过比较样本的反应产物产生的光电信号和定标液得出cut off值进行结果判定。HBsAg≥1.0 COI为有反应性,<1.0 COI为无反应性。Elecsys HBsAg确证试验的样本和阳性Ⅱ质控品同时经确认试剂、质控试剂预处理30 min后经Roche Modular cobas 6000全自动生化分析仪检测COI,在审核检测的有效性条件下(在确证试剂检测中Elecsys Preci Control HBsAgⅡ的COI必须小于质控试剂检测的COI 50%),若质控试剂检测的标本COI为100%,确证试剂检测的标本COI 为X%,则结果解释为X>50%,且质控试剂检测的COI ≥0.9确证试验结果为无反应性;X<50%且质控试剂检测的COI≥0.9确证试验结果为阳性。
2 结 果
2.1 ECLIA法与Elecsys HBsAg 确证试验检测HBsAg结果比较 213例ECLIA法检出HBsAg COI临界及弱反应性标本再次进行Elecsys HBsAg确证试验结果比较见表1。
2.2 Elecsys HBsAg确证试验阴、阳性标本乙肝两对半模式分析 213例ECLIA法检出HBsAg COI灰区标本经Elecsys HBsAg 确证试验阳性183例,检出6种乙肝两对半模式,其中HBsAg、HBV e抗体(HBeAb)、HBV核心抗体(HBcAb)阳性模式155例占大多数,检出率为72.77%(155/213);经Elecsys HBsAg 确证试验阴性30例,检出7种乙肝两对半模式,其中HBeAb、HBcAb阳性模式16例,检出率为7.51%(16/213)。
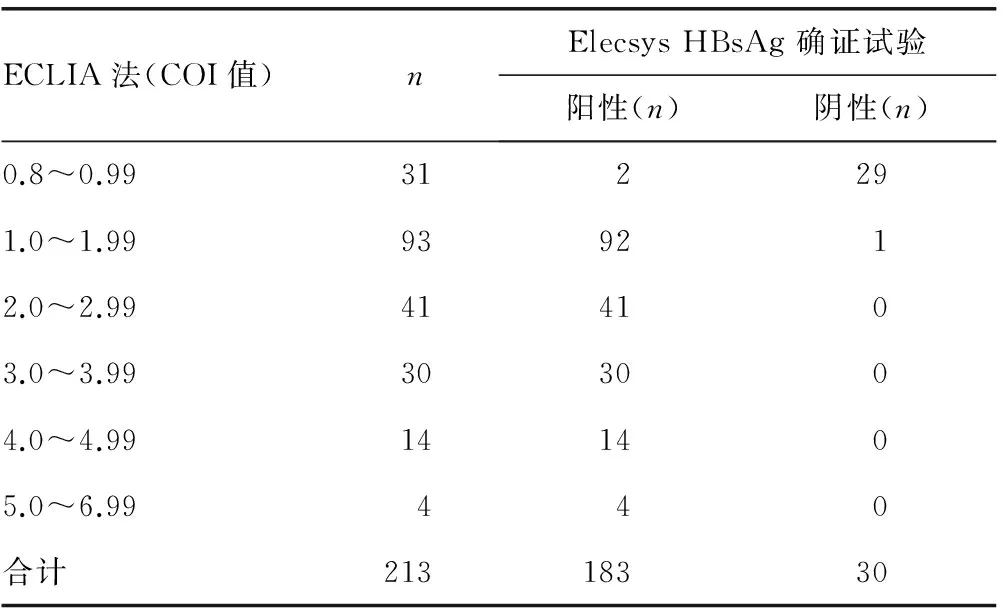
表1 ECLIA法与Elecsys HBsAg 确证试验检测HBsAg结果比较
3 讨 论
ECLIA法是将发光系统与免疫相结合以检测抗原或抗体的方法,是继放射免疫、酶免疫、荧光免疫、化学发光免疫之后的新一代标记免疫技术,其具有操作简便、试剂贮存有效期长、检测速度快、灵敏度高(可达0.05 ng/mL)、线性范围宽、应用范围广等特点[4]。有研究证实,单克隆捕捉抗体技术的测定方法不能检测到HBsAg突变的重组株和自然突变株,而多克隆捕捉抗体的检测技术对HBsAg突变株具有良好的识别能力,为避免HBsAg突变株引起的假阴性,Elecsys HBsAg Ⅱ定量试验与确证试验采用的是多克隆抗体。该检测方法根据在选择性压力(由抗病毒治疗或免疫系统本身引起)下,病毒可表达多种不同的HBsAg突变株,而一些HBsAg检测试剂可能无法检测到,Roche coche cobas 6000全自动生化分析仪的ECLIA法Elecsys HBsAgⅡ检测试剂是特别针对检测这些突变株而研发的,其检测的特异性、灵敏度更高,线性范围更宽[5-6]。本研究213份标本中ECLIA法检测HBsAg COI结果为0.80~0.99 31例,经 Elecsys HBsAg确证试验阳性2 例,COI值分别为0.924、0.890,占6.45%(2/31);HBsAg COI结果为1.0~1.99 93例,经Elecsys HBsAg确证试验阳性92例[98.92%(92/93)];HBsAg COI结果2.0~6.99 89例,经 Elecsys HBsAg确证试验均为阳性,阳性率为100.00%(89/89),表明ECLIA法检出HBsAg COI <2.0标本应经Elecsys HBsAgⅡ确证试验再次分析,由于Roche coche cobas 6000全自动生化分析仪的Elecsys HBsAgⅡ检测试剂具有上述优势,因而 HBsAg COI>2.0标本可以结合其他HBV标志物不必再次进行HBsAg确证试验分析。所以对采用ECLIA法检测的灰区样本再用确诊的方法进行确认分析,获得的结果对临床工作中试剂的选择及乙型肝炎的诊治具有指导价值。
近年来ECLIA法在一些医院已经被用于HBV血清标志物的检测,是一种灵敏度和可信度较高的分析技术[7-8]。尤其HBsAg COI临界及弱反应标本已被临床和检验医生高度关注,经Elecsys HBsAgⅡ确证试验检测后结果将成为临床医生评价病情及疗效的重要参考依据。本研究低浓度HBsAg标本中HBsAg、HBeAb、HBcAb结果有反应性,该模式标本共155例,检出率最为多见[72.77%(155/213)],在临床绝大多数情况下,HBsAg和HBcAb同时存在,单独存在的情况并不多见,本研究所有经确证HBsAg低浓度弱反应性标本HBcAb均同时阳性,经Elecsys HBsAg 确证试验阴性标本30例,以模式HBeAb、HBcAb结果有反应性较多16例,检出率为7.51%(16/213)。因而日常检验过程中由于方法学等因素不能检测到低浓度HBsAg时若同时检测HBcAb,结合HBV-DNA和前S蛋白等检测作为HBV感染的佐证相关指标,完善各种模式的意义解释,对于上述人群的流行病学筛查和临床诊断会有较大帮助,特别是在保证输血安全和控制医院感染方面具有重要价值。另值得关注的是HBsAg与HBsAb同时存在的模式也占一定数量,共16例[7.51%(16/213)],有研究表明,二者同时存在的内在机制可能是HBV发生变异,但也说明在极少部分HBsAb阳性人群中仍存在较低水平的HBsAg不易检出。李金明等[9]和徐克等[10]等研究表明,可能的解释为其前S、S基因的突变,使得突变型HBsAg和针对野生型HBsAg的抗体同时产生不同亚型特异的HBsAb或新的HBV病毒株感染。因此,作者认为必须执行乙肝两对半检测标准操作程序,对HBsAg灰区标本、可疑或乙肝两对半模式不常见的标本需再次用灵敏度更高的ECLIA等方法复检,甚至送到有条件的实验室对检测结果再次确证分析以防假阴性或假阳性出现。
[1]盛欢,胡晓波,许洁.两种方法检测HBsAg定量结果的临床互认研究[J].检验医学,2013,28(9):828-834.
[2]姚家奎,韩东升,周林,等.ECLIA法定量检测乙肝血清标志物的临床应用[J].国际检验医学杂志,2014,35(22):3122-3123.
[3]Brunetto MR,Moriconi F,Bonino F,et al.Hepatitis B virus surface antigen levels:a guide to sustained response to peginterferon alfa-2a in HBeAg-negative chronic hepatitis B[J].Hepatology,2009,49(4):1141-1150.
[4]马红霞,周运恒,杨蔺,等.ELISA法和电化学发光免疫法检测血清HBsAg结果比较分析[J].检验医学,2010,25(6):473-474.
[5] 姚家奎,丁德坤,张素华,等.Elecsys HBsAg确证试验在灰区及弱反应性标本检测中的应用[J].现代检验医学杂志,2013,28(6):106-109.
[6] Jia JD,Hong M,Wei L,et al.Multicentre evaluation of the Elecsys hepatitis B surface antigen Ⅱassay for detection of HBsAg in comparison with other commercially available assays[J].Med Microbiol Immunol,2009,198(4):265-269.
[7] 刘佳,陈霖,徐军,等.HBsAg和HBsAb双阳性乙肝患者血清中HBsAb确认方法的建立[J].中华实验和临床病毒学杂志,2011,25(6):492-494.
[8]谷娅楠,程艳杰,朱鸿,等.HBsAg弱阳性标本4种检测方法敏感性的比较[J].医学与哲学,2013,34(8B):31-33.
[9]李金明,张瑞.常用乙型病毒性肝炎血清学标志物检测结果报告解释及临床应用[J].中华检验医学杂志,2012,35(4):296-300.
[10]徐克,池胜英,吴丽英,等.电化学发光法测定10 409例乙型肝炎病毒标志物的结果分析[J].检验医学,2011,26(10):700-702.
10.3969/j.issn.1673-4130.2016.02.064
B
1673-4130(2016)02-0277-02
2015-06-28)
△通讯作者,E-mail:2460672142@qq.com。
