清胰复方制剂对大鼠的长期毒性研究*
2016-09-08茆芮婕姚晓东何芋岐周旭美遵义医学院贵州遵义563003遵义医学院药学院临床药学系贵州遵义563003
雷 蕾,茆芮婕,汪 巍,姚晓东,何芋岐,周旭美△(.遵义医学院,贵州遵义563003;.遵义医学院药学院临床药学系,贵州遵义563003)
清胰复方制剂对大鼠的长期毒性研究*
雷蕾1,茆芮婕2,汪巍1,姚晓东1,何芋岐1,周旭美2△(1.遵义医学院,贵州遵义563003;2.遵义医学院药学院临床药学系,贵州遵义563003)
目的通过大鼠长期毒性实验,从临床前研究角度评价清胰复方制剂的临床用药安全性。方法将80只SD大鼠分为A组和B组,每组40只,分别用于观察毒性反应、迟发性毒性反应及毒性消失时间。两组大鼠均分别再分为空白组(生理盐水同体积灌胃)及清胰复方制剂高(81.0 g/kg)、中(27.0 g/kg)、低(13.5 g/kg)剂量组,每组10只。A组大鼠连续给予药物及相应对照物(生理盐水),4周后观察大鼠行为学变化、体质量等常规指标、血常规及转氨酶等血液学指标及主要器官脏器指数的变化。B组大鼠连续给药4周后停药2周观察相关指标(同A组)的变化。结果给药4周后,清胰复方制剂高剂量组(A4组)大鼠各项血液学指标显著变化,脏器指数明显升高,体质量显著降低;中剂量组(A3组)大鼠丙氨酸氨基转移酶、总胆红素、血红蛋白、肝脏脏器指数显著变化,与空白组(A1组)比较,差异均有统计学意义(P<0.05);而低剂量组(A2组)大鼠除总胆红素升高外,其他各项指标均无明显变化。停药2周后,高、中、低剂量组(B4、B3、B2组)各项相关指标均无明显变化,与空白组(B1组)比较,差异均无统计学意义(P>0.05)。结论实验设置的最低剂量为临床剂量的5倍,给药时间远长于临床给药时间,故清胰复方制剂按现有临床给药方案基本安全,但该结论尚需进一步的临床数据加以验证。
中草药/毒性;复方合剂;胰腺炎/中药疗法;清胰复方制剂;大鼠
清胰复方制剂是遵义医学院附属医院药剂科制剂室参照相关文献[1-2]研制并长期应用于临床的院内中药复方制剂,主要由大黄、赤芍、栀子等组成,遵义医学院附属医院长期应用该方治疗急性胰腺炎。已有研究证实,该复方制剂治疗胰腺炎具有显著疗效[3-5]。该方含有大黄等具有明显消化道不良反应的中药[6],但其安全性长期未能得到评价。尽管在现有的治疗方案中未发现明显毒性反应,但是安全性评价的缺乏对该方进一步的二次开发和临床剂量及疗程调整造成了阻碍。本研究旨在从对清胰复方制剂进行再开发的角度,在临床前对其安全性进行研究,并着重于对其长期毒性的评价。
1 材料与方法
1.1材料
1.1.1实验动物清洁级SD大鼠80只[雌雄各半、体质量(250±20)g]购自第三军医大学大坪医院实验动物中心,实验动物生产许可证号:SCXK(渝)2012-1005。
1.1.2药物与试剂清胰复方制剂处方组成:大黄(批号:150323)、栀子(批号:150327)、延胡索(批号:150323)、木香(批号:150323)、赤芍(批号:150327)、牡丹皮(批号:150323)、厚朴(批号:150323)、芒硝(批号:150203)由遵义医学院附属医院药剂科中药房提供。浸膏按文献[7]的制备工艺制备。给药溶液制备:将2g/mL的浸膏分别稀释6倍和3倍制备成中、低剂量,原质量浓度作为高剂量。试剂为血常规检测试剂(日本希森美康株式会社)、生化检测试剂(美国雅培制药有限公司)、水合氯醛(HG 3-1004-76,天津市兴复精细化工研究所)等。
1.1.3仪器ME204E型电子分析天平(梅特勒-托利多仪器有限公司)、H1650-W型离心机(湖南湘仪实验室仪器开发有限公司)、101-4A型电热鼓风干燥箱(北京中兴伟业仪器有限公司)、RE-5205旋转蒸发器(上海亚荣生化仪器厂)、AU5800全自动生化分析仪(美国贝克曼库尔特有限公司)、XE5000全自动血细胞分析仪(日本希森美康株式会社)等。
1.2方法将80只SD大鼠分为A组和B组,每组40只,两组大鼠再分别分为4个小组,每组10只,雌雄各半。其中A1~A4组用于观察长期毒性反应,B1~B4组用于观察毒性消失时间及迟发性毒性反应。两组大鼠中,1组为空白组(生理盐水),2~4组分别为清胰复方制剂低(13.5 g/kg)、中(27.0 g/kg)、高(81.0 g/kg)剂量组。A组大鼠连续给药4周,随时监测行为学及体质量变化,4周后检测各项血清生化指标及脏器指数等变化;B组大鼠给药4周后停药2周,观察指标同A组。各组大鼠实验结束后,用水合氯醛(7%,0.5 mL/100g)麻醉,腹主动脉取血,取心、肝、脾、肺、肾、胰腺等器官,称质量并保存于-80℃冰箱备用。
1.2.1行为学观察每天观察大鼠外观、行为活动、饮食、排泄物、中毒反应及死亡情况,并每周称体质量1次。
1.2.2血液学检查A组大鼠给药4周后、B组大鼠给药4周后停药2周分别眼眶取血检查血液生化指标[天门冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、总胆红素(TBIL)],腹主动脉取血检查血常规(白细胞计数、红细胞计数和血红蛋白)。
1.2.3组织检查A组大鼠给药4周后、B组大鼠给药4周后停药2周分别对大鼠进行解剖,取心、肝、脾、肺、肾和胰腺,肉眼观察并称质量,计算脏器指数。
1.3统计学处理采用SPSS11.5统计软件进行数据分析,计量资料以±s表示,组间比较采用t检验,P<0.05为差异有统计学意义。
2 结 果
2.1大鼠行为学观察结果给药4周后,低、中剂量组(A2、A3组)大鼠毛色光泽,行为正常,而高剂量组(A4组)大鼠则毛色暗淡,行为萎靡。两组高、中、低剂量组(A4、A3、A2、B4、B3、B2组)大鼠均出现腹泻并具有剂量依赖关系。停药2周后,高、中、低剂量组(B4、B3、B2组)大鼠行为学观察结果与空白组(B1组)比较,差异均无统计学意义(P>0.05)。
2.2清胰复方制剂对大鼠体质量的影响清胰复方制剂造成大鼠体质量连续降低,并具有剂量依赖关系。高剂量组(A4组)大鼠从给药第1周体质量即出现降低,至给药4周,体质量显著降低;中剂量组(A3组)从给药第2周、低剂量组(A2组)从给药第3周开始体质量显著降低,与空白组(A1组)比较,差异均有统计学意义(P<0.05)。停药2周后,高、中、低剂量组(B4、B3、B2组)大鼠体质量均无明显变化,与空白组(B1组)比较,差异均无统计学意义(P>0.05)。
2.3清胰复方制剂对大鼠血常规及血清生化指标的影响
2.3.1清胰复方制剂对大鼠血常规的影响给药4周后,与空白组(A1组)比较,高剂量组(A4组)白细胞计数、红细胞计数、血红蛋白均显著升高,中剂量组(A3组)血红蛋白显著升高,差异均有统计学意义(P<0.05);而低剂量组(A2组)无明显变化,差异均无统计学意义(P>0.05)。停药2周后,高、中、低剂量组(B4、B3、B2组)各项指标均无明显变化,与空白组(B1组)比较,差异均无统计学意义(P>0.05)。见表1。
表1 清胰复方制剂对大鼠血常规的影响(±s)
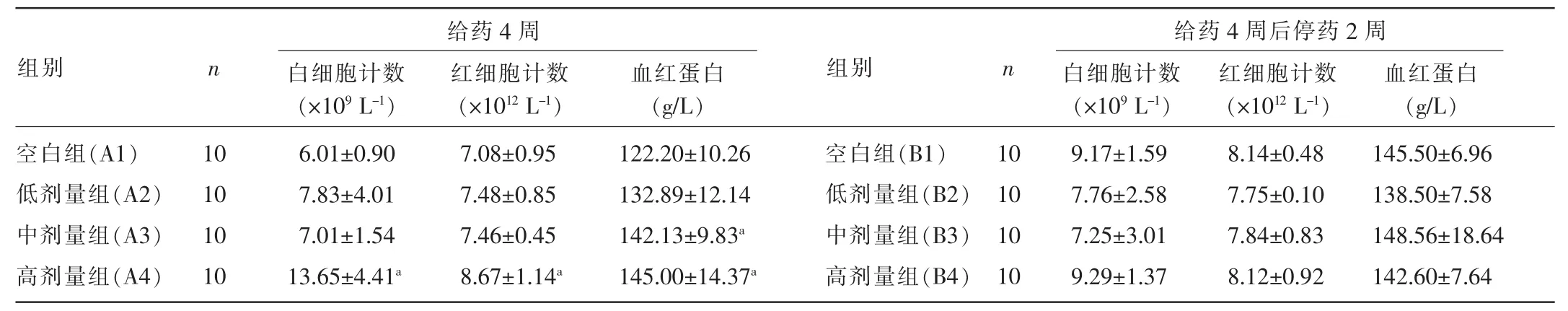
表1 清胰复方制剂对大鼠血常规的影响(±s)
注:与空白组比较,aP<0.05。
给药4周组别n 白细胞计数(×109L-1)红细胞计数(×1012L-1)血红蛋白(g/L)给药4周后停药2周组别n 白细胞计数(×109L-1)红细胞计数(×1012L-1)血红蛋白(g/L)空白组(A1)低剂量组(A2)中剂量组(A3)高剂量组(A4)10 10 10 10 6.01±0.90 7.83±4.01 7.01±1.54 13.65±4.41a7.08±0.95 7.48±0.85 7.46±0.45 8.67±1.14a122.20±10.26 132.89±12.14 142.13±9.83a145.00±14.37a空白组(B1)低剂量组(B2)中剂量组(B3)高剂量组(B4)10 10 10 10 9.17±1.59 7.76±2.58 7.25±3.01 9.29±1.37 8.14±0.48 7.75±0.10 7.84±0.83 8.12±0.92 145.50±6.96 138.50±7.58 148.56±18.64 142.60±7.64
2.3.2清胰复方制剂对大鼠血清生化指标的影响给药4周后,与空白组(A1组)比较,高剂量组(A4组)ALT、AST、TBIL显著变化,尤其是TBIL明显升高;中剂量组(A3组)ALT和TBIL显著变化,差异均有统计学意义(P<0.05);低剂量组(A2组)除TBIL升高外,ALT、AST均无明显变化,差异无统计学意义(P>0.05)。停药2周后,与空白组(B1组)比较,高、中、低剂量组(B4、B3、B2组)ALT、AST、TBIL均无明显变化,差异均无统计学意义(P<0.05)。见表2。
表2 清胰复方制剂对大鼠血清生化指标的影响(±s)

表2 清胰复方制剂对大鼠血清生化指标的影响(±s)
注:与空白组比较,aP<0.05。
给药4周组别n给药4周后停药2周组别n ALT(U/L)AST(U/L) TBIL(μmol/L)ALT(U/L)AST(U/L) TBIL(μmol/L)空白组(A1)低剂量组(A2)中剂量组(A3)高剂量组(A4)空白组(B1)低剂量组(B2)中剂量组(B3)高剂量组(B4)10 10 10 10 37.60±6.70 31.20±10.44 31.20±4.47a46.80±3.70a117.80±23.72 111.70±19.23 100.90±22.32 75.60±13.16a1.87±1.20 6.95±2.28a12.00±2.06a21.28±4.94a10 10 10 10 43.70±17.14 36.00±4.07 51.33±35.11 42.40±10.31 130.30±50.11 100.13±17.33 104.44±19.92 118.40±42.41 1.11±0.71 0.66±0.48 1.03±0.77 2.08±1.64
2.4清胰复方制剂对大鼠脏器指数的影响给药4周后,高剂量组(A4组)大鼠心、肝、脾、肺、肾、胰腺等脏器指数,中剂量组(A3组)大鼠肝脏脏器指数均高于空白组(A1组),差异均有统计学意义(P<0.05);低剂量组(A2组)大鼠各脏器指数均无明显变化,与空白组(A1组)比较,差异均无统计学意义(P>0.05)。停药2周后,高、中、低剂量组(B4、B3、B2组)大鼠心、肝、脾、肺、肾、胰腺等脏器指数均无明显变化,与空白组(B1组)比较,差异均无统计学意义(P>0.05)。见图1、2。

图1 A组大鼠主要脏器指数变化
图2 B组大鼠主要脏器指数变化
3 讨 论
清胰复方制剂是具有较长使用历史的院内制剂,其疗效得到了临床的肯定。但其应用剂型至今仍然采用汤剂形式服用,使用效率不高,制约了其在临床的推广应用。因此,迫切需要对其进行二次开发。安全性是新药研发的重要关注点,同时对临床安全用药具有重要指导意义[8]。但迄今为止,有关清胰复方制剂的安全性评价仍鲜见报道。方中大黄的不良反应是本研究尤其关注的,在处方分析阶段即引起研究者的注意。大黄泻下作用非常显著[9],已有动物实验证明了单味药大黄的泻下作用[10],复方是否会导致严重腹泻值得考虑。事实上,本研究的确观察到高、中、低剂量组大鼠均存在不同程度腹泻,尤其在高剂量组,腹泻非常明显。这种腹泻会扰乱整个消化系统平衡,并通过各种潜在机制造成脏器损伤。例如,由胆汁酸介导的整个消化道循环可能受到破坏,而胆汁酸紊乱是造成肝损伤的重要诱因[11],也是临床上重要的检测指标[12]。因此,胆汁酸介导的清胰复方制剂的作用及不良反应机制将成为作者未来研究的重点。除此之外,在其余指标上,低剂量组大鼠无明显变化。由于低剂量组已经高于临床用药的5倍剂量,而且本研究设置的给药时间远长于临床,停药2周后,B组高、中、低剂量组大鼠各项相关指标均无明显变化,说明不会出现药物积蓄而产生毒性反应。因此,从动物实验角度可以说明清胰复方制剂基本安全,但仍需进一步的临床数据加以验证。
[1]解发良.古今名方[M].2版.郑州:河南科学技术出版社,2001:638-639.
[2]兑丹华,舒涛,余德刚.清胰Ⅱ号治疗急性胰腺炎疗效观察[J].现代中西医结合杂志,2002,11(5):399-400.
[3]兑丹华,高占峰,赵鹏,等.清胰Ⅱ号和粉防己碱对实验性重症急性胰腺炎的治疗作用[J].第三军医大学学报,2005,27(24):2418-2421.
[4]蔡治方,兑丹华,王俊,等.清胰Ⅱ号方对重症急性胰腺炎大鼠肠黏膜屏障功能的影响[J].中国中西医结合杂志,2012,32(4):490-493.
[5]彭慈军,赵鹏,兑丹华.清胰Ⅱ号对大鼠重症急性胰腺炎肺损伤的保护作用[J].第四军医大学学报,2007,28(19):1757-1759.
[6]张新立.浅议中药大黄的临床应用[J].内蒙古中医药,2012,31(9):68.
[7]姚晓东,周旭美,张倩茹,等.清胰利胆口服液质量标准研究[J].遵义医学院学报,2011,34(6):580-582.
[8]张雪梅,骞秀芳.术竭异位安胶囊对大鼠的长期毒性实验研究[J].中国药物警戒,2014,11(3):129-133.
[9]张燕,李治建,夏木西努尔,等.土大黄化学成分及药理作用研究进展[J].中药药理与临床,2012,28(3):173-176.
[10]刘亮亮,隋峰,闫美娟,等.大黄炮制品各组分泻下作用的比较研究[J].中国实验方剂学杂志,2012,18(17):161-165.
[11]徐祎骏,赵丛,尹艳茹.法尼酯X受体在肝胆、胃肠道疾病中的作用[J].生理科学进展,2013,44(6):420-424.
[12]沈红.胆汁酸测定在肝胆疾病诊断中的临床价值[J].吉林医学,2014,35(29):6519.
Long-term toxicity study of Qingyi Compound Preparation on rats*
Lei Lei1,Mao Ruijie2,Wang Wei1,Yao Xiaodong1,He Yuqi1,Zhou Xumei2△(1.Zunyi Medical College,Zunyi,Guizhou 563003,China;2.Department of Clinical Pharmacy,College of Pharmacy,Zunyi Medical College,Zunyi,Guizhou 563003,China)
ObjectiveTo evaluate the safety of clinical medication of Qingyi Compound Preparation from the angle of preclinical study by conducting the rat long term toxicity experiments.Methods80 SD rats were divided into the group A and B for observing the toxicity reaction,delayed toxicity reaction and toxicity disappearance time,40 cases in each group.The two groups were re-divided into the blank group(gavage by same volume of normal saline),Qingyi Compound Preparation high dose (81.0g/kg),middle dose(27.0 g/kg)and low dose(13.5 g/kg)groups,10 cases in each group.The group A was continuously given the medication and corresponding contrast(normal saline).The behavior change,routine indicators of body mass(BS),blood routine,transaminase and visceral index of main organs were observed after 4 weeks.The group B was continuously given the medication for 4 weeks,after 2-weeks medication withdrawal,the related indicators(same as the group A)were observed.ResultsThe various hematological indicators in the high dose group(A4)were significantly changed,the visceral indexes were obviously increased,while the body mass was significantly decreased;alanine aminotransferase,total bilirubin,Hb,visceral index of liver in the middle dose group(A3)were significantly changed,showing statistical difference compared with the blank group(A1)(P<0.05);except the total bilirubin increase,other indicators in the low dose group had no obvious change.The various indicators after 2-week medication withdrawal in the high,middle and low doses groups(B4,B3 and B2)had no obvious changes,compared with the blank group(B1),there was no statistical difference(P>0.05).ConclusionThe lowest dose set by the experiments is 5 times of clinical dose,the medication time is much longer than clinical medication time,therefore Qingyi Compound Preparation is basically safe according to present medication regimen,but this conclusion needs to be verified by further clinical data.
Drugs,chinese herbal/toxicity;Drug combinations;Pancreatitis/zhong yao liao fa;Qingyi prescription;Rats
10.3969/j.issn.1009-5519.2016.01.004
A
1009-5519(2016)01-0011-03
上海市复方中药重点实验室开放基金资助项目(2014OP01);遵义医学院大学生创新创业训练计划项目(院发[2014]5802)。
雷蕾(1991-),在读硕士研究生,主要从事药物分析研究。
△,E-mail:zmczxm@163.com。
(2015-10-03)
