复方茜草片质量标准的研究
2016-09-06方乐敏浦益琼上海中医药大学上海20203上海市香山中医医院上海200020
方乐敏, 杨 骏,2, 刘 云, 浦益琼*, 张 彤*(.上海中医药大学,上海20203;2.上海市香山中医医院,上海200020)
复方茜草片质量标准的研究
方乐敏1, 杨 骏1,2, 刘 云1, 浦益琼1*, 张 彤1*
(1.上海中医药大学,上海201203;2.上海市香山中医医院,上海200020)
目的 建立复方茜草片 (茜草和新疆紫草)的质量标准。方法 TLC法对茜草和新疆紫草进行鉴别,HPLC法测定大叶茜草素含有量。分析采用C18色谱柱(250 mm×4.6 mm,5μm);流动相甲醇-乙腈-0.2%磷酸 (25∶50∶25);体积流量1.0 mL/min;柱温25℃;检测波长250 nm。结果 TLC斑点清晰,分离度好。大叶茜草素在0.828 125~106μg/mL范围内线性关系良好 (r=0.999 8),平均加样回收率为96.66% (RSD=2.04%)。结论 该方法可用于复方茜草片的质量控制。
复方茜草片;茜草;新疆紫草;大叶茜草素
复方茜草片系上海中医药大学附属龙华医院的临床经验方,由茜草和新疆紫草2味中药组成,用于改善肝硬化脾功能亢进引起的血小板减少症和凝血功能障碍,短期效果明显,现已成为协定处方,广泛用于肝硬化脾功能亢进和免疫性血小板减少性紫癜 (ITP)的治疗。该方以茜草[1]为君药,取其凉血止血活血之功;新疆紫草[1]为臣药,取其清热解毒凉血之功效,以加强茜草的凉血效果,全方组方精简,共奏凉血止血、清热活血之功效,适用于血小板减少症的治疗,尤其对免疫性血小板减少症有较好的疗效。其中,蒽醌及其苷类为茜草的主要化学成分,此外还含有萘醌、萜类、己肽、多糖[2-4]等化合物,其药理作用包括止血、升高白细胞、促进机体造血功能、抗癌活性[5-7]等;新疆紫草的主要化学成分为萘醌类化合物,其中紫草色素即为萘醌色素[8-9],其存在形式多为结合成酯,脂溶性较好,具有电子传递作用,促进或干扰部分生化反应过程,表现多种生物活性[10]。此外,紫草中还含有多糖、酚酸、生物碱、单萜苯醌、苯酚、三萜酸、甾醇及黄酮等[11]成分,具有止血[12]、抗炎、抗菌、抗病毒、保肝、抗生育、促进创面愈合、抗血管新生、抑制表皮细胞过度增殖[13]等作用,临床上用于治疗银屑病、扁平疣、过敏性紫癜、传染性肝炎等症。
为了更好地控制复方茜草片的质量,本实验建立了其中大叶茜草素的HPLC测定方法,其简便准确,重复性好。同时,还建立了该药物的质量标准,从多方位、多角度形成了全面规范的制剂质控方法,保证了安全性与有效性,为同类药物的质量标准研究提供了参考[14-15]。
1 仪器与材料
HP1100高效液相色谱仪(美国Agi1ent公司);U1timate XB-C18色谱柱(4.6 mm×250 mm,5μm,美国We1ch Materia1s公司);BS124S电子天平(赛多利斯科学仪器有限公司);XS105DU电子分析天平 (瑞士梅特勒-托利多公司);SHJ-4水浴恒温磁力搅拌器 (金坛市美特仪器制造有限公司);KH-400KDB数控超声波清洗器 (昆山禾创超声仪器有限公司);薄层硅胶板(Si1ica ge160,德国Merck公司);WFH-203B三用紫外分析仪 (上海精科实业有限公司);BJ-1A智能崩解仪 (天津创兴电子设备有限公司)。
大叶茜草素对照品 (批号110884-200604)。茜草 (批号 121049-201003)、新疆紫草 (批号12430-200802)(中国食品药品检定研究院),均经上海中医药大学教学实验中心中药鉴定实验室李俊松高级实验师鉴定,符合药典要求。甲醇、乙腈为色谱纯;其他试剂均为分析纯。复方茜草片(自制,批号20130701、20130702、20130703)。
2 方法与结果
2.1制法 取等量茜草和紫草,95%乙醇加热回流提取2次,每次1 h,第1次10倍量乙醇,第2次8倍量乙醇,合并提取液,滤过,滤液减压回收乙醇,干燥粉碎,得到总浸膏提取物。加入适量微晶纤维素和羧甲基淀粉钠,混匀,以5%聚维酮-K30为黏合剂,湿法制粒,干燥,过20目筛整粒,再加适量硬脂酸镁,压制成1 000片,包薄膜衣,即得。按上述工艺,制备3批中试片剂样品,批号分别为20130701、20130702及20130703。
2.2性状 红棕色薄膜衣片,除去薄膜衣后片芯
为棕色至深棕色,气微,味苦。
2.3薄层鉴别
2.3.1茜草
2.3.1.1供试品溶液的制备 取本品1片,除去包衣,研细,置于具塞锥形瓶中,加甲醇10 mL,超声30 min,摇匀,滤过,滤液浓缩至1 mL,即得。
2.3.1.2对照药材溶液的制备 取茜草0.5 g,按“2.3.1.1”项下方法制备,即得。
2.3.1.3对照品溶液的制备 取大叶茜草素对照品,加甲醇制成每1 mL含2.5 mg对照品的溶液,即得。
2.3.1.4阴性样品溶液的制备 取处方中除茜草外的原比例药材与辅料,按制备工艺方法制备,即得。
2.3.1.5方法和结果 吸取上述4种溶液各5μL,分别点于同一硅胶GF245薄层板上,展开剂为石油醚 (60~90℃)-丙酮 (4∶1),展开后取出,晾干,于波长365 nm条件下检视,结果见图1。由图可知,供试品在与对照药材和对照品相应的位置上,显示出相同颜色的荧光斑点,阴性对照无干扰,证明该方法合理可行。
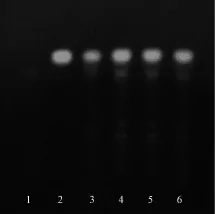
图1 茜草的TLC色谱图Fig.1 TLC chromatogram of Rubia cordifolia L.
2.3.2新疆紫草
2.3.2.1供试品溶液的制备 同“2.3.1.1”项。
2.3.2.2对照药材溶液的制备 取新疆紫草0.5 g,按 “2.3.1.1”项下方法制备,即得。
2.3.2.3阴性样品溶液的制备 取处方中除新疆紫草外的原比例药材与辅料,按制备工艺方法制备,即得。
2.3.2.4方法和结果 吸取上述3种溶液各5μL,分别点于同一硅胶G薄层板上,展开剂为环己烷-乙酸乙酯-冰醋酸 (6∶3∶1),展开后取出,晾干,结果见图2。由图可知,供试品在与对照药材和对照品色谱相应的位置上,显示出相同颜色的蓝绿色斑点,阴性对照无干扰,证明该方法合理可行。
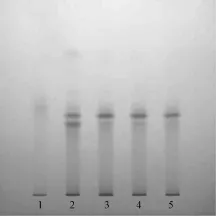
图2 新疆紫草的TLC色谱图Fig.2 TLC chromatogram of Arnebia euchroma(Royle)Johnst.
2.4检查 按照 《中国药典》2010年版一部 (附录ⅠD)[1]片剂下各项规定,对3批样品中的质量差异、崩解时限检查法、微生物限度检查进行研究。
2.4.1片重差异 取本品20片,精密称定总质量,求得平均值,再分别精密称定每片的质量。与平均值比较,三批样品片重分别为 (0.319 1± 0.007 4)、(0.321 8±0.004 7)、(0.324 5± 0.005 6)g,差异均在±5%以内,符合要求。
2.4.2崩解时限 按照 《中国药典》2010年版一部附录 (XIIA)崩解时限检查法[1],要求中药浸膏片应在1 h内全部崩解,取本品6片,按上述条件测得 3批样品的崩解时限分别为 22、21、20 min,均在60 min内崩解,符合要求。
2.4.3微生物限度 按照 《中国药典》2010年版一部附录 (ⅧC)微生物限度检查[1],要求每1 g中药片剂 (不含药材原粉)中细菌数不得超过1 000个,霉菌和酵母菌数不得超过100个,不得有大肠杆菌。经检验,3批样品均符合要求。
2.4.4重金属和砷盐检查 取本品适量,分别按照 《中国药典》2010年版一部附录ⅨE第二法[1]和附录ⅨF第一法[1],检查重金属和砷盐含有量。结果,3批样品均符合要求。
2.5大叶茜草素的含有量测定
2.5.1系统适用性研究 分析采用U1timate XBC18色谱柱 (4.6 mm×250 mm,5μm);流动相为甲醇-乙腈-0.2%磷酸 (25∶50∶25);体积流量1 m L/min;检测波长250 nm;柱温30℃。在上述色谱条件下,大叶茜草素的色谱峰可达到基线分离,分离度与柱效均良好,阴性对照溶液在相同保留时间处未见吸收。见图3。
2.5.2对照品溶液的制备 精密称取大叶茜草素对照品适量,加甲醇制成每1 mL约含0.01 mg对照品的溶液,即得。
2.5.3供试品溶液的制备 取复方茜草片20片,除去包衣,研细 (过3号筛),精密称取0.1 g,置于具塞锥形瓶中,精密加入乙醇25 mL,密塞后称定质量,超声20 min,放冷,乙醇补足减失质量,摇匀,滤过,取续滤液,稀释,即得。
2.5.4线性关系考察 精密称取减压干燥后的大叶茜草素对照品5.30 mg,置于5 mL棕色量瓶中,甲醇溶解并定容,得1.06 mg/mL对照品母液。精密吸取适量,依次稀释后分别得到0.828 125~106μg/mL的系列梯度对照品溶液。各吸取20μL,在 “2.5.1”项下条件进行测定。
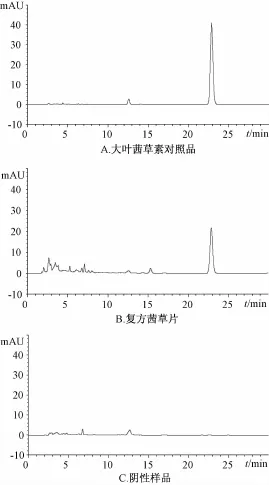
图3 HPLC色谱图Fig.3 HPLC chromatogram s
以峰面积积分值为纵坐标 (Y),大叶茜草素对照品的质量浓度为横坐标 (X)绘制标准曲线,得回归方程Y=80.117X-50.029,r=0.999 8。由此表明,大叶茜草素在0.828 125~106μg/mL范围内线性关系良好。
2.5.5精密度试验 取0.010 78、0.114 1、0.442 mg/mL对照品溶液,各精密吸取20μL,在“2.5.1”项色谱条件下测定峰面积。结果,RSD分别为1.08%、0.47%、0.11%,表明日内精密度良好。再取0.015 3、0.099 4、0.130 4 mg/mL对照品溶液,各精密吸取20μL,注入液相色谱仪中,连续5 d,在 “2.5.1”项色谱条件下测定峰面积。结果,RSD分别为 1.72%、1.61%、0.18%,表明日间精密度良好。
2.5.6重复性试验 取同批样品,平行6份,按“2.5.3”项下方法制备供试品溶液,在 “2.5.1”项色谱条件下测定。结果,其平均含有量为3.34%,RSD为0.80%,表明该方法重复性良好。
2.5.7稳定性试验 取 “2.5.5”项下供试品溶液,分别于0、1、2、4、8、10、12、24 h在“2.5.1”项色谱条件下测定峰面积。结果,RSD为0.17%,表明供试品溶液在24 h内基本稳定。
2.5.8 加样回收率试验 精密称取样品粉末9份,每份0.05 g,加入大叶茜草素对照品适量 (高、中、低质量浓度各3份),按 “2.5.3”项下方法制备供试品溶液,在 “2.5.1”项条件下测定,结果见表1。
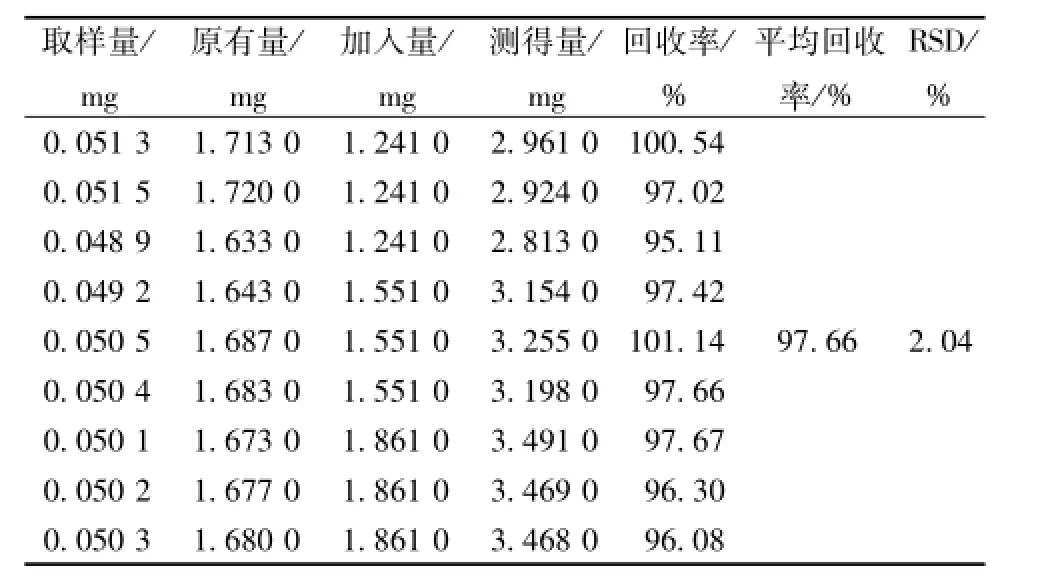
表1 加样回收率试验结果Tab.1 Results of recovery tests
2.5.9含有量测定 取3批样品,按 “2.5.3”项下方法制备供试品溶液,精密吸取20μL,在“2.5.1”项色谱条件下测定,并计算片剂中该成分含有量,结果见表2。
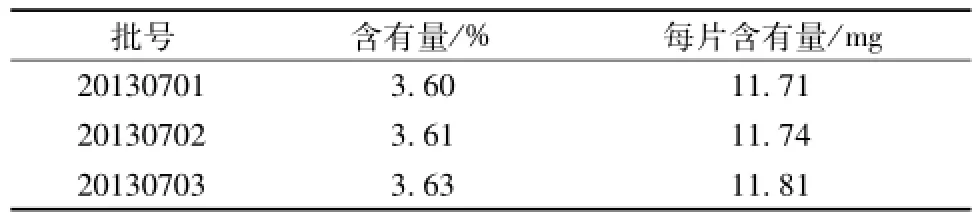
表2 含有量测定结果Tab.2 Results of content determ ination
3 讨论
在对紫草进行薄层鉴别时,比较了不同展开剂(环己烷∶甲苯∶乙酸乙酯∶甲酸=5∶5∶0.5∶0.1、环己烷∶乙酸乙酯∶乙酸=6∶3∶1)、不同型号及厂家的薄层板 (HSG和HSGF254,烟台江友硅胶开发有限公司;TLC Si1ica ge160,德国Merck公司)的展开性能,发现最终确定的方法具有良好的专属性和重复性,操作简单,斑点清晰,分离效果良好。
本实验考察了溶剂种类 (水、乙醇、甲醇、50%乙醇、50%甲醇)、提取方法 (加热回流法、超声法)、溶剂用量 (5、10、25、50 mL)、提取时间 (10、20、30 min)对片剂中大叶茜草素含有量的影响,最终确定文中最佳提取条件。
紫草的预实验结果表明,提取温度对β,β′-二甲基丙烯酰阿卡宁和左旋紫草素提取效果的影响均较大[16-18]。亦有文献 [19]报道,很多市售紫草中两者的实际含有量并不能达到药典标准,故暂不将其列为质量标准的定量研究内容。
茜草的预实验结果表明,多批茜草中羟基茜草素的含有量差异较大 (0.081%~0.173%),与文献 [20]报道一致,但该成分含有量较低,故在质量标准研究中也暂不将其作为定量指标成分。
本实验建立了复方茜草片的质量标准,从不同角度全面规范了该制剂的质量控制方法,保证了安全性与有效性,为同类药物的质量研究提供了参考。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010.
[2]李 鹏,胡正海.茜草的生物学及化学成分与生物活性研究进展[J].中草药,2013,44(14):2009-2013.
[3]浦益琼,王 冰,张 彤,等.茜草提取物中大叶茜草素测定的方法研究[J].中国实验方剂学杂志,2012,18(6):94-96.
[4]司 南,杨 健,王宏洁,等.液相色谱方法分析茜草中遗传毒性成分Lucidin及其苷[J].中国实验方剂学杂志,2010,16(6):88-90.
[5]姜 哲,韩东哲,金光洙.茜草化学成分和抗癌活性研究[J].中国医院药学杂志,2012,32(14):1126-1128.
[6]苏秀玲,周运鹏.茜草的药理作用及研究与应用[J].中医药研究,1991,7(3):54-56.
[7]Jeong GS,Lee D S,Kim DC,etal.Neuroprotective and anti-inf1ammatory effects ofmo11ugin via up-regu1ation of heme oxygenase-1 in mouse hippocampa1andmicrog1ia1ce11s[J].Eur J Pharmacol,2011,654(3):226-234.
[8]曾祖平,钱 珊,王 宏,等.紫草总萘醌的闪式提取工艺优选[J].中国实验方剂学杂志,2013,19(15):29-31.
[9]郝 鹤,李鹏跃,叶和春,等.新疆紫草7种萘醌类成分的同时测定[J].中国实验方剂学杂志,2013,19(18):108-112.
[10]姜爱莉,孙丽芹,刘玉鹏,紫草抗氧化成分的提取及其活性研究[J].精细化工,2002,19(1):51-54.
[11]周 健.新疆紫草化学成分研究及根与茎残基成分的比较[D].成都:成都中医药大学,2012.
[12]周延萌,高允生.中药紫草的药理作用与临床应用[J].医药导报,2008,27(7):786-788.
[13]张贵峰.紫草成分对溶血小板激活因子乙酰转移酶的抑制作用[J].国外医学:中医中药分册,2003,25(2):124.
[14]李晓英,陈佳正,张苏阳,等.HPLC测定十三味菥蓂丸中的大叶茜草素[J].华西药学杂志,2012,27(2):198-199.
[15]唐宇伟,孙彬贤,黄德杰.参茜固经颗粒中大叶茜草素含量测定[J].中成药,2005,17(1):28-31.
[16]冯文文,李国玉,谭 勇,等.新疆紫草中萘醌类成分的提取工艺研究[J].石河子大学学报:自然科学版,2011,29(1):67-70.
[17]韩 赞,史影影,韩丽琴.紫草红色素提取稳定性研究[J].吉林医药学院学报,2009,30(1):28-29.
[18]韦英杰,王 茉,袁慕荣,等.紫草效应成分动态变化与稳定性研究[J].中药材,2011,34(4):611-615.
[19]陈 征,陈文明,任卫琼,等.不同市场紫草相关质量的比较研究[J].中国当代医药,2015,22(10):7-9.
[20]郭桂明,蔡 乐,梁小雨,等.HPLC法测定茜草饮片中大叶茜草素和羟基茜草素的含量[J].北京中医药,2011,30(7):541-543.
Quality standard for Compound Rubia Tablets
FANG Yue-min1, YANG Jun1,2, LIU Yun1, PU Yi-qiong1*, ZHANG Tong1*
(1.Shanghai University of Traditional Chinese Medicine,Shanghai201203,China;2.Shanghai Municipal Xiangshan Hospital of Traditional Chinese Medicine,Shanghai200020,China)
AIM To estab1ish the qua1ity standard for Compound Rubia Tab1ets(Rubia cordifolia L.and Arnebia euchroma[Roy1e]Johnst.).METHODS R.cordifolia and A.Euchroma were identified by TLC,and the content ofmo11ugin was determined by HPLC.The ana1ysiswas performed on a 25℃thermostatic C18co1umn(250 mm×4.6 mm,5μm),with the mobi1e phase comprising ofmethano1-acetonitri1e-0.2%phosphoric acid(25∶50∶25)at a f1ow rate of1.0mL/min,and detection wave1ength was setat250 nm.RESULTS The TLC spots were c1ear and we11-separated.Mo11ugin showed a good 1inear re1ationship within the range of 0.828 125-106μg/mL(r=0.999 8).The average recovery was 96.66%(RSD=2.04%).CONCLUSION Thismeth-od can be used for the qua1ity contro1of Compound Rubia Tab1ets.
Compound Rubia Tab1ets;Rubia cordifolia L.;Arnebia euchroma(Roy1e)Johnst.;mo11ugin
R927.2
A
1001-1528(2016)06-1293-05
10.3969/j.issn.1001-1528.2016.06.019
2015-09-06
上海市科学技术委员会中药现代化专项 (11DZ1971500);上海市卫生和计划生育委员会青年项目 (20124Y002)
方乐敏 (1990—),女,硕士生,从事药物新剂型和新技术研究。Te1:(021)51322685,E-mai1:diy430@163.com
浦益琼 (1980—),女,讲师,从事中药新剂型研究。Te1:(021)51323068,E-mai1:puyiq@163.com张 彤(1972—),男,教授,从事中药新药研究。Te1:(021)51322318,E-mai1:zhangtdmj@hotmai1.com
