CLSI头孢吡肟折点改变对肠杆菌科细菌的药敏变化分析
2016-08-11林伟苗邱芳华李秋明梁冬艳薛志锋
林伟苗 邱芳华 李秋明 梁冬艳 薛志锋
广州市中医医院检验科(广州 510130)
CLSI头孢吡肟折点改变对肠杆菌科细菌的药敏变化分析
林伟苗邱芳华李秋明梁冬艳薛志锋
广州市中医医院检验科(广州 510130)
【摘要】目的探讨不同年份CLSI文件中头孢吡肟折点变化对肠杆菌科细菌药敏结果的影响,辅助临床合理调整用药。方法应用2013年(S23)与2014年(S24)CLSI文件中的头孢吡肟折点回顾性分析我院2014年肠杆菌科细菌的药敏变化情况。结果与S23折点相比,肠杆菌科细菌中大肠埃希菌、肺炎克雷伯菌对头孢吡肟的耐药率分别上升了2.6%、2.8%,耐药率差异有统计学意义(P<0.05);产ESBLs大肠埃希菌、产ESBLs肺炎克雷伯菌以及非产ESBLs肺炎克雷伯菌对头孢吡肟的耐药率分别上升了3.8%、2.4%、2.0%,耐药率差异有统计学意义(P<0.05); 对于其它肠杆菌科细菌如非产ESBLs大肠埃希菌、阴沟肠杆菌等对头孢吡肟的耐药率变化无差异(P>0.05)。与S23相比,在S24中头孢吡肟MIC值分布在4 μg/mL、8 μg/mL、16 μg/mL时对细菌的药敏变化最为显著。结论依照S24折点,肠杆菌科细菌对头孢吡肟的耐药率有不同程度的升高;尤其对产ESBLs菌株耐药率影响更大;临床应结合实验室报告合理调整用药。
【关键词】肠杆菌科细菌头孢吡肟微生物敏感性试验药敏折点
折点是微生物试验中被用于定义菌株对抗菌药物耐药性和敏感性的流行病学临界值[1]。我国现行普遍使用的是美国临床和实验室标准化研究所(clinical and laboratory standards institute,CLSI)的药敏试验方法和折点。2014年CLSI M100-S24[2]文件修订了头孢吡肟的折点,并在折点后增加了对应的用药方案。本研究旨在探讨 2013年CLSI M100-S23[3](S23)和2014年M100-S24(S24)文件中头孢吡肟的不同折点值对肠杆菌科细菌药敏结果的影响,为指导临床合理用药提供依据。
1对象与方法
1.1菌株来源2184株细菌分离自广州市中医医院2014年不同患者送检的各类标本,剔除重复菌株,其中大肠埃希菌1156株、肺炎克雷伯菌570株、阴沟肠杆菌119株。细菌鉴定采用Vitek2-compact全自动微生物分析系统。质控菌株为大肠埃希菌ATCC 25922,阴沟肠杆菌ATCC 700323。
1.2药敏试验用Vitek 2-compact配套商用卡片AST-GNl3对所有实验菌株进行药敏试验。
1.3肠杆菌科细菌分别用S23与S24中相应的头孢吡肟药敏试验最低抑菌浓度(minimal inhibitory concentration,MIC)判读折点(μg/mL)见表1。

表1 S23和S24中肠杆菌科细菌药敏试验MIC判读折点(μg/mL)
注: S代表敏感;I代表中介;R代表耐药;SDD代表剂量依赖性敏感
1.4数据分析方法药敏结果用WHONET 5.6软件进行分析,用SPSS 17.0软件进行药敏变化的卡方检验,P<0.05为差异有统计学意义。
2结果
2.1肠杆菌科细菌在S23与S24折点下头孢吡肟的药敏结果肠杆菌科细菌中大肠埃希菌、肺炎克雷伯菌对头孢吡肟的耐药率分别由S23折点下17.6%、18.1%上升为S24折点下20.2%、20.9%,药敏结果耐药率差异有统计学意义(P<0.05),阴沟肠杆菌对头孢吡肟的耐药率上升无差异(P>0.05)。见表2。

表2 肠杆菌科细菌在S23与S24折点下头孢吡肟的药敏结果(%)
注: S代表敏感;I代表中介;R代表耐药;SDD代表剂量依赖性敏感;*代表不同折点下病原菌耐药率差异有统计学意义(P<0.05)
2.2不同表型的肠杆菌科细菌在S23与S24折点下头孢吡肟的药敏结果 产ESBLs大肠埃希菌、产ESBLs肺炎克雷伯菌以及非产ESBLs肺炎克雷伯菌对头孢吡肟的耐药率由S23折点下28.4%、37%、2.8%上升为S24折点下32.2%、39.4%、4.8%,药敏结果耐药率差异有统计学意义(P<0.05),非产ESBLs大肠埃希菌对头孢吡肟的耐药率上升无差异(P>0.05)。见表3。

表3 不同表型的肠杆菌科细菌在S23与S24折点下头孢吡肟的药敏结果(%)
注: S代表敏感;I代表中介;R代表耐药;SDD代表剂量依赖性敏感;*代表不同折点下病原菌耐药率差异有统计学意义(P<0.05)
2.3大肠埃希菌和肺炎克雷伯菌对头孢吡肟的MIC分布 非产ESBLs大肠埃希菌与非产ESBLs肺炎克雷伯菌对头孢吡肟的MIC值主要分布为≤1 μg/mL;而头孢吡肟的各MIC折点范围均可检出产ESBLs菌株,其中产ESBLs大肠埃希菌对头孢吡肟的MIC值分布范围为≤2 μg/mL占48.2%,4-8 μg/mL占20.4%,≥16 μg/mL占31.4%,产ESBLs肺炎克雷伯菌对头孢吡肟的MIC值分布范围为≤2 μg/mL占47.7%,4-8 μg/mL占13.2%,≥16 μg/mL占39.1%。见表4。
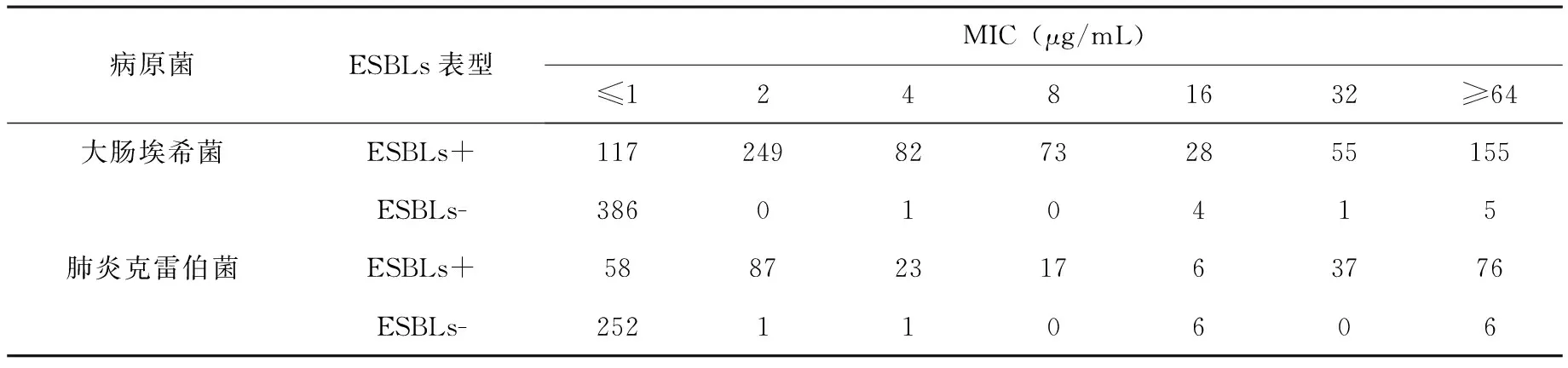
表4 大肠埃希菌和肺炎克雷伯菌对头孢吡肟的MIC分布
2.4大肠埃希菌和肺炎克雷伯菌受头孢吡肟折点改变的影响情况根据S23和S24中肠杆菌科细菌药敏试验MIC值判读折点,其变化主要分布在4 μg/mL、8 μg/mL、16 μg/mL三个折点值。产ESBLs大肠埃希菌、肺炎克雷伯菌受折点改变影响的菌株百分比分别为24.1%、15.1%,非产ESBLs大肠埃希菌、肺炎克雷伯菌受折点改变影响的菌株百分比分别为1.3%、2.6%。见表5。

表5 大肠埃希菌和肺炎克雷伯菌受头孢吡肟折点改变的影响情况
3讨论
2014年CLSI M100-S24文件最大改变之处是修改了肠杆菌科细菌头孢吡肟的药敏折点,并引入“SDD”的概念[2]。“SDD”系指依赖于患者所用剂量的菌株敏感性。当菌株的药敏结果(MIC或纸片扩散法)在“SDD”范围时,临床应提高给药方案,如更高剂量和(或)更频繁给药,以达到临床疗效。以前的“S”折点≤8 μg/mL基于高剂量给药方案,但通常用于治疗的剂量较低。对于头孢吡肟MIC值为4-8 μg/mL的(以前的“S”)菌株,临床给予常用的低剂量,有时表现为治疗失败[4]。我国学者卢龙坤等[5]认为肠杆菌科细菌对头孢吡肟药敏折点引入“SDD”可以帮助临床医师更合理使用头孢吡肟。我们研究发现按照S24折点,肠杆菌科细菌对头孢吡肟剂量依赖性敏感的百分率为9.2%,要达到临床治疗有效的目的,需要使用更高剂量和(或)更频繁给药次数方案,以增加药物暴露的剂量和时间。
通过对本实验室2014年肠杆菌科细菌的药敏试验数据进行回顾性分析。依照CLSI M100-S24的判读折点,头孢吡肟的耐药率较2013年有了一定程度的升高,主要原因为S23折点下判读为中介(MIC值为16 μg/mL)的菌株,在新折点下均被判读为耐药。本研究中数据显示新旧折点下,肠杆菌科细菌中大肠埃希菌、肺炎克雷伯菌对头孢吡肟的耐药率分别上升了2.6%、2.8%,药敏结果耐药率差异有统计学意义(P<0.05),阴沟肠杆菌对头孢吡肟的耐药率上升无差异(P>0.05)。
本次研究中,产ESBLs大肠埃希菌、肺炎克雷伯菌所占的比例分别为65.7%(759/1156)、53.3%(304/570)。S23与S24折点比较下,产ESBLs大肠埃希菌、肺炎克雷伯菌以及非产ESBLs肺炎克雷伯菌对头孢吡肟的耐药率分别上升了3.8%、2.4%、2%,药敏结果耐药率差异有统计学意义(P<0.05), 非产ESBLs大肠埃希菌对头孢吡肟的耐药率上升无显著差异(P>0.05)。与非产ESBLs菌株相比,产ESBLs菌株受到新旧判读折点变化的影响更大(P<0.05),这是因为后者位于新旧判读折点之间(MIC值分布在4 ug/ml、8 ug/ml、16 ug/ml)的菌株比例较前者偏高。此外,在产ESBLs菌株中,受头孢吡肟折点变化影响的大肠埃希菌的百分比要高于肺炎克雷伯菌(P<0.05)。耐药分子机制与MIC之间具有一定的相关性,产ESBLs菌株的MIC值大多数高于非产ESBL菌株,不同型别ESBLs水解底物谱有差异,不同菌株的产酶量也有差异,产酶量多时MIC会升高。MIC与临床预后的相关性强于菌株携带的耐药机制,MIC是判断产酶株感染治疗预后的最佳指标[1,6],当产ESBLs菌株的头孢吡肟MIC值足够低时,临床应用有效。与此类似,为了符合临床的治疗效果,CLSI M100-S20建议,如果使用修正后头孢他啶、氨曲南等β内酰类抗菌药物的折点时不必再做ESBLs的筛选和确证试验,如果出于感染控制和流行病学调查的目的,需要做ESBLs的筛选和确证试验[7]。
值得我们注意的是,CLSI规定肠杆菌科细菌头孢吡肟的药敏折点分别为敏感≤2 μg/mL,SDD为4-8 μg/mL;耐药≥16 μg/mL。而欧洲药敏委员会(EUCAST)[8]将肠杆菌科细菌头孢吡肟的药敏折点分别定为敏感≤1 μg/mL,中介为2- 4 μg/mL,耐药≥8 μg/mL。基于上述原因,临床在使用该类抗菌药物时一定要结合地区差异,同时参照当地的药敏监测数据。对于我们探讨的S24中新折点下的用药方案与临床疗效的符合度问题仍需积累更多的临床资料来佐证。
参考文献:
[1] 杨启文,朱任媛,王辉.药敏试验折点的设定及对临床的指导意义[J]. 内科急重症杂志,2010,16(4):181-183.
[2] Clinical and Laboratory Standards Institute.Performance Standards for Antimicrobial Susceptibility Testing;Twenty-Fourth Informational Supplement[S].CLSI document M100-S24,Wayne,PA:CLSI,2014.
[3] Clinical and Laboratory Standards Institute.Performance Standards for Antimicrobial Susceptibility Testing;Twenty-Fourth Informational Supplement[S].CLSI document M100-S23,Wayne,PA:CLSI,2013.
[4] 张雅薇,王辉.2014年CLSI M100-S24主要更新内容解读[J]. 中华检验医学杂志,2014,37(4),256-260.
[5] 卢龙坤,陈渊成,时小媛,等.肠杆菌科细菌对头孢吡肟药敏折点引入剂量依赖性敏感的临床意义[J]. 中华医院感染学杂志,2014,24(21):5264-5266.
[6] CRAIG WA. Pharmacokinetic/pharmacodynamic parameters:rationale for antibacterial dosing of mice and men[J]. Clin Infect Dis,1998,26:1-10.
[7] Clinical and Laboratory Standards Institute.Performance Standards for Antimicrobial Susceptibility Testing;Twenty-Fourth Informational Supplement[S]. CLSI document M100-S20,Wayne,PA:CLSI,2010.
[8] European Committee on Antimicrobial Susceptibility Testing.Breakpoint tables for interpretation of MICs and zone diameters[S]. Switzerland,v1.1:EUCAST,2014.
基金项目:国家自然科学基金-青年科学(81503424);广东省自然科学基金(2014A030313802);2014广东省中医药局建设中医药强省科研课题(2014021 );广州市卫生局医药卫生科技项目,(20141A011016);广州市卫生局中医药科技项目,20152A011010)
通信作者:邱芳华,E-mail:qiufanghua1976@163.com
DOI:10.3969/j.issn.1000-8535.2016.02.005
(收稿日期:2015-11- 05)
Drug sensitivity analysis of CLSI breakpoint change of cefepime toward Enterobacteriaceae bacteria
LinWeimiao,QiuFanghua,LiQiuming,etal.
DepartmentofClinicLaboratory,GuangzhouHospitalofTraditionalChineseMedicine,Guangzhou510130,China
【Abstract】ObjectiveTo investigate the change of the break point of the CLSI in different years on the drug sensitivity of Enterobacteriaceae bacteria. This is valuable for rational use of antibiotics.MethodsTo retrospective analyze 2014 Enterobacteriaceae bacteria susceptibility variation by CLSI file cefepime breakpoint of 2013(S23) and 2014(S24).ResultsCompared with breakpoint of S23, E. coli and Klebsiella pneumonia, cefepime resistant rate rose by 2.6% and 2.8% respectively, and the resistance difference was statistically significant (P<0.05); ESBLs-producing E. coli, ESBLs-producing Klebsiella pneumoniae and ESBLs non-producing Klebsiella pneumoniae toword cefepime resistant rate rose by 3.8%, 2.4% and 2.0% respectively, and the resistance difference was statistically significant (P<0.05); For other Enterobacteriaceae bacteria, such as ESBLs non-producing E. coli and Enterobacter cloacae with cefepime in drug resistance rate had no significant difference (P>0.05). Compared with S23, variety in drug susceptibility of bacteria was most significant in S24, during cefepime MIC of 4 μg/mL, 8 μg/mL, 16 μg/mL.ConclusionAccording to the S24 breakpoint, the drug resistance rates of the bacteria in the intestines of the bacteria is increasing, especially in ESBLs strain; antibiotics use should be following laboratory results.
【Key words】Enterobacteriaceae bacteria; Cefepime; Microbial sensitivity test; Susceptibility to breakpoint
