绿色过程系统工程
2016-03-19张锁江张香平聂毅鲍迪董海峰吕兴梅
张锁江,张香平,聂毅,鲍迪,董海峰,吕兴梅
(中国科学院过程工程研究所绿色过程与工程重点实验室,多相复杂系统国家重点实验室,离子液体清洁过程北京市重点实验室,北京 100190)
绿色过程系统工程
张锁江,张香平,聂毅,鲍迪,董海峰,吕兴梅
(中国科学院过程工程研究所绿色过程与工程重点实验室,多相复杂系统国家重点实验室,离子液体清洁过程北京市重点实验室,北京 100190)
摘要:发展从源头消除污染的绿色技术是过程工业可持续发展的必然要求,任何单元技术的突破对过程工程的绿色化都是不可或缺的。然而过程工程是一个系统科学,不仅要考虑单个技术,重点还要考虑从原料替代、介质创新到单元强化及系统集成的整个链条,归根到底是要通过新介质(如催化剂、溶剂等)的原始创新和新工艺集成创新实现过程工业的绿色化。基于系统论的科学思想综合考虑过程工程这一复杂大系统,以离子液体介质创新为核心,综述了在原料替代、新型介质设计、传递规律、系统集成方面的新进展,以期为绿色化工技术的发展提供重要的科学基础。
关键词:绿色过程系统工程;过程系统;绿色技术;离子液体;氢键作用;模拟
2015-05-13收到初稿,2015-07-21收到修改稿。
联系人及第一作者:张锁江(1964—),男,研究员。
Received date: 2015-05-13.
引 言
随着全球性环境和化石资源严重匮乏问题的加剧,过程绿色化成为推动工业可待续发展的重要途径,其关键则是开发从源头消除污染的绿色技术。20世纪90年代末国际公认的绿色化学12条原则[1]高度概括了绿色化学的特点、宗旨和内容,将绿色化学的原理与化学工程的特点相结合,形成了绿色化工科学,其显著特征是面向工业应用,追求高转化率、高选择性和能源的高效利用,原料、介质和产品的无毒或低毒,废弃物、副产物排放最小等,总体目标是经济效益和环境效益的协调最优[2]。
开发绿色化工技术,仅仅考虑原料、溶剂和催化剂以及单元设备的创新和高效是远远不够的,还需要从系统的角度,通过分子→纳微→界面→设备→系统的多尺度调控实现经济、环境和安全的多目标最优。进一步将绿色技术产业化,则可实现循环经济和清洁生产[3-4]。从时间尺度来看,发展绿色技术,从设计之初就必须考虑环境、健康和安全对新过程或产品的影响,从而在原料筛选、溶剂/催化剂开发、过程优化设计、系统运行等全过程中体现绿色化。基于此,本课题组提出绿色过程系统工程的思想(图1)。与前期提出的绿色过程系统集成相比[2],绿色过程系统工程不仅强调从分子到系统的多尺度模拟计算和全局多目标优化,同时将实验研究与模拟计算紧密结合,强调将理论方法用于实际技术研发链和工程设计,即包括基本理论分析、实验室小试及中试、工艺设计、设备优化和工程放大全过程,为绿色化工技术研发和产业化提供重要的依据。
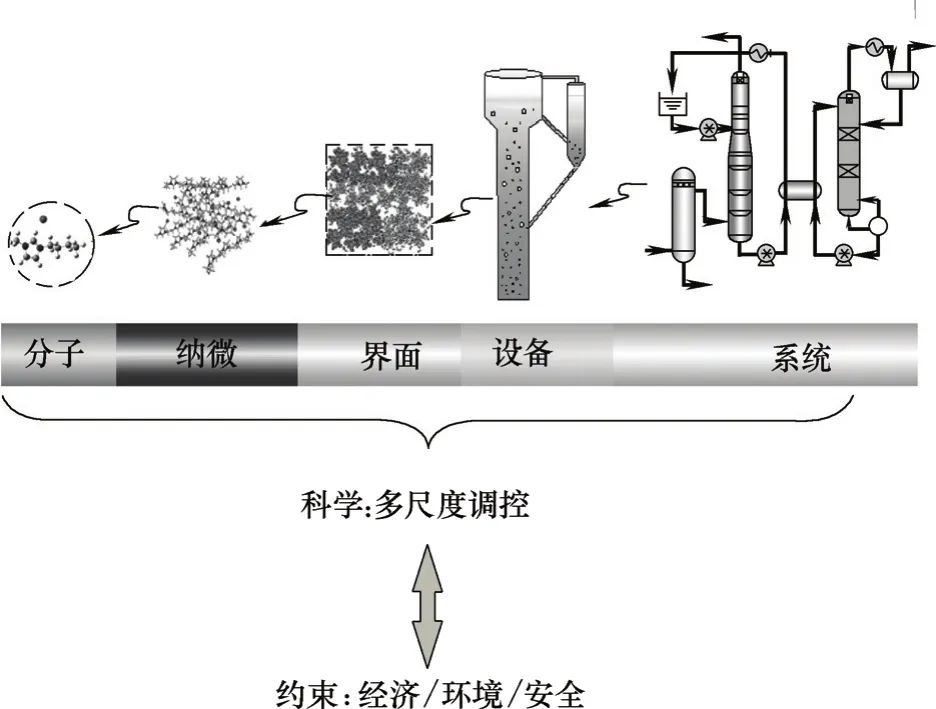
图1 绿色过程系统工程的研究思想Fig.1 Scope of green process system engineering
绿化过程系统工程主要包括如图2所示的4方面内容,分别简要论述如下。
(1)原料替代:从传统的不可再生的化石资源向可再生能源如生物质、太阳能过渡,这是人类社会发展的必然趋势,同时有毒有害原料如氢氰酸等也将被更加绿色的原料替代,从而实现从源头消除污染的目标。
(2)工艺创新:包括介质、材料、反应器和工艺路线的创新,目标是开发高原子经济性反应和低能耗高效分离过程。
(3)设备强化:通过单元设备强化和创新,如设计和使用微通道、超重力、旋转床、磁场/电场强化等反应器,达到强化传热传质的目标,实现反应过程的高转化率、高选择性及高分离效率。
(4)系统集成:基于系统工程的理论和方法,考虑经济效益和环境效益双重目标,建立系统的综合、优化、分析、设计、控制等的从分子到生态系统的多尺度模型,形成可持续发展的化工过程或产品的绿色技术。
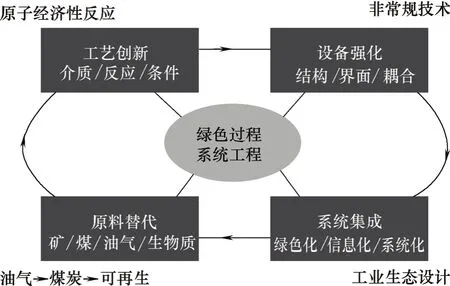
图2 绿色过程系统工程的主要研究内容Fig.2 Content of green process system engineering
在化工过程中,约90%的反应及分离过程需要介质(溶剂和催化剂)才能完成,因而介质创新是实现化工过程温和高效转化的重要途径。新型介质和材料的出现,常常会带来重大的技术变革,同时也会对传统的理论方法、研究手段和计算模型提出挑战。与水、有机溶剂等传统溶剂相比,离子液体介质具有液态温度范围宽、不易挥发、溶解能力强、电化学窗口宽等一系列优点。更重要的是,离子液体的可设计性使其可通过修饰或调整正负离子的结构及种类来调控其物理化学性质。此外,理论上离子液体体系可能高达10的18次方(1018)种,化学家可从中选择适合自己需要的类型和结构加以应用。因此,目前离子液体作为溶剂、催化剂、电解液等,已在石油化工、煤化工、合成材料、环境控制、电化学等方面展现了广阔的应用前景,成为科学界和工业界研究热点。也发表了多篇综述性论文,近年来广泛引用的综述文章如离子液体气体分离[5-11]、离子液体催化反应[12-16]、精馏或萃取分离[17-18]、电化学[19]、离子液体材料[20-21]、生物质[22-24]、环境性能[25-26]等,但通常是针对某一具体领域或应用。本文则以系统工程思想为指导,以资源能源转化重大需求为导向,简要综述了以离子液体核心介质/材料在介质设计、传递规律、系统集成、原料替代及工业应用方面的国内外最新研究进展,提出系统科学的理论和方法,为发展绿色化学化工技术提供重要的指导。
1 离子液体介质创新及设计原理
1.1 离子液体氢键结构
与广泛而重要的过程工业应用相对应,离子液体体系相关科学理论及规律的研究将为实际工业应用提供有利的科学支撑。设计功能化离子液体,首先要认识离子液体的构效关系。在离子液体这一复杂的体系中,离子间相互作用不是单一的,而是静电力、氢键作用和范德华力(包括诱导力、扩散力以及偶极-偶极作用)等相互作用共存,这些相互作用对离子液体的物理化学性质产生重要的影响。由于离子液体的阳离子通常是咪唑、吡啶和季铵类等,阴阳离子液体中的N、S、F等元素容易和阴离子形成特殊的氢键及网络结构[27-28],因此离子液体中的氢键被认为是除静电力之外最重要的作用力,决定了离子液体的特殊功能[29-31]。氢键的提出改变了人们对于离子化合物是由静电作用组成的常规认识,阐明了离子液体不同于熔盐和离子水溶液的微观本质,对于全面理解离子液体体系的相互作用有重要意义。
阴、阳离子是组成离子液体的基本单位,是阐明和理解离子液体结构和性质关系的基础。氢键的作用方式与阴、阳离子单体的结构有密切关系,在某种程度上决定了阴阳离子对的结构形式。以[Emim][BF4]和[Bmim][PF6]离子液体为例[29],阴、阳离子间可形成多个氢键。理论分析发现,离子液体中静电作用占总相互作用能约70%,其他相互作用(主要为氢键作用)等占30%。阴、阳离子间的氢键具有不同的键长、键角和作用位置,决定了其特殊的连接方式,而最终导致三维氢键网络结构的形成。
Ludwig等[27, 32-33]观察到在一些离子液体中多个离子通过特定的氢键链接在一起形成准三维的氢键网络(quasi-3D hydrogen-bonded network),并以[DMAN][NO3]离子液体为例给出了在理论计算和实验结果上获得的网络结构(图3)。Reichert 等[34]通过X射线晶体分析(X-ray crystallographic analyses)对固态[Dmim][PF6]离子液体进行检测,并给出了[PF6]-与阳离子咪唑环通过氢键连接所形成的聚集结构(图4)。在离子液体的固体和液体中,X射线衍射和Raman光谱等的表征都显示离子液体中氢键网络结构的广泛存在,它们之间相互作用被认为是离子液体高黏度和难以彻底除去微量水的原因之一[35-36]。
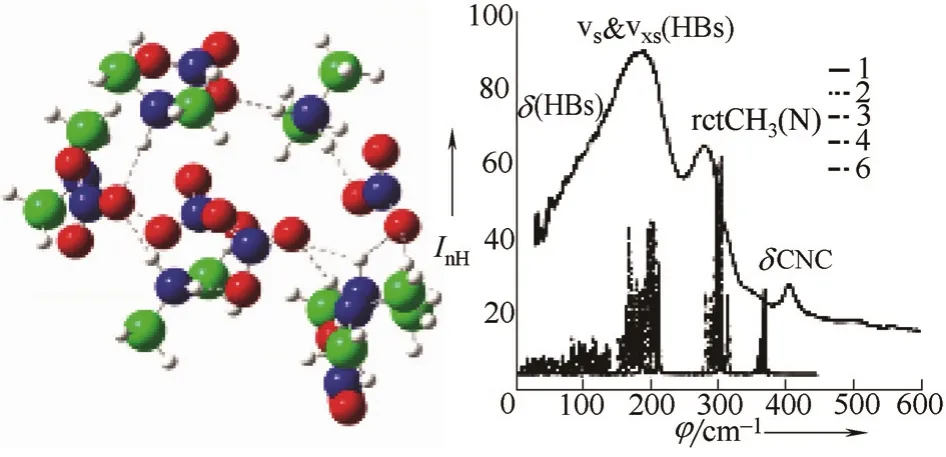
图3 [DMAN][NO3]离子液体在353 K低频振动 FTIR光谱数据及B3LYP/6-31+G*密度泛函理论方法计算所得网络结构Fig.3 Hydrogen bond network of [DMAN][NO3] ionic liquid and experimental low-frequency vibrational FTIR spectrum at 353 K compared to vibrational modes of corresponding PIL clusters [(DMA)(NO3)]xwith x=1, 2, 3, 4, and 6 calculated by DFT at B3LYP/6-31+G* level of theory. Major vibrational bands are in agreement with calculated frequencies, which are corrected for harmonic approximation
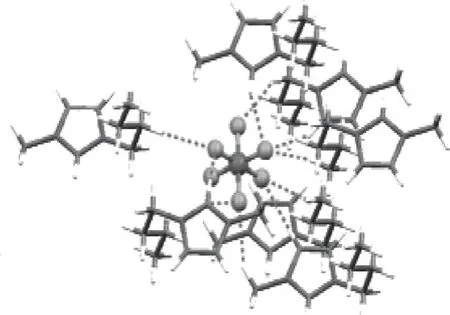
图4 [DMAN][NO3]离子液体在353 K低频振动 FTIR光谱数据及B3LYP/6-31+G*密度泛函理论方法计算所得网络结构; 3b X射线晶体分析检测获得的[Dmim][PF6] 离子液体聚集结构[34]Fig.4 Ion packing of [Bmim][PF6] by X-ray measurement[34]
作者所在团队的研究表明,离子液体中的氢键不同于传统意义上分子溶剂(如水)中的氢键,其耦合了强的静电作用,离子液体的氢键在几何结构、电子轨道、动力学和光谱吸收峰等方面都表现出特殊性,这种特殊的相互作用可以用+[A-H…B]-这样的模型描述,其中+和-分别代表阳离子和阴离子,A和B代表其中的重原子。如在离子液体如[Emim]Cl中,体积大的咪唑阳离子堆积形成zig-zag的基本形状,体积小的阴离子通过和阳离子环上或支链的H原子作用,位于烷基的中间。为了更好地描述这种作用方式,将其命名为Z-bond。相对于传统氢键,Z-bond呈现许多特征,存在较大的相互作用能,其A-H…B的角度在120°~150°间。因耦合了强静电力,有更大的电荷从阴离子转移到阳离子(如0.247e的电荷从Cl-转移到[Emim]+),轨道呈现出典型的σ-型的重叠[37],如图5所示。
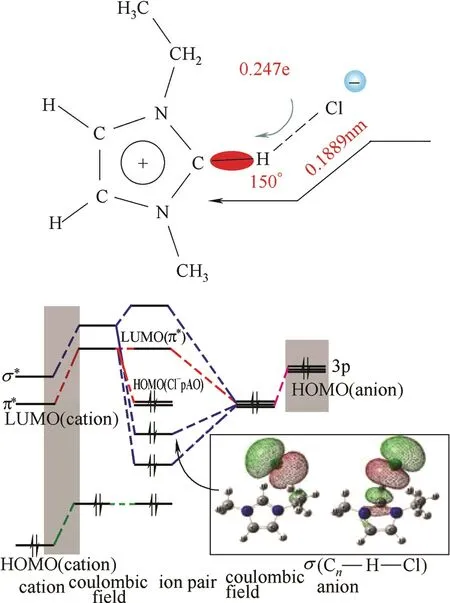
图5 [Emim]Cl的Z-bond和轨道交互作用[37]Fig.5 Z-bond and orbital overlap of [Emim]Cl ion-pair[37]
此外,氢键作用不仅存在于纯的离子液体中,也存在于离子液体和其他溶剂中,如与水、二甲基亚砜、醇类等的混合体系中[38-39]。研究者采用红外光谱、超额红外光谱及量子化学计算研究其中的氢键相互作用,发现在[Emim][LAC]-甲醇混合体系中氢键广泛存在并对体系的稳定性及互溶性起着至关重要的作用[40]。超额红外光谱分析表明,随着甲醇浓度不断增加,离子液体阳离子上C—H基团和阴离子—COO-基团参与形成的氢键都呈减弱趋势,说明甲醇的加入可以影响体系中阴阳离子的相互作用,进而影响离子液体体系的物理化学性质如黏度等。
1.2 离子液体团簇结构
在宏观尺度上呈现均匀液体状态的离子液体,由于氢键、静电力及范德华力等分子间相互作用力的影响,在分子、纳微、流场尺度上可能呈现静态或动态的不均匀结构,从而影响离子液体宏观物理化学性质和催化/分离性能。对于咪唑类、胍类、季盐类等离子液体,在原子/分子尺度上离子对之间形成氢键,在离子簇尺度上形成氢键网络结构,在纳微尺度上则形成团簇或局域分相结构。
研究表明,随着碳链的增长,均匀的离子液体内部容易形成不均质的团簇结构。Voth等[41-43]率先采用分子模拟方法发现了离子液体中存在的非均质结构,并采用多尺度粗粒化方法(multiscale coarse-graining)研究了咪唑类离子液体中的团簇现象。Liu等[44]研究发现,离子液体的阳离子是由带电荷的极性中心与非极性的烷基链构成,碳链之间的范德华吸引作用与极性中心之间的排斥作用相互竞争,是形成团簇的原因之一。以咪唑类离子液体为例,随着阳离子碳链的增长,[C6min]+及[C10mim]+的末端烷基受咪唑环的影响逐渐减小,电荷基本可以忽略不计,在范德华吸引作用下这些电中性基团逐渐聚集,形成团簇结构。研究发现,离子液体的碳链增加到一定程度,宏观上会呈现液晶的特性[45]。实验证实,[C12mim]Br在不同浓度的水溶液中会呈现不同的团簇构象。图6模拟得到的[C12mim]Br离子液体在水溶液中的棒状团簇示意图(x=0.59 mol·L-1)与实验所得的结果吻合。图中由咪唑环及相连原子构成的极性基团由红色标注,烷基链由绿色标注,可见极性基团朝向水分子,而非极性基团远离水分子[46]。
离子液体体系内部的团簇阻碍了离子的自由运动,例如咪唑类、胍类等同系列的离子液体,因此随着碳链的增长黏度增加[47-48]。而且这种团簇结构并不是孤立和静止的,在实际应用过程中通常表现出非常复杂的变化。离子液体体系中多个尺度的结构(包括原子、分子、离子簇、纳微结构)影响和控制着体系的分离、反应等过程。因此,采用分子模拟、量化计算等方法,深入认识离子液体的反应及分离的多层次机理,为从海量离子液体中筛选和设计适合的离子液体提供科学依据。
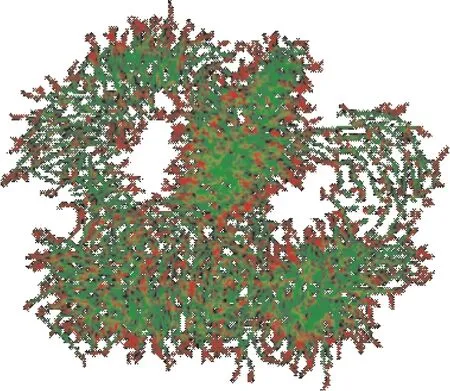
图6 离子液体水溶液中离子液体团簇构型图(阴离子及水都被忽略)[46]Fig.6 Simulation snapshot for [C12mim]Br in aqueous solution. Water is not shown for clarity. Red and green colors are used to stand for polar part (imidazolium ring, connected alkyl and anion) and nonpolar part (alkyl chain in cation, not connected with imidazolium ring), respectively[46]
2 离子液体体系的动力学与传递规律
离子液体清洁技术要实现工业化,还需要系统研究离子液体体系的流动及传递规律,为设计开发高效新型反应器提供基础。对于气液或气液固反应体系,气泡行为是认识流体流动和传递性质必不可少的性质。目前,针对传统分子型溶剂中气泡行为的研究比较深入,如水体系[49-52]、甘油体系[53, 54]、乙醇体系[55]和硅油体系[56]。然而,有关离子液体的研究主要还是集中在物理化学性质和构效关系等方面,与其相关的流动、传递和转化规律等的研究较少,导致反应器的开发和放大存在困难,缺乏理论的指导,成为离子液体体系工业化应用的重要瓶颈之一。
2.1 流动及传质规律的实验研究
通常传递规律的研究装置主要是针对分子介质的,不适用于离子型介质。根据离子液体的导电特性,作者研制开发了离子液体中传递-转化耦合过程的原位研究装置,成功地将阵列电极传感器和电阻层析成像系统集成到高温高压反应器中,实现了高温高压条件下离子液体中传递及转化规律的连续监测和数据自动采集处理。采用高速摄像技术研究了气泡在上升过程中大小、速度和变形规律。利用无因次分析方法提出了适合离子液体体系的曳力系数关联式,该关联式的预测结果与实验结果符合较好,相对误差在±10%以内。根据气泡在离子液体内上升过程中的变形特点提出了新的量纲1参数IL,变形率的预测相对偏差在±2%的范围内[57]。实际的反应体系通常含有一定量的水,为此系统研究了不同水含量下的气泡行为。研究表明,微量水对离子液体体系的气泡行为有很大影响。随着水含量增大,气泡运动速度加快,气泡变形加剧,当体系水含量达到10%左右时气泡在离子液体内从直线运动上升转变为“Z字形”运动上升[58]。基于单气泡的实验研究进一步开展了多气泡流动行为研究,清楚地观察到气泡在离子液体反应器内从分布器处生长,继而脱离,并不断聚并破碎的全过程。基于大量的实验数据提出了预测离子液体体系多气泡平均直径的新关联式,与实验值吻合良好(图7),相对误差在±6%以内[59]。进一步研究了离子液体体系的气液传质过程,测定CO2在不同离子液体内的液相传质系数,发现CO2在离子液体内的传质过程不仅与离子液体的黏度有关,还与离子液体的结构及吸收能力有关(图8)[60]。
2.2 流体动力学模拟
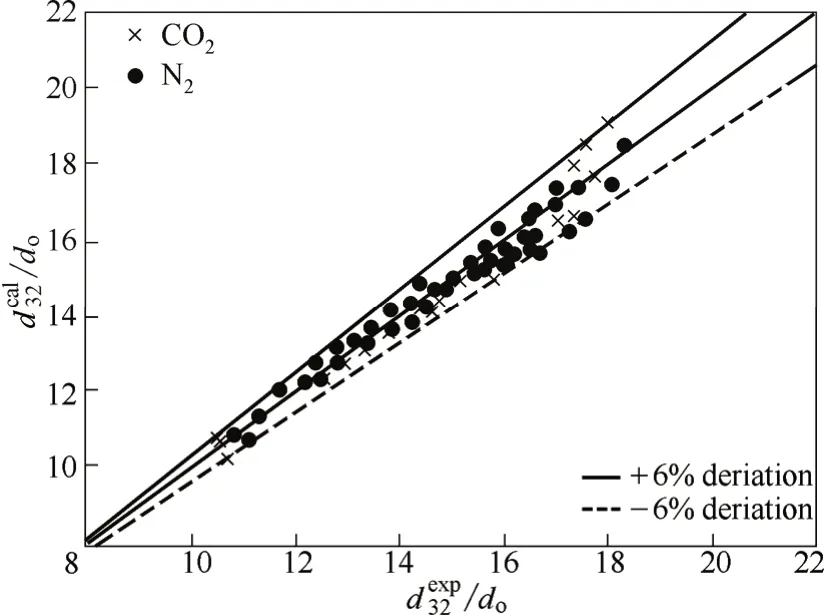
图7 预测离子液体体系多气泡直径[59]Fig.7 Predicting mean bubble diameter in ILs[59]
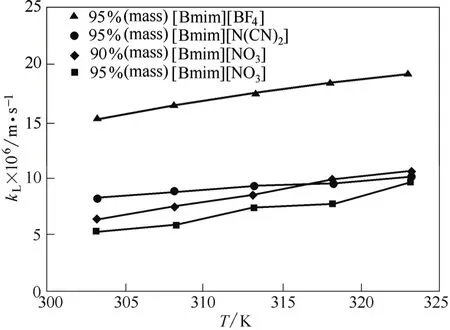
图8 离子液体体系液相传质系数[60]Fig.8 Gas-liquid mass transfer coefficients in ILs[60]
流体动力学计算是研究反应器内的流动及传递行为的有效方法之一。近几年,作者开展了离子液体吸收CO2流体动力学模拟计算,包括气含率、气泡速度、流场分布、气液接触表面积等[61-62],通过引入考虑离子液体性质的新的相间作用力源项来改进VOF模型组,可实现对离子液体体系的流体动力学模拟。对3种不同的离子液体[Bmim][BF4]、[Bmim][PF6]和[Omim][BF4]中气泡的上升速度、变形和等效直径进行了模拟,并计算获得了气泡内部以及气泡周围的压强场和速度场,取得了与实验结果较好的一致性。采用Euler-Euler双流体模型与群平衡模型(PBM)相耦合的方法(Euler-Euler模型模拟气液两相流行为,PBM模型对过程中的气泡尺寸进行预测),引入实验拟合获得的气液相间曳力系数模型,对鼓泡塔内离子液体-空气两相流的流体力学行为进行模拟,得到气含率、相界面积、气泡尺寸大小分布和传质系数以及反应器中的速度场和压力场。结果表明,低气速下气泡分布范围宽,气泡较大,鼓泡塔全塔气含率随气速增大而增加,而且气速增加,气含率的径向分布更加均匀;气含率沿鼓泡塔轴向呈周期性分布,气速越高,周期越短;离子液体在鼓泡塔内的速度场分布还受表观气速影响,表观气速为0.02 m·s-1时液相速度随塔高增加而增大,随气速增大液相速度沿塔轴向变化不大,说明该气速下塔内湍流发展充分[63]。
3 离子液体体系的系统集成
一个离子液体新工艺的技术、经济及环境性能是在其进入工业化之前就必须首先回答的问题,目的是将未来的产业化风险降低到最小。随着离子液体新技术逐渐走向工业化,离子液体的技术、经济和环境影响评价也越来越引起人们的关注[64],Seddon等[25]也撰文对离子液体的毒性、环境生态影响等进行了详细综述。
准确的流程模拟是进行工艺评价和系统集成的基础。传统的过程模拟技术主要基于经验或半经验模型,不仅需大量实验数据对参数进行拟合,而且难以从微观层次解析宏观现象。针对种类繁多的离子液体体系,仅靠实验拟合模型参数显然是不可行的。因此,离子液体体系的物性计算模型和热力学新模型开发至关重要。作者开发了离子液体数据库,提出了物性随离子液体阴阳离子结构的周期性变化规律[65-66],并在此基础上提出基于“离子片”的划分新策略,建立了预测离子液体物性新方法,以表面张力为例,误差由传统基团贡献法的约30%降到3%[67]。为了进一步降低对实验数据的依赖性,提出了基于分子层次的过程集成思路,采用从头算法(ab initial)在量化层次获得优化的分子结构信息,基于COSMO-RS方法获得溶剂体积、面积参数,通过UNIFAC获得交互参数并预测宏观性质如气液平衡、分配系数等,进而对全过程进行模拟[68]。针对离子液体的毒性,采用QSAR方法建立离子液体毒性预测模型,初步分析表明阳离子对毒性影响较为明显而阴离子影响较弱,相关研究为筛选环境友好离子液体提供了定量指标[69-71]。
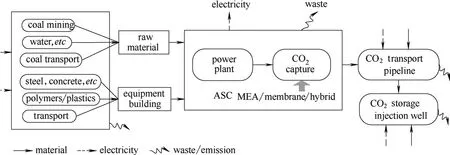
图9 考虑不同碳捕集技术的CCS全生命周期分析框架[72]Fig.9 Whole life cycle of power generation system containing CCS[72]
在系统集成方面,重点需要从全局把握和判断系统的性能,因此考虑一个过程的全生命周期具有重要的意义。以碳捕集-运输-储存(CCS)为例,不仅要考虑CCS技术本身,还需要研究其整个生命周期的性能。图9为考虑CCS的发电系统的全生命周期框图,除了包括烟气分离CO2技术外,还包括上游的电厂及原料系统以及下游的压缩、运输和贮存的整个碳链(carbon chain)的全生命周期。由此可见,尽管考虑CCS的发电系统在碳减排方面具有良好的环境效益,但其他很多环境指标均有上升,如图10所示[72],这些定量结果为决策者提供了重要的支撑。由于每个子系统之间存在复杂的物质能量交换,需要从全局和不同尺度评价、判断和优化这些过程。
总之,针对离子液体体系,一方面要开发离子液体体系的技术、经济及环境性能评价方法,建立离子液体的物性和环境性能数据库以及相关技术的物质能量利用效率,另一方面还需要建立离子液体原料选取合成使用废弃回收的全生命周期的评价方法。近年来,国际上开始探索离子液体的全生命周期评价研究[73]。近期作者对离子液体法分离生物气中的CO2的能耗和绿色度也进行了评价,获得了有价值的结果[74]。但总体来讲,相关的工作处于起步阶段,因此需要强化离子液体清洁技术的生命周期评价和系统集成研究,为产业化提供重要的指导。
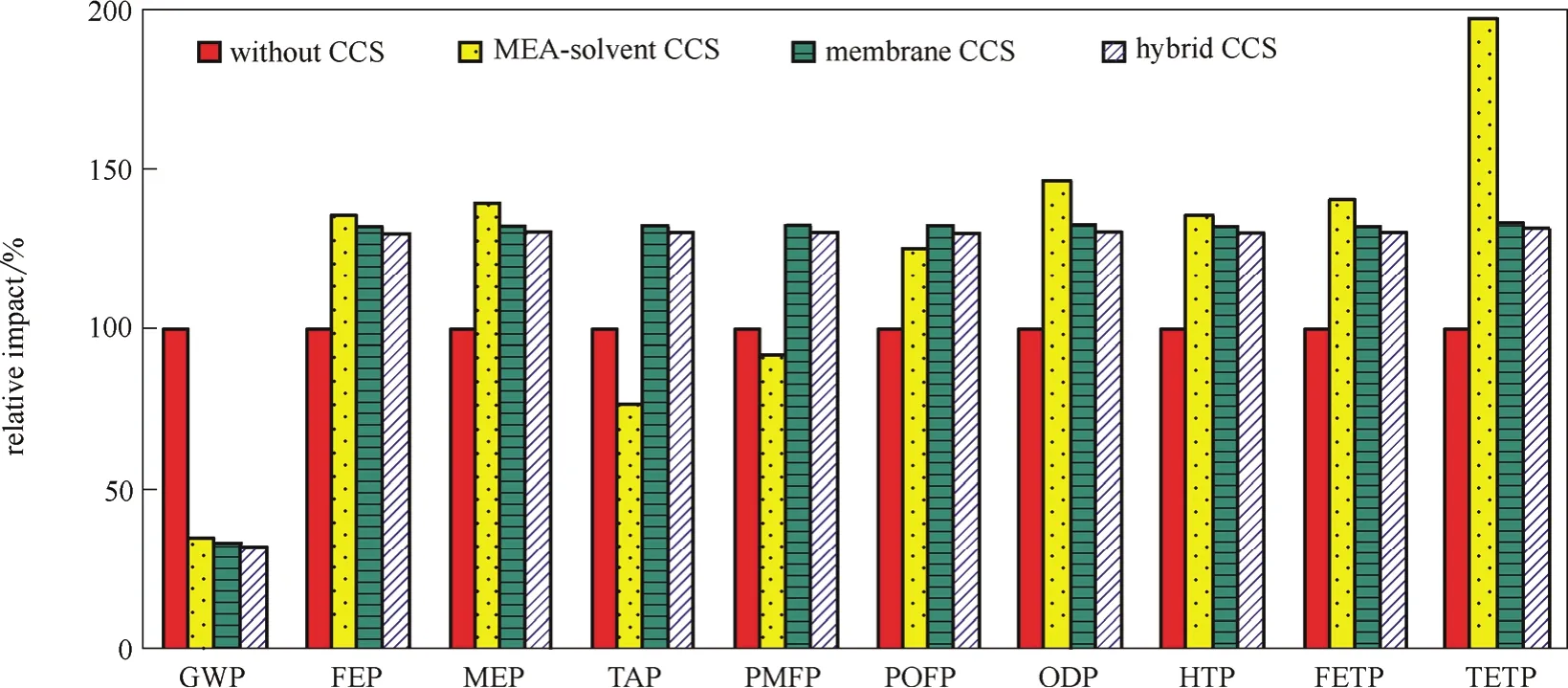
图10 考虑不同碳捕集技术的全生命周期的环境影响评价[72]Fig.10 Environmental impact of whole life cycle with CCS technologies[72]GWP (global warming): CO2eq; FEP (freshwater eutrophication): P eq; MEP (marine eutrophication): N eq; TAP (terrestrial acidification): SO2eq; PMFP (particulate matter formation): PM10 eq; POFP (photochemical oxidant formation): NMVOC; ODP (ozone depletion): CFC-11 eq; HTP (human toxicity): 1,4-DCB eq; FETP (freshwater ecotoxicity): 1,4-DCB eq; TETP (terrestrial ecotoxicity): 1,4-DCB eq
4 离子液体工艺创新
4.1 离子液体催化的乙二醇/碳酸酯新工艺
乙二醇(ethylene glycol, EG)是重要的有机化工原料,主要用于生产聚酯纤维、防冻液、聚酯多元醇等,2010年我国对乙二醇的总需求量达950万吨,而年总生产能力仅为323万吨,缺口严重。通常乙二醇生产采用环氧乙烷(EO)直接水合生产工艺,存在水比高、选择性差、反应条件苛刻、能耗高等缺点。在改进的技术中,代表性的有催化水合和催化水解法。相对于直接水合法,催化水合法是在催化剂存在下进行反应的,催化水解法则是以EO 和CO2为原料,先经羰基化反应生成碳酸乙烯酯(EC),而后EC水解生产EG。催化水解法与直接水合法相比,具有反应条件温和、水比低(H2O:EO=1.2:1)、EG选择性高(>99%)、能耗低等优势,在该工艺中,EO与CO2反应生成EC的羰基化反应是关键。
碱金属盐(如KI)较早用于催化合成环状碳酸酯的催化剂,而且已工业化。该催化剂价格低廉、稳定性高,但反应效率相对较低、反应条件较为苛刻、用量较大[75]。近年研究表明离子液体可作为CO2羰基化反应的良好的催化剂,如[Bmim][BF4]离子液体首次被报道用于羰基化反应且显现了较好的活性[76],机理在于阴阳离子协同催化有效地降低了反应活化能,提高了羰基化反应效率[77]。研究表明含羟基和羧基修饰的功能化离子液体较常规离子液体具有更高的活性[78-80]。图11表明,与单一的Bu4NBr相比,少量水的存在可以有效地降低反应的活化能[81],因此微量的水、醇、酸、酚的加入可明显降低反应体系的活化能,提高反应活性[82]。
在实际工业应用中,为了便于催化剂和产物分离,简化分离、降低能耗、减少损失、避免二次污染且保证产物的纯度,通常采用负载型固体催化剂,将均相反应器转变为固定床反应器。如采用载体的化学接枝方法,通过离子液体与载体间形成化学键实现负载,可解决物理负载存在的吸附法活性组分易流失的难题,现有研究的载体包括分子筛[83]、二氧化硅[84]、树脂[85-86]等。研究发现,离子液体负载后反应活性仍然保持较高(环氧乙烷转化率接近100%,乙二醇选择性99%),性能稳定,易与产物分离。聚合离子液体是目前的另一种固载化方法,当离子液体的阴、阳离子上带有不饱和键时容易发生离子液体的自聚或共聚,也同样具有很好的催化效果[87-89]。该方法与物理或化学负载法相比更为灵活,不受载体限制,具有很好的研究及应用发展前景。
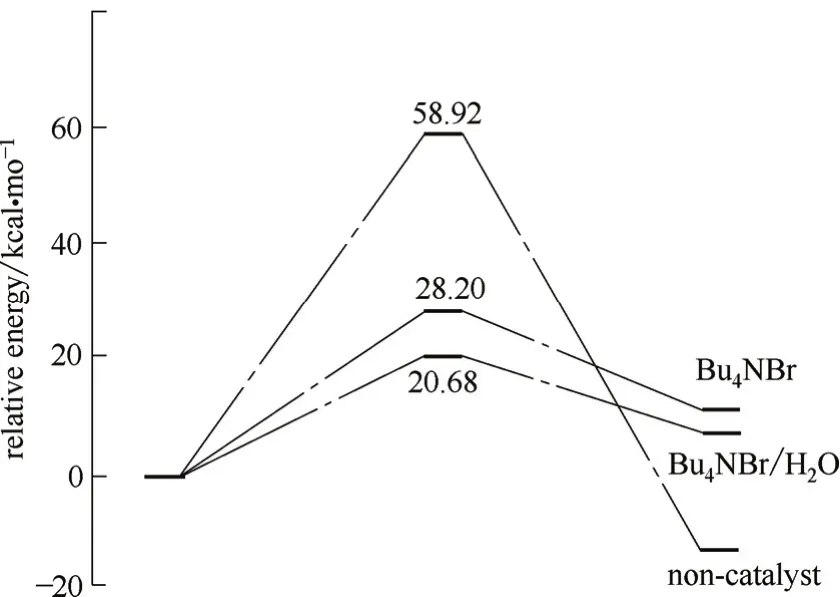
图11 离子液体催化羰基化反应速率决定步骤的相对能耗比较[81]Fig.11 Comparison of relative energy for rate-determining step[81](1 cal=4.1868 J)
4.2 基于离子液体的CO2分离技术
离子液体对CO2具有良好的吸收性能,研究成果最早发表于“Nature”[90],随后具有高物理吸收(如[Bmim][BF4]、[Emim][Tf2N])和化学吸收的功能化离子液体(如氨基酸类、双氨基膦类等)不断被报道[6, 91-93]。具有物理吸收CO2能力的离子液体,是由于其内部特殊的微观结构和作用力,使CO2在离子液体中有较大的溶解度。ATR-IR光谱技术研究,发现高的溶解性是由于CO2和离子液体的阴离子之间存在路易斯酸-碱作用[94-95],阳离子咪唑环C-2原子上的H 质子则可和CO2形成氢键作用[96]。量子化学和分子模拟表明,在咪唑类离子液体中多个阴、阳离子形成氢键网络,使得CO2分子能够“镶嵌”在阳离子形成的网络结构中,导致CO2在离子液体中有较高的溶解度[30]。总体来讲,CO2在离子液体中溶解度的大小主要取决于阴离子,与阴离子之间形成的氢键是导致CO2具有较高溶解度的原因[55]。Yu等[97]通过量子化学计算发现,离子间氢键和离子间强静电作用使[TMG]L阴阳离子作用能值比常规的咪唑离子液体高65.3~109.3 kJ·mol-1,因而其吸收能力强于[Bmim][PF6]。
为了显著提高吸收性能,研究开发功能化离子液体是该领域的一个发展趋势[98-101]。目前主要以氨基功能化离子液体为主,如[aemmim][Tau]离子液体吸收能力可达0.9 mol CO2·(mol IL)-1[100]。但通常这些离子液体的质量吸收能力小于0.1 g CO2·(g IL)-1[6]。Wang等[102]合成了质子型离子液体,以[MTBDH][Im]为例,其质量吸收能力达0.205 g CO2·(g IL)-1,但稳定性还需提高。作者所在团队[103]合成的双氨基功能化离子液体,其质量吸收量可达约18%。在离子液体黏度方面,一般功能化离子液体本身黏度就较高,吸收后由于发生了化学反应,其黏度更高,如[aP4443][AA]吸收CO2后的黏度较吸收前增加了将近3倍[101],又如[P66614][Isoleucinate]吸收后黏度增加了200倍[104]。因此,需要合成低黏离子液体。Gurkan等[105]报道了较低黏度的[P66614][2-CNpyr],50℃时其黏度低于100 mPa·s,而且在吸收CO2后其黏度变化很小,优越于早期的氨基功能化离子液体,而[MEA][BF4]离子液体50℃时黏度也仅为34 mPa·s。
除了设计功能化离子液体外,通过溶剂复配或负载是解决离子液体高黏度的有效途径。如将离子液体与有机胺复合,由于在再生过程中只需打破溶剂与CO2化学能,无须消耗大量水蒸发的能量,被认为是颇有前景的技术[106]。研究表明,复配后吸收性能几乎无损失或略有升高,但黏度明显降低[91],过程能耗降低约20%。采用负载方法形成离子液体基固体材料也是解决黏度问题的另一有效途径。如将功能化氨基酸离子液体负载在SiO2上,可实现良好的吸收-解吸[98]。此外,由于膜分离技术具有操作简单、能耗低、环境影响小等特点,有望降低捕集费用且成为当前气体分离的研究热点[107]。相比于现有膜材料,采用离子液体修饰的膜材料可显著提高选择性和渗透度,降低能耗和膜面积[9, 108-109]。Scovazzo总结了多种离子液体对CO2的溶解性及CO2/N2选择性,发现[Emim][DCA]的渗透率高达1234 barrers, 选择性达到57[110]。将不同离子液体负载到聚醚砜载体上,获得的渗透率最高可达610 barrers,选择性达到60[111]。Li等[112]合成的聚合物离子液体-离子液体组合膜渗透率可达340 barrers,选择性达到50,接近Robeson线上限。然而,尽管功能化离子液体可显著提高CO2/N2选择性,但考虑到渗透率是扩散系数和溶解度的乘积,而且扩散系数与黏度的开方呈正比,黏度增加10倍相当于渗透率降低3倍[110],因此有效提高功能化离子液体负载后的性能还有待深入研究。
4.3 废旧塑料降解新工艺
伴随着塑料工业的迅猛发展,废旧塑料数量急剧增长,其中聚对苯二甲酸乙二醇酯(PET)塑料已成为城市垃圾的主要来源之一,不仅造成巨大的资源浪费,而且产生严重的环境污染。目前,世界PET年产量已超过5千万吨,而其消耗量仍以每年11%的速度增长。塑料的原料主要为石油和天然气等不可再生资源,原料供应日趋紧张。因此,PET的回收利用具有重要的经济和环境意义。
目前,废聚酯再生方法可分为物理回收和化学回收。化学回收是将固态的聚合物材料解聚,转化为较小的分子、中间原料或是直接转化为单体的过程[113-114]。传统的化学回收PET 制取单体主要有水解法、甲醇醇解法和乙二醇醇解法。其中,水解法需要在高温高压条件下,PET 可水解为对苯二甲酸和乙二醇[115-117];乙二醇醇解法目前已实现了商业化装置运转[118]。但由于这是一个复杂的可逆反应,反应后的生成物较为复杂,反应条件苛刻,需要高温高压,反应速率低,如果反应过程中用到易挥发的有机溶剂则产生二次污染。因此,开发反应条件温和的PET降解绿色新技术具有重要意义。
2000年,Seddon等[119]报道了酸性[Emim][AlCl4]离子液体用于降解聚乙烯的研究,证明了离子液体降解聚合物的作用。其他探索研究包括以离子液体为溶剂可解聚尼龙-6制取单体[120]、氯铝酸类离子液体作为催化剂可降解聚碳酸酯[121]。研究表明,碱性离子液体[Bmim][OH]可催化醇解PET,其转化率和单体选择性均大于常规离子液体[Bmim]Cl、[Bmim]Br和[Bmim][HCO3],PET转化率可达100%,单体选择性可达71.4%,但[Bmim][OH]不能够稳定存在[122]。作者所在团队相继开展了离子液体醇解PET的系统研究[123-125],合成了系列常规及功能化离子液体。研究发现,使用性能良好的离子液体不仅能减少溶剂损失,在反应之后还可循环利用,节省溶剂用量,而且反应条件温和,减小设备腐蚀性,不会对环境产生污染。
对离子液体催化降解PET的反应机理进行了初步探讨,发现离子液体[Bmim][FeCl4]在催化醇解PET反应中的高催化活性主要是其阴、阳离子的协同作用,阳离子[Bmim]+与PET 羰基上的氧相互作用,同时阴离子[FeCl4]-进攻乙二醇羟基上的氢,使得乙二醇羟基上氧的电负性增加,氧原子更容易进攻PET 酯基上的碳正离子,阴、阳离子与反应物活性中心的协同作用使PET的降解更易进行。例如采用[Bmim]Cl溶剂来直接降解PET,推测机理是阳离子咪唑环上的氢与PET 中羰基上的氧相互作用,形成氢键,同时离子液体中的Cl-进攻PET 酯基上的带正电荷的碳,形成四面体结构中间体。离子液体阴阳离子与PET 酯基的这两种相互作用导致PET 酯基中C—O键的断裂,进而引起PET的分子量降低,降解成为单体。
5 展 望
本文以新型介质离子液体的基础及应用研究为特例展开论述,以诠释绿色化工系统工程的内涵、思想及内容。绿色化工系统工程为支撑化学工业可持续发展提供了重要的理论和实践方法,其结合了全局观念和系统论的思想,同时将理论分析、实验研究、工业实践三者有机结合,采用从分子到系统的多尺度研究思路和计算模拟以及先进的实验研究、测试和原位表征手段,实现从原子、分子、聚集体等多层次认识反应和分离过程的微观及宏观机理,开发更加有效的介质和材料(如催化剂、溶剂),进一步通过深入研究反应分离过程的传递规律、强化单元设备及优化工艺开发更加绿色的新技术,彻底改变化学工业多年来已经形成的先污染后治理的模式,在满足人类需求的同时实现与自然环境的和谐共处。
可以预想,绿色化工系统工程在集成传统的三传一反规律的同时,将重点突破分子-介尺度-宏观的关键科学问题,形成对三传一反过程的新认识和规律,进而发展绿色化工的理论体系和方法,为重大资源能源转化利用及环境问题的解决提供重要的科学支撑。
References
[1] ANASTAS P, WARNER J. Green Chemistry: Theory and Practice[M]. Oxford, UK: Oxford University Press, 1998
[2] ZHANG S, ZHANG X, LI C. Researches and trend on green process synthesis and design [J]. The Chinese Journal of Process Engineering, 2005, 5(5): 580-590.
[3] ZHANG Y. The green process engineering science [J]. The Chinese Journal of Process Engineering, 2001, 1(1): 10-15.
[4] 张懿. 清洁生产与循环经济[R]. 河南省第二届循环经济发展论坛会议. 河南, 2007.
[5] KENARSARI S D, YANG D L, JIANG G D, et al. Review of recentadvances in carbon dioxide separation and capture [J]. RSC Adv., 2013, 3(45): 22739-22773.
[6] ZHANG X P, ZHANG X C, DONG H F, et al. Carbon capture with ionic liquids: overview and progress [J]. Energ. Environ. Sci., 2012, 5(5): 6668-6681.
[7] ZHANG S J, ZHANG X P, ZHAO Y S, et al. A novel ionic liquids-based scrubbing process for efficient CO2capture [J]. Sci. China Chem., 2010, 53(7): 1549-1553.
[8] KARADAS F, ATILHAN M, APARICIO S. Review on the use of ionic liquids (ILs) as alternative fluids for CO2capture and natural gas sweetening [J]. Energy & Fuels, 2010, 24: 5817-5828.
[9] HASIB-UR-RAHMAN M, SIAJ M, LARACHI F. Ionic liquids for CO2capture-development and progress [J]. Chemical Engineering and Processing, 2010, 49(4): 313-322.
[10] FREEMANTLE M. Green process uses ionic liquid and CO2[J]. Chem. Eng. News., 1999, 77(19): 9-9.
[11] HU Y F, LIU Z C, XU C M, et al. The molecular characteristics dominating the solubility of gases in ionic liquids [J]. Chemical Society Reviews, 2011, 40(7): 3802-3823.
[12] XU B H, WANG J Q, SUN J, et al. Fixation of CO2into cyclic carbonates catalyzed by ionic liquids: a multi-scale approach [J]. Green Chemistry, 2015, 17(1): 108-122.
[13] ZHANG J M, SUN J, ZHANG X C, et al. The recent development of CO2fixation and conversion by ionic liquid [J]. Green Gases, 2011, 1(2): 142-159.
[14] YANG Z Z, ZHAO Y N, HE L N. CO2chemistry: task-specific ionic liquids for CO2capture/activation and subsequent conversion [J]. RSC Adv., 2011, 1(4): 545-567.
[15] HUBBARD C D, ILLNER P, VAN ELDIK R. Understanding chemical reaction mechanisms in ionic liquids: successes and challenges [J]. Chemical Society Reviews, 2011, 40(1): 272-290.
[16] OLIVIER-BOURBIGOU H, MAGNA L, MORVAN D. Ionic liquids and catalysis: recent progress from knowledge to applications [J]. Appl. Catal. A-Gen., 2010, 373(1/2): 1-56.
[17] VIDAL L, RIEKKOLA M L, CANALS A. Ionic liquid-modified materials for solid-phase extraction and separation: a review [J]. Anal. Chim. Acta, 2012, 715: 19-41.
[18] PEREIRO A B, ARAUJO J M M, ESPERANCA J, et al. Ionic liquids in separations of azeotropic systems—a review [J]. J. Chem. Thermodyn., 2012, 46: 2-28.
[19] ENDRES F. Ionic liquids for electrochemical deposition: prospects and challenges [J]. Chem. Ing. Tech., 2011, 83(9): 1485-1492.
[20] NOBLE R D, GIN D L. Perspective on ionic liquids and ionic liquid membranes [J]. Journal of Membrane Science, 2011, 369(1/2): 1-4.
[21] GIN D L, NOBLE R D. Designing the next generation of chemical separation membranes [J]. Science, 2011, 332(6030): 674-676.
[22] LIU C Z, WANG F, STILES A R, et al. Ionic liquids for biofuel production: opportunities and challenges [J]. Appl. Energy, 2012, 92: 406-414.
[23] ANDREANI L, ROCHA J D. Use of ionic liquids in biodiesel production: a review [J]. Braz. J. Chem. Eng., 2012, 29(1): 1-13.
[24] MORA-PALE M, MELI L, DOHERTY T V, et al. Room temperature ionic liquids as emerging solvents for the pretreatment of lignocellulosic biomass [J]. Biotechnol. Bioeng., 2011, 108(6): 1229-1245.
[25] PETKOVIC M, SEDDON K R, REBELO L P N, et al. Ionic liquids: a pathway to environmental acceptability [J]. Chemical Society Reviews, 2011, 40(3): 1383-1403.
[26] PHAM T P T, CHO C W, YUN Y S. Environmental fate and toxicity of ionic liquids: a review [J]. Water Research, 2010, 44(2): 352-372.
[27] ROTH C, PEPPEL T, FUMINO K, et al. The importance of hydrogen bonds for the structure of ionic liquids: single-crystal X-ray diffraction and transmission and attenuated total reflection spectroscopy in the terahertz region [J]. Angew. Chem. Int. Edit., 2010, 49(52): 10221-10224.
[28] PEPPEL T, ROTH C, FUMINO K, et al. The influence of hydrogen-bond defects on the properties of ionic liquids [J]. Angew. Chem. Int. Edit., 2011, 50(29): 6661-6665.
[29] DONG K, SONG Y, LIU X, et al. Understanding structures and hydrogen bonds of ionic liquids at the electronic level [J]. The Journal of Physical Chemistry B, 2011, 116(3): 1007-1017.
[30] DONG K, ZHANG S, WANG D, et al. Hydrogen bonds in imidazolium ionic liquids [J]. The Journal of Physical Chemistry A, 2006, 110(31): 9775-9782.
[31] MEOT-NER M. Update 1 of: strong ionic hydrogen bonds [J]. Chemical Reviews, 2012, 112(10): PR22-PR103.
[32] FUMINO K, WULF A, LUDWIG R. Strong, localized, and directional hydrogen bonds fluidize ionic liquids [J]. Angew. Chem. Int. Edit., 2008, 47(45): 8731-8734.
[33] WULF A, FUMINO K, LUDWIG R. Spectroscopic evidence for an enhanced anion-cation interaction from hydrogen bonding in pure imidazolium ionic liquids [J]. Angew. Chem. Int. Edit., 2010, 49(2): 449-453.
[34] REICHERT W M, HOLBREY J D, SWATLOSKI R P, et al. Solid-state analysis of low-melting 1,3-dialkylimidazolium hexafluorophosphate salts (ionic liquids) by combined X-ray crystallographic and computational analyses [J]. Cryst. Growth. Des., 2007, 7(6): 1106-1114.
[35] SOUTULLO M D, ODOM C I, WICKER B F, et al. Reversible CO2capture by unexpected plastic-, resin-, and gel-like ionic soft materials discovered during the combi-click generation of a tsil library [J]. Chem. Mater., 2007, 19(15): 3581-3583.
[36] SLATTERY J M, DAGUENET C, DYSON P J, et al. How to predict the physical properties of ionic liquids: a volume-based approach [J]. Angew. Chem. Int. Edit., 2007, 46(28): 5384-5388.
[37] DONG K, ZHANG S, WANG Q. A new class of ion–ion interaction: Z-bond [J]. Sci. China. Chem., 2014, DOI: 10.1007/s11426-014-5147-2.
[38] JIANG J C, LIN K H, LI S C, et al. Association structures of ionic liquid/DMSO mixtures studied by high-pressure infrared spectroscopy [J]. Journal of Chemical Physics, 2011, 134(4): 044506.
[39] LOPEZ-PASTOR M, AYORA-CANADA M J, VALCARCEL M, et al. Association of methanol and water in ionic liquids elucidated by infrared spectroscopy using two-dimensional correlation and multivariate curve resolution [J]. Journal of Physical Chemistry B, 2006, 110(22): 10896-10902.
[40] HE H, CHEN H, ZHENG Y, et al. The hydrogen-bonding interactions between 1-ethyl-3-methylimidazolium lactate ionic liquid and methanol [J]. Aust. J. Chem., 2013, 66(1): 50-59.
[41] WANG Y, VOTH G A. Unique spatial heterogeneity in ionic liquids [J]. Journal of the American Chemical Society, 2005, 127(35): 12192-12193.
[42] WANG Y, JIANG W, YAN T, et al. Understanding ionic liquids through atomistic and coarse-grained molecular dynamics simulations [J]. Accounts of Chemical Research, 2007, 40(11): 1193-1199.
[43] WANG Y, VOTH G A. Tail aggregation and domain diffusion in ionic liquids [J]. The Journal of Physical Chemistry B, 2006, 110(37): 18601-18608.
[44] LIU X, ZHOU G, ZHANG S, et al. Molecular simulation of imidazolium amino acid-based ionic liquids [J]. Molecular Simulation, 2010, 36(14): 1123-1130.
[45] CANONGIA LOPES J N A, P DUA A A H. Nanostructural organization in ionic liquids [J]. The Journal of Physical Chemistry B, 2006, 110(7): 3330-3335.
[46] CHEN S, ZHANG S, LIU X, et al. Ionic liquid clusters: structure, formation mechanism, and effect on the behavior of ionic liquids [J]. Phys. Chem. Chem. Phys., 2014, 16: 5893-5906.
[47] YU G, ZHAO D, WEN L, et al. Viscosity of ionic liquids: database, observation, and quantitative structure-property relationship analysis [J]. AIChE J., 2012, 58(9): 2885-2899.
[48] GAO Y, ARRITT S W, TWAMLEY B, et al. Guanidinium-based ionic liquids [J]. Inorganic Chemistry, 2005, 44: 1704-1712.
[49] CELATA G P, D’ANNIBALE F, DI MARCO P, et al. Measurements of rising velocity of a small bubble in a stagnant fluid in one-and two-component systems [J]. Exp. Therm. Fluid. Sci., 2007, 31(6): 609-623.
[50] ALVES S S, ORVALHO S P, VASCONCELOS J M T. Effect of bubble contamination on rise velocity and mass transfer [J]. Chem. Eng. Sci., 2005, 60(1): 1-9.
[51] PARKINSON L, SEDEV R, FORNASIERO D, et al. The terminal rise velocity of 10—100 mm diameter bubbles in water [J]. Journal of Colloid and Interface Science, 2008, 322(1): 168-172.
[52] RUZICKA M C, BUNGANIC R, DRAHOS J. Meniscus dynamics in bubble formation(Ⅰ): Experiment [J]. Chemical Engineering Research &Design, 2009, 87(10A): 1349-1356.
[53] MAXWORTHY T, GNANN C, K RTEN M, et al. Experiments on the rise of air bubbles in clean viscous liquids [J]. Journal of Fluid Mechanics, 1996, 321(1): 421-441.
[54] SNABRE P, MAGNIFOTCHAM F I. Formation and rise of a bubble stream in a viscous liquid [J]. European Physical Journal B, 1998, 4(3): 369-377.
[55] KAWAHARA A, SADATOMI M, NEI K, et al. Experimental study on bubble velocity, void fraction and pressure drop for gas-liquid two-phase flow in a circular microchannel [J]. International Journal of Heat and Fluid Flow, 2009, 30(5): 831-841.
[56] PANCHOLI K, STRIDE E, EDIRISINGHE M. Dynamics of bubble formation in highly viscous liquids [J]. Langmuir, 2008, 24(8): 4388-4393.
[57] DONG H F, WANG X L, LIU L, et al. The rise and deformation of a single bubble in ionic liquids [J]. Chemical Engineering Science, 2010, 65(10): 3240-3248.
[58] ZHANG X, DONG H, BAO D, et al. Effect of small amount of water on CO2bubble behavior in ionic liquid systems [J]. Ind. Eng. Chem. Res., 2014, 53(1): 428-439.
[59] ZHANG X, DONG H F, HUANG Y, et al. Experimental study on gas holdup and bubble behavior in carbon capture systems with ionic liquid [J]. Chem. Eng. J., 2012, 209: 607-615.
[60] ZHANG X, BAO D, HUANG Y, et al. Gas-liquid mass-transfer properties in CO2absorption system with ionic liquids [J]. AIChE J., 2014, 60(8): 2929-2939.
[61] WANG X L, DONG H F, ZHANG X P, et al. Numerical simulation of single bubble motion in ionic liquids [J]. Chemical Engineering Science, 2010, 65(22): 6036-6047.
[62] WANG X L, DONG H F, ZHANG X P, et al. Numerical simulation of absorbing CO2with ionic liquids [J]. Chem. Eng. Technol., 2010, 33(10): 1615-1624.
[63] 徐琰, 董海峰, 田肖, 等. 鼓泡塔中离子液体-空气两相流的CFD-PBM耦合模拟[J]. 化工学报, 2001, 62(10): 2699-2706. XU Y, DONG H F, TIAN X, et al. CFD-PBM coupled simulation of ionic liquid-air two-phase flow in bubble column [J]. CIESC Journal, 2011, 62(10): 2699-2706.
[64] SHIFLETT M B, DREW D W, CANTINI R A, et al. Carbon dioxide capture using ionic liquid 1-butyl-3-methylimidazolium acetate [J]. Energy & Fuels, 2010, 24: 5781-5789.
[65] ZHANG S J, SUN N, HE X Z, et al. Physical properties of ionic liquids: database and evaluation [J]. J. Phys. Chem. Ref. Data, 2006, 35(4): 1475-1517.
[66] ZHANG S J, SUN N, ZHANG X P, et al. Periodicity and map for discovery of new ionic liquids [J]. Sci. China Ser. B, 2006, 49(2): 103-115.
[67] HUANG Y, DONG H, ZHANG X, et al. A new fragment contribution-corresponding states method for physicochemical properties prediction of ionic liquids [J]. AIChE J., 2013, 594(4): 1348-1359.
[68] TIAN X A, ZHANG X P, WEI L, et al. Multi-scale simulation of the 1,3-butadiene extraction separation process with an ionic liquid additive [J]. Green Chem., 2010, 12(7): 1263-1273.
[69] ZHAO Y S, ZHANG X P, ZHAO J H, et al. Research of QSPR/QSAR for ionic liquids [J]. Prog. Chem., 2012, 24(7): 1236-1244.
[70] ZHAO Y S, ZHAO J H, HUANG Y, et al. Toxicity of ionic liquids: database and prediction via quantitative structure-activity relationship method [J]. J. Hazard. Mater., 2014, 278: 320-329.
[71] DE MELO E B. A structure-activity relationship study of the toxicity of ionic liquids using an adapted Ferreira-Kiralj hydrophobicity parameter [J]. Phys. Chem. Chem. Phys., 2015, 17(6): 4516-4523.
[72] ZHANG X, SINGH B, HE X, et al. Post-combustion carbon capture technologies: energetic analysisand life cycle assessment [J]. Int. J. Greenh. Gas Con., 2014, 27: 289-298.
[73] ZHANG Y, BAKSHI B R, DEMESSIE E S. Life cycle assessment of an ionic liquid versus molecular solvents and their applications [J]. Environ. Sci. Technol., 2008, 42(5): 1724-1730.
[74] ZHAO X, XING H B, LI R L, et al. Gas separation based on ionic liquids [J]. Prog. Chem., 2011, 23(11): 2258-2268.
[75] GAO J, ZHONG S H. The research progress in preparation of ethylene carbonate directly from CO2and ethylene oxide [J]. Prog. Chem., 2002, 14(2): 107-112.
[76] PENG J J, DENG Y Q. Cycloaddition between propylene oxide and carbon dioxide catalysed by ionic liquids [J]. New J. Chem., 2001, 25: 639-641.
[77] ZHANG S, CHEN Y, LI F, et al. Fixation and conversion of CO2using ionic liquids [J]. Catalysis Today, 2006, 115(1/2/3/4): 61-69.
[78] SUN J, WANG L, ZHANG S J, et al. ZnCl2/phosphonium halide: an efficient lewis acid/base catalyst for the synthesis of cyclic carbonate[J]. Journal of Molecular Catalysis a-Chemical., 2006, 256(1/2): 295-300.
[79] SUN J, ZHANG S, CHENG W, et al. Hydroxyl-functionalized ionic liquid: a novel efficient catalyst for chemical fixation of CO2to cyclic carbonate [J]. Tetrahedron Letters, 2008, 49(22): 3588-3591.
[80] SUN J, HAN L, CHENG W, et al. Efficient acid-base bifunctional catalysts for the fixation of CO2with epoxides under metal- and solvent-free conditions [J]. Chemsuschem., 2011, 4(4): 502-507.
[81] WANG J Q, SUN J, CHENG W G, et al. Experimental and theoretical studies on hydrogen bond-promoted fixation of carbon dioxide and epoxides in cyclic carbonates [J]. Phys. Chem. Chem. Phys., 2012, 14(31): 11021-11026.
[82] SUN J, REN J, ZHANG S, et al. Water as an efficient medium for the synthesis of cyclic carbonate [J]. Tetrahedron Letters, 2009, 50(4): 423-426.
[83] CHENG W G, CHEN X, SUN J, et al. Sba-15 supported triazolium-based ionic liquids as highly efficient and recyclable catalysts for fixation of CO2with epoxides [J]. Catalysis Today, 2013, 200: 117-124.
[84] TAKAHASHI T, WATAHIKI T, KITAZUME S, et al. Synergistic hybrid catalyst for cyclic carbonate synthesis: remarkable acceleration caused by immobilization of homogeneous catalyst on silica [J]. Chem. Commun., 2006, (15): 1664-1666.
[85] SUN J, CHENG W, FAN W, et al. Reusable and efficient polymer-supported task-specific ionic liquid catalyst for cycloaddition of epoxide with CO2[J]. Catalysis Today, 2009, 148(3/4): 361-367.
[86] CHEN X, SUN J, WANG J, et al. Polystyrene-bound diethanolamine based ionic liquids for chemical fixation of CO2[J]. Tetrahedron Letters, 2012, 53(22): 2684-2688.
[87] XIE Y, ZHANG Z, JIANG T, et al. CO2cycloaddition reactions catalyzed by an ionic liquid grafted onto a highly cross-linked polymer matrix [J]. Angew. Chem. Int. Edit., 2007, 46(38): 7255-7258.
[88] SHI T Y, WANG J Q, SUN J, et al. Efficient fixation of CO2into cyclic carbonates catalyzed by hydroxyl-functionalized poly(ionic liquids) [J]. RSC Adv., 2013, 3(11): 3726-3732.
[89] HAN L, CHOI H-J, KIM D-K, et al. Porous polymer bead-supported ionic liquids for the synthesis of cyclic carbonate from CO2and epoxide [J]. Journal of Molecular Catalysis A-Chemical, 2011, 338(1/2): 58-64.
[90] BLANCHARD L A, HANCU D, BECKMAN E J, et al. Green processing using ionic liquids and CO2[J]. Nature, 1999, 399(6731): 28-29.
[91] ZHAO Y, ZHANG X, ZHEN Y, et al. Novel alcamines ionic liquids based solvents: preparation, characterization and applications in carbon dioxide capture [J]. Int. J. Greenh. Gas Con., 2011, 5(2): 367-373.
[92] WAPPEL D, GRONALD G, KALB R, et al. Ionic liquids for post-combustion CO2absorption [J]. Int. J. Greenh. Gas Con., 2010, 4(3): 486-494.
[93] VEGA L F, VILASECA O, LLOVELL F, et al. Modeling ionic liquids and the solubility of gases in them: recent advances and perspectives [J]. Fluid Phase Equilib., 2010, 294(1/2): 15-30.
[94] KAZARIAN S G, BRISCOE B J, WELTON T. Combining ionic liquids and supercritical fluids: ATR-IR study of CO dissolved in two ionic liquids at high pressures [J]. Chem. Commun., 2000, (20): 2047-2048.
[95] CAMMARATA L, KAZARIAN S G, SALTER P A, et al. Molecular states of water in room temperature ionic liquids [J]. Phys. Chem. Chem. Phys., 2001, 3(23): 5192-5200.
[96] CROWHURST L, MAWDSLEY P R, PEREZ-ARLANDIS J M, et al. Solvent-solute interactions in ionic liquids [J]. Phys. Chem. Chem. Phys., 2003, 5(13): 2790-2794.
[97] YU G, ZHANG S. Insight into the cation-anion interaction in 1,1,3,3-tetramethylguanidinium lactate ionic liquid [J]. Fluid Phase Equilib., 2007, 255(1): 86-92.
[98] ZHANG J M, ZHANG S J, DONG K, et al. Supported absorption of CO2by tetrabutylphosphonium amino acid ionic liquids [J]. Chem. Eur. J., 2006, 12(15): 4021-4026.
[99] ZHANG Y, ZHANG S, LU X, et al. Dual amino-functionalised phosphonium ionic liquids for CO2capture [J]. Chemistry – A European Journal, 2009, 15(12): 3003-3011.
[100] XUE Z M, ZHANG Z F, HAN J, et al. Carbon dioxide capture by a dual amino ionic liquid with amino-functionalized imidazolium cation and taurine anion [J]. Int. J. Greenh. Gas Con., 2011, 5(4): 628-633.
[101] LIU X, ZHOU G, ZHANG S, et al. Molecular dynamics simulation of dual amino-functionalized imidazolium-based ionic liquids [J]. Fluid Phase Equilib., 2009, 284(1): 44-49.
[102] WANG C, LUO H, JIANG D-E, et al. Carbon dioxide capture by superbase-derived protic ionic liquids [J]. Angew. Chem. Int. Edit., 2010, 49(34): 5978-5981.
[103] ZHANG J Z, JIA C, DONG H F, et al. A novel dual amino-functionalized cation-tethered ionic liquid for CO2capture [J]. Ind. Eng. Chem. Res., 2013, 52(17): 5835-5841.
[104] GURKAN B, GOODRICH B F, MINDRUP E M, et al. Molecular design of high capacity, low viscosity, chemically tunable ionic liquids for CO2capture [J]. Journal of Physical Chemistry Letters, 2010, 1(24): 3494-3499.
[105] ZHAO Y S, ZHANG X P, DONG H F, et al. Solubilities of gases in novel alcamines ionic liquid 2-[2-hydroxyethyl (methyl) amino] ethanol chloride [J]. Fluid Phase Equilib., 2011, 302(1/2): 60-64.
[106] CAMPER D, BARA J E, GIN D L, et al. Room-temperature ionic liquid-amine solutions: Tunable solvents for efficient and reversible capture of CO2[J]. Ind. Eng. Chem. Res., 2008, 47(21): 8496-8498.
[107] MERKEL T C, LIN H, WEI X, et al. Power plant post-combustion carbon dioxide capture: an opportunity for membranes [J]. Journal of Membrane Science, 2010, 359(1/2): 126-139.
[108] BARA J E, CAMPER D E, GIN D L, et al. Room-temperature ionic liquids and composite materials: Platform technologies for CO2capture [J]. Accounts of Chemical Research, 2010, 43(1): 152-159.
[109] LOZANO L J, GODINEZ C, DE LOS RIOS A P, et al. Recent advances in supported ionic liquid membrane technology [J]. Journal of Membrane Science, 2011, 376(1/2): 1-14.
[110] SCOVAZZO P. Determination of the upper limits, benchmarks, and critical properties for gas separations using stabilized room temperature ionic liquid membranes (silms) for the purpose of guiding future research [J]. Journal of Membrane Science, 2009, 343(1/2): 199-211.
[111] SCOVAZZO P, KIEFT J, FINAN D A, et al. Gas separations using non-hexafluorophosphate PF6anion supported ionic liquid membranes [J]. Journal of Membrane Science, 2004, 238(1/2): 57-63.
[112] LI P, PAUL D R, CHUNG T S. High performance membranes based on ionic liquid polymers for CO2separation from the flue gas [J]. Green Chem., 2012, 14(4): 1052-1063.
[113] GENTA M, IWAYA T, SASAKI M, et al. Depolymerization mechanism of poly(ethylene terephthalate) in supercritical methanol [J]. Ind. Eng. Chem. Res., 2005, 44(11): 3894-3900.
[114] YOSHIOKA T, SATO T, OKUWAKI A. Hydrolysis of waste pet by sulfuric-acid at 150-degrees-c for a chemical recycling [J]. J. Appl. Polym. Sci., 1994, 52(9): 1353-1355.
[115] SAMMON C, YARWOOD J, EVERALL N. An FT-IR study of the effect of hydrolytic degradation on the structure of thin pet films [J]. Polym. Degrad. Stabil., 2000, 67(1): 149-158.
[116] DE CARVALHO G M, MUNIZ E C, RUBIRA A F. Hydrolysis of post-consume poly(ethylene terephthalate) with sulfuric acid and product characterization by WAXD,13C NMR and DSC [J]. Polym. Degrad. Stabil., 2006, 91(6): 1326-1332.
[117] HOSSEINI S S, TAHERI S, ZADHOUSH A, et al. Hydrolytic degradation of poly(ethylene terephthalate) [J]. J. Appl. Polym. Sci., 2007, 103(4): 2304-2309.
[118] YANG Y, LV Y, XU Y, et al. Chemical recycling of waste poly(ethylene terephthalate) [J]. Prog. Chem., 2001, 13(1): 65.
[119] ADAMS C J, EARLE M J, SEDDON K R. Catalytic cracking reactions of polyethylene to light alkanes in ionic liquids [J]. Green Chem., 2000, 2(1): 21-23.
[120] KAMIMURA A, YAMAMOTO S. An efficient method to depolymerize polyamide plastics: a new use of ionic liquids [J]. Org. Lett., 2007, 9(13): 2533-2535.
[121] GU Y L, YANG H Z, DENG Y Q. Catalytic degradation of polycarbonate cd in ionic liquids: Recovery of diphenyl carbonate [J]. Acta Chimica Sinica., 2002, 60(4): 753-757.
[122] YUE Q F, WANG C X, ZHANG L N, et al. Glycolysis of poly(ethylene terephthalate) (PET) using basic ionic liquids as catalysts [J]. Polym. Degrad. Stabil., 2011, 96(4): 399-403.
[123] WANG H, LI Z X, LIU Y Q, et al. Degradation of poly(ethylene terephthalate) using ionic liquids [J]. Green Chem., 2009, 11(10): 1568-1575.
[124] WANG H, YAN R Y, LI Z X, et al. Fe-containing magnetic ionic liquid as an effective catalyst for the glycolysis of poly(ethylene terephthalate) [J]. Catal. Commun., 2010, 11(8): 763-767.
[125] ZHOU X Y, LU X M, WANG Q, et al. Effective catalysis of poly(ethylene terephthalate) (PET) degradation by metallic acetate ionic liquids [J]. Pure. Appl. Chem., 2012, 84(3): 789-801.
Foundation item: supported by the National Basic Research Program of China(2015CB251403) and the National Science Fund for Distinguished Young Scholars (21425625).
Green process system engineering
ZHANG Suojiang, ZHANG Xiangping, NIE Yi, BAO Di, DONG Haifeng, LÜ Xingmei
(Beijing Key Laboratory of Ionic Liquids Clean Process, State Key Laboratory of Multiphase Complex Systems, Key Laboratory of Green Process and Engineering, Institute of Process Engineering, Chinese Academy of Sciences, Beijing 100190, China)
Abstract:One of the main tendencies of sustainable chemical engineering is to develop green technologies with the aim of eliminating pollution by preventing it in the first place, and thus, any breakthrough of single unit technology could make significant contributions to a new green technology. However, process engineering is a complex system which covers multiple units and sub-systems, including utilities, waste treatment and so on. Hence, besides single technology innovation, the whole chain covering raw material substitute, unit intensification and system should be highlighted during process development, and meanwhile considering the economic and environmental constraints. Also, along this chain, the novel materials/solvents and processes innovation are important for the process greening. On the base of the principles of system engineering and considering the research frontiers of the green process engineering, and taking new ionic liquids as key material, this article reviews the latest progresses in the aspects of raw material substitution, solvent innovation, transfer properties and process integration. The proposed viewpoints and methodology could become important bases to develop new green technologies, and also construct the science of green process system engineering subject.
Key words:green process system engineering; process systems; green technology; ionic liquid; hydrogen-bond; simulation
Corresponding author:Prof. ZHANG Suojiang, sjzhang@ipe. ac.cn
基金项目:国家重点基础研究发展计划项目(2015CB251403);国家杰出青年基金项目(21425625)。
中图分类号:TQ 021.8
文献标志码:A
文章编号:0438—1157(2016)01—0041—13
DOI:10.11949/j.issn.0438-1157. 20150611
