不同侵袭危险性胃间质瘤的超声内镜图像特点比较及相关危险因素分析*
2016-03-18卢光荣周羽翙钟金伟金健威符媚虞晨黄智铭薛战雄
卢光荣,周羽翙,钟金伟,金健威,符媚,虞晨,黄智铭,薛战雄
(1.温州医科大学附属第二医院消化内科,浙江温州325000;2.浙江省温州市中心医院消化内科,浙江温州325000;3.温州医科大学第一临床医学院,浙江温州325000;4.温州医科大学附属第一医院消化内科,浙江温州325000)
不同侵袭危险性胃间质瘤的超声内镜图像特点比较及相关危险因素分析*
卢光荣1,周羽翙1,钟金伟1,金健威2,符媚3,虞晨3,黄智铭4,薛战雄1
(1.温州医科大学附属第二医院消化内科,浙江温州325000;2.浙江省温州市中心医院消化内科,浙江温州325000;3.温州医科大学第一临床医学院,浙江温州325000;4.温州医科大学附属第一医院消化内科,浙江温州325000)
摘要:目的寻找不同侵袭危险性胃间质瘤(GSTs)的超声内镜(EUS)图像特点差异。方法收集温州市3大医院286例经病理及免疫组化确诊为GSTs患者,根据肿瘤大小、核分裂象将其分为极低危组、低危组、中危组以及高危组;回顾分析不同侵袭危险性GSTs组间临床资料及EUS图像特征,寻找差异并进行相关危险因素分析。结果286例GSTs形状绝大多数规则(262/286),最常起源于胃固有肌层(219/286),病灶多呈低回声改变(254/286)、回声均匀(212/286)、边界清楚(264/286),有一部分可见钙化(79/286)、溃疡(75/286)以及囊性变(54/286)。286例GSTs中极低危组60例(20.98%),低危组112例(39.16%),中危组73例(25.52%),高危组41例(14.34%);单因素分析显示侵袭危险性越高,溃疡越好发,内部回声不均匀、钙化及囊性变现象越常见;而进一步多因素分析显示溃疡的发生(=2.44,95%CI:1.36~3.18)是唯一预测GSTs侵袭危险性分级的独立因素(P<0.05)。结论不同侵袭危险性GSTs在EUS图像的表现有所差异,除肿瘤大小、核分裂象外,表面溃疡的发生同样是预测GSTs侵袭危险性的重要标志。
关键词:侵袭危险性;胃间质瘤;超声内镜;危险因素
胃间质瘤(gastrointestinal stromal tumors,GSTs)是消化系统常见的间叶组织肿瘤,大约占胃肠道肿瘤的60.00%~70.00%[1],是上消化道最常见的非上皮性肿瘤。目前多数学者认为GSTs均有潜在恶性,不能简单的以良恶性划分,而是应该进行侵袭危险性的分级。Fletcher等[2]综合GSTs直径大小和核分裂象等因素将GSTs侵袭危险度分为极低、低、中和高4个等级。超声内镜(endoscopic ultrasound,EUS)目前已成为消化道黏膜下隆起性病变的首选检查,其对GSTs的诊断有较高的敏感性,但目前国内研究GSTs不同侵袭危险性分级的EUS图像特点之间比较的文献较少。本研究收集温州地区正常开展EUS检查技术的医院(温州医科大学附属第二医院、温州医科大学附属第一医院和温州市中心医院)经病理及免疫组化确诊的286例GSTs EUS图像进行总结分析,以期为以后临床工作中术前通过EUS检查辅助判断GSTs的侵袭危险性。
1 资料与方法
1.1一般资料
选取2004年11月-2015年5月就诊于温州医科大学附属第二医院、温州医科大学附属第一医院和温州市中心医院的因胃黏膜下隆起性病变行EUS检查的患者。其中,行外科手术或内镜下切除治疗经病理、免疫组化检查确诊为GSTs 286例,男160例,女126例,平均58.6岁。
1.2研究方法
根据肿瘤大小、核分裂象将其分为极低危组、低危组、中危组以及高危组,回顾分析不同侵袭危险性GSTs组间临床资料及EUS图像特征,临床资料包括:性别、年龄;EUS图像特征分析包括:肿瘤形状、发病部位、起源层次、有无溃疡、有无钙化、有无囊性变、有无黏膜桥形成、边界是否清楚、回声强度和回声异质性。由于Fletcher分级评估(见表1)已包含肿瘤直径大小,故本研究未将肿瘤直径纳入分析。超声图像的特征交由我院具有多年操作EUS经验的两位主任医师盲法分析并取得一致(未告知其分组结果),重点分析的内容包括:有无溃疡、有无钙化、有无囊性变、边界是否清楚、回声强度及回声异质性。
1.3统计学方法
本研究采用SPSS 19.0软件进行数据统计学分析,临床资料及EUS图像特点采用秩和检验,多因素分析采用多值多元Logistics回归检验,P<0.05表示差异有统计学意义。
2 结果
2.1Fletcher分级结果及EUS图像特征
其中极低危组60例(20.98%),低危组112例(39.16%),中危组73例(25.52%),高危组41例(14.34%);GSTs平均直径3.38cm,形状绝大多数规则,最常起源于胃固有肌层(219/286),病灶多呈低回声改变(254/286)、回声均匀(212/286)、边界清楚(264/286),有一部分可见钙化(79/286)、溃疡(75/286)以及囊性变(54/286)。
2.2不同侵袭危险性GSTs的EUS图像特点比较
按照Fletcher分级,各组EUS图像特点比较见表2。单因素分析显示侵袭危险性越高,溃疡越好发,内部回声不均匀、钙化及囊性变现象越常见;而进一步多因素分析,以有无溃疡、内部回声异质性、有无钙化及有无囊性变为自变量显示除肿瘤大小外,溃疡的发生(=2.44,95%CI:1.36~3.18)是唯一预测胃GSTs侵袭危险性分级的独立因素(P< 0.05)。见表3。
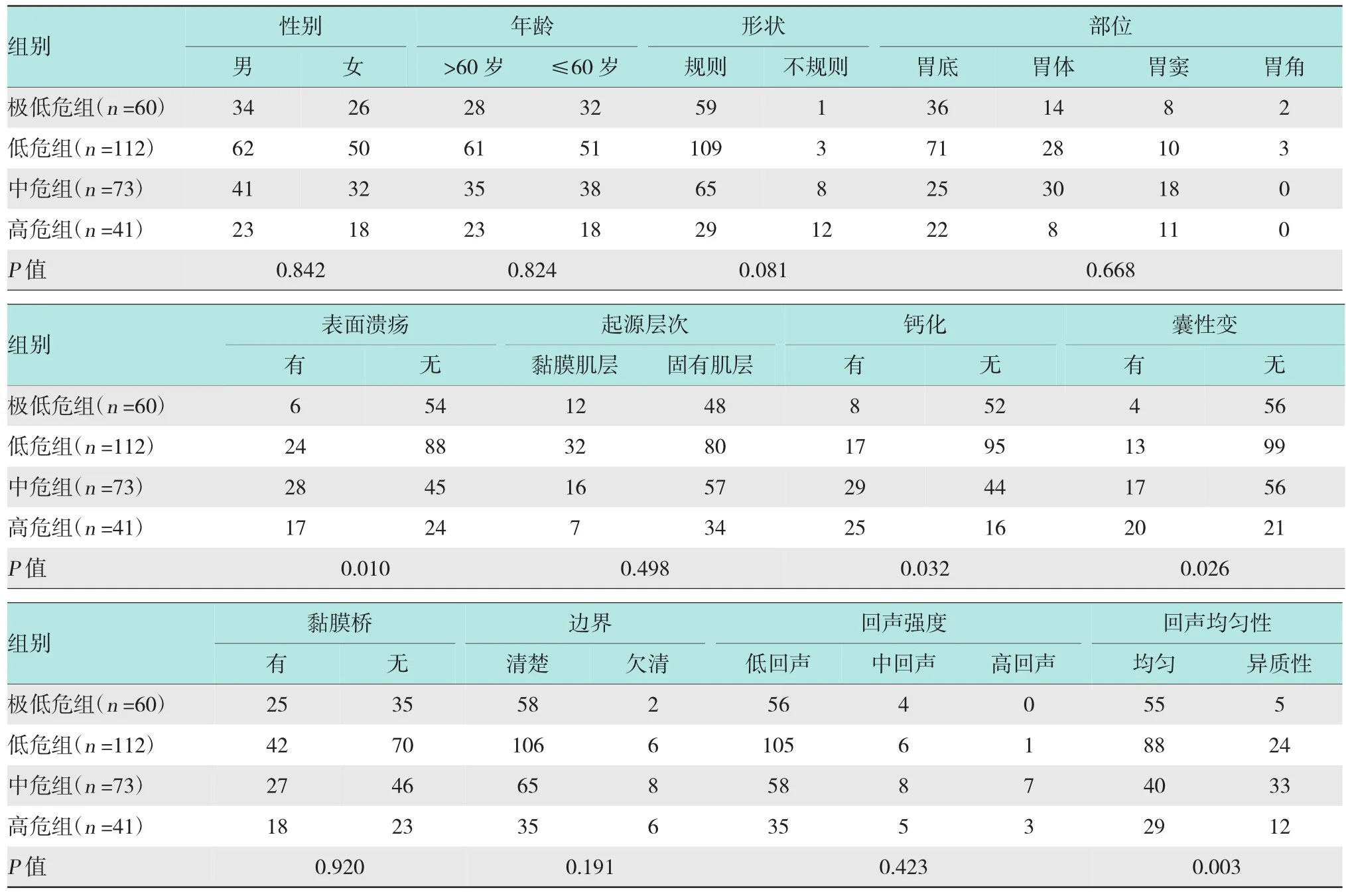
表2 不同侵袭危险性GSTs的临床资料及EUS特点比较 例
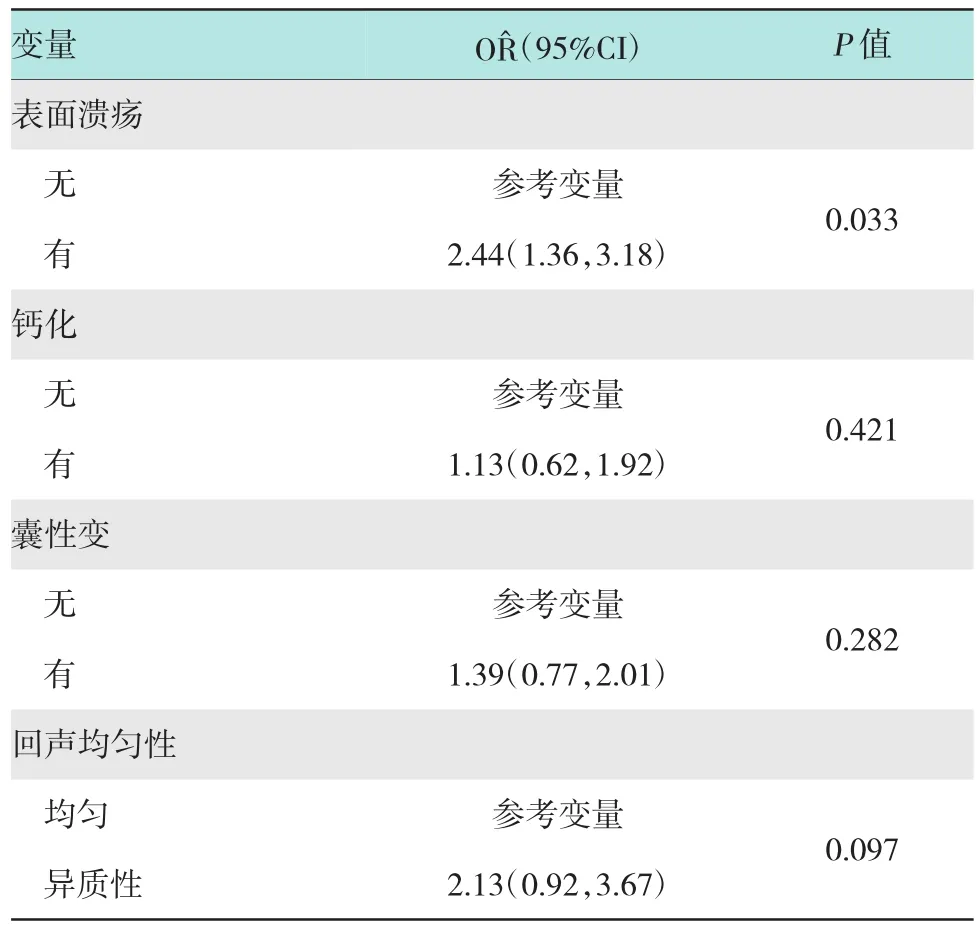
表3 GSTs不同侵袭危险性分级多因素分析
3 讨论
胃肠道间质瘤(gastrointestinal stromal tumors,GISTs)是消化系统最常见的间叶组织源性肿瘤,主要发生于胃和小肠,其中GSTs约占60.00%~70.00%[1]。有学者曾根据肿瘤大小及核分裂相将GISTs分为良性、恶性及交界性[3],但随后研究发现即使体积很小(<2 cm)、核分裂象很低(<5/50高倍视野)的GISTs也偶见转移或复发[4]。因此,目前多数学者认为GISTs具有一定的恶性潜能,以侵袭危险性评估其生物学行为更为合理。目前,国际上采用F letcher等[2]的分级标准,综合肿瘤大小和核分裂象量因素将GSTs分为极低危、低危、中危和高危4个等级,侵袭危险性越高,存活率越低。目前认为极低度侵袭危险性GSTs可选择内镜下随访,而低度、中度、高度侵袭危险性GSTs则建议内镜下切除或外科手术治疗。因此,GSTs侵袭危险性的分级对进一步的治疗及疾病的预后存在着一定的指导意义。由于普通内镜下活检常难以取到病变组织,并且活检可出现出血、穿孔、感染等风险,故GSTs不推荐术前常规活检,GSTs侵袭危险性在术前较难予以准确评估。
EUS兼具内镜的直观性与超声的穿透性,因其能清晰显示病变的起源层次、大小、形状、边界、回声特点和有无浸润征象等[5],已成为消化道黏膜下隆起性病变的首选检查。有较多研究显示,EUS对GSTs的诊断具有较高的敏感性及特异性。典型的GSTs 在EUS下表现为多起源于胃固有肌层,少数起源于黏膜肌层,病灶呈低回声,回声均匀或者不均匀,边界清楚。由于GSTs具有潜在恶性潜能,近年来EUS 对GSTs术前良恶性评估逐渐成热点,相关文献亦较多。Shah等[6]认为肿瘤大小、不规则腔外边界、局部侵犯及内部回声不均匀是预测GSTs恶性潜能的重要指标。Palazzo等[7]研究发现肿瘤直径<3 cm,边界整齐,回声均匀是良性特征;肿瘤直径>4 cm,表面有溃疡,回声不均匀伴囊腔,形状不规则且突出于腔壁,局部淋巴结侵犯是恶性特征。如果上述特征具备1种及以上则诊断GSTs具有恶性潜能的敏感度达91.00%,特异度达88.00%,阳性预测值达83.00%。但目前国内针对Fletcher分级后对GSTs不同侵袭危险性分级的EUS图像特点之间比较的研究较少。王晓凡等[8]曾将38例GSTs患者的EUS图像依据EUS侵袭危险性评分标准进行分级,并与术后病理分级结果进行比较,符合率约79.00%,但该研究中度侵袭危险性分级及高度侵袭危险性分级病例较少,结果准确性仍需进一步验证。本研究收集分析了已开展EUS检查的温州市3大医院经确诊的286例GSTs EUS图像发现:GSTs侵袭危险性越高,溃疡越好发,内部回声不均匀及钙化现象越常见,而进一步多因素分析显示,溃疡的发生是唯一预测胃GSTs侵袭危险性分级的独立因素(P<0.05),结果与国外学者研究发现基本一致[9]。但本研究有如下局限性:①EUS对病灶的回声强度,均匀性判断无具体量化值,存在经验论、主观性强的缺点[10],故本研究交由本院两位操作经验丰富的主任医师进行图像共同分析并取得一致,以尽量减少该误差;②本研究属回顾分析类研究,选择性偏移不可避免,为尽量减少此类偏移,本研究收集大量的外院病例。
综上所述,EUS对术前GSTs侵袭危险性的评估有一定的价值,不同侵袭危险性GSTs在EUS图像的表现有所差异,除肿瘤大小、核分裂象外,表面溃疡的发生同样是预测GSTs侵袭危险性的重要标志,这将有助于内镜医师在术前综合判断GSTs侵袭危险性。
致谢:特别感谢周羽翙在生病期间仍给予本课题的支持及帮助。
参考文献:
[1] Miettinen M,Sobin LH,Lasota J.Gastrointestinal stromal tumors of the stomach: a clinicopathologic,immunohistochemical,and molecular genetic study of 1765 cases with long-term follow-up[J].Am J Surg Pathol,2005,29(1): 52-68.
[2] Fletcher CD,Berman JJ,Corless C,et al.Diagnosis of gastrointestinal stromal tumors: a consensus approach [J].Int J Surg Pathol,2002,10(2): 81-89.
[3] Miettinen M,Furlong M,Sarlomo-Rikala M,et al.Gastrointestinal stromal tumors,intramural leiomyomas,and leiomyosarcomas in the rectum and anus: a clinicopathologic,immunohistochemical,and molecular genetic study of 144 cases[J].Am J Surg Pathol,2001,25(9): 1121-1133.
[4] Kim IH,Kwak SG,Chae HD.Prognostic factors of patients with gastric gastrointestinal stromal tumor after curative resection: a retrospective analysis of 406 consecutive cases in a multicenter study[J].Eur Surq Res,2015,55(1-2): 12-23.
[5]刘锦涛,余细球,侯华军,等.超声内镜对内镜治疗消化道隆起性病变的指导价值[J].中国内镜杂志,2008,14(3): 243-245.
[6] Shah P,Gao F,Edmundowicz SA,et al.Predicting malignant potential of gastrointestinal stromal tumors using endoscopic ultrasound[J].Dig Dis Sci,2009,54(6): 1265-1269.
[7] Palazzo L,Landi B,Cellier C,et al.Endosonographic features predictive of benign and malignant gastrointestinal stromal cell tumours[J].Gut,2000,46(1): 89-92.
[8]王晓凡,谭诗云,李明,等.术前超声内镜检查对胃间质瘤危险性判断及治疗方式选择分析[J].中华全科医师杂志,2014,13(6): 452-456.
[9] Joensuu H.Risk stratification of patients diagnosed with gastrointestinal stromal tumor[J].Hum Pathol,2008,39(10): 1411-1419.
[10] Hoteya S,Lizuka T,Kikuehi D,et al.Benefits of endoscopic submucosal dissection according to size and location of gastric neoplasm,compared with conventional mucosal resection[J].J Gastroenteral Hepatol,2009,24(6): 1102-1106.
(曾文军编辑)
Comparison of endoscopic ultrasonography image characteristics and analysis of risk factors for different invasive risk of gastric stromal tumors*
Guang-rong Lu1,Yu-hui Zhou1,Jin-wei Zhong1,Jian-wei Jin2,Mei Fu3,Chen Yu3,Zhi-ming Huang4,Zhan-xiong Xue1
(1.Department of Gastroenterology,the Second Affiliated Hospital,Wenzhou Medical University,Wenzhou,Zhejiang 325000,China; 2.Department of Gastroenterology,Wenzhou Central Hospital,Wenzhou,Zhejiang 325000,China; 3.the First Clinical Medical College of Wenzhou Medical University,Wenzhou,Zhejiang 325000,China; 4.Department of Gastroenterology,the First Affiliated Hospital,Wenzhou Medical University,Wenzhou,Zhejiang 325000,China)
Abstract:Objective To find out different endoscopic ultrasonography image characteristics of different invasive risk of gastric stromal tumors.Method The data of 286 patients of gastric stromal tumors that diagnosed by pathology and immunohistochemistry from three hospitals in Wenzhou were investigated retrospectively.Gastric stromal tumors were divided into very low risk group,low risk group,intermediate risk group and high risk group according to tumor size and mitosis,compared of clinical data and endoscopic ultrasonography image characteristics for different invasive risk of gastric stromal tumors,looked for differences and analyzed related risk factors.Results About 286book=2,ebook=7patients of gastric stromal tumor,most of them have regular shapes (262/286),originating from stomach muscularis propria (219/286),and the lesions always showed up hypoechoic (254/286),homogeneous echo (212/286),clear border (264/286); partial of calcification (79/286),ulcers (75/286) as well as cystic degeneration (54/286).And 60 patients were divided into very low risk group (20.98 %),112 patients of low risk group (39.16 %),73 patients of intermediate risk group (25.52 %),41 patients of high risk group (14.34 %).Univariate analysis showed the performances of ulcer,heterogeneous echoes,calcification and cystic degeneration were more common in higher invasive risk groups; then multivariate analysis showed ulcer (= 2.44,95%CI: 1.36~3.18) was the unique independent risk factor to predicting invasive risk of gastric stromal tumors (P < 0.05).Conclusion The performance of ultrasound endoscopic image for different invasive risk of gastric stromal tumors was different; despite of tumor size and mitosis,ulcer was also prognostic significance of invasive risk of gastric stromal tumors.
Keywords:invasive risk; gastric stromal tumors; endoscopic ultrasound; risk factors
[通信作者]薛战雄,E-mail:luguangrong1987@163.com
*基金项目:温州市公益性科技计划项目(No:Y20140511);2015温州医科大学附属第二医院院内科研项目(No:2015-09:04)
收稿日期:2015-08-27
文章编号:1007-1989(2016)01-0001-04
DOI:10.3969/j.issn.1007-1989.2016.01.001
中图分类号:R735.2
文献标识码:A
