补肾疏肝方对神经性厌食大鼠下丘脑-垂体-卵巢轴的调控机制研究*
2016-02-26胡文晓
补肾疏肝方对神经性厌食大鼠下丘脑-垂体-卵巢轴的调控机制研究*
胡文晓
(泰安市妇幼保健院,山东泰安271000)
摘要:目的探讨补肾疏肝方对神经性厌食(anorexia nervosa, AN)应激模型大鼠下丘脑-垂体-卵巢轴(hypothalamus-pituitary-ovarian axis, HPOA)的调控机制。方法按照隔离、限食、束缚的方法建立AN大鼠应激模型,设立正常对照组(以下简称正常组)、模型组、安慰剂组和补肾疏肝方组(以下简称中药组),测定下丘脑多巴胺(dopamine, DA)、去甲肾上腺素(noradrenaline, NE)和5-羟色胺(5-hydroxytryptamine, 5-HT)。结果下丘脑DA水平:安慰剂组明显高于正常组(P<0.05),模型组高于正常组,中药组低于安慰剂组,但无统计学差异。下丘脑NE水平:正常组明显高于模型组和安慰剂组(P<0.05),中药组高于模型组和安慰剂组,但无统计学差异。下丘脑5-HT水平:各组之间无明显差异。结论补肾疏肝方可以调控AN应激模型大鼠的HPOA功能,可能是通过调控下丘脑DA、NE水平来实现的。
关键词:补肾疏肝方;神经性厌食;应激模型;下丘脑-垂体-卵巢轴
神经性厌食(anorexia nervosa, AN)是严重威胁女性青少年身心健康且伴有内分泌异常的心身疾病。常由于特殊的精神心理变态而导致进食量减少,进而造成严重的营养不良、体重减轻及下丘脑-垂体-卵巢轴(hypothalamus-pituitary-ovarian axis, HPOA)功能紊乱[1-2]。AN在治疗方面尚无理想的方法,补肾疏肝方临床治疗AN患者有较好的疗效。本研究应用AN大鼠应激模型,从神经内分泌方面探讨其可能的作用机制。
1 材料和方法
1.1 实验动物 第一批:雌性Wistar大鼠50只,体重约160~180 g。由第二军医大学实验动物中心提供,许可证号为SYXK(沪)2007-0003。动物饲养于12h/12h昼夜交替、室温(22±2)℃的环境中,自由摄食和饮水。在实验环境适应1周后,进行阴道脱落细胞涂片筛选,有连续两个以上正常动情周期的大鼠用于实验。其余则被淘汰。第二批:实验动物同第一批。
1.2 实验药物中药补肾疏肝方:由郁金、石菖蒲、枸杞子、桑椹、牡丹皮、炒山栀等组成,第二军医大学附属长海医院中药房提供;自制成浓度相当于生药2.63 g/ml的溶液。
1.3 AN大鼠应激模型的制作 参考Shimizu N[3]的方法。
1.3.1 隔离和限食实验大鼠放在各自的笼子里相互隔离,17:30将饲料和水移除,20:00再给予饲料和水。7天后开始计算大鼠每天的饮食重量,20:00给予提前称重的饮食,次日17:30移除饮食同时称重,计算出饮食重量,待饮食重量固定不变后进行下一步实验。
1.3.2 束缚Shimizu N采用“固定板”束缚,即用细绳、胶带将大鼠束缚在固定板上,实验操作中发现这种束缚方式的实施非常困难,难以保证大鼠每日束缚2个小时的实验要求。调整束缚方式,将大鼠装入自制固定器中,每日17:30~19:30持续束缚2个小时。(自制固定器为一自制塑料瓶,大小切合大鼠身体,以大鼠被束缚不能移动为度,前后有通气孔,避免大鼠因窒息死亡。)
1.4 动物分组与给药方法 第一批:实验大鼠按照随机数字表法进行随机分组,分为正常对照组(以下简称正常组)、模型组、安慰剂组和补肾疏肝方组(以下简称中药组),每组10只。药物剂量换算按照动物与人体表面积比换算法:人用药剂量(mg/kg)=0.16×大鼠用药剂量(mg/kg),换算相应剂量。从实验造模第一天开始,正常组按10 ml/kg体重灌服生理盐水,不予其它处理;模型组按上述造模方法建立AN应激模型,不予灌胃;安慰剂组在造模的同时按10 ml/kg体重灌服生理盐水;中药组在造模的同时按10 ml/kg体重灌服补肾疏肝方水煎浓缩剂。每日早、晚各1次,持续整个实验过程。实验过程中,正常组大鼠意外死亡1只,安慰剂组和中药组因灌胃各死亡1只。第二批:动物分组和给药同第一批,中药组因灌胃死亡1只。
1.5标本采集 约灌胃第35天时、于动情间期进行标本采集。下丘脑采集:在冰台上迅速取出下丘脑,放入液氮固化,滤纸拭干后称重,放入玻璃匀浆管,用预冷的0.106 mol/L高氯酸1 ml匀浆2 min,静置2 h,4℃ 4000 r/min离心30 min 2次,取上清液,置于-80℃低温冰箱中保存待测。
1.6 指标测定用酶联免疫法测定下丘脑多巴胺(dopamine, DA)、去甲肾上腺素(noradrenaline, NE)和5-羟色胺(5-hydroxytryptamine, 5-HT)。下丘脑DA、NE和5-HT试剂盒由上海端纳生物科技有限公司提供。

2 结果
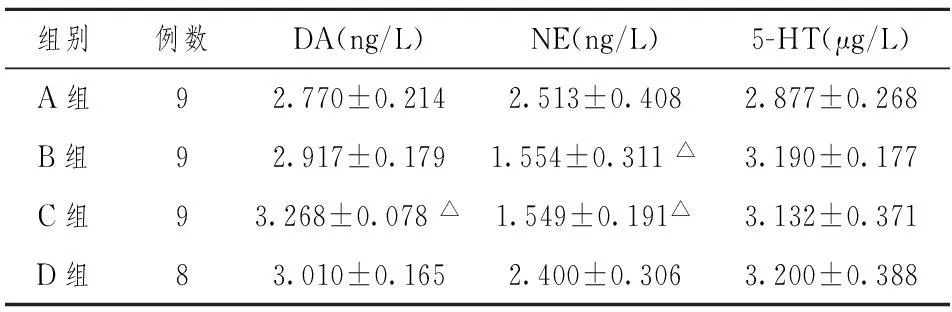
各组大鼠下丘脑DA、NE和5-HT水平 下丘脑DA水平:安慰剂组明显高于正常组(P<0.05),模型组高于正常组,中药组低于安慰剂组,但无统计学差异。下丘脑NE水平:正常组明显高于模型组和安慰剂组(P<0.05),中药组高于模型组和安慰剂组,但无统计学差异。下丘脑5-HT水平:各组之间无明显差异。见表1。

组别例数DA(ng/L)NE(ng/L)5-HT(μg/L)A组92.770±0.2142.513±0.4082.877±0.268B组92.917±0.1791.554±0.311△3.190±0.177C组93.268±0.078△1.549±0.191△3.132±0.371D组83.010±0.1652.400±0.3063.200±0.388
注:与A组比较,△P<0.05。A组:正常组,B组:模型组,C组:安慰剂组,D组:中药组。
3 讨论
中医古代文献中没有“神经性厌食”的病名,现代实验研究也未见中医中药对该病的相关研究报道。根据AN患者的临床表现,可以归属于“闭经”、“虚劳”等范畴。中医理论认为,肝气郁结、疏泄失常是导致AN发生的主要因素,肾虚和肝郁是本病的核心病机。在此理论指导下创立的补肾疏肝方,临床应用取得了较好疗效。本课题应用AN的大鼠应激模型来探讨补肾疏肝方对HPOA的调控机制。
文献报道AN应激动物模型的下丘脑单胺类神经递质(如DA、NE、5-HT)水平发生变化,但其变化的机制尚不明确,甚至不同应激模型的变化趋势也不一样[4]。
我们的研究结果表明,模型组大鼠的下丘脑DA和5-HT高于正常组,但无统计学差异;下丘脑NE明显低于正常大鼠。由此可见,补肾疏肝方可以调控AN应激模型大鼠的HPOA功能,可能是通过调控下丘脑DA、NE水平来实现的,具体有待于大样本证实。目前中医药治疗AN的相关研究国内外尚属空白,本课题初步探讨了补肾疏肝方对AN的HPOA可能的调控机制,其调控途径还有待于深入研究。
参考文献:
[1]赵朋,毛富强,李振涛.神经性厌食症的临床特点及精神科干预对策[J].国际中华神经精神医学杂志, 2005, 6(3):208.
[2]吕朝晖,窦京涛,陆菊明.神经性厌食患者内分泌功能的改变[J]. 临床内科杂志, 2002, 19(6): 449-450.
[3]Shimizu N, Oomura Y, Kai Y. Stress-induced anorexia in rats mediated by serotonergic mechanisms in the hypothalamus[J]. Physiol Behav, 1989, 46(5), 835-841.
[4]Siegfried Z, Berry EM, Hao S, et al. Animal models in the investigation of anorexia[J]. Physiol Behav, 2003, 79(1): 39-45.
收稿日期(2015-10-08)
doi:10.3969/j.issn.1004-7115.2016.01.024
中图分类号:R741.02
文献标识码:B
文章编号:1004-7115(2016)01-0065-02
作者简介:*胡文晓(1986-),女,山东宁阳人,主治医师,硕士研究生,主要从事中医妇科临床工作。
