IMRT与3D-CRT治疗胸部食管癌的剂量学评价*
2015-12-02刘锐锋张秋宁魏世鸿罗宏涛王小虎魏玺义甘肃省肿瘤医院放疗科兰州730050
刘锐锋,张秋宁,魏世鸿,罗宏涛,王小虎,魏玺义(甘肃省肿瘤医院放疗科,兰州730050)
三维适形放疗(3D-CRT)和调强放疗(IMRT)是目前食管癌放疗的两种主要技术,3D-CRT是利用三维治疗计划系统设计共面或非共面的不规则野进行分次照射,使高剂量区分布的形状在三维方向上与病变(靶区)的形状一致。IMRT不仅在照射方向上使照射野的形状与靶区的形状一致,且使靶区内及表面的剂量处处相等,让每个射野内诸点的输出剂量率能按要求的方式进行调整,使靶区得到更精确的放疗,正常组织得到更好的保护。其共同目的是使靶区获得高剂量的同时尽可能降低周围正常组织受量。
食管大部分位于胸部,毗邻肺、脊髓、心脏等重要脏器,且身体外轮廓曲线变化较大。如何能既充分地照射肿瘤靶区,又能保护肺和心脏,长期以来是胸段食管癌放疗的难点。而IMRT技术的出现,从理论上解决了上述难题。按照解剖部位不同,胸段食管可分为上、中、下三段。由于其淋巴引流有各自的特点,放疗靶区勾画有各自不同的区域。既往研究中,张武哲等[1]对比了胸上段食管癌3D-CRT与IMRT的剂量学结果,认为调强放疗较适形放疗有更好的剂量适形性,可更有效地保护脊髓,并显著降低肺10Gy以上的受照射体积。为了进一步探讨IMRT在不同部位食管癌放疗中的应用价值,我们对不同部位的胸段食管癌进行IMRT和3D-CRT剂量学对比分析,为IMRT的临床应用提供参考。
1 资料与方法
1.1 一般资料
选择2013年4月至2013年10月在我院行根治性放疗的胸段食管癌30例进行研究,其中男性21例,女性9例,所有患者均为首次接受放疗。其中胸上段11例,中段13例,下段6例。食管病灶长度为 3.8~10.5cm[中位 7.1cm,平均(6.8 ± 3.0)cm]。其中Ⅱ期患者6例,主要因高龄或存在手术禁忌症而行根治性放疗。所有患者均于瓦里安E-clipse治疗计划系统进行计划设计,在实际治疗中采用3D-CRT计划,同时每例患者再设计一个5野IMRT计划进行对比分析,依据DVH图进行剂量学比较。入组患者一般临床特征见表1。
1.2 定位
患者取仰卧位,双臂上举交叉握固定杆,体膜固定,使用我院东芝CT模拟定位机进行扫描。层厚及层间距均为5mm,扫描范围从下颌角水平至肝下缘,包括整个病灶及双侧颈部、锁骨上区及双肺。重建影像后通过DICOM 3.0传输到Ecelipse计划系统进行靶区勾画和计划制定。

表1 患者一般临床特征Table 1 The clinical characters of included patients
1.3 靶区及危及器官勾画
靶区勾画按照不同部位食管癌的靶区勾画原则进行。大体肿瘤区(gross tumor volume,GTV)包括食管肿瘤病灶和食管旁纵隔肿大淋巴结。临床肿瘤区(clinical tumor volume,CTV)为GTV上下扩3cm,四周外扩0.8cm,包括纵隔相应淋巴引流区。上段:锁骨上淋巴结引流区、食管旁、2区、4区、5区、7区淋巴引流区。中段:食管旁、2区、4区、5区、7区淋巴引流区。下段:食管旁、4区、5区、7区和胃左、贲门周围的淋巴引流区[2]。计划靶区(planing target volume,PTV)在CTV基础上均匀外扩5mm。由于适形计划为该患者治疗的实际计划,在GTV外扩5mm为PGTV进行后段GTV补量。危及器官主要勾画双肺、脊髓、心脏,下段病变时勾画肝脏。
1.4 3D-CRT计划设计
所有计划均为实际治疗采用的计划,根据病灶不同采用不同的3-4野加楔形板组合。计划均分两段执行。第一段主要给PTV给量照射,第二段缩小至PGTV加量照射。处方剂量归一至PGTV中心,计划PGTV 66Gy,分33次,PTV 50Gy分25次。
1.5 IMRT计划设计
用Ecelipse治疗计划系统逆向调强模块进行计划设计,采用均匀间隔5野,机架角度为 0°、72°、144°、216°、288°。危及器官剂量限制:脊髓 <40Gy,脊髓计划区 <45Gy,肺 V20≤30%、V30≤20%;用其约束条件进行IMRT优化。用 PTV平均剂量归一处方剂量,靶区目标:PTVmean51Gy,分30次,单次剂量1.7Gy;GTV 66Gy,分30次,单次剂量2.2Gy。
1.6 计划评价指标
肿瘤靶区指标主要评价CTV和GTV的平均剂量;危及器官受量指标主要包括:脊髓最大受照剂量(SPmax);心脏30Gy和40Gy剂量的体积(V30、V40);5Gy、10Gy、20Gy和30Gy剂量的肺体积比例(V5、V10、V20、V30);双肺平均剂量(MLD)。
1.7 统计学处理
所有观察指标包括剂量绝对值、相对比值和体积百分比,各项指标结果统计学处理用SPSS 16.0软件进行,比较两组间的差异采用配对样本t检验,比较不同段之间的差异采用独立样本t检验,显著性检验水平设为0.05。
2 结果
2.1 两种技术的靶区剂量学指标比较
IMRT与3D-CRT相比,GTVmean(cGy)分别为6 784±64和6 832±88,两种技术差异无统计学意义(P=0.48);而CTVmean(cGy)分别为5 921 ±256和6 255±289,两者之间差异有统计学意义(P=0.000),IMRT低于3D-CRT;两肺受照射的平均剂量(cGy)、V30百分体积、V20百分体积、心脏 V40百分体积、V30百分体积、脊髓最大剂量,两者之间差异均有统计学意义,IMRT明显低于3DCRT;双肺V10 百分体积分别为 43.8 ±4.8 和 42.0 ±11.4,两者之间差异无统计学意义(P=0.232);双肺V5百分体积分别为60.9 ±19.2 和53.9 ±12.8,两者之间差异有统计学意义(P=0.004),IMRT高于3D-CRT(见表2)。
2.2 胸上段与中下段的靶区剂量学指标比较
胸上段病变与中下段病变相比,GTVmean(cGy)分别为6 797±54和6 776±69,CTVmean(cGy)分别为5 866±233和5 951±267,两者之间差异均无统计学意义(p值分别为0.396和0.389);两肺受照射的平均剂量(cGy)、V30百分体积、V20百分体积、V10百分体积、V5百分体积、心脏V40百分体积、V30百分体积、脊髓最大剂量,两者之间差异均有统计学意义,P值均小于0.05,上段病变明显低于中下段病变(见表3)。
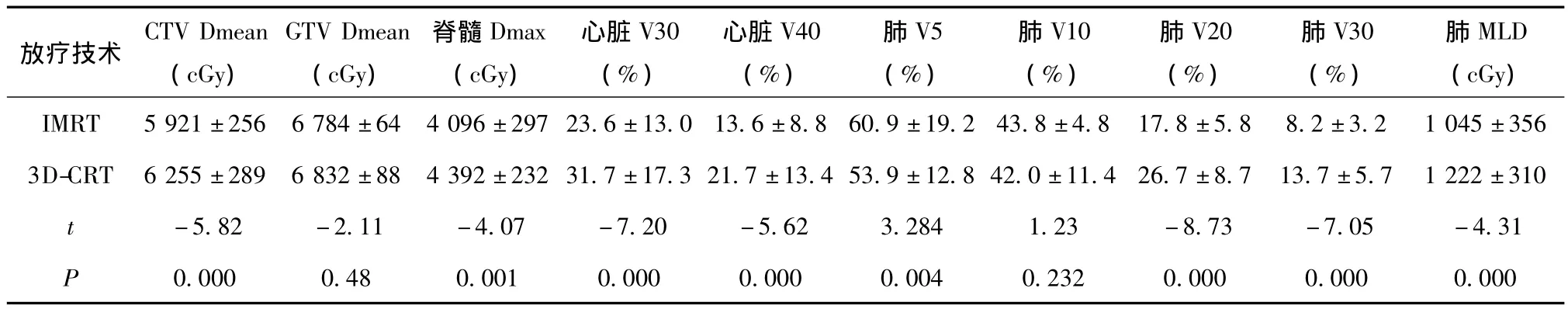
表2 IMRT与CRT肿瘤靶区及危及器官的剂量分布参数比较结果Table 2 Comparison of dose distribution parameters for tumor target volume and OAR between CRT and IMRT
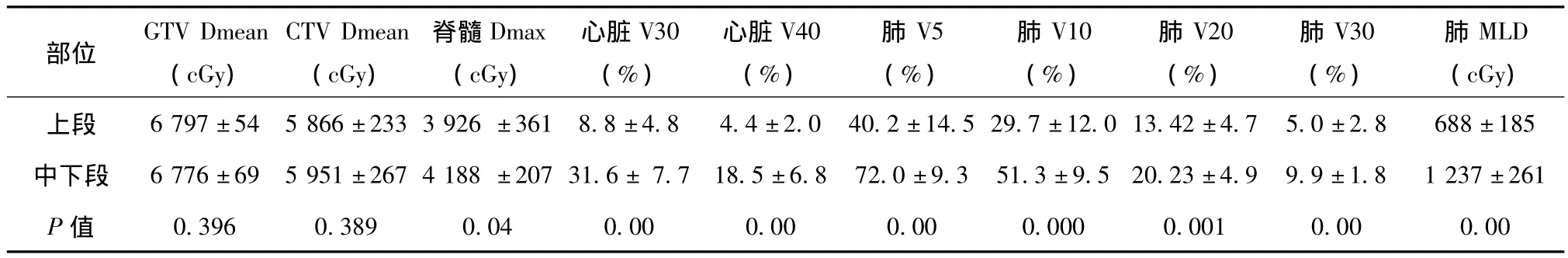
表3 胸上段与中下段病变IMRT肿瘤靶区及危及器官剂量参数的比较Table 3 Comparison of dose distribution parameters for tumor target volume and OAR between upper and middle-distal lesion
3 讨论
长期以来,食管癌放射治疗的总体5年生存率维持在10%~20%左右,而治疗失败的原因70%~80%是由于局部病灶未控和复发造成,而由于正常组织剂量限制导致的靶区剂量不足是制约食管癌放疗疗效的主要原因之一[3]。由于食管位置的特殊,其行程均靠近脊髓,毗邻心脏和肺,造成肿瘤靶区难以达到均匀的剂量分布,如何兼顾肿瘤的充分照射和脊髓、肺等正常组织的的有效保护是放射肿瘤学和放射物理学的主要研究课题。3D-CRT技术的应用较常规放疗明显改善了靶区的适形度,提高了肿瘤靶区的照射剂量,可以说解决了以上的部分难题[4-5]。IMRT技术的优点是适形度高,可以更有效地避开肿瘤邻近的正常组织,并且可同时对不同区域给出不同的放射剂量,IMRT的这些特点正适合用于食管癌的放射治疗,并有望改善食管癌患者预后。
胸上段病变由于其淋巴引流特点,其靶区应包括下颈锁上区及纵隔相应淋巴引流区,其解剖部位特殊,体表轮廓在颈胸交界处变化较大,食管更接近脊髓,既往常规照射和3D-CRT技术一般为“T”形野[6],辅以双侧水平野照射,以较好涵盖病灶和淋巴结区域,但由于胸上段食管距离体表的厚度差别大,淋巴结也深浅不一,范围可从皮下1.0cm至气管食管沟淋巴结5 cm以上[7],同时靶区周围有肺、软组织和肱骨头等组织造成的不均质性,从而造成剂量分布不均匀。但其治疗优势在于双下肺野可免于照射,因此调强放疗在此处会更好地发挥其技术优越性,在提高肿瘤靶区剂量、改善剂量均匀性的同时,更好地保护正常组织,特别是肺组织。既往有多项研究结果表明了胸上段食管癌进行调强放疗的剂量学优势[1,7-9]。杨林等[10]关于胸中段食管癌调强放疗剂量学的研究表明,在相同的野同等的剂量照射情况下,调强放疗对OAR的影响明显比常规3D-CRT放疗方式小。Chandra等[11]关于食管下段癌和贲门癌的结果表明,IMRT与3D-CRT治疗计划比较,V10下降10%,V20下降5%,肺平均剂量下降2.5Gy。在本研究中,我们首先比较了 IMRT与3D-CRT在胸段食管癌的剂量学差异,其结果基本与其他研究结果相一致,只是CTV平均剂量方面,IMRT明显低于3DCRT,这与IMRT同步加量的特点有关,而3D-CRT分段治疗中,GTV补量过程中仍有相当的剂量供应于CTV区域,这也可以解释IMRT能够在提高肿瘤靶区剂量、改善剂量均匀性的同时,更好地保护正常组织的原因。IMRT由于照射野数的增多,降低了双肺平均剂量和高剂量照射的体积,但增加了双肺低剂量照射的范围,特别是双肺V5较3D-CRT明显增高。虽然美国放射肿瘤学协作组(RTOG)[12]研究认为V20是唯一肺的放射性损伤的独立因子,当V20<20%时无放射性肺炎发生,但对于低剂量辐射导致的后果尚无明确结论,相关的研究正在进行中。Gopal等[13]的研究发现,13Gy的放射量就可导致肺功能的受损。在应用IMRT时,我们不仅要关注剂量体积,更应关注双肺平均剂量及低剂量范围,在随访中密切关注其长期疗效和毒副反应。另外我们还比较了胸上段病变与中下段病变IMRT的剂量学差异,结果表明胸上段病变的正常组织受量均低于中下段病变,这与其解剖部位及照射范围有关,在临床实际工作中,对于胸上段病变应更加强烈推荐采用IMRT技术。
在临床疗效方面,由于调强放疗开展时间较短,尚无长期生存及正常组织远期毒副反应方面的报道,就其近期疗效而言,王军等[14]的研究结果表明其1、2 年肿瘤局部控制率分别为 72.9%、72.9%;1、2 年总生存率分别为 80.9%、67.4%;1、2 年无瘤生存率分别为73.5%、51.4%。急性和晚期放射性肺损伤发生率较低。治疗失败的主要原因仍为肿瘤局部未控和复发。调强放疗与常规放疗相比,局部控制和生存稍有优势,而2级以上放射性肺损伤明显减少。王文高等[15]和朱海文等[16]的研究均报道调强放疗与常规放疗相比,局部控制和生存稍有优势,而2级以上放射性肺损伤明显减少。虽然一些研究显示调强放射治疗食管癌具有较好的初期治疗效果,严重影响患者生活质量的2级及以上晚期放射性肺损伤发生率较低,患者耐受性较好,但以上研究均为小组病例,且为回顾性结果,随访时间较短,结果尚缺乏说服力,能否提高长期生存率,有待于设计严谨的临床多中心前瞻性随机对照试验来进一步验证。在治疗失败的病例中,局部失败仍是治疗失败的主要原因,说明肿瘤的局部未控和复发仍是挑战食管癌放射治疗疗效的一个难题。但如何能够把调强放疗在剂量学方面的优势真正转化为患者的临床获益,应在IMRT技术的基础上,结合同期化疗、分子靶向治疗等综合治疗手段进一步研究。
综上所述,IMRT对胸段食管癌是一种合理、可靠的治疗技术,可最大程度提高靶区剂量的均匀性,而降低OAR受量,特别是胸上段病变,具有更大的剂量学优势。但能否提高远期生存率有待于设计严谨的大样本多中心前瞻性随机临床研究来进一步验证。
[1] 张武哲,陈志坚,李德锐,等.胸上段食管癌调强放疗与适形放疗计划的剂量学比较[J].癌症,2009,28(11):1127-1131.
[2] 殷蔚伯,余子豪,徐国镇,等.肿瘤放射治疗学[M].第4版.北京:中国协和医科大学出版社,2008:558-559.
[3] 陈尔成,刘孟忠,胡永红,等.食管癌同期放化疗后局部失败相关因素分析[J].癌症,2005,24(4):498-501.
[4] 刘 慧,曾智帆,崔念基,等.颈段和胸上段食管照射野设计的探讨[J].中华放射肿瘤学杂志,2006,15(4):286-289.
[5] 王 澜,韩 春,祝淑钗,等.食管癌常规照射与三维适形放疗的剂量学研究[J].中华放射瘤学杂志,2006,15(3):176-180.
[6] 许素玲,王巨武,王海峰,等.颈段胸上段食管癌T形野三种照射技术的剂量学比较[J].中国医学物理学杂志,2008,25(5):781-784.
[7] 钱普东,陆进成,梅泽如,等.食管癌术后锁骨上野放疗与食管气管沟淋巴结转移关系探讨[J].中华放射肿瘤学杂志,2007,14(5):401-403.
[8] 张 莉,罗 辉.中上段食管癌3D-CRT与IMRT肺损伤剂量学的对比研究[J].南昌大学学报(医学版),2011,51(2):52-57.
[9] 童 涛,杜 伟,罗海峰,等.颈段和胸上段食管癌常规照射、三维适形放疗与调强放疗的剂量学研究[J].山东医药,2010,50(1):47-48.
[10]杨 林,洪 浩,唐 虹,等.中段食管癌常规放疗与三维适形、调强放疗对危及器官影响的比较[J].安徽医科大学学报,2009,44(6):729-731.
[11] Chandra A,Guerrero T,Liu H,et al.IMRT reduces lung radiation in distal esophageal cancer over 3D-CRT[J].Int J Rdiat Oncol Biol Phys,2003,57(Supp 12):S384-385.
[12] Graham MV,Purdy JA,Emami B,et al.Clinial dose-volume histogram ananlysis for pnumonitis after 3D treatment for nonsmall cell lung cancer(NSCLC)[J].Int J Radiat Oncol Biol Phys,1995,33(1):65-75.
[13] Gopal R,Tucker SL,Komaki R,et al.The relationship between local dose and loss of function for irradiated lung[J].Int J Radiat Oncol Biol Phys,2003,56(1):106-113.
[14]王 军,韩 春,李晓宁,等.食管癌调施放射治疗初期疗效分析[J].癌症,2009,11:1138-1142.
[15]王文高,闫爱云,王 琍,等.胸上段颈段食管鳞癌调强放疗疗效观察[J].安徽医学,2009,30(11):1318-1320.
[16]朱海文,陈龙云,王汉华,等.调强放射治疗食管癌的近期疗效观察[J].中外医疗,2008,36(12):41.
