多指标综合评价优选葶苈生脉方中丹参、红花提取工艺△
2015-09-25史红星张华潭张静宜李春花
史红星,张华潭,张静宜,李春花
(1.衡水市中医医院,河北 衡水 053000;2.河北医科大学 研究生学院,河北 石家庄 050017;3.河北中医学院 药剂教研室,河北 石家庄 050091)
·中药工业·
多指标综合评价优选葶苈生脉方中丹参、红花提取工艺△
史红星1,张华潭2,张静宜2,李春花3*
(1.衡水市中医医院,河北 衡水 053000;2.河北医科大学 研究生学院,河北 石家庄 050017;3.河北中医学院 药剂教研室,河北 石家庄 050091)
目的:优选葶苈生脉方中丹参、红花的提取工艺。方法:以丹参酮I、丹参酮ⅡA、隐丹参酮、羟基红花黄色素A为综合评价指标,通过正交试验设计考察乙醇浓度、料液比、提取次数和提取时间对提取工艺的影响;采用高效液相色谱法测定4种成分的含量。结果:最优提取工艺为加10倍量60%乙醇超声提取4次,每次50 min。结论:优选的提取工艺稳定、可行。
丹参;红花;提取工艺;正交试验;丹参酮I;丹参酮ⅡA;隐丹参酮;羟基红花黄色素
葶苈生脉方由葶苈子、丹参、红花、红参、黄芪等组成,是全国名老中医邢月朋治疗气虚血瘀、阳虚水停型充血性心力衰竭(CHF)的经验方。经临床验证能有效缓解症状,改善生活质量,减少住院时间。“邢月朋益气活血、温阳利水法”治疗慢性心力衰竭诊疗方案被列为国家“十一五”科技支撑计划项目。方中丹参与红花所含成分不稳定,长时间受热易分解[1-2],为将葶苈生脉方开发为现代制剂,笔者探索适于方中丹参、红花工业生产的工艺参数。药理实验证明,丹参酮Ⅰ、丹参酮ⅡA、隐丹参酮、羟基红花黄色素A可使冠脉血流量明显增加,显著改善缺氧动物的氧分压和血氧饱和度,降低血粘度,抑制凝血和血栓形成,防止和减轻缺氧心肌超微结构的变化,对缺氧心肌有保护作用[3-5]。而在煎煮过程中这些成分很难保留,为保证药物疗效,本试验采用L9(34)正交试验法,以HPLC测定丹参酮Ⅰ、丹参酮ⅡA、隐丹参酮、羟基红花黄色素A含量为综合评价指标,优选出丹参、红花的最佳超声波提取工艺,为实际生产和临床应用提供参考。
1 仪器与试药
1.1仪器
LC-15C高效液相色谱仪、SIL-10AF自动进样系统、SPD-15C紫外检测器(日本岛津公司);RE-52型旋转蒸发仪(上海亚荣生化仪器厂);Mill-Q超纯水处理系统(MilliporeBedford,MA,美国);TG328B型分析天平(上海精科仪器厂);KQ-100E型超声波清洗器(昆山市超声仪器有限公司)。
1.2药材与试剂
丹参(SalviamiltiorrhizaBge.)、红花(CarthamustinctoriusL.)购于石家庄乐仁堂,经河北中医学院侯芳洁讲师鉴定,符合《中华人民共和国药典》2010版一部相关项下规定;丹参酮I、丹参酮ⅡA、隐丹参酮对照品(中国食品药品检定研究院,批号分别为110867-200406,110766-200518,110852-200806);羟基红花黄色素A对照品(成都曼思特生物科技有限公司,批号:MUST-13121913);甲醇(色谱纯,批号:A2005-0001,美国 Grace公司);乙腈(色谱纯,批号:TEN7949768,美国Grace公司)。
2 方法与结果
2.1丹参酮I、丹参酮ⅡA、隐丹参酮含量测定
2.1.1 色谱条件 色谱柱:Diamonsil C18(200 mm×4.6 mm,5 μm);流动相:甲醇-水(82∶18);流速:1.0 mL·min-1;检测波长:270 nm;柱温:室温;进样量:10 μL。见图1~2[6-8]。
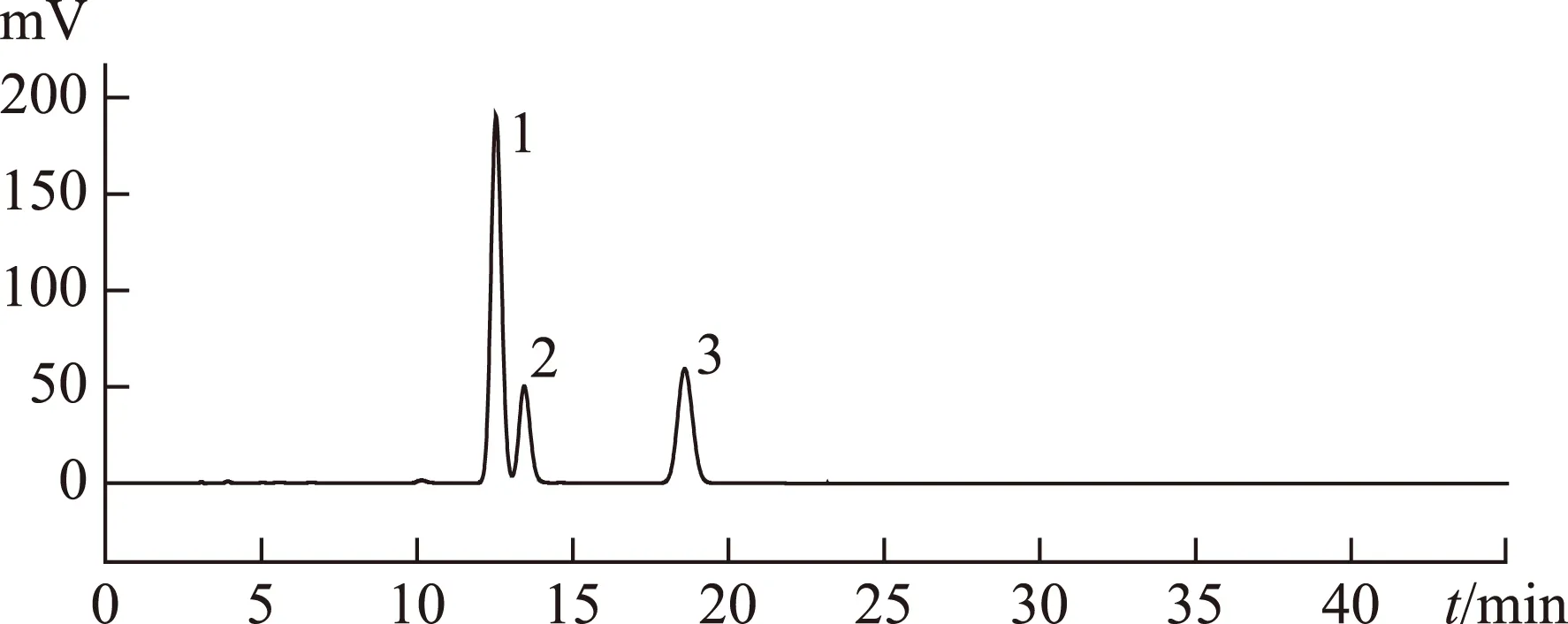
注:1.隐丹参酮;2.丹参酮I;3.丹参酮ⅡA。下同。图1 混合对照品高效液相色谱图
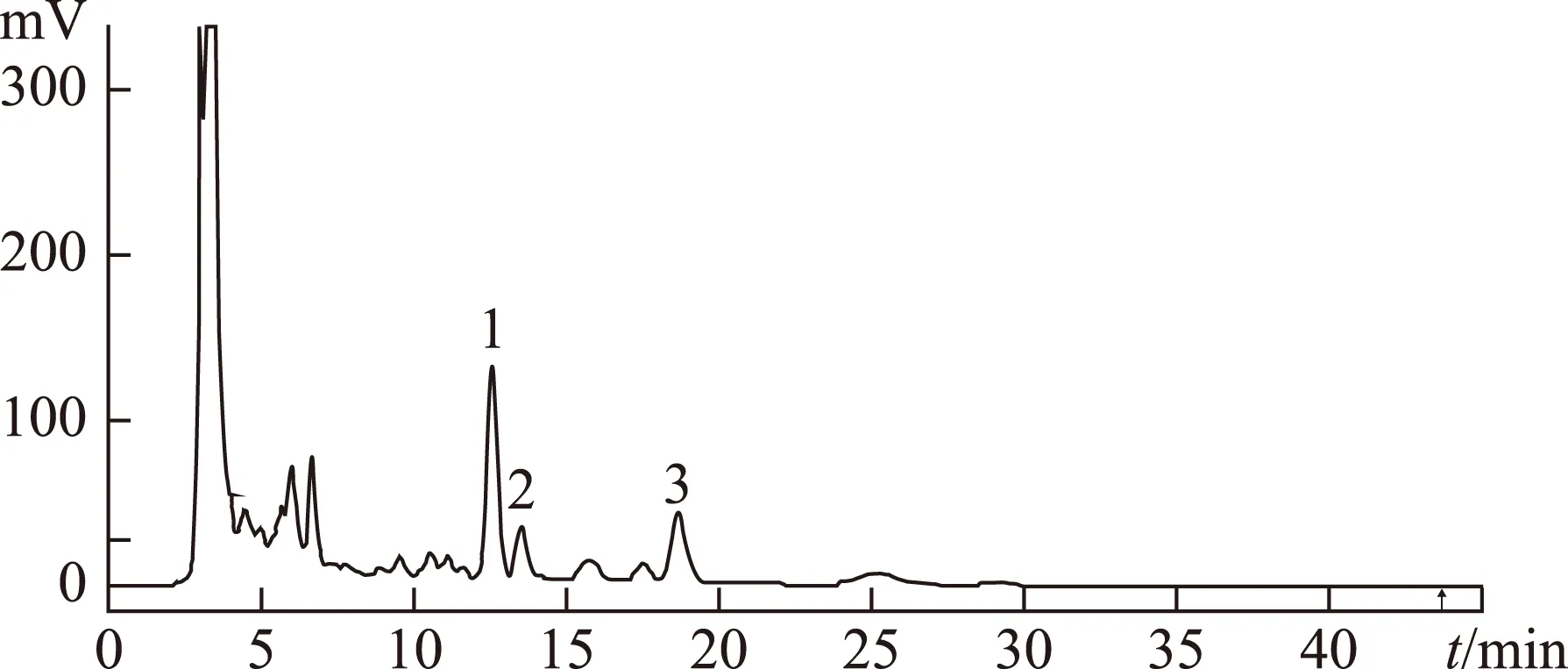
图2 样品高效液相色谱图
2.1.2 对照品溶液制备 取经五氧化二磷减压干燥的丹参酮I、丹参酮ⅡA、隐丹参酮适量,精密称定,置于25 mL棕色容量瓶中,加甲醇溶解并定容,于4 ℃冰箱中避光保存。丹参酮I、丹参酮ⅡA、隐丹参酮质量浓度分别为30.24、34.8、61.06 μg·mL-1。
2.1.3 供试品溶液制备 按处方比例称取1/2处方量的丹参、红花各7.5、6 g,加入15倍量50%甲醇,超声(电功率为100 W,频率为40 KHZ)提取2次,每次40 min,合并提取液。精密量取提取液适量,减压回收溶剂至近干,用甲醇溶解并定容于10 mL容量瓶中,即得供试品溶液。
2.1.4 方法学考察 1)标准曲线:取对照品溶液,按2.1.1色谱条件分别进样5、8、10、15、18、20、25 μL,记录峰面积,以峰面积积分值为纵坐标(Y),进样量(X,μg)为横坐标,进行线性回归,得线性回归方程,见表1。结果表明,在相应线性范围内,丹参酮I、丹参酮ⅡA、隐丹参酮进样量与峰面积呈良好线性关系;2)精密度试验:丹参酮I、丹参酮ⅡA、隐丹参酮峰面积的RSD分别为0.40%、0.37%、0.40%(n=6),表明仪器精密度良好;3)稳定性试验:供试品中丹参酮I、丹参酮ⅡA、隐丹参酮峰面积的RSD分别为1.68%、1.67%、0.40%(n=6),结果表明供试品溶液在24 h内稳定性较好;4)重复性试验:丹参酮I、丹参酮ⅡA、隐丹参酮含量的RSD分别为1.53%、1.75%、1.04%(n=6),表明方法重复性良好;5)加样回收率试验:精密吸取已知含量的供试品溶液9份于5 mL容量瓶中,3份为一组,加入混合对照品溶液1.06、1.33、1.60 mL,甲醇定容,测定,计算丹参酮I、丹参酮ⅡA、隐丹参酮平均加样回收率分别为97.17%、101.40%、99.22%,RSD分别为1.43%、1.54%、1.42%(n=9)。
2.2羟基红花黄色素A含量测定
2.2.1色谱条件 色谱柱:Diamonsil C18(200mm×4.6mm,5μm),流动相:乙腈-0.1%磷酸(12∶88);流速:1.0mL·min-1;检测波长:403nm;柱温:室温;进样量:10μL。见图3~4。
2.2.2对照品溶液制备 取羟基红花黄色素A适量,精密称定,置于25mL棕色容量瓶中,加25%甲醇溶解并定容,于4℃冰箱中避光保存。羟基红花黄色素A质量浓度为111.20μg·mL-1。
2.2.3供试品溶液制备 按处方比例称取1/2处方量的丹参、红花各7.5、6g,加入10倍量50%甲醇,超声(电功率为100W,频率为40KHZ)提取3次,每次30min,合并提取液,精密量取提取液适量,减压回收溶剂至近干,用25%甲醇溶解并定容于10mL容量瓶中,即得供试品溶液。

表1 标准曲线的制备结果(n=7)
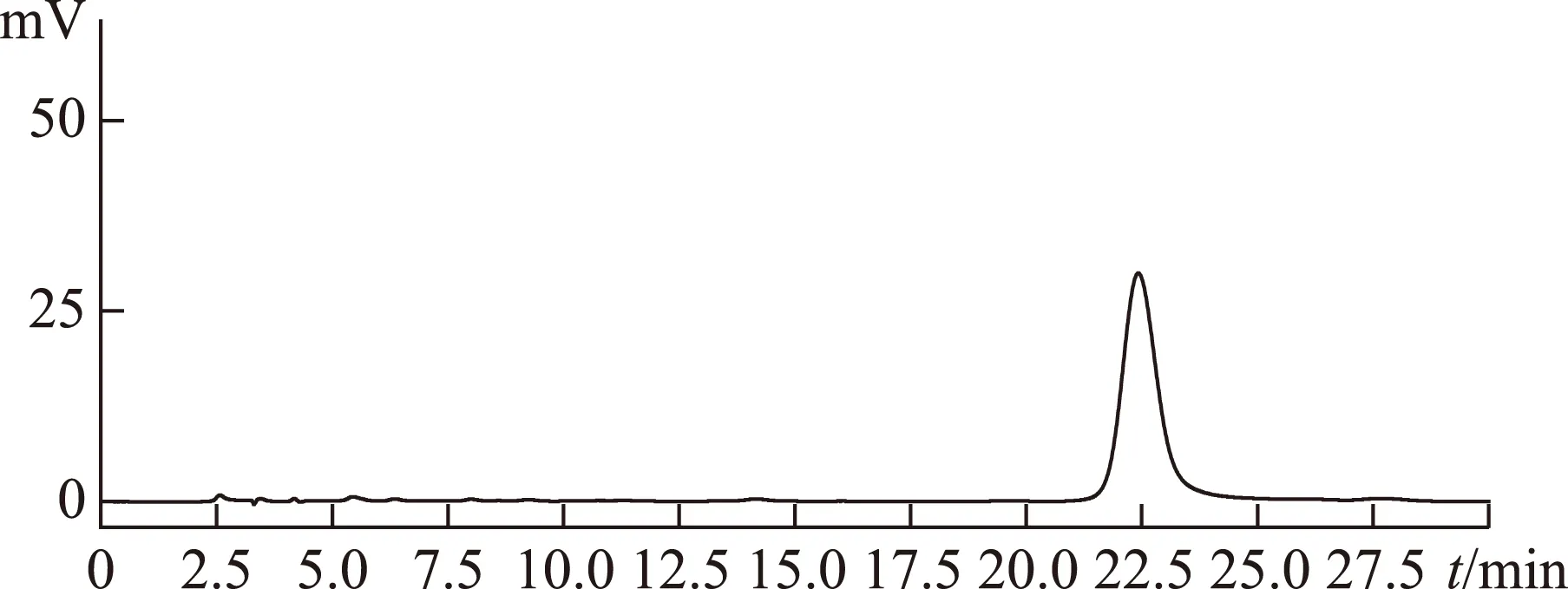
图3 羟基红花黄色素A高效液相色谱图
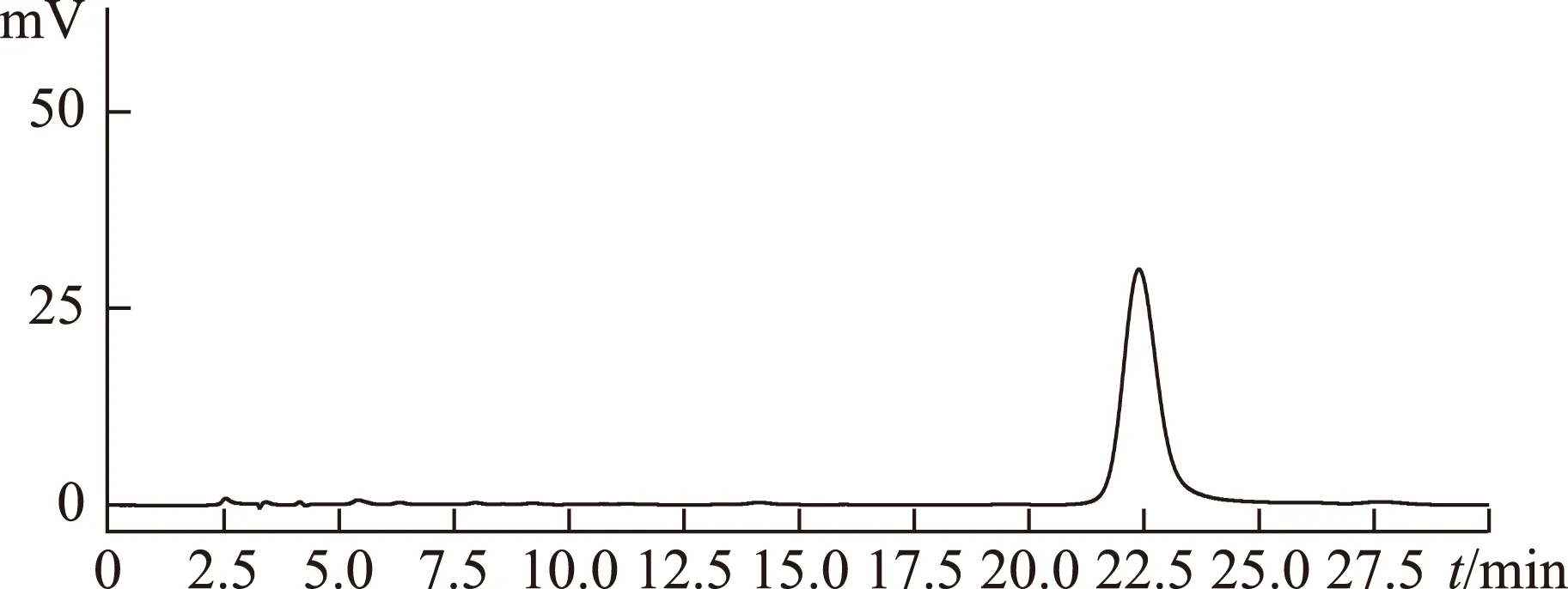
图4 样品高效液相色谱图
2.2.4 方法学考察 1)标准曲线:取2.2.2对照品溶液,按2.2.1色谱条件分别进样2、5、8、10、15、18、20 μL,记录峰面积,以峰面积积分值为纵坐标(Y),进样量(X,μg)为横坐标,进行线性回归,得线性回归方程:Y=984 785.340 3X-34 569.875 4(r=0.999 7)。结果表明,在0.222 4~2.224 0 μg,羟基红花黄色素A进样量与峰面积呈良好线性关系;2)精密度试验:羟基红花黄色素A峰面积的RSD为1.45%(n=6),表明仪器精密度良好;3)稳定性试验:供试品中羟基红花黄色素A峰面积的RSD为0.55%(n=6),结果表明,供试品溶液在24 h内稳定性较好;4)重复性试验:羟基红花黄色素A含量的RSD为2.57%(n=6),表明方法重复性良好;5)加样回收率试验:精密吸取已知含量的供试品溶液9份,3份为一组,于10 mL容量瓶中,加入对照品溶液1.20、1.50,1.80 mL,25%甲醇定容,测定,计算羟基红花黄色素A平均加样回收率为101.62%,RSD为1.50%(n=9)。
2.3正交试验优选丹参、红花提取工艺
2.3.1 正交试验设计与结果 在预试验基础上,选定乙醇浓度(A)、乙醇用量(B)、提取次数(C)、提取时间(D)为主要影响因素,以丹参酮I、丹参酮ⅡA、隐丹参酮、羟基红花黄色素A为综合评价指标,综合评分[12]=(丹参酮I含量/最大丹参酮I含量+丹参酮ⅡA含量/最大丹参酮ⅡA含量+隐丹参酮含量/最大隐丹参酮含量)×25+羟基红花黄色素A含量/最大羟基红花黄色素A含量×75。采用L9(34)安排正交试验。提取工艺的因素与水平见表2,正交试验直观分析结果见表3,方差分析结果见表4[9-11]。
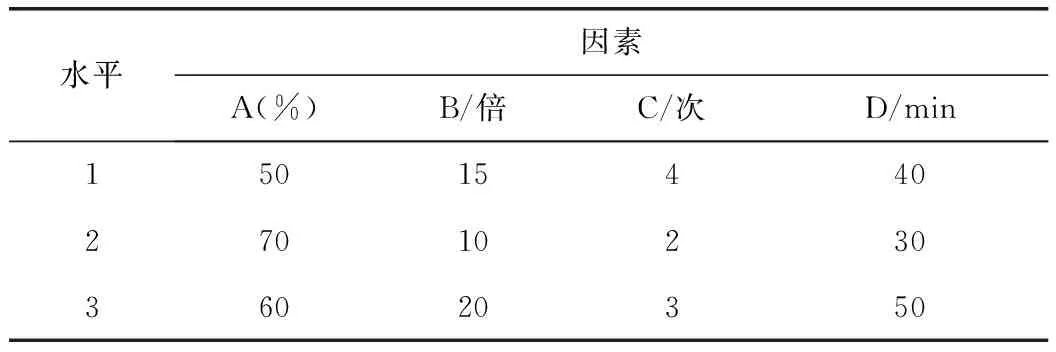
表2 提取工艺因素水平表
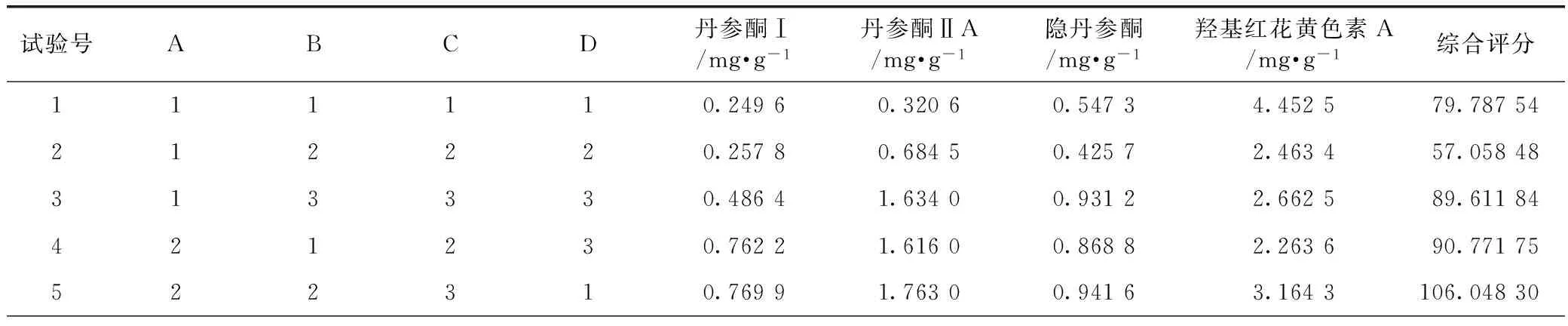
表3 提取工艺的正交试验结果
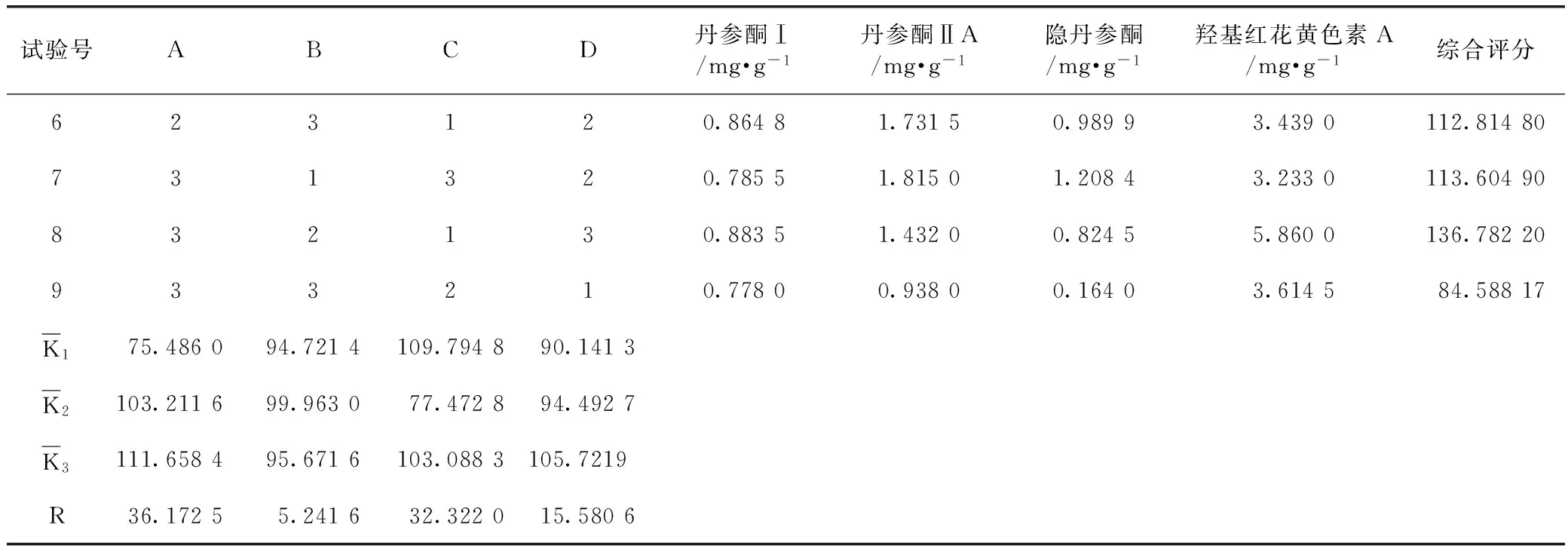
表3(续)
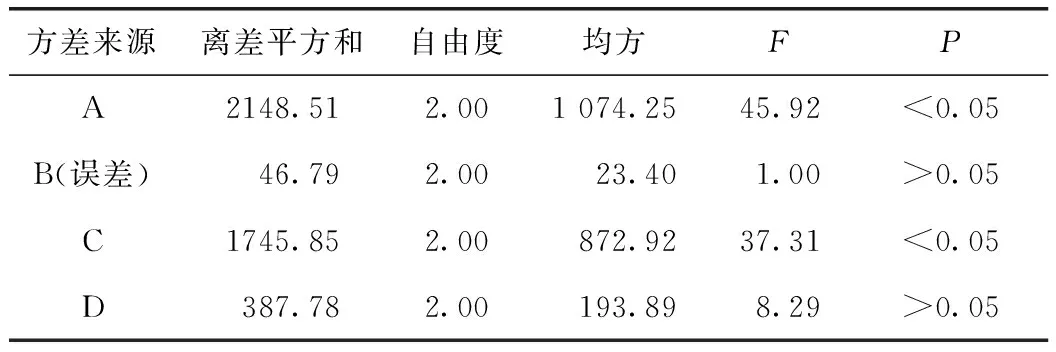
表4 提取工艺的方差分析结果
注:F0.05(2,2)=19。
由表4直观分析可知,各因素对提取效率影响大小为A>C>D>B。由方差分析结果可知,乙醇浓度和提取次数对提取效果的影响具有统计学意义。结合正交试验结果最佳提取工艺为A3B2C1D3,即加10倍量60%乙醇超声提取4次,每次50 min。考虑到试验效率并结合试验结果,确定每次提取时间为40 min。
2.3.2 最优提取工艺验证试验 按处方规定量称取丹参、红花药材,共3份,依据确定的最优工艺参数进行验证试验,结果丹参酮I、丹参酮ⅡA、隐丹参酮、羟基红花黄色素A的平均质量分数分别为0.91、1.42、0.84、6.13 mg·g-1,RSD分别为1.65%、2.10%、2.31%、1.96%。结果表明优选的工艺稳定、可行。
3 讨论
为将葶苈生脉口服液开发为新药,“葶苈生脉口服液研究与开发”被列入2015年度河北省科技支撑计划项目。方中丹参、红花、川芎活血祛瘀,丹参中的丹参酮ⅡA等对光、热均较敏感,其溶液在光照、高温条件下易分解[13];红花中的羟基红花黄色素A是红花活血化瘀有效成分,由于羟基红花黄色素A为热不稳定物质,在常压沸腾状况下随着时间的延长不断分解[14]。因此,本研究采用超声波提取,可以很好地控制提取过程中温度、光照对不稳定物质的影响。
丹参、红花中的药效成分性质相同,我们采用高效液相色谱法测定丹参中丹参酮I、丹参酮ⅡA、隐丹参酮与红花中羟基红花黄色素A含量,为平衡各指标对工艺优化的影响,使丹参与红花成分含量在综合评分中所占比例相同,最终确定综合评价指标为(丹参酮I含量/最大丹参酮I含量+丹参酮ⅡA含量/最大丹参酮ⅡA含量+隐丹参酮含量/最大隐丹参酮含量)×25+羟基红花黄色素A含量/最大羟基红花黄色素A含量×75[12],旨在筛选更合理的提取工艺参数。
[1] 林恒标,林恒宽.丹参酮IIA的稳定性研究[J].中医研究,2005,18(8):16-16.
[2] 姚苗苗,董仲才,任爱农.羟基红花黄色素A的研究进展[J].中南药学,2009,7(12):931-934.
[3] 许继文,付春梅.丹参的药理作用研究进展[J].医学综述,2006,12(23):1467-1469.
[4] 付辛芳,刘晓红.丹参的药理作用与临床应用研究进展[J].中国药业,2006,15(1):76-77.
[5] 朴永哲,金鸣.红花抗心肌缺血研究进展[J].中草药,2001,32(5):473-475.
[6] 汤瑶,李佐刚,王秀文,等.超高效液相色谱法同时测定丹参酮提取物中隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA[J].药物分析杂志,2014,34(5):813-818.
[7] 闫豫君,杨广德,贺浪冲.RP-HPLC法同时测定丹参中丹参酮ⅡA和隐丹参酮的含量[J].中草药,2002,33(4):363-365.
[8] 姚苗苗,任爱农,董仲才.RP-HPLC法同时测定红花中羟基红花黄色素A与红花黄色素A的含量[J].药物分析杂志,2010,30(2):263-265.
[9] 郁晓艺,刘红,李炳奇,等.均匀设计优化红花黄色素提取工艺[J].时珍国医国药,2005,16(5):391-392.
[10] 贲永光,丘泰球,李坤平,等.正交试验法优选双频复合超声提取丹参的工艺研究[J].中药材,2009,32(5):802-804.
[11] 张华潭,郑文丽,魏艳婷,等.大孔树脂纯化黄蜀葵花总黄酮的工艺优选[J].中国实验方剂学杂志,2015,21(1):28-31.
[12] 陈卓瀚,张慧,陆海玲,等.正交试验优选复方广金钱草颗粒的提取工艺[J].中国实验方剂学杂志,2014,20(20):43-47.
[13] 金文淑,张炜煜.丹参有效部位的提取工艺优选[J].中国实验方剂学杂志,2013,19(3):33-36.
[14] 王若菁,杨滨.红花的化学成分及质量标准研究进展[J].中国实验方剂学杂志,2007,13(5):65-68.
Multi-indexEvaluationofIntegrationTechniqueforExtractingofSalviamiltiorrhizaandCarthamustinctoriusfromTingliShengmaidecoction
SHIHongxing1,ZHANGHuatan2,ZHANGJingyi2,LIChunhua3*
(1.HengshuiHospitalofTraditionalChineseMedicine,Hengshui053000,China;2.Past-graduateSchool,HebeiMedicalUniversity,Shijiazhuang050017,China;3.Dept.ofTCM,HebeiUniversityofChineseMedicine,Shijiazhuang050091,China)
Objective:To optimize an integration technique for extracting ofSalviamiltiorrhizaandCarthamustinctoriusfrom Tingli Shengmai decoction.Methods:With composite score of contents of tanshinone I,tanshinone ⅡA,cryptotanshinone and hydroxyl safflower yellow A as index,orthogonal test was adopted to optimize extraction technology by taking the concentration of ethanol solid-liquid ratio extraction times and extraction time as factors.Contents of tanshinone I,tanshinone ⅡA,cryptotanshinone and hydroxyl safflower yellow A were determined by HPLC.Results:The optimal extraction process is thatSalviawas added with 10 times ethanol of 60% and extracted 50 minutes for 4 times.Conclusion:These optimized extraction processes are stable,feasible and suitable for industrial production of Tingli Shengmai decoction.
Salviae Miltiorrhizae Radix et Rhizoma;CarthamustinctoriusL.;extracting technology;orthogonal design;tanshinone I;tanshinone ⅡA;cryptotanshinone;hydroxyl safflower yellow A
河北省科技支撑计划项目(15272701D)
*
李春花,教授,研究方向:中药制剂新技术、新方法;E-mail:13803369966@163.com
10.13313/j.issn.1673-4890.2015.12.022
2015-07-12)
