碳点-荧光桃红荧光共振能量转移体系在铜离子检测中的应用研究
2015-04-27陶慧林廖秀芬徐铭泽王海洋易忠胜覃宏伟
陶慧林,孙 超,廖秀芬,徐铭泽,王海洋,易忠胜,覃宏伟
(桂林理工大学 化学与生物工程学院,广西 桂林 541004)
碳点-荧光桃红荧光共振能量转移体系在铜离子检测中的应用研究
陶慧林*,孙 超,廖秀芬,徐铭泽,王海洋,易忠胜,覃宏伟
(桂林理工大学 化学与生物工程学院,广西 桂林 541004)
在pH 8.4的溶液中,碳量子点(Carbon quantum dots,CQDs) 和荧光桃红(Fluorescent pink,FP)之间发生荧光共振而使后者的荧光增强。体系中加入痕量Cu2+后,FP的荧光被猝灭,且在一定范围内体系的荧光猝灭程度与Cu2+浓度呈良好的线性关系。据此建立了荧光猝灭法测定河水、农田水、自来水中痕量Cu2+的新方法。方法的线性范围为9.42~23.55 μmol/L,检出限(3σ/k)为3.14 μmol/L。将该方法应用于河水、农田水及自来水中Cu2+的检测,其相对标准偏差(RSD) 不大于0.91%,加标回收率为98.7%~99.0%,结果令人满意。
碳量子点;荧光桃红;荧光共振能量转移;痕量Cu2+
铜是一种重要的工业原料,因具有优良的机械性能、良好的可塑性等被广泛用于冶金、地质、环境、化工、材料科学等领域。铜也是人体必需的微量元素之一,广泛参与多种酶的代谢活动,且是30多种酶的活性成分,是人体必需的微量元素之一,具有造血、影响铁代谢、强壮骨骼、软化血管、增强防御机能等功能。铜在人体内(尤其是心脏中)主要以含铜蛋白酶和血浆细胞素形式存在,影响造血过程,促进铁的吸收和利用,加速细胞成熟。人体缺铜将引起心脏增大,血管变弱,主动脉弹性组织变性,导致动脉病变,引起胆固醇增高,导致冠心病发生等。因此,建立高灵敏度测定微量或痕量Cu2+的方法具有重要意义。目前对于Cu2+的测定主要有火焰原子吸收光谱法[1]、催化动力学法[2]、电化学法[3-5]、流动注射分析法[6]、联用技术[7-9]、荧光分析法[10-13]等。如王尚芝等[1]使用火焰原子吸收光谱法测定小米中铜的含量,先使用浊点萃取进行一步预处理后检测,该方法的检出限为1.1 ng/mL,但需要复杂的预处理。朱庆仁等[2]使用催化动力学法检测面粉和大米中的痕量铜,该方法的检出限为8.0×10-12g/mL,然而检测时间超过1 d,无法进行快速检测。代仕均等[6]应用流动注射分析法成功地检测了几种地表水中的痕量铜,方法的检出限良好,然而线性范围窄。
荧光共振能量转移(Fluorescence resonance energy transfer,FRET) 技术由于灵敏度高、方法简单,在分析检测方面得到了广泛应用[14]。碳量子点(CQDs)是一种新型的纳米材料,具有发光性质稳定、荧光寿命长等特点,且与其他的荧光材料相比具有更好的生物安全性,是一种优良的光学材料,在分析检测中具有良好的应用前景。目前已广泛应用于无机离子、生物和药物分析等领域[15-16]。而将具有优良光学性质的CQDs应用于FRET体系中鲜有报道。本实验以CQDs作为能量给体,荧光桃红(FP)作为能量受体,构建新型的能量转移体系,Cu2+能够使体系中FP的荧光发生猝灭,在最佳实验条件下,FP的荧光猝灭值与Cu2+的加入量在一定范围内呈良好的线性关系,从而建立了测定痕量Cu2+的新方法。所建立的方法具有灵敏度高、仪器简便、操作简单等特点,能较好地克服现有方法中存在的一些缺陷。
1 实验部分
1.1 仪器与试剂
RF-5301PC荧光光度计(日本岛津公司),TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限公司),电子分析天平FA1104(中国江苏泰兴市电子仪器厂),pHS-3C精密pH计(上海雷磁仪器厂);荧光桃红(国际集团试剂有限公司):直接用二次水配成1.0×10-4mol/L荧光桃红储备液,2 mg/mL Cu2+标准贮备液(南京效率科技有限公司),pH 8.4的水溶液(用NaOH调节pH值),以上所用试剂均为分析纯,实验用水为二次蒸馏水。
1.2 碳量子点的合成
水溶性碳量子点的制备:根据文献[17]的方法稍作修改,将0.2 g柠檬酸钠、1.5 g碳酸氢铵和10 mL水加入聚四氟乙烯衬里的高温反应釜中,密封后置于180 ℃烘箱中水热处理4 h,自然冷却至室温后,转移到50 mL容量瓶中,用水稀释至刻度,摇匀,置于4 ℃冰箱中避光保存。
1.3 实验方法
在一系列10 mL比色管中依次加入一定量的CQDs,FP和Cu2+,用pH 8.4的水溶液定容至刻度,并于30 ℃恒温反应6 min后,在λex=300 nm处测定相应的荧光强度IF。仪器的激发和发射狭缝宽度均为5 nm。
2 结果与讨论
2.1 CQDs的光学性质
用透射电镜分析了CQDs的分布情况,由图1A的透射电镜图可知,CQDs粒径分布较均匀,多分布在2.0~3.0 nm 之间。CQDs的紫外吸收光谱和荧光光谱见图1B,由图1B可知其最大吸收峰在352 nm,荧光发射峰为432 nm。CQDs的量子产率可采用参比法计算获得:Φu=(Φs×Fu×As)/(Fs×Au)。其中Φu,Φs为待测物质和参比物质的荧光量子产率;Fu,Fs为待测物质和参比物质的积分荧光强度;Au,As为待测物质和参比物质在该激发波长的入射光的吸光度(A=εbc)。参照文献[18],以0.05 mol/L H2SO4介质中的硫酸奎宁(荧光量子产率0.55)为参比,测得CQDs的量子产率为0.67。以上结果表明本实验所获得的CQDs具有粒径小、分布均匀、量子产率较高、峰形窄(半峰宽为76 nm)且对称等特点。
2.2 碳量子点-荧光桃红荧光共振能量转移体系的构建
给体的发射光谱和受体的吸收光谱有一定程度上的重叠是分子间发生能量转移的必要条件之一。CQDs的荧光光谱和FP的吸收光谱见图2。由图2可知CQDs的荧光峰在432 nm处(曲线a),FP的紫外吸收峰在535 nm处(曲线b),二者间有较好的光谱重叠,这为发生能量转移提供了前提条件。其中CQDs为能量给体,FP为能量受体。

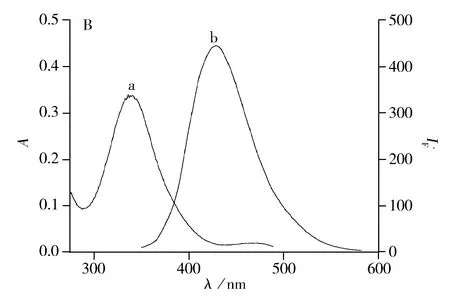
图1 CQDs的透射电镜(A)及吸收光谱和荧光光谱(B)
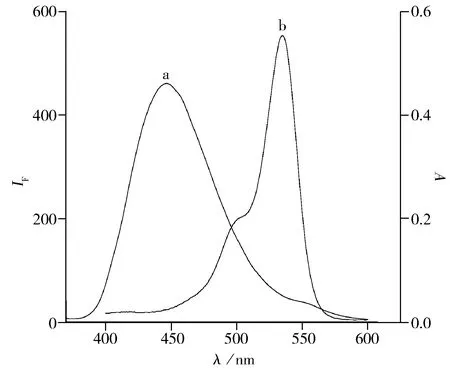
图2 CQDs的荧光光谱(a)及 FP的吸收光谱(b)
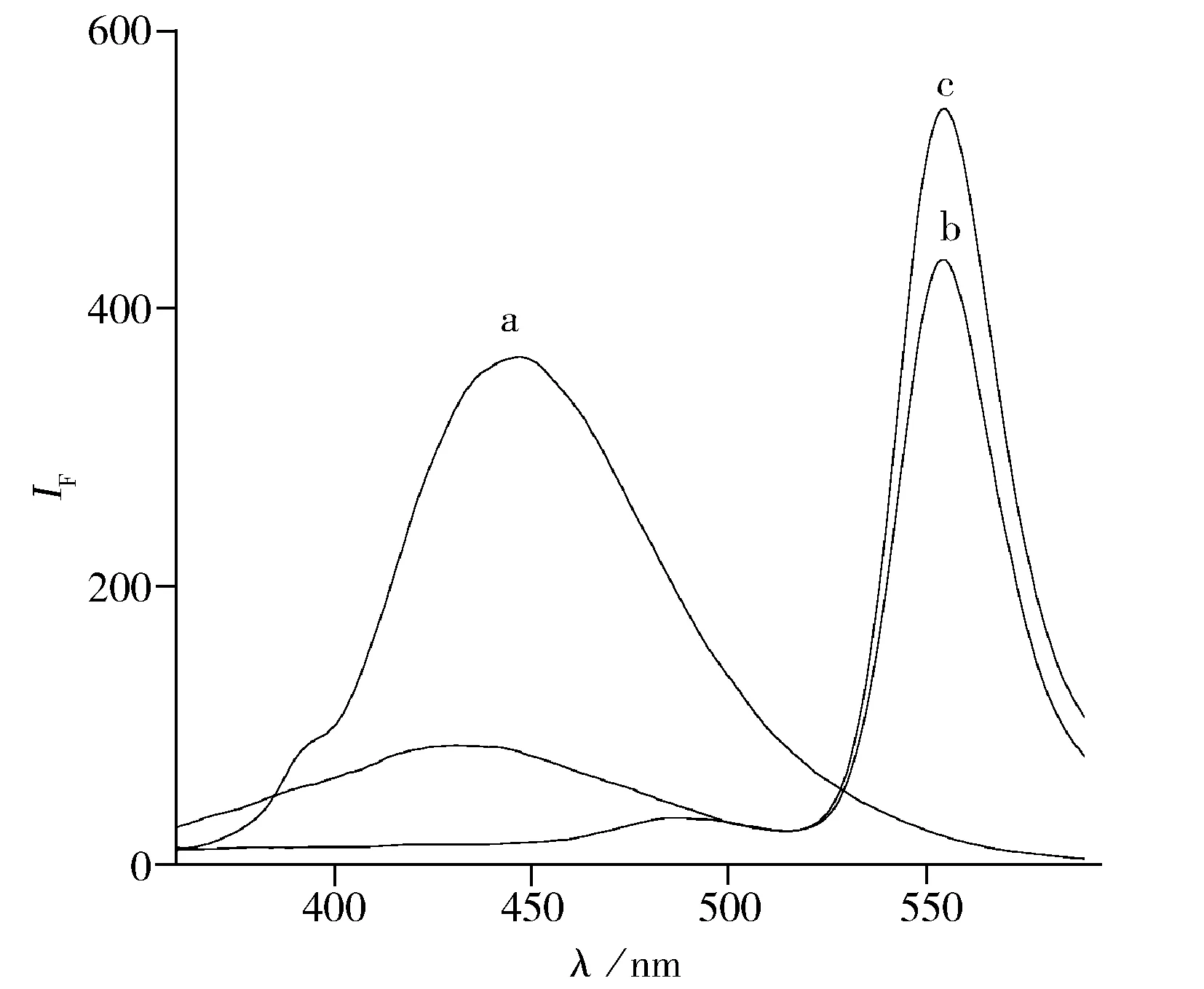
图3 CQDs(a),FP(b)和CQDs-FP (c)的荧光发射光谱
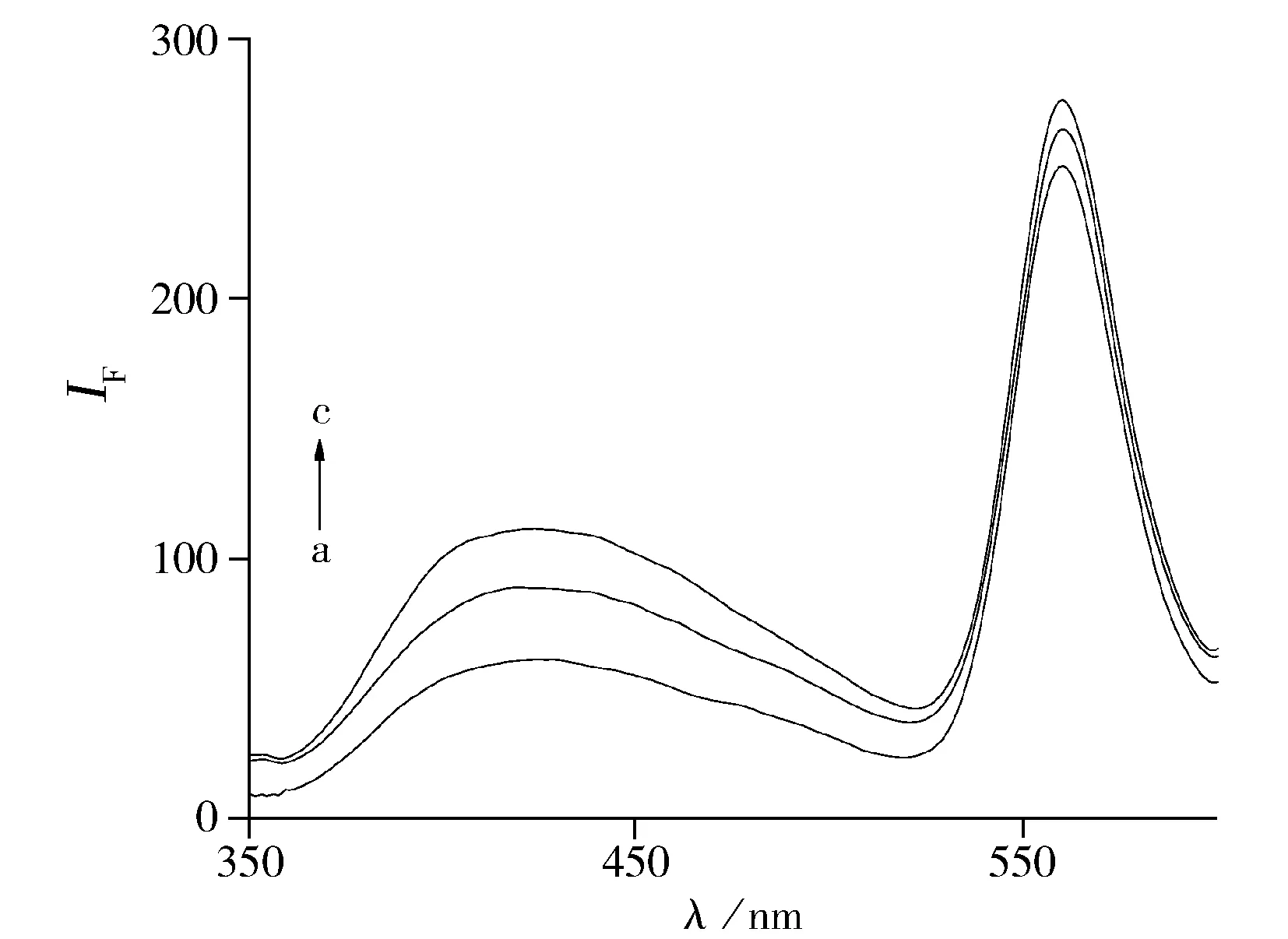
图4 CQDs浓度对CQDs-FP间能量转移的影响

图5 FP浓度对CQDs-FP间能量间转移的影响
为了确保能量转移的效果,选用CQDs吸收较弱的端部波长300 nm来激发混合体系,既可以保证FP有较大的吸收,同时CQDs又不会被激发。如图3所示,给体和受体混合后,给体CQDs发生明显的荧光猝灭,FP的荧光增强,证明CQDs-FP之间发生了荧光共振能量转移现象,CQDs-FP体系的荧光能量转移效率与二者的浓度有着密切联系。为找出给、受体间的最佳配比,实验探究了CQDs与FP的不同体积比对体系的影响。按“1.3”实验方法固定FP的加入量为1.67×10-6mol/L,改变CQDs的加入量,测定二者不同配比时相应的荧光强度IF。由图4可知,随着CQDs浓度的增大,更多的给体将能量转移给FP,使FP荧光强度逐渐增强。而图5表明,当固定供体CQDs浓度不变时,随FP浓度的增大,CQDs的荧光逐渐猝灭,FP的荧光增强,从而进一步说明CQDs-FP之间发生了有效的能量转移。由图5可知,当体系中CQDs 与FP的浓度分别为4.64×10-5mol/L和1.67×10-6mol/L 时,混合体系中给体的荧光峰猝灭最大,而受体的荧光峰升高最多,即此时获得最佳的能量转移效率。
2.3 相关参数的计算
根据能量转移Förster理论,能量转移效率E、能量转移临界距离R0、给体与受体之间的能量转移距离r满足如下关系:
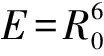
(1)
E=1-F/F0
(2)
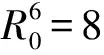
(3)
(4)
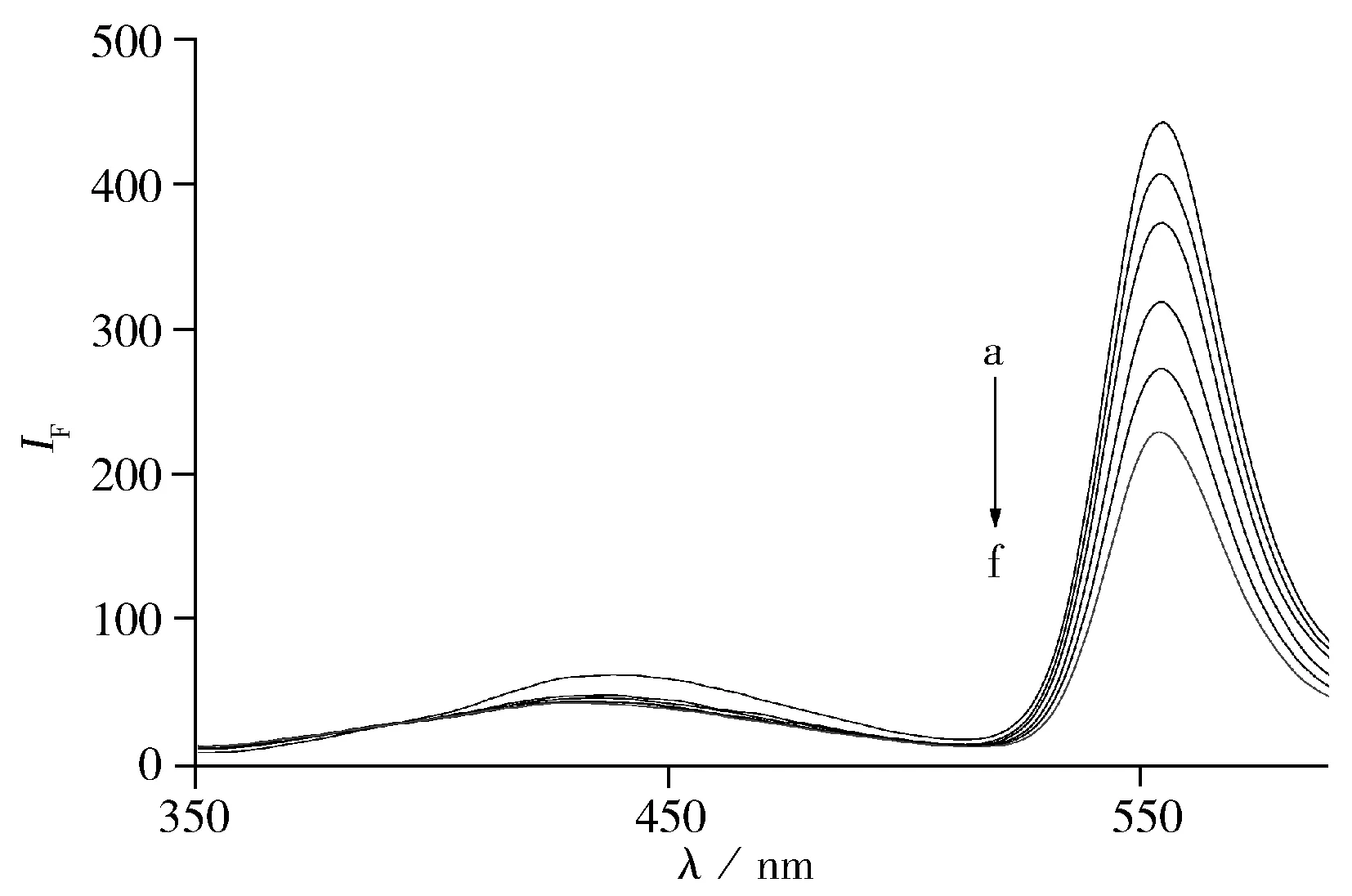
图6 Cu2+对CQDs-FP间能量转移的影响
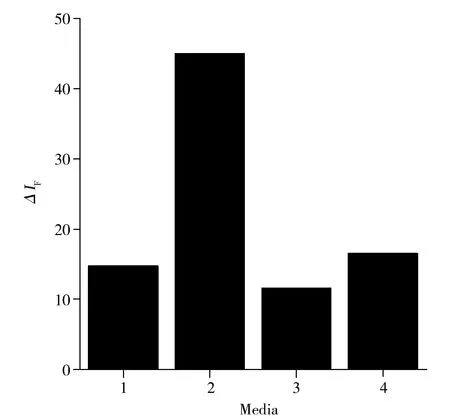
图7 不同介质对体系荧光猝灭的影响
F(λ)为波长λ处荧光给体的荧光强度,ε(λ)为波长λ处受体的摩尔吸光系数,F为加入能量受体后给体的荧光强度;F0为未加入受体时给体的荧光强度;k2为偶极空间取向因子,能量给体和受体的空间分布可认为是随机且均等的,因此取k2=2/3;N为水和有机溶剂的平均折射率(取1.37);J为给体的荧光发射光谱与受体的吸收光谱之间的光谱重叠积分。通过以上公式计算得到E=0.76,J=5.12×10-12cm3·L·mol-1,R0=9.02 nm,r=7.44 nm,结果表明R0和r均小于10 nm,说明CQDs和FP之间能够发生荧光共振能量转移。
2.4 Cu2+对体系的荧光猝灭作用
按照实验方法考察了Cu2+对CQDs-FP能量转移体系的影响。如图6所示,随着Cu2+的加入,体系的荧光强度不断被猝灭。在一定范围内,体系的荧光猝灭程度与Cu2+用量呈良好的线性关系。基于此,建立了测定Cu2+的新方法。
2.5 实验条件的优化
在不同酸度中,CQDs具有不同的形态,因此酸度对其荧光性质有较大影响。实验考察了不同酸度对CQDs-FP-Cu2+体系的影响,结果表明在pH 6.8~9.0范围内,Cu2+对体系的荧光猝灭均有影响,而在pH 8.4时体系的荧光猝灭达到最大,因此实验选择pH 8.4作为最佳酸度。并且分别考察了巴比妥钠-HCl,Tris-HCl,硼酸-硼砂缓冲溶液以及pH 8.4的水溶液(用NaOH调节pH值)所构建体系的荧光猝灭情况,结果如图7所示。由图7可知在pH 8.4的水溶液中,体系的荧光猝灭达到最大,故选择用pH 8.4的水溶液定容。
此外还对反应时间、温度等条件的影响进行考察。结果表明,在pH 8.4的水溶液中,体系在30 ℃下反应6 min可达稳定,并且可稳定1 h左右。
2.6 工作曲线
在最佳条件下,考察了不同浓度Cu2+对体系荧光猝灭强度的影响。结果表明,Cu2+浓度在9.42~23.55 μmol/L范围内与体系荧光猝灭程度呈良好的线性关系:y=0.108 2x-0.581 8(其中y为lg(F0/F);x为Cu2+的浓度,mol/L),相关系数(r)为0.993 1。根据IUPAC规定,检出限(DL)用3σ/k计算(其中σ为测定11次空白溶液的标准偏差,k为工作曲线的斜率),测得方法的DL为3.14 μmol/L。
2.7 干扰实验
当Cu2+浓度为11 μmol/L时,在最优实验条件下考察了部分共存物质对实验体系的影响,结果如表1所示。当控制相对误差在±5%以内时,水中常见金属离子和阴离子对体系基本无影响,说明体系对Cu2+具有较高的选择性。
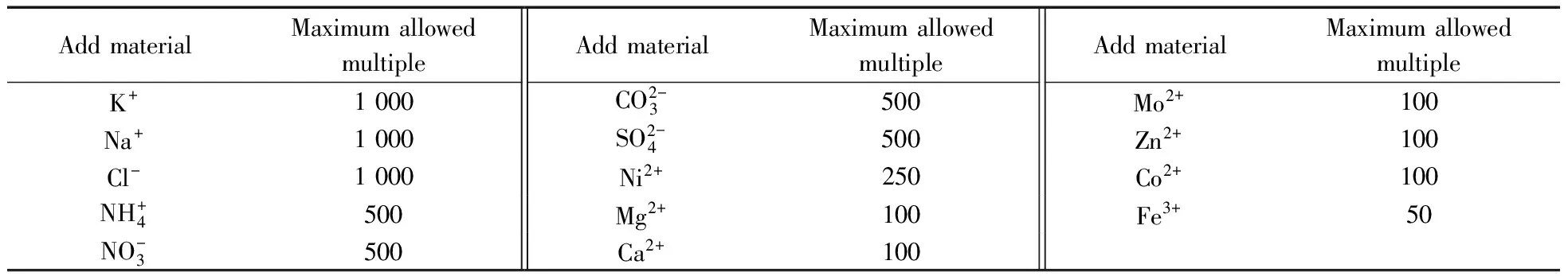
表1 共存离子对荧光强度的影响
2.8 实际样品的测定
为考察本方法测定水体中Cu2+的可行性和实用性,采集桂林市茶江村中茶江河水、村中农田沟渠水,以及实验中的自来水3种水样。参考文献[19],进行水样简单处理:采集样品在塑料瓶中静置3 d,取上层清液,用长颈漏斗、慢速滤纸过滤,使用50 mL锥形瓶接液。按实验方法进行样品测定,并进行加标回收实验,结果如表2所示。Cu2+的回收率为98.7%~99.0%,RSD不大于0.91%,说明方法具有良好的精密度和准确度。

表2 样品分析结果
3 结 论
本文利用CQDs-FP间的能量转移构建了荧光共振能量体系,探究该体系的影响因素以提高荧光能量转移的效率,并且基于Cu2+能够使CQDs-FP体系的荧光发生猝灭,通过优化实验条件,成功建立了测定痕量Cu2+的新方法。Cu2+的线性范围为9.42~23.55 μmol/L,检出限为3.14 μmol/L,回收率为98.7%~99.0%。该方法操作简单、选择性好、灵敏度高、线性范围宽,应用于水体样品中Cu2+的测定,结果令人满意。
[1] Wang S Z,Meng S M,Guan C L,Liu Y C.Chin.J.Anal.Lab.(王尚芝,孟双明,关翠林,刘月成.分析试验室),2013,32(2):36-38.
[2] Zhu Q R,Geng M,Sun D M.J.Anal.Sci.(朱庆仁,耿明,孙登明.分析科学学报),2010,26(2):240-242.
[3] Li C A,Ge C W,Liu Z H,Zhang H Q,Gu N.J.SoutheastUniv.:Nat.Sci.Ed.(李昌安,葛存旺,刘战辉,张海黔,顾宁.东南大学学报:自然科学版),2004,34(1):78-81.
[4] Guo C Z,Li Z B,Chen C G,Liu L.J.ChongqingUniv.ArtsSci.:Nat.Sci.Ed.(郭朝中,李忠彬,陈昌国,刘莉.重庆文理学院学报:自然科学版),2010,29(4):41-44.
[5] Zhuang J M,Zhang L,Zhang C R,Shen D Z,Pan D W.Environ.Sci.Technol.(庄建梅,张丽,张春荣,申大忠,潘大为.环境科学与技术),2012,35(7):138-141.
[6] Dai S J,Zhang X S.LeatherSci.Eng.(代仕均,张新申.皮革科学与工程),2011,21(1):62-67.
[7] Liu L,Zhou G M,Zhang X S.Chin.J.Anal.Chem.(刘玲,周光明,张新申.分析化学),2002,30(4):478-481.
[8] Fan J,Ye C L,Qin Y X,Zhu G F,Feng S L.Chin.J.Appl.Chem.(樊静,叶存玲,秦玉霞,朱桂芬,冯素玲.应用化学),2010,27(9):1088-1092.
[9] Lin S.FujianAnal.Test.(林松.福建分析测试),2008,17(3):21-23.
[10] Gao L J,Zhao Y,Sun X H,Chai H M,Chen L.Chin.J.Anal.Lab.(高楼军,赵艳,孙雪花,柴红梅,陈露.分析试验室),2012,31(3):59-61.
[11] Yuan Y H,Feng F,Tian M Z,Meng S M,Bai Y F.Chem.J.Chin.Univ.(袁跃华,冯锋,田茂忠,孟双明,白云峰.高等学校化学学报),2011,32(1):62-66.
[12] Wang S M,Song X P.J.AnhuiAgric.Univ.(汪松美,宋晓朋.安徽农业大学学报),2013,40(1):155-158.
[13] Sheng L,Zhao Y L,Liu G L,Su B Q.Chin.J.Spectrosc.Lab.(盛丽,赵玉玲,刘改兰,苏碧泉.光谱实验室),2012,29(5):3185-3188.
[14] Xie S F,Bao S X,Ouyang J J,Zhou X,Kuang Q,Xie Z X,Zheng L S.Chem.Eur.J.,2014,20(18):5244-5252.
[15] Wang Z H,Gao Y L,Zhang F F,Xia Y Z,Li Y H.J.Anal.Sci.(王宗花,高艳丽,张菲菲,夏延致,李延辉.分析科学学报),2012,28(1):119-125.
[16] Ma H L,Liu H Z,Wang L P,Xu S K,Li W.Chin.J.Anal.Chem.(马慧莲,刘含智,王丽萍,徐淑坤,李惟.分析化学),2005,33(9):1335-1338.
[17] Guo Y M,Wang Z,Shao H W,Jiang X Y.Carbon,2013,5(2):583-589.
[18] Xu X T,Du Z Y,Lu Y J,Huang H R,Zhang R R,Zhang K.J.Instrum.Anal.(徐学涛,杜志云,卢宇靖,黄华容,张瑞瑞,张焜.分析测试学报),2011,30(10):1183-1186.
[19] Wang S W,Hu W F.ShanghaiEnviron.Sci.(王素文,胡文福.上海环境科学),1995,14(1):30-34.
Study on Fluorescence Resonance Energy Transfer of Carbon Dots-Fluorescent Pink System and Its Application in Detection of Trace Copper(Ⅱ)
TAO Hui-lin*,SUN Chao,LIAO Xiu-fen,XU Ming-ze,WANG Hai-yang,YI Zhong-sheng,QIN Hong-wei
(College of Chemistry and Bioengineering,Guilin University of Technology,Guilin 541004,China)
A new fluorescence method for the determination of trace Cu2+was developed by using fluorescence resonance energy transfer between carbon quantum dots and fluorescent pink,in which carbon dots acted as an energy donor and FP as an acceptor.It was found that under the conditions ofλex=581 nm and pH=8.4 aqueous solution,energy transfered from carbon dots to FP and led to enhance the fluorescence of FP.However,the addition of trace Cu2+made FP fluorescence quenching.The quenching degree was quantitatively in proportion to the trace Cu2+content.Therefore,a novel fluorescence quenching platform for determination of trace Cu2+was constructed.Under the optimum conditions,the calibration curve for Cu2+concentration was linear in the range of 9.42-23.55 μmol/L with a detection limit(3σ/k) of 3.14 μmol/L.The method was applied in the determination of trace Cu2+in river,farmland water and tap water,with spiked recoveries of 98.7%-99.0% and relative standard deviations(RSD) not more than 0.91%.
carbon dots;fluorescent pink;fluorescence resonance energy transfer;trace Cu2+
2014-09-23;
2014-11-20
国家自然科学基金项目(21267008);广西自然科学基金项目(2013GXNSFAA019034)
10.3969/j.issn.1004-4957.2015.02.009
O657.3;O614.121
A
1004-4957(2015)02-0177-06
*通讯作者:陶慧林,副教授,研究方向:光谱分析,Tel:0773-5898551,E-mail:thl@glut.edu.cn
