石墨烯量子点印迹传感器检测盐酸罗哌卡因
2015-04-27张晓蕾孙如宁杨小弟
张晓蕾, 孙如宁, 杨小弟
(1.中国药科大学 高等职业技术学院,江苏 南京 211198;2.南京师范大学化学与材料科学学院,江苏 南京 210097)
石墨烯量子点印迹传感器检测盐酸罗哌卡因
张晓蕾1, 孙如宁1, 杨小弟2*
(1.中国药科大学 高等职业技术学院,江苏 南京 211198;2.南京师范大学化学与材料科学学院,江苏 南京 210097)
采用热聚合法合成石墨烯量子点,再将石墨烯量子点通过π-π作用吸附在聚邻氨基苯酚膜表面,基于石墨烯量子点表面电化学印迹,制备石墨烯量子点-分子印迹传感器检测盐酸罗哌卡因。同时采用原子力显微镜表征石墨烯量子点尺寸,示差脉冲伏安法研究印迹响应机理。安培I~t曲线法发现传感器对盐酸罗哌卡因的响应线性范围为2.0×10-6~6.1×10-4mol/L,检出限(S/N=3)为1.1×10-6mol/L,与未使用石墨烯量子点的分子印迹传感器对比,石墨烯量子点-分子印迹传感器的线性范围变宽,检出限降低,空白加标回收率为91.0%~101%。将传感器用于血浆样品中盐酸罗哌卡因的检测,测得其浓度为4.21×10-6mol/L,高效液相色谱法验证显示该方法的检测结果可靠,可用于临床样品的检测。
石墨烯量子点;分子印迹;盐酸罗哌卡因;邻氨基苯酚
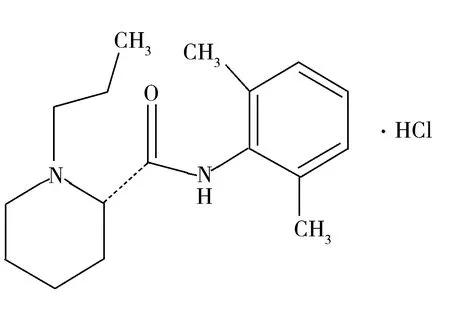
图1 盐酸罗哌卡因的分子结构
罗哌卡因(Ropivacaine,RP)是瑞典Astra制药公司研发的新型长效酰胺类局麻药,主要用于外科麻醉和硬膜外阻滞麻醉,可用于各种手术,以及手术后或分娩后急性止痛[1]。麻醉剂用量直接影响麻醉作用效果,麻醉剂过量更有可能导致死亡,因此临床常用注射剂盐酸罗哌卡因(Ropivacaine hydrochloride,RH)(见图1)含量的准确检测,对有效控制麻醉剂用量具有重要意义。目前检测罗哌卡因的主要方法有高效液相色谱法、液相色谱-质谱法、气相色谱-质谱法等[2-4]。这些方法相对复杂,使用设备昂贵,而电化学法比较简便,且目前使用电化学法检测盐酸罗哌卡因的研究尚无报道。
分子印迹是一种合成对某一特定分子(印迹分子)具有选择性的聚合物的方法[5-6]。分子印迹聚合物内部具有固定大小和形状的孔穴,并具有确定排列的功能基团,其对模板分子的立体结构具有记忆功能。石墨烯量子点是尺寸小于100 nm的石墨烯片[7],其显著的量子限域和边缘效应,使之呈现出多种新的物理和化学性质[8-9],可用于传感器研制[10-11]。石墨烯量子点具有良好的电子迁移速率和化学稳定性,有望成为电化学传感器的理想电极材料[12-14]。本研究以盐酸罗哌卡因为模板分子,邻氨基苯酚为功能单体,使用分子印迹技术在石墨烯量子点表面电化学聚合印迹修饰玻碳电极制备传感器(GQDs-MIP/GCE),并将其用于盐酸罗哌卡因的检测。该方法操作简单、检测线性范围宽、重现性和稳定性好,为临床样本中盐酸罗哌卡因的检测提供了一种新方法。
1 实验部分
1.1 仪器与试剂
CHI830C电化学工作站(上海辰华仪器公司);VNS5型原子力显微镜(美国Veeco公司),Agilent Technologies 1260 高效液相色谱仪(Agilent Eclipse XDB-C18色谱柱,Agilent 1260DAD检测器)。
盐酸罗哌卡因(RH,纯度>99%,中国药科大学药剂实验室);柠檬酸(纯度>99.5%)、邻氨基苯酚(OAP)、抗坏血酸(国药集团化学试剂有限公司);盐酸多巴胺(98%,阿拉丁试剂);苯丙氨酸、色氨酸(上海惠兴生化试剂有限公司);血浆样品(中国药科大学药剂实验室);甲醇(色谱纯,美国Tedia公司);其余均为分析纯试剂,实验用水为二次蒸馏水。
1.2 实验方法
1.2.1 石墨烯量子点的合成 石墨烯量子点(GQDs)的合成使用 “从下至上”的方法[15]。称取2 g柠檬酸置于20 mL烧杯中,在控温电热套中加热至200 ℃,保持恒温,在5 min内柠檬酸融化成无色液体再转变成淡黄色,在30 min内变成橙色时得到石墨烯量子点,加入10 mL水充分搅拌30 min得到石墨烯量子点贮备液,置于4 ℃冰箱中保存。
1.2.2 石墨烯量子点印迹电极的制备 玻碳电极依次用1.0,0.3,0.05 μm的氧化铝粉抛光,在水和无水乙醇中分别超声洗涤5 min,并重复3次,进行电化学抛光处理,在0.5 mol/L的H2SO4中于-0.3~1.5 V进行循环伏安电化学处理,直至获得稳定的循环伏安响应。
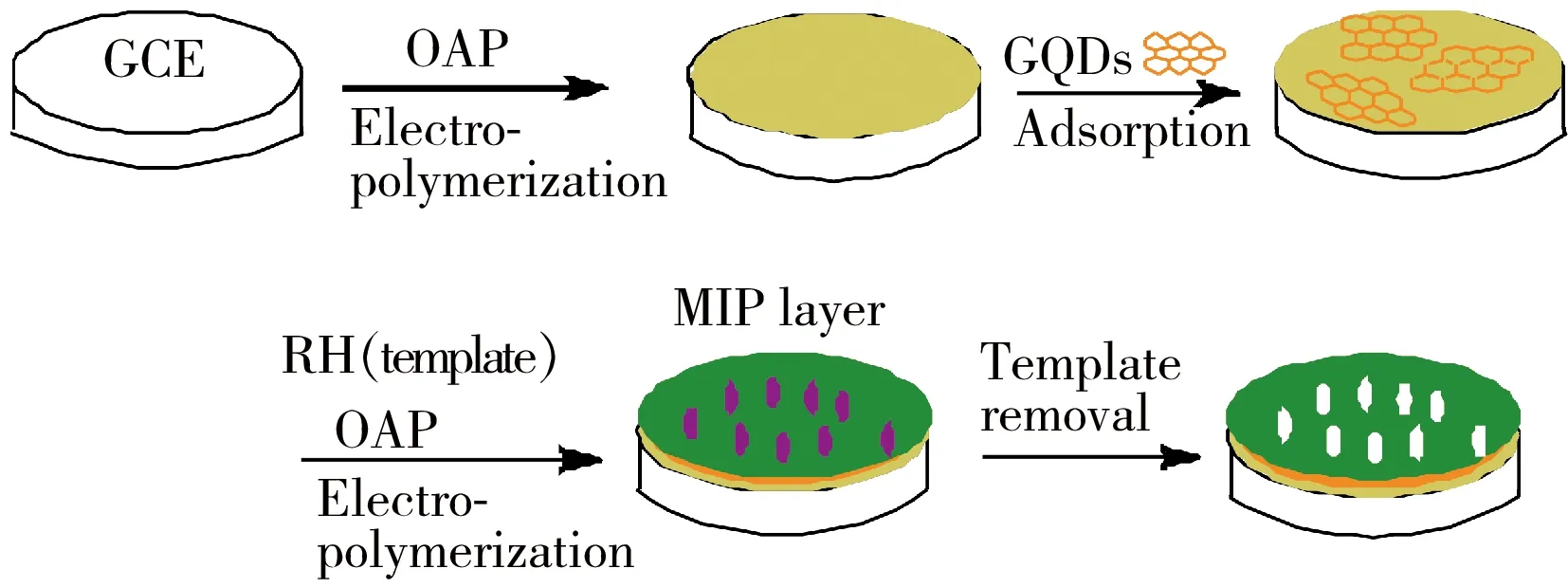
图2 GQDs-MIP/GCE电极制备过程示意图
如图2所示,电化学聚合在含有50 mmol/L 邻氨基苯酚(OAP)的1 mol/L H2SO4和0.5 mol/L NaSO4溶液中进行,用循环伏安法扫描10次,扫描范围-0.2~0.8 V,扫描速率100 mV/s,在玻碳电极表面形成导电聚合膜,得聚邻氨基苯酚膜修饰电极。
取1 mL 0.2 g/mL GQDs贮备液稀释10倍,将聚邻氨基苯酚膜(POAP)修饰电极浸入稀释后的GQDs溶液中6 h,待GQDs充分吸附于膜表面后取出,用水清洗电极表面得POAP-GQDs修饰电极。
在0.2 mol/L NaCl介质中,以5 mmol/L RH为模板分子,25 mmol/L 邻氨基苯酚为功能单体,在GQDs表面采用“致孔剂印迹技术”[16-17]电化学印迹聚合,循环伏安法扫描30次,扫描范围-0.2~1.2 V,扫描速率50 mV/s,使印迹聚合膜沉积在电极表面,再用0.5 mol/L的H2SO4溶液洗涤12 h,除去聚合物基质中的RH,制成保留有模板分子构型孔穴的石墨烯量子点印迹(GQDs-MIP/GCE)电极。
1.2.3 石墨烯量子点无印迹电极的制备 实验步骤与“1.2.2”同,在印迹聚合液中不加入模板分子RH,即制得石墨烯量子点无印迹(GQDs-NIP/GCE)电极。
1.2.4 未掺杂石墨烯量子点印迹电极的制备 除电极不浸入GQDs溶液中,其它实验步骤与“1.2.2”相同,即制得无石墨烯量子点印迹(MIP/GCE)电极。
1.3 电化学测量
电化学测量在传统三电极电化学池中进行,分别以GCE,GQDs-MIP/GCE,GQDs-NIP/GCE,MIP/GCE电极为工作电极,铂丝电极为辅助电极,饱和甘汞电极为参比电极。采用循环伏安法表征电极表面的修饰膜,支持电解质为含有0.1 mol/L KNO3的5 mmol/L K3[Fe(CN)6]/K4[Fe(CN)6(1∶1)溶液,电位扫描范围-0.1~0.6 V,扫描速率50 mV/s。用示差脉冲伏安法表征电极印迹效应,扫描速率为20 mV/s,脉冲振幅为50 mV,脉冲宽度为50 ms,安培I~t曲线法研究电极性能,电解质溶液均为含有0.1 mol/L KNO3的5 mmol/L K3[Fe(CN)6]/K4[Fe(CN)6](1∶1)的PBS缓冲溶液(pH 7.4)。
1.4 血浆样品处理
将血浆样品离心,取上层清液与甲醇按照体积比1∶3充分混合,在5 ℃以8 000 r/min转速离心分离7 min后,取上层清液定容。
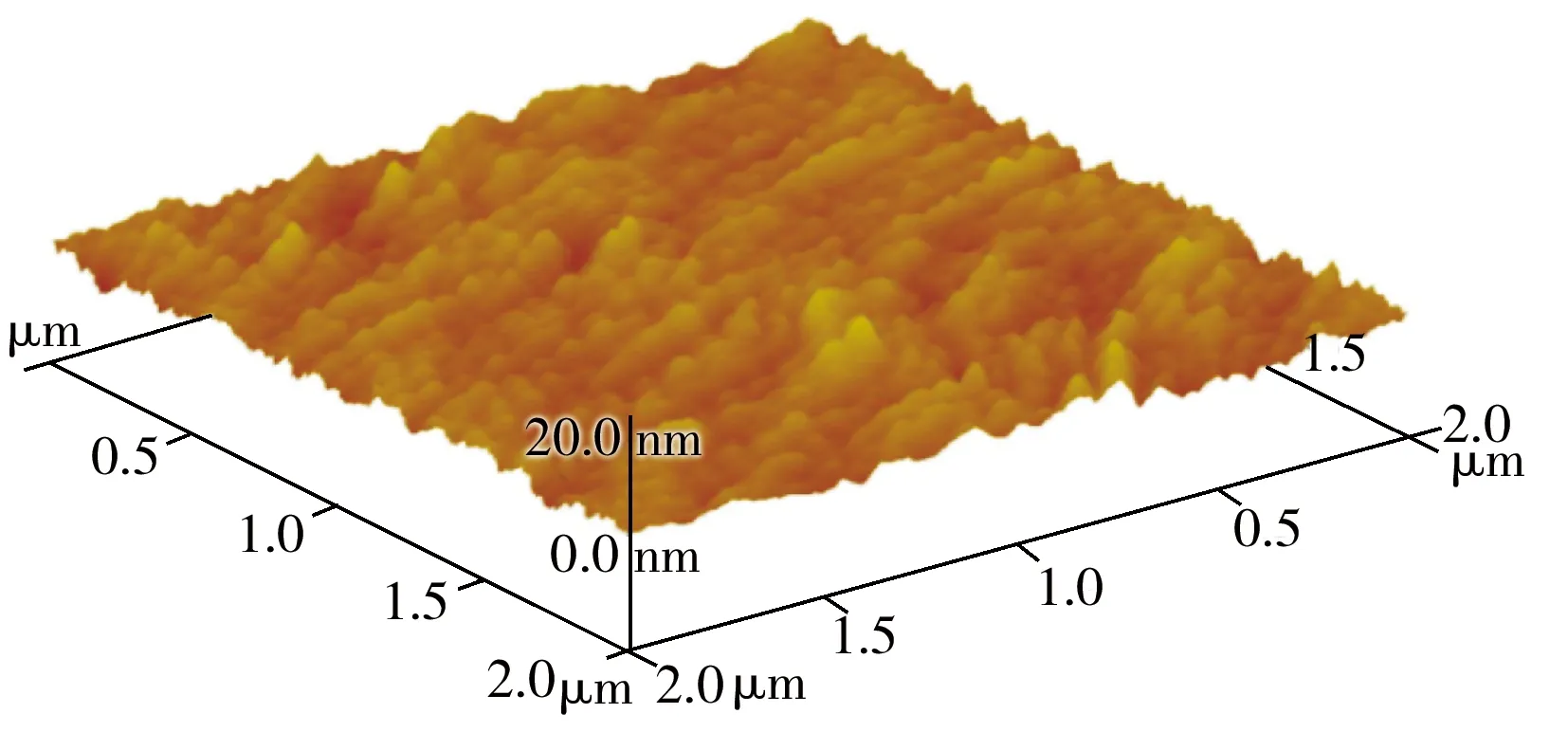
图3 GQDs 的原子力显微镜图
1.5 高效液相色谱条件
流动相为甲醇-水(40∶60),加入磷酸二氢钾调节流动相pH值至3.8,流速1 mL/min,柱温30 ℃,检测波长215 nm,柱压182 bar。
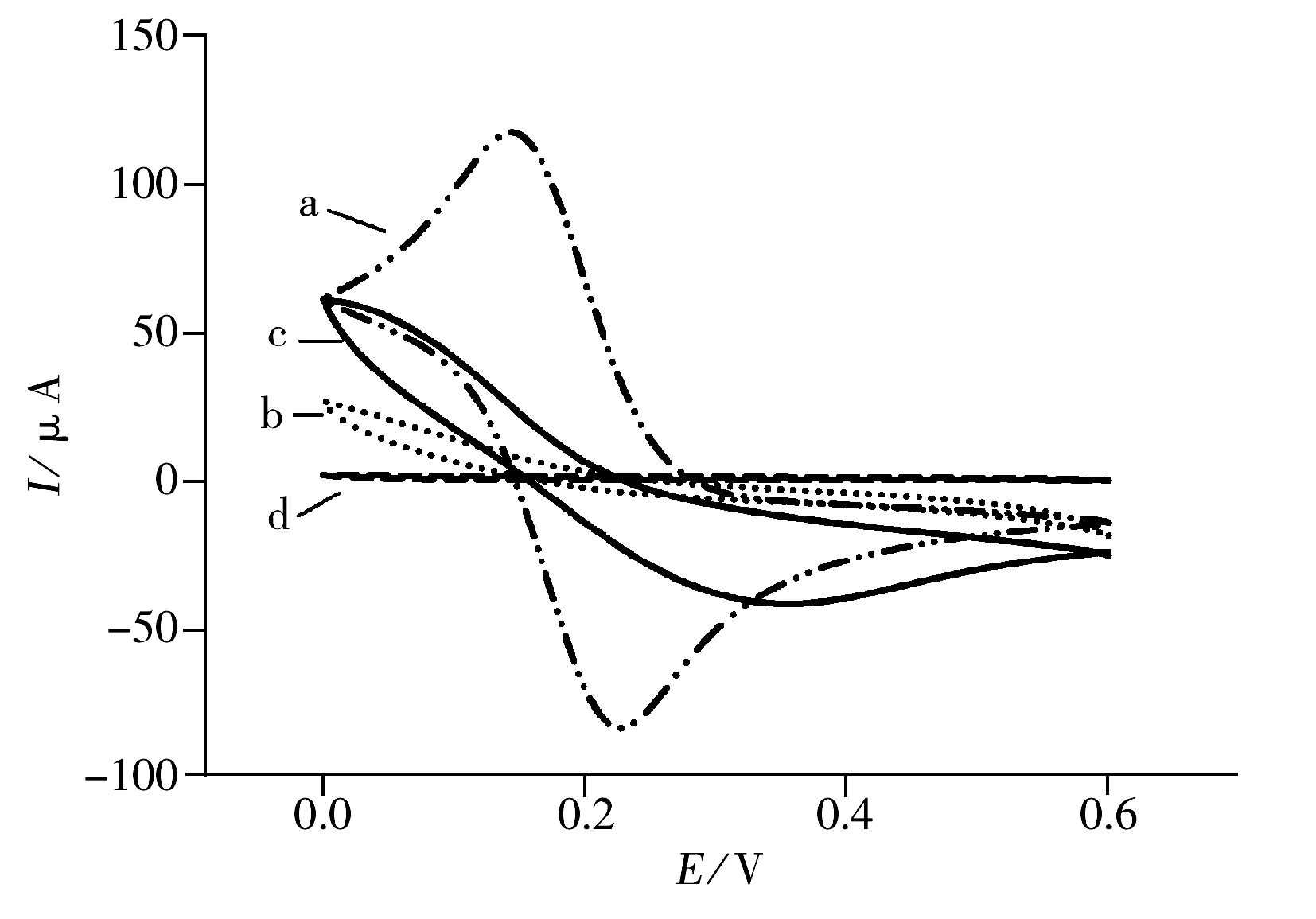
图4 4种电极在含0.1 mol/L KNO3的5 mmol/L [Fe(CN)6]3-/4-(1∶1)溶液中的循环伏安图
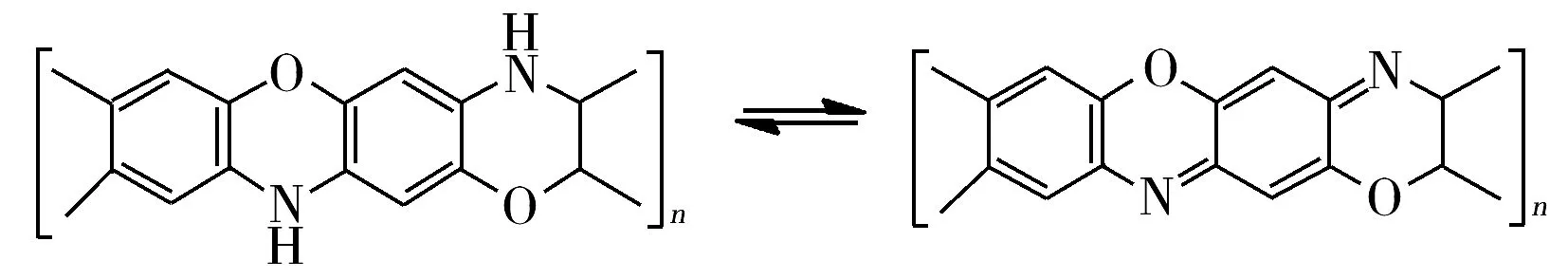
图5 酸性介质中聚邻氨基苯酚膜的结构
2 结果与讨论
2.1 原子力显微镜表征GQDs
本实验通过柠檬酸分子的热聚合生成石墨烯量子点。如图3所示,所制得GQDs粒径控制在20 nm左右,与文献[15]一致。
2.2 修饰电极的电化学表征
采用循环伏安法表征电极膜的导电性能。图4为4种不同电极在含0.1 mol/L KNO3的5 mmol/L [Fe(CN)6]3-/4-(1∶1)溶液中的循环伏安图。图4a是裸玻碳电极表面[Fe(CN)6]3-/4-离子氧化还原反应的循环伏安曲线,邻氨基苯酚在H2SO4酸性介质(pH<3.0)中电聚合成均匀的导电聚邻氨基苯酚膜(膜结构见图5)[18],[Fe(CN)6]3-/4-离子在聚邻氨基苯酚膜(POAP)修饰电极表面的循环伏安曲线见图4b。石墨烯量子点由于π-π堆积作用吸附在聚邻氨基苯酚膜表面,因石墨烯量子点具有优良的电子迁移速率,可以观察到电极表面循环伏安曲线的氧化还原电流增强(图4c),说明电极在吸附石墨烯量子点后,其导电性能增强。然而在中性NaCl介质中,分子印迹溶液中的功能单体邻氨基苯酚电聚合成均匀的非导电性聚合膜,则电极表面循环伏安曲线的氧化还原电流明显减弱(图4d)。
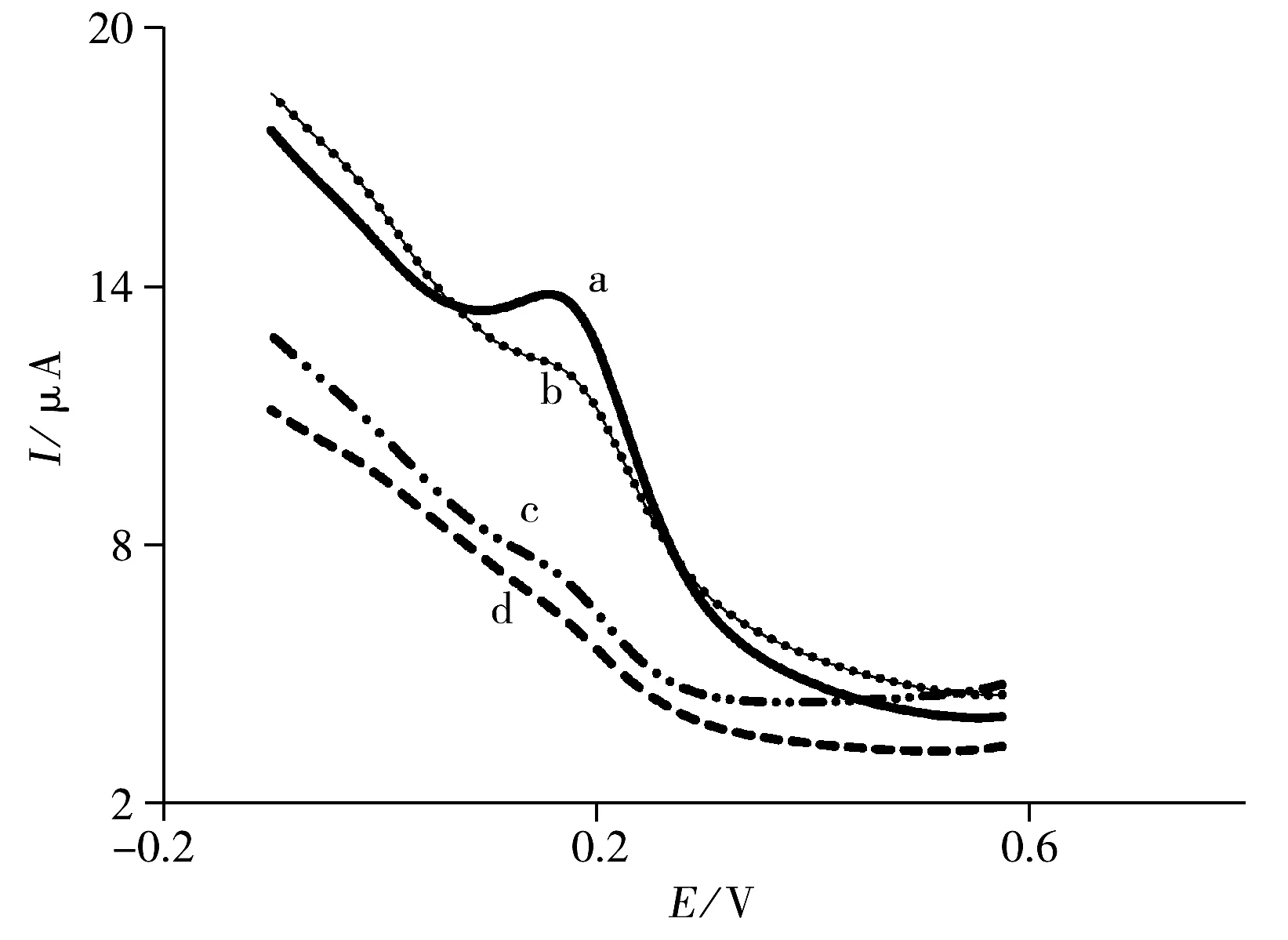
图6 GQDs-MIP/GCE(a,b)与GQDs-NIP/GCE(c,d) 电极对RH响应的示差脉冲伏安图
2.3 传感器印迹效应
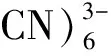
未加模板分子的GQDs-NIP/GCE电极经0.5 mol/L H2SO4洗脱后,在[Fe(CN)6]3-/4-溶液中的示差脉冲伏安曲线(见图6c)无明显的峰电流。再加入0.04 mmol/L RH后,仍未观察到显著的峰电流(图6d),由此可以证明未印迹电极对RH无响应。
2.4 检测溶液pH值的影响
因RH的pKa为8.1,在碱性较强溶液中易发生沉淀,而溶液酸性较强可能会阻碍RH分子进入空穴形成氢键。实验考察了检测溶液pH值在5.8~7.6范围内时传感器对0.01 mmol/L RH的响应。溶液pH值从5.8增加到7.3时,传感器响应电流逐渐增大,在7.3~7.5之间,传感器响应电流值达到最大,而从pH 7.5继续增加到pH 7.6时,响应电流值开始降低,继续增大溶液pH值,RH开始沉淀,无法再检测。同时考虑到人体血液pH值在7.35~7.45之间,故选择pH 7.4的PBS缓冲溶液为检测底液。
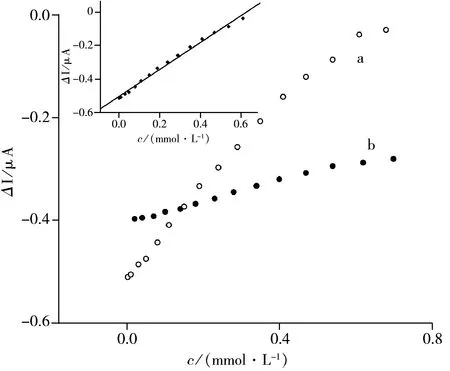
图7 GQDs-MIP/GCE(a) 与MIP/GCE 电极(b) 对RH的响应曲线
2.5 传感器线性范围及检出限
在pH 7.4的PBS缓冲溶液中,应用安培I~t曲线法测定GQDs-MIP/GCE和MIP/GCE电极对不同浓度RH的响应(如图7所示)。对比其响应曲线,结果显示,加入GQDs后增强了电子传导速率以及电极表面对检测物的富集,使得GQDs-MIP/GCE的电极响应信号更灵敏,线性范围更宽。RH浓度在2.0×10-6~6.1×10-4mol/L范围内与电流变量有良好线性关系(图7插图),线性方程为ΔI(μA)=0.803 2c(mmol/L)-0.504 0(r2=0.993 1),检出限(S/N=3)为1.1×10-6mol/L。
2.6 传感器的重现性、抗干扰性及稳定性
在相同实验条件下,用同1支GQDs-MIP/GCE电极对0.01 mmol/L RH平行测定6次,响应值的相对标准偏差(RSD)为2.3%;用相同方法修饰6支电极,并分别测定0.01 mmol/L RH,其RSD为2.4%。
实验还考察了血液中部分生物分子和常见无机盐离子对传感器检测RH的干扰情况。相同实验条件下,浓度均为0.01 mmol/L的盐酸多巴胺、抗坏血酸、苯丙氨酸、色氨酸、葡萄糖以及无机磷、Na+, Mg2+,K+,Ca2+,Cl-离子均无干扰(RSD<5%)。结果表明,此方法的抗干扰性较好。
经实验研究,使用过的电极用0.5 mol/L H2SO4洗涤10 min即可使电极基本恢复至响应前的状态,并可得到重现的响应值。将电极放在4 ℃冰箱保存7 d后,其对RH的响应值仍保持在初始值的90.1%。以上结果表明传感器具有良好的重现性和稳定性。
2.7 空白加标回收实验
在0.1 mol/L KNO3的5 mmol/L K3[Fe(CN)6]/K4[Fe(CN)6](1∶1)PBS缓冲溶液(pH 7.4)中,采用标准加入法测定RH的回收率,结果如表1所示。空白加标回收率为91.0%~101%,RSD为1.3%~2.1%,此结果说明空白基质干扰较小,该方法准确度较好。

表1 空白加标回收率及相对标准偏差
2.8 实际样品的检测
为考察方法实用性,将传感器用于血浆样品中RH的检测,测得样品中RH浓度为4.21×10-6mol/L,RSD(n=6)为3.1%。同时采用高效液相色谱法检测相同血浆样品,测得样品中RH浓度为3.99×10-6mol/L,RSD(n=6)为2.9%。由此可以证明应用电化学方法测量的可行性。
3 结 论
本文将石墨烯量子点材料与分子印迹技术结合,研制了检测RH的GQDs-MIP/GCE电化学传感器。该传感器具有制备简便、耗时短、线性范围宽,选择性、重现性和稳定好等优点,有望用于临床样本中RH含量的检测。
[1] Xu S J,Tu J S,Pang H.J.ChinaPharm.Univ.(徐盛杰,涂家生,庞卉.中国药科大学学报),2009,40(3):213-217.
[2] Engman M,Neidenström P,Norsten-Höög C,Wiklund S J,Bondesson U,Arvidsson T.J.Chromatogr.B,1998,709(1):57-67.
[3] Stumpe M,Morton N S,Watson D G.J.Chromatogr.B,2000,748(2):321-330.
[4] Daryanavard S M,Jeppsson-Dadoun A,Andersson L I,Hashemi M,Colmsjö A,Abdel-Rehim M.Biomed.Chromatogr.,2013,27(11):1481-1488.
[5] Haupt K,Mosbach K.Chem.Rev.,2000,100(7):2495-2504.
[6] Ye L,Mosbach K.J.Am.Chem.Soc.,2001,123(12):2901-2902.
[7] Zhang Z P,Zhang J,Chen N,Qu L T.EnergyEnviron.Sci.,2012,5(10):8869-8890.
[8] Liu R L,Wu D Q,Feng X L,Müllen K.J.Am.Chem.Soc.,2011,133(39):15221-15223.
[9] Zhou X J,Zhang Y,Wang C,Wu X C,Yang Y Q,Zheng B,Wu H X,Guo S W,Zhang J Y.ACSNano,2012,6(8):6592-6599.
[10] Shen J H,Zhu Y H,Yang X L,Li C Z.Chem.Commun.,2012,48(31):3686-3699.
[11] Li L L,Wu G H,Yang G H,Peng J,Zhao J W,Zhu J J.Nanoscale,2013,5(10):4015-4039.
[12] Zhao J,Chen G F,Zhu L,Li G X.Electrochem.Commun.,2011,13(1):31-33.
[13] Razmi H,Mohammad-Rezaei R.Biosens.Bioelectron.,2013,41:498-504.
[14] Hou J Y,Bei F,Wang M L,Ai S Y.J.Appl.Electrochem.,2013,43(7):689-696.
[15] Dong Y Q,Shao J W,Chen C Q,Li H,Wang R X,Chi Y W,Lin X M,Chen G N.Carbon,2012,50(12):4738-4743.
[16] Yoshizako K,Hosoya K,Iwakoshi Y,Kimata K,Tanaka N.Anal.Chem.,1998,70(2):386-389.
[17] Shang Z Y,Liu Y L,Liu Y,Song Q J.J.Instrum.Anal.(商哲一,刘艳丽,刘瑛,宋启军.分析测试学报),2013,32(11):1401-1408.
[18] Tucceri R,Arnal P M,Scian A N.Can.J.Chem.,2013,91(2):91-112.
Determination of Ropivacaine Hydrochloride with Graphene Quantum Dots-Molecularly Imprinted Polymer Electrochemical Sensor
ZHANG Xiao-lei1,SUN Ru-ning1,YANG Xiao-di2*
(1.Higher Vocational College,China Pharmaceutical University,Nanjing 211198,China;2.College of Chemistry and Materials Science,Nanjing Normal University,Nanjing 210097,China)
A novel electrochemical sensor for ropivacaine hydrochloride(RH) based on graphene quantum dots-molecularly imprinted polymer(MIP) modified glass carbon electrode was constructed.The graphene quantum dots(GQDs) were synthesized by the pyrolysis method,and adsorbed on the surface of conducting poly(o-aminophenol) membrane by π-π stacking,and then theo-aminophenol as functional monomer and RH as template molecule were electrochemically imprinted on the film of GQDs to develop the GQDs-MIP sensor.The average lateral size of GQDs characterized by atomic force microscope(AFM) is about 20 nm.The response mechanism of the resulting sensor was investigated by differential pulse voltammetry and the linear relationship of sensor was determined by means of amperometricI-tcurve.The results indicated that the calibration curve was linear in the range of 2.0×10-6-6.1×10-4mol/L,and the detection limit(S/N=3)was 1.1×10-6mol/L.Compared with the molecular imprinting sensor without GQDs,the GQDs-MIP sensor exhibited a wide linear range and a lower detection limit.The spiked recoveries were in the range of 91.0%-101%.The sensor was applied in the analysis of RH in plasma samples with RH concentration of 4.21×10-6mol/L.In contrast to the detection result of high performance liquid chromatography(HPLC) method,this electrochemical analytical approach is credible,and could be applied in the detection of RH in clinical samples.
graphene quantum dots(GQDs);molecular imprinting;ropivacaine hydrochloride(RH);o-aminophenol
2014-10-03;
2014-11-20
中国药科大学中央高校基本科研业务费专项资金(JKQZ2013010)
10.3969/j.issn.1004-4957.2015.02.006
O657.1;TQ460.72
A
1004-4957(2015)02-0159-05
*通讯作者:杨小弟,博士,教授,研究方向:环境分析,Tel:13951867138,E-mail:yangxiaodi@njnu.edu.cn
